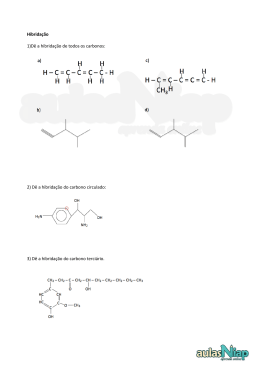
VOLUME 3 | QUÍMICA 3 Resoluções das Atividades Sumário Aula 11 – Hibridização; Geometria molecular; Teoria da Repulsão dos Pares Eletrônicos da Camada de Valência.................................................. 1 Aula 12 – Polaridade molecular e ligações intermoleculares............................ 2 . Aula 11 Hibridização; Geometria molecular; Teoria da Repulsão dos Pares Eletrônicos da Camada de Valência Analisando os três compostos, notamos que nenhum deles apresenta hibridização sp: sp3 sp2 sp3 sp2 sp3 sp2 sp2 sp3 A grafite, que apresenta carbono com hibridização sp2, pode conduzir eletricidade devido à deslocalização de elétrons de ligações (p) acima e abaixo dos planos de átomos de carbono. Observe o modelo de ressonância na figura a seguir. sp2 sp2 sp2 sp sp3 2 sp3 sp2 I-Eugenol 2 sp sp2 sp2 sp2 sp3 sp3 sp2 sp2 H sp2 sp2 sp2 H C 03 E 01 D sp3 H 109,5° Atividades para Sala Esses orbitais são muito semelhantes aos híbridos sp e sp2, mas eles estão dirigidos para os vértices de um tetraedro regular. Isto está de acordo com a forma tetraédrica da molécula CH4. H II-Mentona 04 A III-Vanilina As ligações sigma (s) e pi (p) presentes nos compostos são as seguintes: 02 D O carbono do CH4 possui estado de hibridação sp3: No metano (CH4), o átomo de carbono usa o orbital 2s e os três orbitais 2p para formar quatro orbitais híbridos sp3. Átomo no estado fundamental: 1s2 2s2 2p2 1s2 py px 2s2 s s s s s s sp sp sp sp3 sp3 s s s p p s s acetileno 3 sp 3 O átomo ligado: s p etileno etano pz mistura 3 s s s 3 s s sp3 sp3 elétrons vindos de outros átomos, por exemplo, H. Devido à interpenetração dos orbitais, percebemos que ocorre um encurtamento no comprimento das ligações covalentes, pois quanto maior a fusão de orbitais, maior a aproximação dos núcleos. Comparando os comprimentos de ligação: Ligação simples > Ligação dupla > Ligação tripla Concluímos que: 154 pm > 134 pm > 121 pm > 110 pm. A ligação C H é menor do que a C C, pois o hidrogênio tem o raio menor do que o do carbono. Pré-Universitário | 1 VOLUME 3 | QUÍMICA 3 Atividades Propostas 08 D 01 A Observando a estrutura do SO2, podemos concluir que trata-se de uma molécula angular, polar e que o átomo de S possui hibridação sp2. 119° 09 D No caso do ClF3 temos uma geometria da molécula em forma de T, uma geometria dos pares de elétrons pirâmide de base quadrada e uma hibridação do tipo sp3d e sp3d2. 10 B 0,136nm Observando o composto, temos 26 ligações do tipo sigma e 4 ligações do tipo pi. 0,136nm 0,107nm 02 D 120° 0,107nm d Como no composto temos uma ligação tripla e quatro ligações duplas, há um total de seis ligações p, e o H ligado ao nitrogênio faz ponte de hidrogênio. I. (V) Suas moléculas contêm carbonos sp2. II. (V) São hidrofóbicas, pois são apolares, não se dissolvendo em água. III. (F) A vitamina A possui um álcool primário. Aula 12 06 B I. (F) Por se tratarem de moléculas heteroatômicas simétricas, todas são apolares. II. (V) A molécula BF3 deve ser plana, pois o elemento B apresenta uma hibridização do tipo sp2. III. (F) Apenas a molécula NH3 pode fazer ponte de hidrogênio. 07 C Observando as constituições da questão, podemos observar que todos os carbonos possuem ligação dupla, logo, todos são sp2. 2 | Pré-Universitário 60° a Polaridade molecular e ligações intermoleculares 01 B 05 C a) (F) A fórmula molecular é C18H29N. b) (F) O número de átomos de carbono primário, secundário e terciário é, respectivamente, 2, 12 e 4. c) (V) O número de átomos de carbono com hibridização sp3, sp2 e sp é, respectivamente, 15, 2 e 1. d) (F) O número de ligações pi (p) é igual a 3. e) (F) Todos os átomos de carbono que possuem apenas ligações simples possuem geometria tetraédrica. 0,136nm Atividades para Sala 04 B Podemos observar, na estrutura, que o tronco possui sete ligações pi alternadas (conjugadas) e que, na ligação tripla, apenas uma das ligações pi está no plano de conjugação. 60° a d = a + 0,136 + a a a 1 ⇒ = ⇒ a = 0, 535 cos 60° = 0,107 2 0,107 d = 2 ⋅ 0, 535 + 0,136 = 0, 243nm 03 B 0,107nm 0,107nm A primeira amina a ser separada é a trimetilamina, pois não apresenta o grupo NH, logo não faz pontes de hidrogênio, que são ligações muito intensas. 02 D Tanto o etanol como a água possuem hidroxilas. A hidroxila (OH) é um grupo que faz ligações de hidrogênio ou pontes de hidrogênio. 03 A Das substâncias elencadas nas alternativas, a única com caráter apolar e, portanto, capaz de dissolver a graxa é a gasolina. 04 B A característica presente nas substâncias tóxicas e alergênicas, que inviabiliza sua solubilização no óleo de mamona, é a hidrofilia, ou seja, a capacidade de atrair compostos polares (hidro = água; filia = afinidade). Como o óleo de mamona é predominantemente apolar, os compostos alergênicos polares não se misturam ao óleo. VOLUME 3 | QUÍMICA 3 Atividades Propostas 04 C I. (V)Os compostos 1, 2, 3 e 4 são, respectivamente, butano, metoxietano, propan-1-ol e ácido etanoico. Butano: dipolo induzido - dipolo induzido. Metoxietano: dipolo permanente - dipolo permanente. Propan-1-ol: pontes de hidrogênio. Ácido etanoico: pontes de hidrogênio em maior quantidade. II. (F) As moléculas do propan-1-ol, por apresentarem o grupo hidroxila em sua estrutura, possuem interações moleculares menos fortes do que as moléculas do ácido etanoico. III.(F)O composto orgânico propan-1-ol é um álcool solúvel em água (solubilidade infinita), pois suas moléculas fazem ligações predominantemente do tipo pontes de hidrogênio. IV.(V) V. (F) O composto metoxietano é um éter que apresenta em sua estrutura um átomo de oxigênio. 01 C A uma mesma pressão, o butanol líquido entra em ebulição a uma temperatura mais alta do que o éter dietílico líquido, pois o butanol faz ponte de hidrogênio, que é uma ligação mais intensa do que o dipolo permanente presente no éter dietílico. (pares de elétrons disponíveis para as pontes) 02 A A partir da análise das forças intermoleculares, lembrando que HF faz pontes de hidrogênio, que são interações mais intensas, e que quanto maior a “nuvem” eletrônica (ou massa), maior a interação intermolecular para as moléculas que não fazem pontes de hidrogênio, podemos concluir que: Substância Temperatura de ebulição (°C) HF 20 HI –35 HBr –67 HCl –85 05 B A temperatura de ebulição aumenta com a intensificação das forças intermoleculares do tipo dipolo-induzido. Quanto maior a cadeia carbônica, maior a força de atração e, consequentemente, maior a temperatura de ebulição: TE (eteno) < TE (propeno) <TE (but-1-eno) < TE (hept-1-eno). 06 D 03 B Teremos: Imiscíveis Imiscíveis (V) Água (menor densidade) Ciclo-hexano (menor densidade) Clorofórmio (maior densidade) Água (maior densidade) II V Observação: A solubilidade em água do clorofórmio é baixa: 0,8g/100 mL a 20°C, por isso ocorre a formação de mistura bifásica com a água. 07 A (V) (F)Se compararmos hidrocarbonetos de mesma massa molar, os compostos de cadeia linear têm temperaturas de fusão e de ebulição maiores que os de cadeia ramificada. (V) (V) A trimetilamina não forma ligações de hidrogênio entre suas moléculas, pois não tem átomo de hidrogênio diretamente ligado a nitrogênio, por isso, não faz ligação ou ponte de hidrogênio. Trimetilamina 08 E Nas mesmas condições de pressão, uma substância no estado líquido possui forças atrativas menores do que a mesma substância no estado sólido. Pré-Universitário | 3 VOLUME 3 | QUÍMICA 3 09 D Teremos: Substâncias mais solúveis Substâncias com solubilidades próximas ao corante amarelo marrom laranja verde amarela azul cor do confeito vermelha Substâncias menos solúveis 2cm 10 A a)(V)Correta, porém mal formulada. Por apresentar cinco grupos hidroxilas, o corante morina faz ligação de hidrogênio com a água. As ligações de hidrogênio são mais intensas do que as forças de van der Waals. A temperatura de ebulição da solução aquosa é maior do que a do soluto puro. b) (F) O composto mostrado na figura 1 apresenta a função fenol, enol, cetona e éter. fenol éter fenol enol cetona c) (F) O carbono da carbonila, no composto mostrado, e os demais apresentam hibridização sp2. d) (F) O composto apresenta 8 elétrons p e não possui carbonos quirais. e) (F) O composto mostrado apresenta isômeros geométricos, mas não possui carbonos quirais ou assimétricos. 4 | Pré-Universitário
Baixar