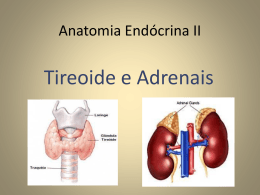
0 FACULDADE ASSIS GURGACZ DETERMINAÇÃO DOS NÍVEIS SÉRICOS DE TRIIODOTIRONINA E TIROXINA LIVRE EM OBESOS NA CIDADE DE RENASCENÇA-PR CASCAVEL 2013 1 GIOVANA PAOLA MATIAS DETERMINAÇÃO DOS NÍVEIS SÉRICOS DE TRIIODOTIRONINA E TIROXINA LIVRE EM OBESOS NA CIDADE DE RENASCENÇA-PR Trabalho de conclusão de curso apresentado a Faculdade Assis Gurgacz, FAG, curso de Farmácia. Prof. Orientador: Claudinei Mesquita da Silva. Prof.ª coorientadora: Leyde D. Peder. CASCAVEL 2013 de 2 GIOVANA PAOLA MATIAS DETERMINAÇÃO DOS NÍVEIS SÉRICOS DE TRIIODOTIRONINA E TIROXINA LIVRE EM OBESOS NA CIDADE DE RENASCENÇA-PR Trabalho apresentado no Curso de Farmácia da Faculdade Assis Gurgacz, como requisito parcial para obtenção do título de Bacharel em Farmácia, sob a orientação do Professor Claudinei Mesquita da Silva. BANCA EXAMINADORA _______________________________ Claudinei Mesquita da Silva Mestre _______________________________ Emerson da Silva Machado Especialista _______________________________ Maria das Graças Hirata Takizawa Mestre Cascavel, 01 de Novembro de 2013. 3 DEDICATÓRIA Dedico este trabalho a todos que contribuíram direta ou indiretamente em minha formação acadêmica. 4 AGRADECIMENTOS Agradeço a todos que contribuíram no decorrer desta jornada, especialmente a Deus, a quem devo minha vida; A minha mãe Soeli e meu padrasto Derly que sempre me apoiaram nos estudos e nas escolhas tomadas; Aos meus avós maternos pelo apoio, incentivo e compreensão; Ao orientador Prof. Claudinei Mesquista da Silva que teve papel fundamental na elaboração deste trabalho; À professora coorientadora Leyde D. de Peder pela atenção e esclarecimento de dúvidas sempre que necessário; À professora e coordenadora Patrícia Lucca pela competência e incentivo durante o período acadêmico; À enfermeira Cleide Soster pela disposição em ajudar e colaborar direta e indiretamente para a realização de algumas etapas desta pesquisa; A todos os pacientes, muito obrigada pela disponibilidade e paciência durante a coleta de dados e realização do estudo; Aos meus colegas pelo companheirismo e disponibilidade para me auxiliar em vários momentos; Por último, manifesto um profundo reconhecimento à minha família pelo apoio incondicional ao longo destes anos. Expresso sentimento idêntico em relação a todos os meus amigos de longa data; A todos que me ajudaram a ser quem sou que depositaram confiança em mim e para os quais sou uma esperança. Muito Obrigada. 5 SUMÁRIO REVISÃO DA LITERATURA .................................................................................... 06 REFERÊNCIAS BIBLIOGRÁFICAS ......................................................................... 21 ARTIGO .................................................................................................................... 26 NORMAS DA REVISTA CIENTÍFICA ....................................................................... 38 ` 6 REVISÃO DA LITERATURA GLÂNDULA DA TIREOIDE A tireoide é uma glândula endócrina importante que proporciona harmonia no funcionamento do organismo. É a maior das glândulas endócrinas e está localizada na parte anterior do pescoço. Mede cerca de cinco cm de diâmetro e pesa cerca de 30 gramas, mas com grande possibilidade de crescimento, uma vez que há relatos na literatura médica da presença de bócios com mais de um quilo (SAAD et al., 2007). A tireoide que produz hormônios responsáveis pela regulação de todo o metabolismo do nosso organismo. Os hormônios produzidos são regulados pelo eixo hipotálamo-hipófise-tireoide, através do feedback positivo e negativo. A tireoide produz a triiodotironina (T3) e a tiroxina (T4) pela estimulação do hormônio tireoestimulante hipofisário (TSH) produzido na hipófise, que por sua vez é regulada pelo hormônio liberador da tireotrofina (TRH) produzido no hipotálamo (BLATT et al., 2007). O que garante o funcionamento regular da tireoide é a glândula hipófise, que se localiza na base do cérebro. Essa glândula produz uma substância denominada TSH, ou Hormônio Estimulador da Tireoide que, pelo sangue, chega à tireoide e a estimula para que produza mais T3 e T4. O TSH é um hormônio glicoproteico. Também pertencem a essa família de hormônios glicoproteicos o hormônio luteinizante (LH), o folículo-estimulante (FSH) e a gonadotrofina coriônica (HCG). Estes são compostos por duas subunidades, a subunidade α e a subunidade β que confere especificidade biológica a cada hormônio. Além da especificidade que confere ao TSH, a cadeia β é também responsável pela sua ligação ao seu receptor (TSHr). Quando a hipófise secreta o TSH, ela o faz para regular a secreção de T4 (tiroxina) e T3 (triiodotironina) (GRAF E CARVALHO, 2002; SAAD et al., 2007). Qualquer alteração nesta regulação pode provocar distúrbios na glândula tireoide, podendo ocasionar tanto um hipotireoidismo, causado pela diminuição dos níveis dos hormônios tireoidianos, quanto um hipertireoidismo, causado pelo aumento dos níveis dos hormônios tireoidianos (MILHORANSA; SOARES, 2009). 7 A prevalência de hipotireoidismo no Brasil não é conhecida com precisão devido à falta de estudos nesta área, mas estima-se que esteja entre 5% e 10%, sendo mais frequente no sexo feminino. A prevalência de hipertireoidismo no Brasil está em torno de 6,5%, mas pelo excesso de iodo na dieta provavelmente essa doença deve estar se tornando mais prevalente (DUARTE et al., 2009). HIPOTIREOIDISMO O hipotireoidismo se caracteriza pela produção diminuída de hormônios tireoidianos (HT), ou raramente, como um estado clínico resultante da produção de uma ação inadequada destes hormônios em nível celular. Dependendo do aumento ou diminuição na produção desses hormônios, variações no quadro clínico do paciente podem ocorrer com maior ou menor gravidade. Os hormônios tireoidianos são importantes reguladores metabólicos durante a vida toda; porém, durante o início da vida é que sua atuação é de fundamental relevância para o desenvolvimento do indivíduo (MURAHOVSCHI, 1994; SETIAN, 2002). Um número considerável de medicamentos pode contribuir para o hipotireoidismo, sendo que um dos mais comuns é o Lítio, usado no tratamento de algumas desordens psiquiátricas. Outra causa do hipotireoidismo é a deficiência de iodo, essencial para a produção dos hormônios da tireoide, que se dá ou pela carência de exposição ao iodo ou por seu excesso (GÜELL, 1998; LA FRANCHI, 1998). Muitas mulheres desenvolvem o hipotireoidismo transitório durante ou depois da gravidez, havendo risco de nascimento prematuro e pré-eclampsia com maior risco durante os últimos três meses, onde pode ocorrer uma forte pressão sanguínea da mãe e afetar o feto. Este tipo de hipotireoidismo transitório tem se mostrado mais comum na Europa onde as mães estão menos expostas ao iodo do que as mães norte-americanas (LA FRANCHI, 1998). A principal forma de hipotireoidismo pode ser causada por cirurgia ou por tratamento com iodo radioativo. A forma primária idiopática desta doença está associada a anticorpos circulantes antitireoidianos, que pode bloquear o 8 receptor de hormônio estimulante da tireoide (BARZEL EUA, 1995; KHAIRA JS, 1999). Em alguns casos, medicamentos, como amiodarona e lítio podem agir como esses anticorpos. O hipotireoidismo pode coexistir com outras doenças auto-imunes como Diabetes Mellitus, doença de Addison, anemia perniciosa, vitiligo e hepatite crônica. Ele também pode ser associado a anomalias renais (FRANKLYN et al.,1998). Doenças auto-imunes ocorrem quando o sistema imunológico produz anticorpos que atacam o seu próprio tecido. Algumas vezes, vírus ou bactérias podem produzir essa mesma resposta, apesar de alguns autores acreditarem que fatores genéticos estejam aí envolvidos (LA FRANCHI, 1998). Sintomas do hipotireoidismo, como intolerância ao frio, ganho de peso, pele seca, constipação intestinal ou lentidão mental e física podem ser confundidos com os sinais normais ou efeitos do envelhecimento (REHMAN et al., 2005). Doenças como depressão e demência podem ser causadas ou agravadas por hipotireoidismo. Pode também ser responsável pela síndrome do túnel cárpico, problema de pé (fraqueza muscular), reações musculares mais lentas, ataxia e neuropatia. Em idosos com múltiplas doenças, o uso de diferente tipo de medicação e seu efeito colateral pode imitar ou mascarar os sintomas de hipotireoidismo. As anormalidades laboratoriais decorrentes de hipotireoidismo são bastante variadas: macrocitose com ou sem anemia, colesterol e triglicerídeos elevados, hiponatremia inexplicável e elevação das enzimas creatinoquinase e lactato desidrogenase (REHMAN et al., 2005). Alguns estudos sugeriram que o hipotireoidismo deve ser avaliado em doentes com anormalidades nos rins. Esta deficiência hormonal pode conduzir a doenças renais: uma vez que os hormônios da tireoide são responsáveis pelo crescimento e desenvolvimento dos rins, que têm uma influência no transporte da substância através membrana e modificar o metabolismo electrolítico. Isto leva a déficits de função renal, associado com a redução do débito cardíaco (KATZ, 1975). Ele também pode causar glomerulopatia (nefrítica e / ou síndrome nefrótica) e ocorrem em diversas formas de doença renal crônica, inclusive em pacientes em hemodiálise, assim, piorar o prognóstico. A maioria das 9 anomalias renais (estruturais, metabólicas e morfológicas), causada por hipotireoidismo pode ser revertido após a suplementação com tiroxina (KAPTEIN EL, 1996). A avaliação da tireoidopatia como causa de obesidade deve ser criteriosa. Quando avaliamos o hipotireoidismo como causa de obesidade devemos verificar um aspecto clínico diferencial importante: o hipotireoideo apresenta redução no crescimento, enquanto o obeso exógeno é maior. Analisar a velocidade de crescimento através da curva ponderal e estatural é o primeiro passo. A seguir, deve-se distinguir entre a simples constatação de doença presente na tireoide com disfunção do órgão. A presença de autoanticorpos séricos, por exemplo, indica a ocorrência de provável tireoidite, mas não que já esteja ocorrendo um hipotireoidismo clínico. A dosagem do T4 livre baixa, acompanhada de elevação do TSH, que caracteriza o hipotireoidismo (DAMIANI D, 2007). Para que se possa diagnosticar a presença do hipotireoidismo, basta um exame de sangue onde se possa dosar o TSH e os hormônios T3 e T4 Livre. Caracteriza-se o hipotireoidismo quando o paciente apresenta TSH aumentado e T4 livre baixo no sangue. Em alguns casos desse distúrbio, considerados mais leves ou iniciais, “pode-se encontrar TSH aumentado com T4 livre normal. Ou seja, o nível de TSH aumenta antes que o nível de T4 livre caia abaixo do normal. Essa situação, em que o TSH está elevado com T4 livre normal, é chamada de hipotireoidismo subclínico” (DIEHL, 2011). HIPOTIREOIDISMO SUBCLÍNICO O Hipotireoidismo subclínico é uma disfunção caracterizada por valor sérico aumentado do TSH com concentrações normais T3 e T4, na ausência de sintomas clínicos manifestos. Esta entidade já foi denominada de hipotiroidismo pré-clínico, diminuição da reserva da tiroide ou mixedema préclínico (EVERED DC, 2002). Incide mais no sexo feminino, e principalmente em pacientes com mais de 60 anos de idade, podendo alcançar, nesta faixa etária, índices de 15%. Um estudo conduzido na comunidade de Whickham, na Inglaterra, a prevalência de hipotireoidismo subclínico (SHT) foi de 6% a 7,5% no sexo feminino e 2,4% a 10 3% no sexo masculino. Mais recentemente, estudo realizado no Colorado, Estados Unidos, em 25.862 indivíduos, TSH sérico elevado foi encontrado em 9,5%, comprometendo 20% da população idosa (CANARIS et al., 2000). A progressão do SHT depende da causa e do grau de dano da função tireoidiana. Quando a causa do SHT é tireoidite de Hashimoto, a progressão é mais rápida, isto porque, nestas condições, o dano autoimune para a glândula tiroide parece ser um processo contínuo. Anticorpo antitiroglobulina (antiTg) e, principalmente, o anticorpo antiperoxidase tireoidiana (anti-TPO), são marcadores úteis de progressão para hipotireoidismo clínico (ROSENTHAL MJ, JAMA, 1987). As causas desencadeantes do SHT são as mesmas do hipotireoidismo clínico. As doenças autoimunes são as causas mais frequentes e responsáveis por mais de 50% dos casos (TUNBRIDGE et al., 1981). A reposição inadequada para o tratamento do hipotireoidismo clínico é outra causa de TSH sérico elevado e, algumas vezes, a inadequação da dose é decorrente da diminuição da absorção intestinal de levotiroxina (TUNBRIDGE et al., 1981). A hipercolesterolemia ocorre concomitantemente com o hipotireoidismo clínico, de moderado a severo, sendo um fator de risco para o desenvolvimento da doença arterial coronariana. Elevação na concentração sérica de colesterol total (CT) é provocada, principalmente, por um aumento na lipoproteína de baixa densidade (LDL-c) do colesterol, refletindo uma diminuição no clearance do LDL-c mais do que um aumento na sua produção. A diminuição na atividade da lipase lipoproteica produz pequeno aumento dos triglicérides. Alterações dos valores da lipoproteína de alta densidade (HDL-c) do colesterol são menos aparentes e menos consistentes (ALTHAUS et al., 1988). No SHT, as concentrações de CT e do LDL-c estão, dentro dos valores da normalidade, somente aumentando no hipotireoidismo clínico. Entretanto, em alguns estudos, os valores de LDL-c estavam aumentados, enquanto que os valores de HDL-c estavam diminuídos. Outros efeitos periféricos podem ser observados no SHT, tais como encurtamento do tempo de reflexo aquíleo e elevação sérica da concentração de mioglobulina (ROMALDINI et al., 1996). 11 TIREOIDITE DE HASHIMOTO O médico, Hakaru Hashimoto, descreveu pela primeira vez em 1912, a tireoidite linfocítica crônica. A tireoidite linfocítica é um infiltrado de T células e, possivelmente, células B. A doença ocorre secundária a anticorpos peroxidase/tiroglobulina ou ambos. Histologicamente, ela começa com raros centros germinativos que se transformam em vários centros germinativos maduros. Esta é também a razão pela qual estes pacientes têm um risco aumentado de linfomas, geralmente linfoma não-Hodgkin (KAPTEIN EL, 1996; KATZ, 1975). A apresentação típica de um paciente com doença de Hashimoto são mulheres jovens ou de meia-idade com um bócio firme, difuso bilateral. Como é uma doença auto-imune, é muito mais comum em mulheres e, muitas vezes associada a outras doenças auto-imunes. Também tem uma história familiar positiva e componentes genéticos (HLA-DR5 e CTLA-4). Alguns dos sintomas são: ganho de peso, depressão, transtorno bipolar, sensibilidade ao frio, fadiga, bradicardia, infertilidade, menorragia, fraqueza muscular e perda de cabelo (O INST. DA TIREOIDE, 2011). É importante confirmar o diagnóstico com exames laboratoriais. Em primeiro lugar, pedir um TSH, T4 livre e T3. Normalmente os níveis de TSH estarão altos. Após a confirmação do diagnóstico, o tratamento consiste em levotiroxina e a monitorização frequente da tireoide pelo exame físico. Além disso, um PAAF é frequentemente recomendado quando há presença de bócio. Uma ultrassom também é recomendada se um nódulo for percebido (O INST. DA TIREOIDE, 2011). O Instituto da Tiroide (2011) informa que iodo em excesso na alimentação, uso de medicação com iodo, aplicação repetida de contrastes radiológicos, podem fazer aparecer essa doença. Além desses fatores, o uso médico de remédios como, por exemplo, o Interferon, “pode levar a maior agressividade do sistema imunitário e desencadear Tireoidite de Hashimoto” (INST. DA TIROIDE, 2011). 12 HIPERTIREOIDISMO Este é um distúrbio mais comum em mulheres com idades entre 20 e 40 anos, conforme ensina Diehl, (2011). Os portadores desse distúrbio têm aumento na dosagem de T3 e T4 e diminuição do TSH. Os principais sintomas do hipertireoidismo, comumente, são fraqueza muscular; tremores nas mãos; taquicardia; fadiga e cansaço fácil; perda de peso importante, mesmo alimentando-se de forma normal; fome excessiva; diarreia ou aumento do número de evacuações; irritabilidade, agitação, ansiedade; insônia; problemas nos olhos (irritação, ardência ou dificuldades para enxergar); irregularidade menstrual; suor excessivo e sensação de calor exagerado; infertilidade (DIEHL, 2011). O médico Roberto Graves, afirma que também são causas de hipertireoidismo alguns nódulos da glândula, bócio multinodular, uma doença que acontece em pessoas mais idosas, geralmente com tireoides aumentadas há muitos anos; tireoidite subaguda, que é a inflamação dolorosa da tireoide, devido a uma infecção viral que destrói parte da tireoide e lança no sangue o hormônio que estava armazenado dentro da glândula; tireoidite linfocítica e tireoidite pós-parto (tipos de inflamação indolor da tireoide que podem levar a uma descarga de hormônios tireoidianos no sangue e a um hipertireoidismo de curta duração) e a ingestão de hormônio tireoidiano em excesso, para tratamento de hipotireoidismo ou como componente de outras medicações (por exemplo, “fórmulas” para emagrecer) (CAMARGO, 2011). Esse distúrbio pode ser tratado com medicamentos os antitireoidianos destinados a fazer com que diminua a produção hormonal da tireoide e os betabloqueadores, drogas destinadas não ao bloqueio da produção de hormônios tireoidianos, mas, sim, ao controle das manifestações como os batimentos cardíacos acelerados, os tremores, a ansiedade e o calor excessivo. Alguns casos, no entanto, requerem tratamento definitivo, como a cirurgia para remoção de parte ou toda a glândula, e o iodo radioativo (DIEHL, 2011). 13 DOENÇA DE GRAVES O hipertireoidismo da Doença de Graves é caracterizado imunologicamente por infiltração linfocitária da glândula tireoide e por ativação do sistema imune com elevação dos linfócitos T circulantes, aparecimento de autoanticorpos que se ligam ao receptor do TSH (TRAb) e que estimulam o crescimento e a função glandular (ANDRADE VA, 2001). As razões do desencadeamento deste processo auto-imune ainda não estão completamente entendidas, mas estão possivelmente envolvidos fatores como susceptibilidade genética, fatores constitucionais (hormônios sexuais e alterações da função imunológica) e fatores ambientais (estresse, ingestão de iodo e a ação dos agentes infecciosos). Do ponto de vista clínico, o hipertireoidismo da Doença de Graves caracteriza-se por aumento difuso e hiperatividade da glândula tireoide, associada ou não a oftalmopatia infiltrativa e, mais raramente, ao mixedema localizado (ANDRADE VA, 2001). O tratamento envolve o uso de beta-bloqueadores para combater a hiperatividade autonômica e à utilização de propiltiouracilo (PTU) ou Methimazole para diminuir a quantidade de hormônios liberados pela tireoide. PTU é preferido, pois não só funciona para diminuir a liberação do hormônio, mas também impede a conversão periférica de T4 para T3. O tratamento definitivo envolve a utilização de iodo radioativo terapia (RAI) ou tireoidectomia. RAI é claramente menos invasiva, mas demora meses para ter um efeito completo (DAMIANI D, 2007). IODO RADIOATIVO O iodo radioativo foi empregado pela primeira vez em 1941 no Massachussets General Hospital, quando Hertz e Roberts trataram pacientes com hipertireoidismo. Esta forma de tratamento já vem sendo utilizada há aproximadamente 60 anos sendo considerado de fácil administração, efeito rápido e de baixo custo (WARD et al., 1986). O tratamento com Iodo radioativo produz uma tireoidite intensa secundária à radiação, seguida por progressiva fibrose intersticial e atrofia glandular, resultando em destruição da capacidade de síntese da glândula 14 tireoide. Além disso, o tratamento com iodo radioativo pode induzir a alterações de resposta imune aos antígenos tireoidianos, descritas como inicial e tardia. Inicialmente, ocorre morte das células tireoidianas e liberação de antígenos na circulação, associada com elevação das imunoglobulinas e na imunoreatividade celular contra o receptor do TSH. Posteriormente, pode ocorrer ablação de todo o tecido tireoidiano e a consequente ausência de antígenos tireoidianos levaria à redução da autoimunidade (DEGROOT L.J, 1997). Em estudo comparativo entre custo de tratamento com drogas antitireoidianas, radioterapia com I131 ou cirurgia, demonstra que o tratamento com I131 apresenta menor custo, melhores índices custo/eficácia e custo/efetividade, tanto em pacientes privados como no sistema público. Apresenta como vantagem adicional à redução do volume glandular, dose dependente, observada no primeiro ano de tratamento (PETERS H; FISCHER C. et al., 1996). OBESIDADE De acordo com Ballone (2002), qualquer definição de obesidade é arbitrária dado que não existe um parâmetro que separe com precisão os indivíduos obesos dos não obesos. Este autor defende ainda que a obesidade possui duas dimensões: uma antropométrica/fisiopatológica e outra emocional/psicodinâmica. A primeira define como obeso aquele que possui uma percentagem de gordura corporal acima de um determinado critério. Nas mulheres, essa percentagem seria superior a 30% e nos homens a 25%. A dimensão psicodinâmica define como obeso aquele indivíduo que está insatisfeito com o seu próprio corpo, por ter o seu peso acima do ideal antropométrico. Borges, Guarisi, Giatti, e Bastos (2000) consideram que as definições de obesidade deveriam basear-se em critérios de saúde, sobretudo em estatísticas de morbilidade e mortalidade. Já segundo Lemos (2002), a obesidade pode ser definida como um excesso de gordura corporal que leva, com frequência, a uma perda significativa de saúde. A própria OMS consideraa uma doença por diminuir tanto a qualidade de vida como a esperança média 15 de vida dos indivíduos. A OMS (2002) refere que a obesidade pode ser definida de uma forma simples como uma condição de acumulação anormal ou excessiva de gordura no organismo, o que acarreta um comprometimento da saúde. No entanto, entre os indivíduos obesos, o grau de excesso de gordura, a sua associação, distribuição e consequências para a saúde variam de indivíduo para indivíduo. A obesidade é, deveras, uma situação grave, uma vez que traduz uma acumulação excessiva, mais ou menos generalizada, de tecido adiposo, induzindo um aumento de peso acima do valor considerado normal, numa fração superior a 25% (GUERREIRO, 2011). Também Czepielewski (2001) afirma que “a obesidade é uma enfermidade caracterizada pelo acúmulo excessivo de gordura corporal, associada a problemas de saúde”. Esta definição foi partilhada e defendida no Congresso de Obesidade, Nutrição e Alimentação onde se definiu esta patologia como uma doença em que o excesso de gordura corporal acumulada pode atingir graus capazes de afetar a saúde, tanto mais que, uma vez instalada, tende a autoperpetuar-se, constituindo-se como verdadeira doença crônica (CONEA, 2001). A obesidade é uma realidade que atinge todos os estratos etários da população, daí ser considerada como um dos maiores problemas de Saúde Pública. Lioret et al., (2001) afirmam que, a obesidade é particularmente preocupante nas crianças e nos adolescentes, pois estes estão em risco de se tornarem, também, adultos obesos. Segundo Wang, Monteiro e Popkin (2002) estima-se que 30% da população adulta esteja acima do peso normal, dos quais 6,8 milhões são obesos. Esta doença alcança níveis epidêmicos em vários países, como é o caso dos EUA em que 40% da população é obesa. Ainda nos EUA, morrem por ano cerca 300.000 pessoas direta ou indiretamente devido à obesidade. A prevalência da obesidade na população adulta dos países ocidentais varia entre os 20% e 50%, dependendo da região, sexo, idade e raça. Segundo dados do NHANES III, nos EUA, 63% dos homens e 55% das mulheres com idade superior a 25 anos, têm excesso de peso ou são obesos. (MUST A, SPADANO J et al., 1999). Mais é importante salientar que a percentagem de indivíduos obesos tem vindo a aumentar nas últimas décadas (STRAUSS et 16 al., 2001). Estudos epidemiológicos sugerem uma marcada variabilidade individual na susceptibilidade para a ocorrência de excesso de peso e de obesidade. Os fatores genéticos determinam a susceptibilidade dos indivíduos para o excesso de peso e para a obesidade quando expostos a determinados fatores ambientais (OMS, 2004). Assim, os valores do IMC podem ser influenciados de modo variável por fatores genéticos e ambientais. Separar o peso relativo de cada um destes fatores é uma tarefa complicada devido ao fato de os familiares partilharem uma herança genética, mas, simultaneamente, partilharem um conjunto de exposições de natureza ambiental (OMS, 2004). HORMÔNIOS TIREOIDIANOS Frente ao importante papel dos hormônios tireoidianos na regulação da termogênese, a dinâmica do eixo hipotálamo-hipófise-tireoidiano na obesidade já foi amplamente estudada. Quando se avalia a função tireoidiana no indivíduo obeso, devem-se considerar os efeitos do balanço energético atual, caso esteja submetido à dieta hipocalórica ou em plena hiperalimentação (ALVES RL, 2007). Vários estudos foram conduzidos com administração de hormônios tireoidianos em obesos com dieta restrita, na tentativa de reverter às alterações metabólicas que conduzem à redução da taxa metabólica basal (TMB). Diversos estudos utilizaram doses elevadas de T3, obtendo-se aumento do nível sérico de T3 e correlação negativa com o peso final (ALVES RL, 2007). Pacientes com hipotireoidismo pesam, em média, 15% a 30% mais que indivíduos eutireoidianos. Mesmo após terapia adequada, cerca de 7% ainda permanece acima do peso. Em estudo transversal, foi encontrada uma associação discreta entre hipotireoidismo subclínico e IMC em mulheres, mas uma associação em direção oposta em homens. Hipotireoidismo clínico ou subclínico parece não ser mais comum em obesos do que indivíduos de peso normal (ALVES RL, 2007). Apesar disto, numa casuística de 72 indivíduos com obesidade mórbida com indicação cirúrgica de derivação gastrojejunal, a incidência de hipotireoidismo subclínico foi de 25%, tendo o TSH normalizado um ano após a 17 cirurgia em todos os indivíduos. Pacientes hipotireóideos em reposição com levotiroxina apresentam variações na TMB quando se apresentam em eutireoidismo, hipertireoidismo leve ou hipotireoidismo. As implicações destas variações da TMB no IMC não estão definidas (IOSSA S; LIONETTI L, 2001). Estudos nos quais T4 foi administrado à pacientes com hipotireoidismo leve não mostraram mudança significativa de IMC em seguimento de até 6 meses. A leptina influencia a regulação central da função tireoidiana, através do estímulo hipotalâmico do TRH. No hipotireoidismo, os níveis de leptina são elevados, talvez como forma de contrapor ao acúmulo de lipídeos e energia na ausência de T3 (IOSSA S, LIONETTI L, 2001). O feedback negativo dos hormônios tireoidianos sobre a secreção de TSH é exercido de várias formas: bloqueio da produção de TRH ou redução da expressão de seus receptores de membrana no tireotrófico (REICHLIN, 1992; KAKUCSKA, 1992), estímulo da secreção de outras substâncias hipotalâmicas inibidoras do TSH, como a somatostatina (SCALON, 1991) e, a mais importante, inibição da secreção de TSH por ação direta de T3 no tireotrófico (SHUPNIK et al., 1986), sendo este proveniente principalmente da desiodação intra-hipofisária do T4 circulante. Além disso, existe um efeito inibitório indireto através da neuromedina B ou do GRP, que tem sua importância fisiológica comprovada através de estudos que utilizaram inibidores da ação destes peptídeos (MOURA et al., 2004). A maior parte dos hormônios tireoidianos circula acoplada a proteínas transportadoras, que são: a TBG (globulina ligadora de tiroxina), a TTR (transtirretina) e a albumina. No homem aproximadamente 70% de T3 e T4 estão ligados a TBG, 10% do T4 é ligado à TTR e 15% são carreados pela albumina. Enquanto uma pequena fração de T3 plasmático encontra-se ligado à TTR e cerca 25% à albumina (UTIGER, 1996). Os hormônios tireoidianos regulam a atividade de algumas enzimas importantes no transporte de lipoproteínas. A HMGCoA redutase tem sua síntese estimulada pelos hormônios tireoidianos. No hipertireoidismo não ocorre aumento do colesterol sérico porque o T3 também induz a degradação de LDL e Apo B, ao estimular a expressão dos receptores de LDL (DUNTAS, 2002). De modo geral, cerca de 10 a 25% dos obesos mostram algum grau de 18 hipotireoidismo. Isso é um índice maior do que a população geral, cuja incidência clínica fica entre 2% e 5%, sendo mais comum em mulheres. Essa diferença na prevalência já é por si só, um forte indicativo dessa relação. E parece haver mesmo uma explicação científica razoável que liga os obesos com o hipotireoidismo (JIN et al., 2004). Em uma das explicações possíveis, a leptina um hormônio produzido especialmente pelo tecido gorduroso e que, logicamente, costuma estar aumentada nos indivíduos obesos. A leptina, em concentrações acima do normal, pode interferir negativamente na capacidade da glândula tireoide de liberar os hormônios tireoidianos vitais na regulação do metabolismo do ser humano (JIN et al., 2004). Uma vez que a leptina se correlaciona com o grau de obesidade, quanto maior for o IMC (Índice de Massa Corpórea), maior a chance de desenvolvimento da doença, seja com claros sinais e sintomas (hipotireodismo clínico) ou não tão manifesta (hipotireoidismo subclínico). Diversos estudos têm mostrado a relação entre leptina e função tireoidea. A ação da leptina pode ocorrer em todo o eixo hipotálamo-hipófise-tireóide, assim como sobre a conversão de T3 a T4 (JIN et al., 2004). A leptina pode regular a função tireoidea direta e indiretamente. Foi demonstrado que a leptina estimula a secreção de TSH por estimular a expressão do gene do pró-TRH. Já foi evidenciada a de síntese local de leptina, sugerindo-se um efeito direto deste hormônio sobre a secreção de TSH (JIN et al., 2004). Ortiga-Carvalho (2002) mostrou que a leptina “in vivo” tem um efeito estimulatório sobre a liberação de TSH, enquanto que “in vitro” inibe a secreção de TSH, sugerindo uma inibição autócrina/parácrina local. A diminuição da leptina age como um mediador dessa adaptação do eixo hipotálamo-hipófisetireóide no jejum, pois o tratamento com leptina reduz a diminuição na tiroxinemia observada no jejum (AHIMA et al., 1996; ORBAN et al., 1998; NILLNI ET AL., 2000). Legradi et al., (1997) demonstraram que o RNAm para o pro-TRH, que diminui no jejum, é restaurado com a administração de leptina. Seoane et al., (2000) demonstraram haver um estímulo da leptina, na restauração da secreção de TSH, inibida pelo jejum. No jejum, o mecanismo de regulação da 19 secreção de SHT está alterado, de tal forma que os baixos níveis destes estão associados a uma resposta sub-normal de TRH e TSH (HERMUS et al., 1992). A redução da atividade do TSH e do eixo hipófise-tireóide, que ocorre durante o jejum, tem consequências dramáticas na concentração de leptina e subsequente diminuição de melanocortina, levando à redução da síntese do hormônio liberador da tirotrofina (TRH) e da sensibilidade do TSH. Têm sido encontrados níveis mais elevados de TSH em indivíduos obesos do que em magros. Entretanto, foi observado que o T3 era reduzido e o T4 e TSH não se alteravam em crianças obesas após seis semanas de dieta hipocalórica e, apenas o T3 era associado ao gasto energético de repouso (GER) (HERMUS et al., 1992). Em pacientes obesos, o hipotireoidismo subclínico (TSH ”4,38 µU/ml e T3 e T4 normais) afeta o GER, somente quando o TSH está claramente acima dos valores normais, e isto não muda a composição corporal e o perfil lipídico. A dosagem dos níveis de TSH em obesos pode ser útil para avaliar a piora do GER, em razão da diminuição dos efeitos periféricos dos hormônios da tireoide (WANG et al., 2002). O status nutricional pode influenciar a conversão periférica de T4 para T3, alterando esses valores entre anoréxicos, desnutridos, eutróficos e obesos. A perda de peso em indivíduos obesos está associada à redução do GER e dos níveis circulantes de T3, e por outro lado, o exercício intenso aumenta os níveis de hormônios da tireoide (WANG et al., 2002). QUIMIOLUMINESCÊNCIA Quimiluminescência é a produção de radiação luminosa eletromagnética por uma reação química. Quando esta radiação é emitida a partir de um sistema químico presente num organismo ou dele derivado, acaba sendo conhecida como biolumenescência (ALBERTIN, R.; 1998). O processo químico de quimiluminescência envolve a absorção, pelos reagentes, de energia suficiente para a geração de um complexo ativado, o qual se transforma em um produto eletronicamente excitado. Se esta espécie excitada for emissiva, produz a radiação diretamente, caso contrário, pode ocorrer à transferência de energia do estado excitado formado para uma 20 molécula aceptora apropriada, resultando na emissão indireta da radiação. (CORREA FE; ROSSI VA, 2002). As condições da reação tem um efeito significativo na quimiluminescência. O tempo de reação e uma duração da radiação emitida variam de períodos muito pequenos (menores que 1 s) até muitos longos (cerca de 1 dia). A mudança de parâmetros experimentais como forma de mistura dos reagentes, temperatura, concentrações de espécies reacionais ou interferentes, pH, podem modificar totalmente a emissão, podendo até mesmo extingui-la (CORREA FE; ROSSI VA, 2002). 21 REFERÊNCIAS BIBLIOGRÁFICAS AHIMA RS, PRABAKARAN D, MANTZOROS C, QU D, LOWELL B, MARATOS-FLIER E, FLIER SJ. Papel da leptina na resposta neuroendócrina ao jejum. Nature, v. 382, p.250-252, 1996 ALBERTIN, R.; ARRIBAS M. A. G.; BASTOS, E. L.; ROPKE, E.; SAKAI, P. N.; SANCHES, A. M. M.; STEVANI, C. V.; UMEZU.; Quim Nova 1998, 21, 772. ALTHAUS BU, STAUB JJ, RYFF-DE LÈCHE A, OBERHANSIL A, STAHELIN HB. LDL/HDL-changes in subclinical hypothyroidism: possible risk factors for coronary heart disease. Clin Endocrinol (Oxf) 1988; 28:157-63. ALVES RL; Eixos hormonais na obesidade: causa ou efeito? Arq Bras Endocrinol Metab vol.51 no1 São Paulo Feb. 2007 ANDRADE V.A; GROSS L. J; MAIA L. A. Tratamento do Hipertireoidismo da Doença de Graves. Arq Bras Endocrinol Metab vol.45 no6. São Paulo Dec. 2001 BALLONE, G. J.; ORTOLANI, I. V.; PEREIRA NETO, E. Da Emoção a Lesão. Um Guia de Medicina Psicossomática. São Paulo. Ed. Manole 2002 BARZEL EUA. Hipotireoidismo. Diagnóstico e tratamento. Geriatr Med. Clin. 1995,11 (2): 239-49. BLATT, JUCELENE MARCHI; LANDMANN, ZULEIKA MACHADO. Alterações das dosagens do hormônio tireoestimulante em pacientes atendidos em um laboratório escola. Revista Brasileira de Análises clínicas, vol. 39(3): 227230, 2007. BORGES, GUARISI, GIATTI, BORGES E BASTOS. Obesidade e Hipercolesterolemia na Adolescência. Publicado na Revista de Ginecologia & Obstetrícia, nº 2/2000 CAMARGO, R. Hipotireoidismo. 2011. Disponível <http://medicina.fm.usp.br/endoresidentes/roteiro/hipotireoidismo_rote. Acesso em: 25 abr. 2013. em: > CANARIS GJ, MANOWITZ NR, MAYOR G, RIDGWAY EC. The Colorado thyroid disease prevalence study. Arch Int Med 2000;160:526-634. CARMO I. Prevalência de obesidade na população portuguesa. Int J Obes 2000; 24 (suppl1): S19. CONEA (2001). Congresso de Obesidade, Nutrição E Alimentação alerta para o impacto da patologia em Portugal. Consultado em 27 de abril de 2013, disponível em saude.sapo.pt/gPN/293178.html. 22 CORREA FE.; ROSSI VA. A Quimiluminescência como ferramenta Analítica: Do Mecanismo a aplicações da reação do luminol em métodos cinéticos de analise. Quim. Nova Vol. 25, No. 6 1003-1011, 2002 CZEPIELEWSKI, M. (2001). Obesidade. Consultado em 24 de Abril de 2013, www.abcdasaude.com.br/artigo.php?303. DAMIANI D; Obesidade e doenças tireoidianas - mitos e realidades Pediatria (São Paulo) 2007; 29(2): 82-83 DEGROOT LJ. iodo radioativo e o sistema imunológico 1997: 7:259-63. DIEHL, Leandro A. Tireoide – Visão Geral. In Portal Endocrino. 2011; 142-127 Disponível em: <http://www.portalendocrino.com.br/tireoide_visaogeral.shtml.> Acesso em: 01 maio. 2013 DUARTE, G.C.; TOMIMORI E.K.; CAMARGO R.Y.A. ET AL. The prevalence of thyroid dysfunction in elderly cardiology patients with mild excessive iodine intake in the urban area of São Paulo. Clinics, vol. 64: 135- 142, 2009 DUNTAS L.H. Thyroid Disease and Lipids. Thyroid. New York, v.12, n.4, p. 287-293, 2002. EVERED DC, ORMSTON BJ, SMITH PA, HALL R, BIRD T. Grades of hypothyroidism. Br Med J 2002; 1: 657-62 FRANKLIN HL, KOZAK MJ, CASHMAN LA, et al. Tratamento cognitivocomportamental do transtorno obsessivo-compulsivo em crianças: An open clinical trial. J Am Acad Child Adolesc Psychiatry.1998;37:412–9 GRAF, Hans; CARVALHO, Gisah Amaral. Fatores Interferentes na Interpretação de Dosagens Laboratoriais no Diagnóstico de Hiper e Hipotireoidismo. In. Arq Bras Endocrinol Metab 2002; 46/1:51-64). GÜELL, R. Enfermedades del tiroides en niños y adolescentes. Barcelona, España: Permanyer. 1998. GUERREIRO, S. (2011). Emagrecer com conta, peso e medida. Medicina & Saúde, 43, 38-39 HERMUS RM, SWEEP CG, VAN DER MEER MJ, ROSS HA, SMALS AG, BENRAAD TJ, KLOPPENBERG PW. Continuous infusion of interleukin-1 beta induces a nonthyroidal illnes syndrome in the rat. Endocrinology, v.131, p.2139-46, 1992. INSTITUTO DA TIROIDE. Tireoidite de Hashimoto. 2011. Disponível em: <http://www.indatir.org.br/a_tiroide_tiroidite_hashimoto.htm.> Acesso em: 25 abr. 2013 23 IOSSA S, LIONETTI L,. Equilíbrio de gordura e concentração sérica de leptina em ratos normais, hipotireoidismo e hipertireoidismo. Int J Obes 2001; 25(3):417-25. JIN L, ZHANG S, BURGUERA BG, COUCE ME, OSAMURA RY, KULIG E, LLOYD RV. Leptin and leptin receptor expression in rat and mouse pituitary cells. Endocrinology, 141:333-339, 2004. KAKUCSKA I, RAND W, LECHAN RM. Thyrotropin-releasing hormone gene expression in the hypothalamic paraventricular nucleus is dependent upon feedback regulation by both triiodothyronine and thyroxine. Endocrinology. ; v. 130, p. 2845-50, 1992. KAPTEIN ELES. Metabolismo dos hormônios da tireoide e doenças da tireoide em insuficiência renal crônica. Endocr Rev. 1996; 17 (1); 45-63. KATZ AI, EMMANOUEL DS, LINDHEIMER MD. Hormônio da tireoide e dos rins. Nephron. 1975,15 (3-5): 223-49. KHAIRA JS, FRANKLYN JA. Condições de idosos. Praticante. 1999; 243 (1596): 214-8, 221. tireoide em pacientes LA FRANCHI, S. H. (1998). Triagem de distúrbios da tireoide em recémnascidos. In N. Lavin (Ed.), Manual of endocrinology and metabolism (pp. 393413). Boston: LEGRADI G, EMERSON CH, AHIMA RS, FLIER JS, LECHAN RM. Leptin prevents fasting-induced supresion of prothyrotropin-releasing hormone messsenger ribonucleic acid in neurons of the hypothalamic paraventricular nucleus. Endocrinology, 138:2569-2576, 1997. LEMOS, I. C. M. C. Influência da desnutrição intra-uterina na cicatrização da parede abdominal de ratos lactentes avaliada mediante estudo tensiométrico e da morfometria do colágeno. Curitiba, 2002, 89f. Tese (Doutorado) – Universidade Federal do Paraná. LIORET, S., VOLATIER, J; BASDEVANT, A; POUILLOT, R., MAFFRE, J; & MARTIN, A. Prevalência de obesidade infantil na França: INCA. Livro Nutrição e Dieta. 36, 405-410. 2001 MILHORANSA, P.; SOARES, R. Hormônio de estimulador da tireoide (TSH) e correlações laboratoriais. Revista Brasileira de Análises Clínicas, Rio de Janeiro, v. 41, n. 2, p. 161-164, 2009. MOURA, E.G; MOURA, C.C. Regulação da Síntese e Secreção de Tireotrofina. Arquivos Brasileiros de Endocrinologia e Metabologia, São Paulo, v.48, n.1, fevereiro. 2004. MURAHOVSCHI, J. (1994). Distúrbios do desenvolvimento. In Pediatria, diagnóstico e tratamento (pp. 119-122). São Paulo, SP: Sarvier. 24 MUST A, SPADANO J, COAKLEY EH, FIELD AE, COLDITZ G, DIETZ WH: The disease burden associated with overweight and obesity. JAMA 1999; 282 (16):1523-1529. NILLNI EA, VASLET C, HARRIS M, HOLLENBERG A, BJORBAEK C, FLIER JS. Leptin regulates prothyritropin-releasing hormone biosyntesis. J. Biol. Chem. v.275, p.36124-33, 2000. OMS - Organização Mundial de Saúde. Cuidados inovadores para condições crônicas: componentes estruturais de ação. Relatório mundial. Brasília, DF. 2002 ORBAN Z, BORNSTEIN SR, CHROUSOS GP. A interação entre a leptina e o eixo hipotálamo-hipófise-tireóide. Horm Metab Res. v.30, p.231-5, 1998. ORGANIZAÇÃO MUNDIAL DE SAÚDE. Obesidade: prevenindo e controlando a epidemia global. Relatório da Consultadoria da OMS, Genebra, (2004). ORTIGA-CARVALHO TM, OLIVEIRA KJ, SOARES B A, PAZOS-MOURA CC. O papel da leptina na regulação da secreção de TSH no estado alimentado: em estudos in vivo e in vitro. Jornal da Endocrinologia, 174:121–125, 2002. PETERS H, FISCHER C, BOGNER U, REINERS C, SCHLEUSENER H. redução do volume da tireoide após radioiodoterapia do hipertireoidismo de Graves: Resultados de um, estudo prospectivo, randomizado, multicêntrico Eur J Clin Invest 1996; 26:59-63. REHMAN SU; COPE DW, SENSENEY AD, distúrbios da tireoide em pacientes idosos. Sul Med. J. 2005; 98 (5): 543-9. REICHLIN S. Neuroendocrinologia. In Wilson, J.D. & Foster, D.W. eds., Williams Textbook of Endocrinology 8th ed. W.B. Saunders Company, Philadelphia, p.135-219, 1992. ROMALDINI J. H., SGARBI J. A., FARAH C. S. Disfunções Mínimas da Tiroide: Hipotireoidismo Subclínico e Hipertiroidismo Subclínico. Arq Bras Endocrinol Metab vol 48 nº 1 Fevereiro 2004. ROSENTHAL MJ, HUNT WC, GARRY PJ, GOODWIN JS. Thyroid failure in the elderly. Microsomal antibodies as discriminant for therapy. JAMA 1987; 258: 209-13. SAAD, Mario J. A.; MACIEL, Rui M. B.; MENDONÇA, Berenice B. Endocrinologia. 1ª Ed. São Paulo: Atheneu Editora, 2007. 1251 p. 25 SCALON MF. Controle neuroendócrino da secreção de TSH in: T Braverman, L.E. & Utiger, R.D., A Tireoide – A Fundamental and Clinical Text, 6a ed. J.B. Lippincott Co., Philadelfhia, v. 1,p . 230-256, 1991. SEOANE LM, CARRO E, TOVAR S, CASANUEVA FF, DIEGUEZ C. Regulamento in vivo da secreção de TSH pela leptina. v. 92, p.25-9, 2000. SETIAN, N. (2002). Hipotireoidismo congênito. In N. Setian (Ed.), Endocrinologia pediátrica. Aspectos físicos e metabólicos do recém-nascido ao adolescente (pp. 259-268). São Paulo, SP: Sarvier. SHUPNIK MA, ARDISSON LJ, MESKELL MJ, BORNSTEIN J, RIDGWAY EC. Triiodotironina (T3) regulação da transcrição do gene da subunidade TSH é proporcional à ocupação do receptor nuclear T3. Endocrinology, v. 118, p. 367-71, 1986 STRAUSS RS, POLLACK HA: Epidemic increase in childhood overweight, 2001. JAMA 2001; 286 (22):2845-48. TUNBRIDGE WM, BREWIS M, FRENCH JM, APPLETON D, BIRD T, CLARK F, ET AL. Natural history of autoimmune thyroiditis. Br Med J 1981;282:25862. UTIGER RD. The trioxide: physiology, hyperthyroidism, hypothyroidism, and the painful trioxide. In: Felig P, Baxter JD, Frohman LA. Endocrinology and Metabolism. 4.ed. New York, p. 435-519, 1996. WANG, Y; MONTEIRO, C. & POPKIN, B. Trends of obesity and underweight in older children and adolescents in the United States, Brazil, China, and Russia. American Journal of Clinical Nutrition, 75 (6), 971-977. 2002 WARD LS, FILHO AC, MENABÓ E, RIBEIRO SRR, LIMA MC, MACIEL RMB. Estudo da relação custo/efetividade no tratamento da doença de Basedow-Graves. Rev Ass Med Brasil 1986; 32:147-54. 26 Revista Brasileira de Ciências Farmacêuticas RBCF DETERMINAÇÃO DOS NÍVEIS SÉRICOS DE TRIIODOTIRONINA E TIROXINA LIVRE EM OBESOS NA CIDADE DE RENASCENÇA-PR MATIAS, P. Giovana1*; PEDER, D. Leyde2 MESQUITA, S. Claudinei2 1 2 Acadêmica do Curso de Farmácia, Faculdade Assis Gurgacz; Docentes do Curso do curso de Farmácia, Faculdade Assis Gurgacz. RESUMO Os hormônios tireoidianos são produzidos na glândula tireoide. A síntese e secreção dos hormônios tireoidianos é regulada pelo TSH através de um sistema de retroalimentação negativo que envolve o hipotálamo, hipófise e a glândula tireoide. As disfunções tireoidianas podem se apresentar de forma insidiosa e com manifestações clínicas sutis. Nestes casos, os testes laboratoriais são de extrema importância para o diagnóstico precoce. Assim, este trabalho tem por objetivo avaliar a dosagem dos níveis séricos de T3 e T4L em obesos para que possa auxiliar na prevenção, detecção e também no estadiamento do hipotireoidismo. Após a aprovação do projeto pelo Comitê de Ética e Pesquisa em Seres Humanos Institucional da Faculdade Assis Gurgacz, selecionou-se uma amostra constituída aleatoriamente por 40 voluntários, de ambos os sexos, com IMC acima de 30 kg/m², para a dosagem dos hormônios tireoidianos T3 e T4L. Nos resultados obtidos observou-se alteração nas dosagens de triiodotironina, em apenas 1 caso (2,5%), sendo este homem. Já a diminuição do hormônio tiroxina livre foi encontrada em 4 pacientes (10%), das quais estas eram mulheres. Este estudo apenas enfatizou os distúrbios relacionados ao T3 e T4L, sendo que para uma melhor avaliação das disfunções tireoidianas, seria a dosagem do TSH. UNITERMOS: hormônios tireoidianos, hipotireoidismo, obesidade. *Correspondência: Giovana Paola Matias, Curso de Farmácia, FAG – Faculdade Assis Gurgacz, Avenida das Torres, 500 – Loteamento FAG – 85806-096 – Cascavel – PR, Brasil. Email: [email protected]. 27 INTRODUÇÃO Os hormônios tireoidianos são produzidos na glândula tireoide em um processo que envolve o transporte ativo do iodo para dentro do folículo através do transportador transmembrana específico (NIS), sua oxidação e incorporação em resíduos tirosina na molécula de tireoglobulina. Esta iodinação de tirosinas resulta em resíduos monoiodinados (MIT) e diiodinados (DIT) que são enzimaticamente ligados para formar tiroxina (T4) e triiodotironina (T3). A tireoglobulina iodinada que contém MIT, DIT, T4 e T3 são armazenadas como polipeptídeo extracelular no colóide, próximo ao lúmen das células foliculares da tireoide. A liberação dos hormônios é feita através da endocitose e digestão lisossomal da tireoglobulina na célula folicular. Embora a tireoide produza referencialmente T4, o principal hormônio tireoidiano circulante, é o T3 a forma biologicamente ativa (YEN PM, 2001; FRIESEMA EC et al. 2005). A síntese e secreção dos hormônios tireoidianos é regulada pelo TSH através de um sistema de retroalimentação negativo que envolve o hipotálamo, hipófise e a glândula tireoide. O hormônio liberador de tireotrófica (TRH) é um hormônio secretado pelo hipotálamo e estimula os tireotrofos da hipófise a secretarem TSH (hormônio tireotrófico). Tanto a secreção do TRH quanto do TSH é regulada pelos níveis circulantes dos hormônios tireoidianos, secretados pela tireoide em resposta ao estímulo do TSH (YEN PM, 2001). A transformação metabólica do hormônio tireoidiano nos tecidos periféricos envolve uma série de reações enzimáticas complexas, dentre as quais a desiodação é o mecanismo para a ativação hormonal. As iodotironinas desiodases tipo 1 (D1) e tipo 2 (D2) catalisam esta reação. A iodotironina desiodase tipo I (D1) catalisa a desiodação tanto do anel fenólico quanto do anel tirosínico convertendo T4 a T3, T4 a rT3 e T3 e rT3 a T2, enquanto a desiodase tipo 2 (D2) atua exclusivamente no anel fenólico das iodotironinas, convertendo T4 a T3 e rT3 a T2 (LARSEN PR,1994). Quando os níveis de T4 circulantes estão ajustados às necessidades teciduais, este exerce uma retroalimentação negativa sobre a liberação de TSH. Os níveis plasmáticos médios de iodeto também exercem um controle importante sobre a função tireoidiana. Variações da ingestão de iodo em quantidades fisiológicas modulam sua captação pelas membranas das células 28 folicelulares tireoglobulina. Em doses farmacológicas, o iodo bloqueia a síntese de tireoglobulina, a liberação de T3 e T4 e o crescimento da tireoide (Efeito Wolff-Chaikoff) (CAMARGO, 2011). Em geral, a função tireoidiana está normal na obesidade. Valores normais de T4 e valores normais ou elevados de T3 são relatados, sendo à elevação de T3 provavelmente provocada pelo excesso de ingestão alimentar e não pelo estado de obesidade em si. Os valores basais de TSH são normais e a resposta ao TRH é imprevisível, podendo estar bloqueada, normal ou elevada (GUERREIRO, 2009). A dosagem dos níveis de TSH em obesos pode ser útil para avaliar a piora do gasto energético de repouso, em razão da diminuição dos efeitos periféricos dos hormônios da tireoide. O status nutricional pode influenciar a conversão periférica de T4 para T3, alterando esses valores entre anoréxicos, desnutridos, peso normal e obesidade (LOPES, 2002). A ingestão de alimentos e a atividade física modulam a termogênese basal, sendo que o jejum pode reduzir em até 40% o gasto energético de repouso (GER). A perda de peso em indivíduos obesos está associada à redução do GER e dos níveis circulantes de T3, e por outro lado, o exercício intenso aumenta os níveis de hormônios da tireoide. Uma restrição limitada da ingestão de alimentos que leve à perda de apenas 10% do peso corporal, está associada à redução do GER, mecanismo este contraproducente e que está associado ao chamado efeito ioiô da dieta (LOPES, 2002). O diagnóstico de hipotireoidismo é especialmente importante quando é feito durante a gestação, pois a falta de hormônios tireoidianos pode afetar profundamente o desenvolvimento do bebê, provocando retardo mental e atraso do crescimento. No entanto, esses problemas para o bebê são prevenidos pelo tratamento precoce da mãe com a reposição de hormônio tireoidiano (DIEHL 2011). As disfunções tireoidianas podem se apresentar de forma insidiosa e com manifestações clínicas sutis. Nestes casos, os testes laboratoriais são de extrema importância para o diagnóstico precoce (YEN PM, 2001). Assim, este trabalho tem por objetivo avaliar a dosagem dos níveis séricos de T3 e T4 livre em obesos para que possa auxiliar na prevenção, detecção e também no estadiamento do hipotireoidismo. 29 MATERIAIS E MÉTODOS A presente pesquisa é de caráter descritivo e exploratório. Após a aprovação do projeto pelo Comitê de Ética e Pesquisa em Seres Humanos Institucional da Faculdade Assis Gurgacz (parecer no 233/2013), o termo de consentimento livre e esclarecido foi assinado pelos voluntários. Uma amostra constituída aleatoriamente por 40 voluntários, de ambos os sexos, com IMC acima de 30 kg/m², usuários do Sistema Único de Saúde, foi selecionado na cidade de Renascença-PR. As amostras foram obtidas através da coleta de sangue em tubo de gel separador, o material foi centrifugado por cinco minutos a 3000 rpm para a obtenção do soro, e encaminhado ao laboratório particular na cidade de Cascavel - PR, para a dosagem dos hormônios T3 e T4 livre, através de técnica de quimioluminescência (Unissel DxI 800 da Beckman Coulter). Os valores de referência utilizados para T3 estão entre 0,9 a 2,4 ng/mL e para T4L, entre 0,7 a 1,8 ng/dL, para indivíduos adultos. Os resultados obtidos foram tabulados no Microsoft Excel e transformados em gráficos e tabelas. RESULTADOS E DISCUSSÃO A população do estudo consistiu de 40 pacientes, destes 32 eram mulheres (80%), sendo a idade média de 55 anos, variando entre 31 a 83 anos, com um IMC médio de 32,30 kg/m². A população masculina era constituída por 8 homens (20%), com uma idade média de 64 anos variando entre 56 a 82 anos e um IMC médio de 31,46 kg/m². Observou-se alteração nas dosagens de triiodotironina, em apenas 1 caso (2,5%), sendo este homem. Já a diminuição do hormônio tiroxina livre foi encontrada em 4 pacientes (10%), das quais estas eram mulheres. Ao que se refere à diminuição hormonal de T3, este apresentou uma concentração sérica de 0,7 ng/mL abaixo do limite inferior. Resultados apresentados na figura 1. 30 2,50% T3 Normal 97,50% T3 Diminuído Figura 1: Porcentagem de pacientes com T3 diminuído. Com relação aos pacientes que se submeteram as dosagens do hormônio triiodotironina (T3) observou-se na figura 1, uma porcentagem de 97,5% de T3 normal, e apenas 2,5% de T3 diminuído, sem haver alteração no hormônio, tiroxina livre (T4L). Estas alterações podem ocorrer em situações especiais como, recémnascidos, idosos com inanição, doença de graves, usuários de amiodarona. O que se observa é a transformação do T3 em T3 reverso, níveis normais de TSH e baixa de T3. Isso também é muito comum na Síndrome do Eutiroidiano. (CAMPOS, 2003). Em algumas situações, como inanição, por exemplo, as alterações podem significar uma tentativa de o organismo poupar gasto energético, numa situação de carência (GOICHOT, 1998). Em termos de definição, frequentemente há referência à diminuição do T3, aumento do T3 reverso (T3r), uma forma metabolicamente inativa do hormônio tireoidiano, com ou sem redução de T4, TSH normal ou baixo, em pacientes criticamente enfermos (VASA, 2001; UMPIERREZ 2002; BURMAN, 2001). Nos resultados obtidos para os níveis séricos de tiroxina livre, foi possível observar na figura 2, que 13% da população em estudo, apresentaram uma diminuição do T4 livre. E 88% apresentaram T4 livre normal. 31 13% T4L Normal T4L Diminuído 88% Figura 2: Porcentagem de pacientes com T4 Livre diminuído. A dosagem do T4 livre sanguíneo é o exame que nos dá realmente a noção de quanto hormônio tireoidiano potencialmente útil há na circulação. Se houver muito T4 livre circulante, haverá muita produção de T3 nos órgãos, levando ao hipertireoidismo. Se houver pouco T4 livre circulante, haverá falta de T3 para os tecidos, provocando o hipotireoidismo. Na prática clínica, a dosagem de T4 livre acaba sendo, na maioria dos casos, mais útil que a dosagem de T3 ou T3 livre (EVERED DC, et al., 2002). Em um estudo realizado por Teixeira SF, et al., (2006), observaram-se, por regressão linear, que o T4L diminuiu com a progressão da idade, porém, em análise multivariada, essa associação correlacionou-se de forma dependente com o TSH. Brenta G. et al., (2013), determinaram isoladamente T4 livre em pacientes ambulatoriais, a sensibilidade e especificidade do teste foram calculadas em 82% e 94%, respectivamente, aumentando a probabilidade de detecção da doença 22% no hipotireoidismo e para 60% no hipotireoidismo subclinico. A associação de TSH e T4 livre aumenta a precisão no diagnóstico de hipotireoidismo. A tireoide é uma das principais glândulas do sistema endócrino. Os hormônios tireoidianos (HTs) T3 e T4, atuam em quase todos os tecidos, com ações sobre o desenvolvimento, crescimento, manutenção da termogênese e metabolismo. A tireoide não é uma glândula autônoma, sendo a produção e a 32 secreção dos HTs reguladas pelo hormônio adeno-hipofisário, TSH. Este por sua vez é estimulado pelo neurohormônio hipotalâmico, TRH. Ambos TSH e TRH são controlados por um mecanismo de retroalimentação negativa exercido pelos HTs (BRENT, 1997). Segundo Santos (2004), as mulheres são afetadas pelo menos cinco vezes mais que os homens. O inicio dos sintomas manifesta-se com mais frequência na terceira e quarta década de vida, porém pode aparecer em qualquer idade. TABELA I. Pacientes que apresentaram alterações nas dosagens hormonais de T3 e T4L, por sexo e idade. IDADE (anos) 30 – 35 36 – 41 42 – 47 48 – 53 54 – 59 60 – 65 66 – 71 72 – 77 78 – 83 Total MULHERES T4L 2 1 1 4 HOMENS T3 - T4L - T3 1 1 Na tabela 1, pode-se observar a quantidade de homens e mulheres que apresentaram alterações nas dosagens dos níveis hormonais de T3 e T4L. Num intervalo de idade de 36 a 41 anos, duas mulheres apresentaram T4L diminuído, e de 42 a 47 anos e 66 a 71 anos duas apresentaram uma diminuição do T4L, totalizando 10% das mulheres, sem haver qualquer modificação na dosagem de T3. Para a população masculina, somente 1 homem (2,5%) na faixa de 66 a 71 anos, apresentou algum tipo de disfunção tireoidiana sendo essa, pela queda do hormônio T3. E tendo o T4L em normalidade. Em um estudo feito por Volpe R, (1993), que verificou a prevalência de disfunções tireoidianas e teve como resultados que de 2 a 4% dos indivíduos com mais de 65 anos de idade sofriam alguma disfunção na glândula da tireoide. Vários fatores estão envolvidos na gênese de disfunções tireoidianas, 33 entre os quais os mecanismos autoimunes, os fatores genéticos relacionados ao sistema HLA e os ambientais (VOLPÉ R, 1993). Fatores como, hora da coleta de sangue, ingestão de iodo e diferenças de sexo são bem aceitos como determinantes para os valores séricos de TSH hormônios tireoidianos. Enquanto, idade, fase do ciclo menstrual e fumo parecem influenciar os níveis séricos de TSH, T3 e T4 livres, mas os estudos não são conclusivos (LAURBERG et al., 2001; HANSEN et al., 2004). Estima-se que cerca de 200 milhões de pessoas em todo mundo sofram de algum tipo de doença da glândula da tireoide (MOREIRA TD, 2001). Em relação ao sexo, as disfunções tireoidianas afetam mais pacientes do sexo feminino em relação ao sexo masculino. Isto ocorre devido aos estrogênios aumentarem a concentração de Globulina ligante de Tiroxina (TBG) e assim elevam as concentrações séricas de T4 e T3 no soro, sendo que estes efeitos farmacológicos predominam durante a administração de contraceptivos ou outros usos terapêuticos como reposição hormonal após a menopausa e, também, durante a gravidez (MOREIRA TD, 2001). TABELA II: Média do índice de massa corporal (IMC), por sexo e idade, n=40. IDADE (anos) 30 – 35 36 – 41 42 – 47 48 – 53 54 – 59 60 – 65 66 – 71 72 – 77 78 – 83 Total IMC (ẍ) MULHERES 31,78 32,47 31,37 31,82 32,75 31,13 34,17 32,79 32,42 32,30 IMC (ẍ) HOMENS 31,31 31,68 31,41 31,46 Pode-se verificar na tabela 2 a média do índice de massa corporal, da população em estudo, por sexo e idade. Onde houve a diminuição dos HTs, vistos na tabela 1, verifica-se que os mesmos apresentaram IMC acima de 30 kg/m2. Frente ao importante papel dos HTs na regulação da termogênese, a relação entre obesidade e a dinâmica do eixo hipotálamo-hipófise-tireoidiano 34 tem sido amplamente estudada, mas os mecanismos envolvidos permanecem parcialmente compreendidos (LACOBELLIS et al., 2005). Disfunção da tireoide esta associada às alterações no peso corporal, temperatura do corpo, e repouso de energia independente da atividade física. Além disso, o ganho de peso, muitas vezes desenvolve-se após o tratamento da disfunção da tiroide. Tanto o hipotireoidismo subclínico e hipotireoidismo são frequentemente associados ao ganho de peso, diminuição da termogênese, e da taxa metabólica. (HOOGWERF BJ, et al., 1984). Os obesos exibiram valor para T3 e T4L dentro do limite de normalidade e/ou significativamente menor. Corroborando estes achados, Knudsen et al. (2005) analisaram amostra de mais de 4.000 indivíduos eutireoideos, e demonstraram que quanto maior o grau de obesidade maior o TSH e menor o T4L, enquanto que o T3 não se alterou. Sari et al., (2003) observaram que mulheres na pré-menopausa com IMC ≥ 30 kg/m² apresentaram maior TSH e menor hormônios tireoidianos livres, embora dentro da faixa de normalidade, quando comparadas a mulheres de mesma faixa etária e IMC entre 18,5 e 25 kg/m². Um estudo dinamarquês com 4.082 indivíduos eutireoideos mostrou que o IMC associa-se positivamente com os níveis de TSH e negativamente com o T4 livre, e que o ganho de peso em cinco anos apresenta correlação positiva com o aumento progressivo de TSH (KNUDSEN et al., 2005). Os estudos avaliando a função tireoidiana na obesidade são controversos. Resultados na literatura demonstram que as concentrações de TSH e HTs, podem apresentar-se aumentadas, diminuídos ou similares em obesos comparados a indivíduos eutróficos (KNUDSEN et al., 2005). CONCLUSÕES Obesidade e disfunção da tireoide são doenças comuns e, consequentemente, os clínicos devem estar particularmente atentos à possibilidade de disfunção tireoidiana em pacientes obesos. A prevalência de doenças tireoidianas em idosos é aproximadamente duas vezes maior do que indivíduos mais jovens, ocorrendo mais hipotireoidismo em relação ao hipertireoidismo, porém este estudo apenas 35 enfatizou os distúrbios relacionados ao T3 e T4L livre, sendo que para uma melhor avaliação da prevalência do hipotireoidismo na população em estudo seria a dosagem de outros parâmetros laboratoriais, como por exemplo, a dosagem do TSH. Utilizando os dados desse estudo, é conveniente recomendar aos pacientes que obtiveram alterações nos níveis hormonais de T3 e T4L, que procurem acompanhamento médico para a realização da dosagem do TSH, para complementar o estudo, sobre uma possível disfunção tireoidiana, como por exemplo, o hipotireoidismo. ABSTRATC Thyroid hormones are produced in the thyroid gland. The synthesis and secretion of thyroid hormones is regulated by TSH through a negative feedback system involving the hypothalamus, pituitary and thyroid gland. The thyroid dysfunction may present insidiously and subtle clinical manifestations. In these cases, laboratory tests are extremely important for early diagnosis. This study aims to evaluate the dosage of serum T3 and FT4 in obese so you can assist in the prevention, detection and also in the staging of hypothyroidism. After the project was approved by the Ethics and Human Research Institutional Faculty of Assisi Gurgacz, we selected a sample of 40 randomly by volunteers of both sexes, with a BMI above 30 kg / m², for the dose of hormones thyroid T3 and FT4. Results in an alteration in the dosage of triiodothyronine in only 1 case (2.5%), and this man. Already the reduction of free thyroxine hormone was found in 4 patients (10%), which these were women. This study only emphasized the disorders related to T3 and FT4, and for a better assessment of thyroid dysfunction, TSH would be. KEYWORDS: thyroid hormones, hypothyroidism, obesity. REFERÊNCIAS BIBLIOGRÁFICAS BRENT G. Hormônios da tireoide (T3 e T4) In: Conn P.M & Melmed S.Endocrinology, 1a ed., New Jersey, 19: 291-306,1997. BRENTA G. VAISMAN M, SGARBI J.A, BERGOGLIO L.M, ANDRADA N.C, BRAVO P, ORLANDI A.M, GRAF H. Diretrizes clínicas práticas para o manejo do hipotiroidismo. Arq Bras Endocrinol Metab. 2013; 57/4 BURMAN KD, WARTOFSKY L. A função da tireoide na unidade de cuidados intensivos. Critical Care Clin 2001; 17(1): 43-57. 36 CAMARGO, R. Hipotireoidismo. 2011. Disponível em: <http://medicina.fm.usp.br/endoresidentes/roteiro/hipotireoidismo_rote. > Acesso em: 25 abr. 2013. CAMPOS, S. Endocrinologia/Glândulas - Doenças mais comuns da glândula tireoide. Idelco Ltda. 2003 DIEHL, Leandro A. Tireoide – Visão Geral. In Portal Endócrino. 2011; 142-127 Disponível em: <http://www.portalendocrino.com.br/tireoide_visaogeral.shtml. > Acesso em: 13 de setembro de 2013. EVERED DC, ORMSTON BJ, SMITH PA, HALL R, BIRD T. Grades of hypothyroidism. Br Med J 2002; 1:657-62. FRIESEMA EC, JANSEN J, VISSER TJ. Thyroid hormone transporters. Biochem Soc Trans. 2005; 33:228-32. GOICHOT B, SAPIN R, SCHLIENGER JL. Síndrome do doente Eutireóideo: achados fisiopatológicos recentes. Rev Med Interne 1998; 19(9): 640-8. GUERREIRO, Natália. Abordagem da disfunção tiroideia subclínica. 2009. In Rev Port Clin Geral 2009;25h17min-82. HANSEN PS, HEGEDUS L. Grande influência genética na regulação do eixo hipófise-tireóide: um estudo de gêmeos dinamarqueses saudáveis. J Clin Endocrinol Metab 2004; 89: 1181–1187. HOOGWERF BJ, NUTTALL FQ. Regulação do peso a longo prazo no tratamento de hipertireoidismo e hipotireoidismo. Am J Med 76: 963 -970, 1984. KNUDSEN N, LAURBERG P, RASMUSSEN LB, BULOW I, PERRILD H, OVESEN L, JØRGENSEN T. Pequenas diferenças na função da tireoide podem ser importantes para Índice de Massa Corporal e a ocorrência de obesidade na população. J Clin Endocrinol Metab 2005; 90: 4019–4024. LACOBELLIS, G., M. C. RIBAUDO, ET AL. Prevalência de obesidade não complicada em uma população de italianos obesos. Obes Res, v.13, n.6, Jun, p.1116-22. 2005. LARSEN PR, BERRY MJ. Type I iodothyronine deiodinase: unexpected complexities in a simple deiodination reaction. Thyroid. 1994; 4:357-62. LAUBERG P, PEDERSEN IB, KNUDSEN N. Ingestão de iodo ambiental afeta a doença da tireoide não maligna. Tireoide 2001; 11:457–69 LOPES, Homero J. De Jesus. Função Tireoidiana. Principais Testes Laboratoriais e Aplicações Diagnósticas. 2002. 37 MOREIRA, TEMIS D. et al. A Incidência do hipotireoidismo correlacionado a alterações lipídicas e a importância da investigação laboratorial. Ano VII no 43 p. 128 e 130. São Paulo: Sky/Anima, 2001. SANTOS, Wesley P. Hormônios Tireoidianos. (2002). Disponível em: www.maringa saude.com. br. Acesso em 15 de outubro de 2013. SARI R, BALCI MK, ALTUNBAS H, KARAYALCIN U. The effect of body weight and weight loss on thyroid volume and function in obese women. Clin Endocrinol 2003; 59: 258– 262. TEIXEIRA SF, REUTERS SV, ALMEIDA PC, FERREIRA MM, WAGMAN BM, REIS AA, COSTA LJ, VAISMAN M. Avaliação clínica e de sintomas psiquiátricos no hipotireoidismo subclínico. Rev. Assoc. Med. Bras. vol.52 no.4 São Paulo July./Aug. 2006 UMPIERREZ GE. Síndrome do doente Eutireóideo. Southern Med J 2002; 95:506-13 VASA FR, MOLITCH ME. Problemas endócrinos nos pacientes cronicamente criticamente enfermos. Clin Chest Med 2001; 22(1):193-208 . VOLPÉ R. Tireoidite subaguda ou (De Quervain). A Tireoide Hoje 1993; 3:253 YEN PM. Physiological and molecular basis of thyroid hormone action. Physiol Rev. 2001; 81:1097-142. 38 NORMAS DA REVISTA CIENTÍFICA REVISTA BRASILEIRA DE CIÊNCIAS FARMACÊUTICAS/ BRAZILIAN JOURNAL OF PHARMACEUTICAL SCIENCES Forma de apresentação de manuscritos Estrutura: Cabeçalho: constituído por: Título do trabalho, que deve ser breve e indicativo da exata finalidade do trabalho; Autor(es) por extenso, indicando a(s) instituição(ões) a(s) qual(is) pertence(m) mediante números. O autor para correspondência deve ser identificado com asterisco, fornecendo o endereço completo, incluindo o eletrônico. Estas informações devem constar na margem esquerda do texto e logo após a filiação. Resumo: deve apresentar a condensação do conteúdo, expondo metodologia, resultados e conclusões, não excedendo 200 palavras. Unitermos: devem representar o conteúdo do artigo, evitando-se os de natureza genérica. Observar o limite máximo de 6 (seis) unitermos. Resumo em português: deve ser apresentado junto ao resumo em inglês e ser antecedido do título do artigo em português. O conteúdo deve e acompanhar o resumo em inglês. Unitermos em português: devem acompanhar os unitermos em inglês e estar abaixo do Resumo. Introdução: deve estabelecer com clareza o objetivo do trabalho e sua relação com outros trabalhos no mesmo campo. Extensas revisões de literatura devem ser substituídas por referências aos trabalhos bibliográficos mais recentes, nos quais tais revisões tenham sido apresentadas. 39 Material e Métodos: a descrição dos métodos usados deve ser breve, porém suficientemente clara para possibilitar a perfeita compreensão e repetição do trabalho. Processos e Técnicas já publicados, a menos que tenham sido extensamente modificados, devem ser apenas referidos por citação. Estudos em humanos e em animais devem, obrigatoriamente, fazer referência à aprovação do Comitê de Ética correspondente. Resultados e Discussão: deverão ser apresentados de forma concisa e em ordem lógica. Tabelas ou figuras, quando possível, devem substituir o texto, na apresentação dos dados. Sempre que pertinente, fornecer as faixas, desvios padrão e indicar as significâncias das diferenças entre os valores numéricos obtidos. A discussão deve se restringir ao significado dos dados obtidos e resultados alcançados, procurando, sempre que possível, relacionar sua significância em relação a trabalhos anteriores da área. Especulações que não encontram justificativa para os dados obtidos devem ser evitadas. É facultativa a apresentação desses itens em separado. Conclusões: quando pertinentes, devem ser fundamentadas no texto. Agradecimentos: devem constar de parágrafo à parte, antecedendo as referências bibliográficas, e ser compatíveis com as exigências de cortesia e divulgação. Referências bibliográficas: devem ser organizadas de acordo com as normas da Associação Brasileira de Normas Técnicas - ABNT NBR-6023, ordenadas alfabeticamente no fim do artigo incluindo os nomes de todos os autores. A exatidão das referências bibliográficas é de responsabilidade dos autores. Para exemplos, consultar o site www.bcq.usp.br. Apresentação dos originais: Os trabalhos devem ser apresentados em lauda padrão (de 30 a 36 linhas com espaço 1,5), utilizando o programa Word for Windows. Os trabalhos, acompanhados de carta de encaminhamento assinada por todos os autores, devem ser enviados, apenas por via eletrônica. 40 Informações Adicionais: Citação bibliográfica: As citações bibliográficas devem ser apresentadas no texto pelo(s) nome(s) do(s) autor(es), com apenas a inicial em maiúsculo, seguidas do ano de publicação. No caso de haver mais de três autores, citar o primeiro e acrescentar a expressão et al. Caso haja mais de uma citação com mesmos autores e mesmo ano de publicação, diferenciá-las com letras minúsculas junto ao ano. Ilustrações: As ilustrações (gráficos, tabelas, fórmulas químicas, equações, mapas, figuras, fotografias) devem ser incluídas no texto, o mais próximo possível das respectivas citações. Mapas, figuras e fotografias devem ser, também, apresentados em arquivos separados e digitalizadas em formato TIF ou JPG com resolução de 300 dpi. Cada fascículo da BJPS reproduzirá, na capa, figura escolhida de um dos trabalhos. As tabelas devem ser numeradas consecutivamente em algarismos romanos e as figuras em algarismos arábicos, seguidos do título. As palavras TABELA e FIGURA devem aparecer em maiúsculas apenas no título ou na legenda, respectivamente. Legendas e títulos devem acompanhá-las nos arquivos separados, assim como no texto. Nomenclatura: pesos, medidas, nomes de plantas, animais e substâncias químicas devem estar de acordo com as regras internacionais de nomenclatura. A grafia dos nomes de fármacos deve seguir, no caso de artigos nacionais, as Denominações Comuns Brasileiras (DCB) em vigor, podendo ser mencionados uma vez (entre parênteses, com inicial maiúscula) os registrados.
Baixar