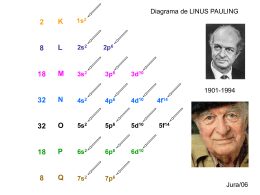
Resolução das atividades complementares Química 3 Q34 — Distribuição de íons p. 11 1 Forneça a configuração eletrônica 2 segundo o diagrama de Linus Pauling 2 dos íons a seguir no estado fundamental em ordem energética e em ordem geométrica. Ti21 b) Ânion iodeto: 127 I12 a) Cátion titanoso: 48 22 53 Resolução: Ti2 apresenta 20 elétrons a) O cátion 48 22 (2 a menos em relação ao átomo 22Ti). Átomo: 1s2 2s2 2p6 3s2 3p6 4s2 3d2 1s2 / 2s2 2p6 / 3s2 3p6 3d2 / 4s2 Cátion: 1s2 2s2 2p6 3s2 3p6 3d2 1s2 / 2s2 2p6 / 3s2 3p6 3d2 b) O ânion 127 I12 apresenta 54 elétrons 53 (1 a mais em relação ao átomo 53I). Átomo: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5 1s2 / 2s2 2p6 / 3s2 3p6 3d10 / 4s2 4p6 4d10 / 5s2 5p5 Ânion: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 1s2 / 2s2 2p6 / 3s2 3p6 3d10 / 4s2 4p6 4d10 / 5s2 5p6 2 (UFSC) Um determinado átomo apresenta sete (7) elétrons no subnível d da camada M. A respeito desses elétrons, é correto afirmar: 01. Todos os elétrons apresentam número quântico principal igual a 2. 02. O número quântico secundário para todos os elétrons é igual a 2. 04. Cinco desses sete elétrons apresentam o mesmo número quântico de spin. 08. O número quântico magnético do primeiro elétron “colocado” nesse subnível é 22. 16. Os números quânticos do sétimo elétron “colocado” nesse subnível d são: n 5 3, , 5 2, m, 5 0 e 1 ms 5 2 . 2 D D D F F Resolução: São corretos os itens: 02, 04 e 08 O item 01 é errado porque todos os 7 elétrons apresentam número quântico principal 3 (o que corresponde à camada M). O item 16 está errado porque, dada a configuração eletrônica do elemento, teremos: 1s2 2s2 2p6 3s2 3p6 4s2 3d7 3d7: 2 1 0 11 12 Números quânticos: n 3, 2, m 21 e s 5 1 . 2 Resposta: 14. 3 (Cefet-PR) O último elétron distribuído na configuração eletrônica de um átomo neutro, no estado 1 fundamental, possui o seguinte conjunto de números quânticos: n 5 4; , 5 1; m 5 11 e s 5 1 . 2 Sabendo-se que esse átomo possui número de massa igual a 84 e que, por convenção, o primeiro elétron a 1 ocupar um orbital possui número quântico de spin igual a 2 , o número de nêutrons existentes no núcleo 2 desse átomo é: 1) 48 3) 36 5) 33 2) 84 4) 45 F F F Resolução: Alternativa 1. Distribuição em orbitais do elétron mais energético: 4p6: 1 0 11 Logo, a configuração eletrônica do elemento será: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 Como para o átomo: p e2, então p 5 36. A p 1 n ⇒ n A 2 p ⇒ n 84 2 36 ⇒ n 5 48. 4 (Unisinos-RS) O elétron mais energético de um átomo apresenta os seguintes números quânticos: 1 n 5 3; , 5 1; m 5 21; s 5 2 . 2 Quantos elétrons há na eletrosfera desse átomo, convencionando que o primeiro elétron a entrar no orbital possui spin positivo? a) 4 c) 8 e) 16 b) 6 d) 10 F D D Resolução: Distribuição em orbitais do elétron mais energético: 3p4: 1 0 11 Logo, a configuração eletrônica do elemento será: 1s2 2s2 2p6 3s2 3p4 O átomo apresenta 16 elétrons. 5 (FEI-SP) A configuração eletrônica de um átomo neutro no estado fundamental é 1s2 2s2 2p6 3s2 3p5. O número de orbitais vazios remanescentes no nível principal M é: a) 0 c) 5 b) 1 d) 6 e) 10 Resolução: O número de orbitais vazios remanescentes pertence ao subnível 3d, que contém 5 orbitais. 6 (UFPel-RS) O ferro, 5626Fe, é um metal de transição branco-acinzentado, reativo, que forma ligas que apresentam aplicações importantes, entre elas o aço. Nos vários compostos químicos em que está presente, o ferro é encontrado em diferentes estados de oxidação, tais como Fe21 e Fe31. Com relação ao Fe, Fe21 e Fe31, são feitas as afirmativas a seguir. I. Os íons ferro II, Fe21, e ferro III, Fe31, são obtidos a partir do átomo de ferro, pela perda de 2 e 3 elétrons, respectivamente. II. O átomo de ferro, Fe, no seu estado fundamental, apresenta 6 elétrons no nível de valência. III. Os íons ferro II, Fe21, e ferro III, Fe31, apresentam 26 prótons, 30 nêutrons, mas diferem entre si pelo número de elétrons. IV. A configuração eletrônica do cátion Fe31 é 1s2 2s2 2p6 3s2 3p6 4s2 3d3. As afirmativas corretas são: a) apenas I e III; c) I, II e III; e) apenas I e IV. b) apenas I e II; d) apenas III e IV; Resolução: I. Verdadeira. II. Falsa. A distribuição eletrônica do 26Fe é: 1s2 2s2 2p6 3s2 3p6 4s2 3d6 III. Verdadeira. IV. Falsa. A distribuição eletrônica do 26Fe31 é: 1s2 2s2 2p6 3s2 3p6 3d5 7 (UFPR) O último elétron de um átomo neutro apresenta o seguinte conjunto de números quânticos: 1 n 5 4; , 5 1; m 5 0 e s 5 1 . 2 1 Convencionando que o primeiro elétron a ocupar um orbital possui número quântico de spin igual a 2 , 2 calcule o número atômico desse átomo. Resolução: n 5 4 ⇒ 4o nível de energia , 5 1 ⇒ subnível p m 5 0 ⇒ orbital central do subnível 4p s 5 11 ⇒ 2o elétron do orbital 2 último subnível preenchido: 4p5 ⇒ 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5 ⇒ Z 5 35. p. 12 8 (UGF-RJ) Leia o texto: No fim da década de 1970, um acidente na empresa Paraibuna de Metais resultou no despejo de mercúrio e cádmio no Rio Paraibuna. Campos, a cidade mais afetada, teve seu abastecimento de água suspenso por 72 horas. (O Globo, 1o de abril de 2003) Os íons dos metais citados são facilmente dissolvidos na água. O número de camadas utilizadas na distribuição eletrônica do cátion bivalente do cádmio é: Dado: número atômico do cádmio 5 48. a) 4 c) 6 e) 10 b) 5 d) 9 Resolução: Cd21: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 4d10 48 9 (UFRGS-RS) O íon monoatômico A22 apresenta a configuração eletrônica 3s2 3p6 para o último nível. O número atômico do elemento A é: a) 8 c) 14 b) 10 d) 16 Resolução: A22: 1s2 2s2 2p6 3s2 3p6 A: 1s2 2s2 2p6 3s2 3p4 ⇒ e) 18 Z 5 16. 10 (PUC-RJ) As respectivas distribuições eletrônicas do último nível das espécies químicas K, K11 e K21 só podem ser: Dado: K possui Z 5 19. a) 4s0; 4s1; 4s2 b) 4s1; 3s2 3p6; 3s2 3p5 c) 4s1; 4s2; 4s2 4p1 d) 4s2; 4s1; 4s2 4p6 e) 4s1; 4s2; 4s3 11 (UFPI) Indique a alternativa que apresenta um conjunto de números quânticos permitido. 1 a) n 5 3; , 5 0; m, 5 1; s 5 1 . 2 1 b) n 5 3; , 5 4; m, 5 1; s 5 1 . 2 1 c) n 5 3; , 5 3; m, 5 0; s 5 1 . 2 Resolução: a) Errada. , 5 0 b) Errada. n 5 3 c) Errada. n 5 3 d) Correta. e) Errada. n 5 4 Alternativa d. 1 d) n 5 3; , 5 2; m, 5 1; s 5 1 . 2 1 e) n 5 4; , 5 0; m, 5 3; s 5 2 . 2 ⇒ subnível s ⇒ m, não pode ser igual a 1. ⇒ nível 3; , 5 4 ⇒ subnível g ⇒ , não pode ser igual a 4. ⇒ nível 3; , 5 3 ⇒ subnível f ⇒ , não pode ser igual a 3. ⇒ nível 4; , 5 0 ⇒ subnível s ⇒ m, não pode ser igual a 3. 12 (UECE) Considere três átomos, A, B e C. Os átomos A e C são isótopos; os átomos B e C são isóbaros e os átomos A e B são isótonos. Sabendo que o átomo A tem 20 prótons e número de massa 41 e que o átomo C tem 22 nêutrons, os números quânticos do elétron mais energético do átomo B são: 1 1 a) n 5 3; , 5 0; m 5 12; s 5 2 . c) n 5 3; , 5 2; m 5 22; s 5 2 . 2 2 1 1 b) n 5 3; , 5 2; m 5 0; s 5 2 . d) n 5 3; , 5 2; m 5 21; s 5 1 . 2 2 Resolução: 41 A é isótopo de 20C, que apresenta 22 nêutrons. 20 Cálculo do número de massa para C: A p 1 n ⇒ A 20 1 22 ⇒ A 42 42 C é isóbaro de 42B e isótono de A. 20 Cálculo do número de nêutrons de A: A p 1 n ⇒ n A 2 p ⇒ n 41 2 20 ⇒ n 21 Cálculo do número de prótons de B: A p 1 n ⇒ p A 2 n ⇒ p 42 2 21 ⇒ p 21 Logo, B apresenta 21 prótons e configuração eletrônica: 1s2 2s2 2p6 3s2 3p6 4s2 3d1 e os números quânticos do elétron mais energético são: n 3, 2, m 22 e s 5 1 . 2 Alternativa c.
Baixar