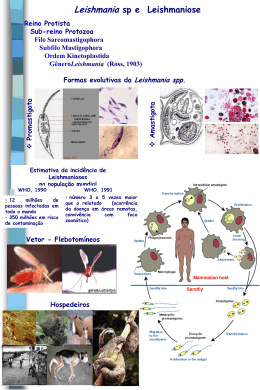
I UNIVERSIDADE FEDERAL DA BAHIA FACULDADE DE MEDICINA DA BAHIA Fundada em 18 de fevereiro de 1808 Monografia Avaliação da capacidade do immucillin-H em modular a resposta imune in vitro em indivíduos com leishmaniose cutânea Rafael de Castro da Silva Salvador (Bahia) 2014 II UFBA/SIBI/Bibliotheca Gonçalo Moniz: Memória da Saúde Brasileira Da Silva, Rafael de Castro S586 Avaliação da capacidade do immucillin-H em modular a resposta imune in vitro em indivíduos com leishmaniose cutânea / Rafael de Castro da Silva. Salvador: RC, da Silva, 2014. viii; 31 fls. : il. Professor orientador: Edgar Marcelino de Carvalho Filho. Anexos. Monografia como exigência parcial e obrigatória para Conclusão do Curso de Medicina da Faculdade de Medicina da Bahia (FMB) da Universidade Federal da Bahia (UFBA). 1 . Leishmaniose. 2. Células T. 3. Immucillin-H. I. Carvalho Filho, Edgar Marcelino de. II. Universidade Federal da Bahia. Faculdade de Medicina da Bahia. III. Título. CDU: 616.928.5 III UNIVERSIDADE FEDERAL DA BAHIA FACULDADE DE MEDICINA DA BAHIA Fundada em 18 de fevereiro de 1808 Monografia Avaliação da capacidade do immucillin-H em modular a resposta imune in vitro em indivíduos com leishmaniose cutânea Rafael de Castro da Silva Professor Orientador: Edgar Marcelino de Carvalho Filho Monografia de Conclusão do Componente Curricular MED-B60/2014.2, como pré-requisito obrigatório e parcial para conclusão do curso médico da Faculdade de Medicina da Bahia da Universidade Federal da Bahia, apresentada ao Colegiado do Curso de Graduação em Medicina Salvador (Bahia) 2014 IV Monografia: Avaliação da capacidade do immucillin-H em modular a resposta imune in vitro em indivíduos com leishmaniose cutânea, de Rafael de Castro da Silva Professor Orientador: Edgar Marcelino de Carvalho Filho COMISSÃO REVISORA: Edgar Marcelino de Carvalho Filho (Professor Orientador), professor do Departamento de Medicina Interna e Apoio Diagnóstico da Faculdade de Medicina da Bahia da Universidade Federal da Bahia. Régis de Albuquerque Campos, professor do Departamento de Medicina Interna e Apoio Diagnóstico da Faculdade de Medicina da Bahia da Universidade Federal da Bahia. Marcus Miranda Lessa, professor do Departamento de Cirurgia Experimental e Especialidades Cirúrgicas da Faculdade de Medicina da Bahia da Universidade Federal da Bahia. Nicolaus Albert Borges Schriefer, professor do Departamento de Biointeração do Instituto de Ciências da Saúde da Universidade Federal da Bahia. Lílian Silva Medina, doutoranda do Programa de Pós-Graduação em Ciências da Saúde (PPgCS) da Faculdade de Medicina da Bahia da Universidade Federal da Bahia. TERMO DE REGISTRO ACADÊMICO: Monografia avaliada pela Comissão Revisora, e julgada apta à apresentação pública no VIII Seminário Estudantil de Pesquisa da Faculdade de Medicina da Bahia/UFBA, com posterior homologação do conceito final pela coordenação do Núcleo de Formação Científica e de MED-B60 (Monografia IV). Salvador (Bahia), em ___ de _____________ de 2014. V “If I have seen further than others, it is by standing on the shoulders of giants” (Vivien Thomas) VI Aos meus pais, Geraldo Gomes da Silva e Vera Lúcia de Castro da Silva VII EQUIPE 1. Edgar Marcelino de Carvalho Filho, Faculdade de Medicina da Bahia/UFBA. [email protected]; 2. Natália Barbosa Carvalho, Complexo Hospitalar Universitário Professor Edgard Santos/UFBA. [email protected]; e 3. Nathália Araújo Lisbôa, acadêmica de medicina, Faculdade de Medicina da Bahia/UFBA. [email protected]. INSTITUIÇÕES PARTICIPANTES UNIVERSIDADE FEDERAL DA BAHIA 1. Faculdade de Medicina da Bahia (FMB) 2. Complexo Hospitalar Universitário Professor Edgard Santos (COM-HUPES) POSTO DE SÁUDE DE CORTE DE PEDRA FONTES DE FINANCIAMENTO 1. National Institute of Health 2. Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq); 3. Fundação de Amparo a Pesquisa do Estado da Bahia (FAPESB); 4. Programa Institucional de Bolsas de Iniciação Científica (PIBIC); e 5. Recursos próprios. VIII AGRADECIMENTOS Ao meu Professor orientador, Doutor Edgar Marcelino de Carvalho Filho, pela orientação, conselhos, disponibilidade e estímulos essenciais para o êxito deste trabalho e para o seguimento da minha vida profissional de futuro médico. À pós-doutoranda Natália Barbosa Carvalho, pela paciência em me instruir nos primeiros passos do manejo das técnicas laboratoriais usadas na execução deste trabalho, e pela constante assistência às dúvidas que por ventura surgiam. Aos Doutores Regis de Albuquerque Campos, Marcus Miranda Lessa, Nicolaus Albert Borges Schriefer, e à Doutoranda Lilian Silva Medina, membros da Comissão Revisora desta Monografia, sem os quais muito deixaria ter aprendido. Meus especiais agradecimentos pela constante disponibilidade. À minha colega, Nathália Araújo Lisbôa, pelo apoio constante e contribuição extensiva nas etapas de revisão bibliográfica e execução de experimentos. 1 SUMÁRIO ÍNDICE DE FIGURAS E TABELAS 02 I. RESUMO 03 II. OBJETIVOS 04 III. FUNDAMENTAÇÃO TEÓRICA 05 IV. METODOLOGIA IV.1. Desenho de estudo 09 IV.2. Local 09 IV.3. Participantes 09 IV.4. Definição de caso 09 IV.5. Metodologia IV.5.1. Separação e cultura de células mononucleares 09 IV.5.2. Determinação de citocinas 10 IV.6. Análise estatística 10 IV.7. Aspectos éticos 10 V. RESULTADOS 11 VI. DISCUSSÃO 16 VII. CONCLUSÕES 19 VIII. SUMMARY 20 IX. REFERÊNCIAS BIBLIOGRÁFICAS 21 X. ANEXOS ANEXO I: Termo de Consentimento Livre e Esclarecido 26 ANEXO II: Parecer Consubstanciado do CEP 29 2 ÍNDICE DE FIGURAS E TABELAS FIGURAS FIGURA 1. Teste de padronização da dose do immucillin-H. 12 IFN-γ em pg/mL. FIGURA 2. Dosagem de IFN-γ, em pg/mL, antes e após a adição 13 de immucillin-H às culturas de CMSPs estimuladas com 1 µg/mL de SLA. TABELAS TABELA 1. Dosagem de IFN-γ, em pg/mL, nos 8 pacientes com 12 leishmaniose cutânea estimulados com SLA 1µg/mL. TABELA 2. Dosagem de IFN-γ, em pg/mL, nos 5 pacientes com 13 leishmaniose cutânea estimulados com SLA 5µg/mL. TABELA 3. Dosagem de TNF-α, em pg/mL, nos 8 pacientes com 14 leishmaniose cutânea estimulados com SLA 1µg/mL. TABELA 4. Dosagem de TNF-α, em pg/mL, nos 5 pacientes com 14 leishmaniose cutânea estimulados com SLA 5µg/mL. TABELA 5. Dosagem de IL-10, em pg/mL, nos 8 pacientes com 15 leishmaniose cutânea estimulados com SLA 1µg/mL. TABELA 6. Dosagem de IL-10, em pg/mL, nos 5 pacientes com leishmaniose cutânea estimulados com SLA 5µg/mL. 15 3 I. RESUMO: FUNDAMENTAÇÃO TEÓRICA/JUSTIFICATIVA: A leishmaniose cutânea (LC), causada pela Leishmania braziliensis, tem grande prevalência na população brasileira. A doença se caracteriza pela presença de úlcera(s) bem delimitadas, com bordas elevadas. Do ponto de vista imunológico, existe uma ativação exagerada de células T contra antígenos do parasita, com produção de citocinas pró-inflamatórias, como IFN-γ e TNF-α. Esta resposta inflamatória não apropriadamente modulada se relaciona com o desenvolvimento da lesão tecidual. O immucillin-H é um inibidor da enzima purina nucleosídeo fosforilase (PNP) e reduz a ativação de células T e, neste contexto, poderá modular a resposta imune na leishmaniose tegumentar. OBJETIVO: Determinar a capacidade do immucillin-H de modular a exagerada resposta imune na LC. MÉTODOS: O estudo foi realizado no Serviço de Imunologia (SIM) do Complexo Hospitalar Universitário Professor Edgard Santos. Participaram do estudo oito pacientes diagnosticados através de uma reação de PCR positiva ou isolamento do parasito em cultura de material da lesão. Estes pacientes foram provenientes da área endêmica de Corte de Pedra, Município de Tancredo Neves, Bahia, local onde pesquisadores do SIM realizam atividades assistenciais e de pesquisa. Células mononucleares do sangue periférico foram estimuladas in vitro com phitohemaglutinina (PHA), antígeno solúvel de Leishmania (SLA) isoladamente ou associado ao immucillin-H. A produção de citocinas (IFN-γ, TNF-α e IL-10) foi avaliada pela técnica de ELISA em sobrenadante de cultura de células. A análise estatística foi feita através de técnicas não paramétricas, utilizando o teste de MannWhitney e teste pareado de Wilcoxon. RESULTADOS: O immucillin-H foi capaz de inibir de maneira relevante a produção de IFN-γ de amostras estimuladas com SLA. A inibição da produção de TNF-α e IL-10 não foi significativa. CONCLUSÃO: O immucillin-H foi capaz de reduzir a ativação de células T em indivíduos com leishmaniose cutânea. Palavras chaves: 1. Leishmaniose. 2. Células T. 3. Immucillin-H 4 II. OBJETIVOS PRINCIPAL Determinar a capacidade do immucillin-H de modular negativamente a resposta imune mediada por células em pacientes com leishmaniose cutânea. SECUNDÁRIOS 1. Avaliar a capacidade do immucillin-H em modular a resposta imune. 2. Avaliar a capacidade do immucillin-H em diminuir a produção de citocinas próinflamatórias em pacientes com leishmaniose cutânea. 5 III. FUNDAMENTAÇÃO TEÓRICA A leishmaniose cutânea é uma morbidade com ampla prevalência na população mundial. Sua incidência mundial alcança de 0.7 a 1.2 milhões de novos infectados a cada ano, com regiões endêmicas na América, Ásia Ocidental e bacia Mediterrânea, sendo o Brasil um dos países com a maior prevalência de casos (Alvar et al., 2012). A infecção mediada pela Leishmania braziliensis induz uma ativação exagerada de macrófagos e de células T específicas contra antígenos do parasita que se associa com o desenvolvimento da úlcera cutânea (Bittencourt AL, Barral A, 1991; Da-Cruz et al., 2002; Antonelli et al., 2005; Holzmuller et al., 2006; Bittar et al., 2007; Giudice et al., 2012). Embora a resposta mediada por células tenha papel importante na defesa contra protozoários, estudos têm mostrado que a depleção de células T CD4+ pode atenuar a patogênese de lesões nas infecções por Leishmania (Soong et al., 1997; Xin et al., 2007). Desse modo, infere-se que a busca de novos agentes imunomoduladores poderia trazer, além de maior esclarecimento a respeito da modulação da resposta imune nesta doença oportunidades terapêuticas para os portadores dessa morbidade, possibilitando o alcance de melhores prognósticos. A leishmaniose tegumentar Americana (LTA) é uma infecção parasitária em expansão, que ocorre desde o sul dos Estados Unidos até o norte da Argentina (Montenegro J, 1926; Grimaldi et al., 1989). No Brasil, são seis as espécies de protozoários do gênero Leishmania associadas à doença no homem (Marzochi MC, 1992; Gramiccia M, Gradoni L, 2005). A LTA apresenta diversas formas clínicas dependendo de variados fatores (Rogers et al., 2002) e a sua manifestação mais comum é a forma cutânea, causada principalmente pela L. braziliensis e caracterizada pelo desenvolvimento de única ou múltiplas lesões dérmicas ulceradas, bem delimitadas e com bordas elevadas (Furtado T, 1994). Além da leishmaniose cutânea e da leishmaniose mucosa que atinge principalmente a mucosa nasal, a L. braziliensis causa a leishmaniose cutânea disseminada, caracterizada por múltiplas lesões papulares, acneiformes e ulceradas, existindo também formas atípicas da doença (Guimarães et al., 2009; Queiroz et al., 2012). A Leishmania é um parasita intracelular obrigatório das células do sistema fagocítico mononuclear. O parasita possui um ciclo vital digenético, com um estado de 6 desenvolvimento extracelular no tubo digestivo do vetor, insetos flebotomíneos fêmeas, e um estágio de desenvolvimento em humanos, intracelular. No vetor, o protozoário se localiza no tubo digestivo em uma conformação flagelada e alongada, denominada promastigota. No intestino do flebotomíneo, o protozoário sofre um processo de metaciclogênese, transformando-se na forma infectante de promastigota metacíclica. A forma infectante é transmitida ao hospedeiro vertebrado através do repasto sanguíneo do flebótomo. Uma vez dentro do hospedeiro vertebrado, a Leishmania adere e penetra no macrófago, onde se transforma numa forma aflagelada, denominada amastigota (Da Silva R, Sacks DL, 1987; Robert MTM, 2006; Brasil, 2010; Mougneau et al., 2011). A resposta imunológica do hospedeiro à infecção por Leishmania é caracterizada pela expansão de linfócitos T CD4+ com um perfil de citocinas TH1 e TH2 (Da-Cruz et al., 2002; Holzmuller et al., 2006; Roberts MTM, 2006; Bittar et al., 2007). A resposta do tipo TH1 a princípio representa um bom prognóstico para leishmaniose cutânea, uma vez que citocinas como o IL-2, IL-12, IFN- e TNF- serão produzidas, ativando os macrófagos e, por consequência, levarão à destruição dos parasitos. Já a resposta do tipo TH2 culminaria na progressão da doença, uma vez que as células T produzirão IL-4 e IL10, que inibem a ativação dos macrófagos, a resposta TH1, e conseqüente destruição parasitária (Lohoff et al., 1998; Liew et al., 1999). Em estudo conduzido com camundongos C3H/He, constatou-se que é necessária uma ativação da resposta TH1 simultânea à uma reduzida ativação do perfil TH2 para gerar proteção contra a leishmaniose cutânea (Sjölander et al., 1998). Em 2007, Darrah et al. publicaram um estudo onde correlacionavam a proteção vacinal contra Leishmania major a um estabelecimento predominante de perfil TH1 em camundongos C57BL/6. O paradigma TH1/TH2, no entanto, não é totalmente claro em alguns casos quando aplicado ao ser humano. Por exemplo, nas infecções causadas pela L. braziliensis tanto a evolução da infecção para a doença como a gravidade da leishmaniose, avaliada pelo tamanho das úlceras ou pela forma clínica da doença, associam-se com maior ativação de células T CD4+ e produção exacerbada de citocinas pró-inflamatórias como o IFN- e TNF- (Sypek et al., 1993; Da-Cruz et al., 1994; Lohoff et al., 1998; Da-Cruz et al., 2002; Antonelli et al., 2005; Carvalho et al., 2007; Schnorr et al., 2012). Enquanto que em um outro estudo realizado com pacientes indianos, o perfil TH2, com produção aumentada de IL-4 e IL-10, foi correlacionado à falha terapêutica e sintomatologia na doença (Sundar et al., 1997). 7 Mais recentemente tem sido documentado que além das células T, macrófagos, através da produção de citocinas pró-inflamatórias de TNF-, também contribuem para a patologia na LTA (Giudice et al., 2012). Células T CD8+ também desempenham um papel importante no processo de controle da leishmaniose, seja através da produção de IFN- e ativação de macrófagos ou por um efeito citolítico das células T citotóxicas em macrófagos parasitados (Da-Cruz et al., 1994; Da-Cruz et al., 2002; Uzonna et al., 2004). Todavia, na infecção pela L. braziliensis, células T CD8+ tem também sido envolvidas na patogênese da leishmaniose cutânea tendo sido demonstrado uma associação de células T CD8+ expressando granzimas com o desenvolvimento da úlcera leishmaniótica e documentada a destruição de células do hospedeiro infectados por Leishmania (Faria et al., 2009). Dando apoio ao papel da célula CD8+ na patologia da LTA foi observado que a citotoxicidade mediada por células T contra macrófagos infectados por L. braziliensis era maior na leishmaniose mucosa, forma mais grave da doença, do que na leishmaniose cutânea (Santos et al., 2013). As drogas de primeira escolha para o tratamento da forma cutânea da LTA, há mais de 50 anos, são os antimoniais pentavalentes, apesar de outras drogas de segunda escolha serem usadas com sucesso variável (Sypek et al., 1993; Carvalho et al., 2007; Brasil, 2010; Oliveira et al., 2011). No Brasil, estudos têm demonstrado ineficácia terapêutica em até 70% dos pacientes (Mayrink et al., 2006; Okwor et al., 2012), além de sérios efeitos tóxicos e colaterais (Da-Cruz et al., 2002; Mayrink et al., 2006; Carvalho et al., 2007; Reis LC, 2007; Oliveira et al., 2011; Esfandiarpour et al., 2012; Okwor et al., 2012). Como a resposta imune participa da patogênese da leishmaniose cutânea e da leishmaniose mucosa causada pela L. braziliensis, e devido ao importante papel do TNF na gênese da úlcera leishmaniótica, estudos têm avaliado a eficácia da associação da pentoxifilina, droga inibidora do TNF-, associado ao antimonial no tratamento da LTA. Estes dados têm mostrado que a associação do antimonial com a pentoxifilina é mais eficaz do que o uso do antimonial isoladamente, acelera a cicatrização da lesão e é eficaz no tratamento de pacientes com leishmaniose cutânea e mucosa refretários ao antimonial (Sadeghian G, Nilforoushzadeh MA, 2006; Lessa et al., 2011). Estes dados demonstram que a associação de uma droga leishmanicida com um agente imunomodulador pode contribuir para um maior sucesso no tratamento da LTA. 8 Atualmente a busca de novas drogas imunomoduladoras se faz necessária para que o tratamento da LTA seja aprimorado. Neste cenário, inibidores de PNP podem representar uma nova classe de agentes imunossupressores a ser utilizada em pacientes portadores de patologias que acometem a proliferação de linfócitos T, como na psoríase (Morris PE, Omura GA, 2000), na leucemia linfocítica crônica (Korycha et al., 2007) e na leishmaniose cutânea. A atividade das células T está fortemente ligada à atividade do PNP, de tal forma que esta enzima se mostra essencial para a manutenção da função linfocitária, bem como atua como elemento primordial para o sucesso replicativo (Bzowksa et al., 2000). É conhecido que indivíduos que apresentam deficiência genética desta enzima tem uma depleção de linfócitos T (Giblett et al., 1975). A PNP atua na catálise fosforilativa reversível de nucleosídeos de purina, levando à produção de suas respectivas bases e de uma pentose fosfatada (Giblett et al., 1975). Dessa forma, esta reação se torna uma via importante de reciclagem de purinas, possibilitando – por exemplo - a síntese de compostos essenciais a processos proliferativos, além de evitar o gasto energético dispendioso de uma síntese de novo de purina (Bantia S, Kilpatrick JM, 2004). De fato, é notório que as células que exibem altos níveis de atividade de PNP são particularmente dependentes desta enzima para sobreviverem (Bantia et al., 2001). Fato que se confirma com a deficiência desta enzima em crianças, o que acarreta deficiência de linfócitos T em seus organismos (Giblett et al., 1975). O immucillin-H (BCX-1777) tem se revelado como o inibidor mais potente, até então conhecido, da enzima PNP, tendo eficácia de 10 a 100 vezes maior que qualquer outro inibidor de PNP (Bantia et al., 2001). Seu efeito modulador é secundário a uma sequência de alterações que culminam com a inibição da síntese de DNA e, portanto, proliferação celular (Galmarini CM, 2006). Em estudo publicado em 2012 por Deves et al., o immucillin-H foi capaz de deter a perda óssea mediada por células T CD4+ em doença periodontal induzida em ratos Wistar, sem efeito direto sobre os osteoclastos. Em outro estudo, de fase I, publicado em 2012 por Ogura et al., o immucillin-H exibiu controle total ou parcial de doenças malignas de células T periféricas recidivantes ou refratárias a outras terapias, demonstrando boa tolerância e segurança. Portanto, o estudo desta droga pode trazer resultados positivos e desejáveis para o maior esclarecimento da modulação de patologias linfoproliferativas e inflamatórias, bem como do seu papel em atenuar a resposta imune de pacientes com LTA. 9 IV. METODOLOGIA IV.1 Desenho do Estudo: Estudo de corte transversal com o objetivo de avaliar a modulação exercida pelo Immucillin-H na resposta imune in vitro em células mononucleares de pacientes com leishmaniose cutânea em Salvador, Bahia. IV.2 Local: O estudo foi realizado no Serviço de Imunologia (SIM) do Hospital Universitário Professor Edgard Santos, 5º andar. IV.3 Participantes: Participaram deste estudo oito pacientes com leishmaniose cutânea acompanhados no Posto de Saúde de Corte de Pedra, município de Tancredo Neves, Bahia. O Posto de Saúde de Corte de Pedra foi criado em 1986 e desde então pesquisadores do SIM desenvolvem atividades assistenciais e de pesquisa nessa importante área endêmica de transmissão de L. braziliensis. Cerca de 2000 novos casos de LTA são vistos anualmente neste posto de saúde gerido pelo SIM da Faculdade de Medicina da Universidade Federal da Bahia. IV.4 Definição de caso: Pacientes com leishmaniose cutânea: Indivíduos de ambos os sexos com lesão típica de leishmaniose cutânea com duração da doença entre 15 e 90 dias e com diagnóstico confirmado pelo isolamento do parasita ou PCR. IV.5 Metodologia: Avaliação do efeito do immucillin-H na resposta imune de células mononucleares de pacientes com leishmaniose cutânea. IV.5.1 Separação e cultura de células mononucleares. Sangue total heparinizado (30 mL) foi colhido para obtenção das células mononucleares. As células mononucleares do sangue periférico (CMSP) foram isoladas através de um gradiente de densidade utilizando o meio de separação de linfócitos (FicollHypaque). Após centrifugação a 400 g, as células da interface foram lavadas com salina 10 estéril e ajustadas para a concentração desejada na dependência do ensaio utilizado. CMSP foram cultivadas em placas de 24 poços e mantidas em meio RPMI 1640 suplementado com 5% de soro fetal bovino e com adição de penicilina/estreptomicina. As células foram mantidas sem estímulo ou estimuladas com fitohemaglutinina (Phytohemagglutnin – PHA) e antígeno solúvel de leishmania (soluble Leishmania antigens – SLA). Posteriormente, estas culturas foram incubadas a 37ºC em 5% de CO2 por 72 horas. Os sobrenadantes foram coletados e estocados a -20ºC até a dosagem de citocinas e avaliação por meio de curva dose-resposta. IV.5.2 Determinação de citocinas. A concentração das citocinas IFN-γ, TNF- e IL-10 foram determinadas no sobrenadante de culturas de CMSP por meio do método de ELISA sandwich. Foram utilizados reagentes comercialmente disponíveis (Pharmigen, San Diego, CA, USA). IV.6 Análise Estatística Considerando que os resultados não obedecem uma curva normal, a análise estatística foi feita por testes não paramétricos. A comparação das medianas foi realizada pelo teste de Mann-Whitman. A avaliação das respostas no mesmo paciente antes e após a adição de immucillin-H foi feita pelo teste pareado de Wilcoxon. Foi considerado estatisticamente significante quando p<0,05. IV.7 Aspectos éticos Os participantes deste projeto assinaram termo de consentimento livre e esclarecido (anexo I) e o projeto foi aprovado pelo Comitê de Ética em Pesquisa da Faculdade de Medicina da Bahia – FMB - sob parecer consubstanciado número 564.409 (anexo II). 11 V. RESULTADOS Foram recrutados oito indivíduos portados de leishmaniose cutânea da área endêmica de Corte de Pedra, Bahia. A média de idade dos pacientes foi de 33,7 ± 8,4 anos, com duração média de doença de 30,1 ± 24,7 dias, do momento do diagnóstico à data de coleta de sangue. Todos os pacientes possuem lesão única, que variaram de 6 x 4mm a 35 x 20mm, abrangendo áreas como coxa, perna e pé. O teste cutâneo intradérmico mostrou reação que variou de 7 x 7mm a 28 x 26 mm. A padronização da dose foi estabelecida a partir da curva dose-resposta apresentada pela CMSPs de controles sadios estimulados por PHA. O Immucillin-H foi adicionado a estas culturas nas concentrações de 150 nM, 300 nM e 600 nM. A figura 1 mostra que a droga teve maior inibição quando na concentração de 300 nM (p=0,0488), não exibindo diferença significativa com o aumento da dose para 600 nM (p=0,9375). Figura 1. Teste de padronização da dose do Immucillin-H. IFN-γ em pg/mL. Com base nos resultados exibidos nos testes de padronização da dose in vitro, ficou estabelecida a utilização das concentrações de 300 nM de Immucillin-H. As CMSPs foram estimuladas com doses de 1 µg/mL e 5 µg/mL de SLA e a produção de IFN-γ, TNF-α e IL10 no sobrenadante de cultura das células de oito pacientes foi determinada por meio do método de ELISA sandwich. * p<0,05 ** p>0,05 A dosagem do IFN-γ é exibida na tabela 1 e 2, nas quais são apontadas as concentrações da citocina nas amostras estimuladas pelo antígeno de Leishmania, com e sem a adição da droga. Tabela 1. Dosagem de IFN-γ, em pg/mL, em culturas de 8 pacientes com leishmaniose cutânea estimulados com SLA 1µg/mL 12 PACIENTES L1 SLA 1μg/mL SLA 1μg/mL + Imm 300 nM 1428 582 % inibição Valor de p 59,2 - L2 1698 657 61,3 - L3 1261 1077 14,6 - L4 301 174 42,2 - L5 780 508 34,9 - L6 668 141 78,9 - L7 625 520 16,8 - L8 987 942 4,6 - MÉDIA 1592 376 39 ± 24,5 0,007 Tabela 2. Dosagem de IFN-γ, em pg/mL, em culturas de 5 pacientes com leishmaniose cutânea estimulados com SLA 5µg/mL PACIENTE SLA 5μg/mL SLA 5μg/mL + Imm 300 nM % inibição Valor de p L4 1104 0 100 - L5 1524 286 81,2 - L6 997 164 83,6 - L7 1605 54 96,6 - L8 1138 1003 11,9 - MÉDIA 1273 301 74,6 ± 36 0,06 Nota-se que com a adição do imunomodulador, há uma redução da produção do IFN-γ, que se mostra estatisticamente significante nas culturas estimuladas com 1 µg/mL de SLA (figura 2). Todas estas amostras apresentaram redução na concentração desta citocina após a adição da droga (p=0,0078). Apesar de a concentração de IFN-γ nas amostras estimuladas com SLA a 5 µg/mL não ter exibido significância estatística ao teste utilizado, é possível verificar que as culturas de CMSPs tiveram um percentual de inibição altamente relevante, expondo percentuais acima de 80% em quatro das cinco amostras analisadas, e com média de inibição de 74,6%. 13 Na tabela são Figura 2. Dosagem de IFN-γ, em pg/mL, antes demonstradas as concentrações de e após a adição de Immucillin-H às culturas de que TNF-α 3 foram e 4 obtidas nos CMSPs estimuladas com 1 µg/mL de SLA. experimentos. Embora possam ser constatadas algumas diminuições pontuais absolutas expressivas na produção de TNF-α, como após a adição da droga à cultura do indivíduo #L7 estimulada com SLA à 5µg/mL (tabela 2), reduções pequenas e até mesmo aumentos da concentração foram verificados em diversas outras amostras. Desta forma, infere-se que não houve - de maneira geral - uma redução significativa da concentração desta citocina quando se utilizou o immucillin-H. Este fato pode ser atestado tanto na concentração de 1 µg/mL (p=0,8438), como na dose de 5 µg/mL (p=0,3125). O percentual inibitório reitera os achados do teste estatístico. Tabela 3. Dosagem de TNF-α, em pg/mL, em culturas de 8 pacientes com leishmaniose cutânea estimulados com SLA 1µg/mL PACIENTES SLA 1μg/mL SLA 1μg/mL + Imm 300 nM % inibição Valor de p L1 24 48 -100 - L2 421 193 54,2 - L3 2278 2113 7,2 - L4 25 38 -52 - L5 234 235 -0,4 - L6 422 774 -83,4 - L7 1436 1374 4,3 - L8 810 800 1,2 - MÉDIA 706 696 -21,1 ± 52 0,84 14 Tabela 4. Dosagem de TNF-α, em pg/mL, em culturas de 5 pacientes com leishmaniose cutânea estimulados com SLA 5µg/mL PACIENTE SLA 5μg/mL SLA 5μg/mL + Imm 300 nM % inibição Valor de p L4 110 134 -21,8 - L5 355 365 -2,8 - L6 1145 1036 9,5 - L7 3790 1968 48,1 - L8 1551 1307 15,7 - MÉDIA 1390 962 9,7 ± 25,7 0,31 A IL-10 tem suas concentrações detalhadas na tabela 5 e 6. Registra-se que em ambas as extrações de SLA utilizadas, o immucillin-H não inibiu de maneira significativa a produção da citocina. Semelhante ao verificado para o TNF-α, reduções pontuais puderam ser presenciadas, porém a inibição inexpressiva associada a aumentos da concentração predominaram. Estes achados foram implicados para as culturas estimuladas em ambas as doses - SLA à 5 µg/mL (p=0,43) e SLA à 1 µg/mL (p=0,81). Os percentuais de inibição sumarizam e reafirmam os dados expostos. Tabela 5. Dosagem de IL-10, em pg/mL, em culturas de 8 pacientes com leishmaniose cutânea estimulados com SLA 1µg/mL PACIENTES SLA 1μg/mL SLA 1μg/mL + Imm 300 nM % inibição Valor de p L1 28 20 28,6 - L2 72 14 80,6 - L3 210 221 -5,2 - L4 170 237 -39,4 - L5 407 371 8,8 - L6 280 244 12,9 - L7 258 354 -37,2 - L8 260 230 11,5 - MÉDIA 210 211 7,57 ± 38 0,81 15 Tabela 6. Dosagem de IL-10, em pg/mL, em culturas de 5 pacientes com leishmaniose cutânea estimulados com SLA 5µg/mL. PACIENTE SLA 5μg/mL SLA 5μg/mL + Imm 300 nM % inibição Valor de p L4 234 225 3,8 - L5 414 488 -17,8 - L6 234 212 9,4 - L7 642 387 39,7 - L8 338 315 6,8 - MÉDIA 372 317 8,3 ± 20,5 0,43 16 VI. DISCUSSÃO A leishmaniose cutânea causada pela L. braziliensis é um exemplo de doença infecciosa na qual a patogênese, e consequentemente a lesão tecidual e formação da úlcera cutânea, está associada a uma resposta imune exagerada e não apropriadamente modulada. O presente estudo mostra que o immucillin-H tem capacidade de reduzir a produção de IFN-γ em culturas estimuladas com antígeno solúvel de leishmania (SLA), colocando este fármaco como um candidato em potencial a ser utilizado em associação com drogas leishmanicidas no tratamento da leishmaniose tegumentar causado por L. braziliensis. O immucillin H, pela sua ação inibitória sobre a enzima PNP, tem a capacidade de reduzir a proliferação dos linfócitos T (Kicska et al., 2001). No homem esta droga foi utilizada em estudo de fase I, que mostrou boa tolerância e segurança no controle total ou parcial de doenças malignas de células T periféricas recidivantes ou refratárias a outras terapias (Ogura et al., 2002). No presente estudo mostra-se que o immucillin-H exerce também influencia na produção de IFN-γ, documentando-se que tanto em culturas estimuladas com um mitógeno (PHA) como em culturas estimuladas com um antígeno, o immucillin-H tem a capacidade de reduzir a produção de IFN-γ. O presente estudo utilizou amostras de sangue de pacientes com leishmaniose cutânea, em doença ativa e antes do tratamento. Todos os indivíduos deste trabalho apresentavam úlcera de aspecto clássico da leishmaniose tegumentar causada pela L. brazilienisis e tiveram o diagnóstico comprovado pelo isolamento do parasita ou pela positividade do PCR em biópsia da pele, bem como teste de hipersensibilidade tardia antígeno de Leishmania positivo. Com a finalidade de determinar a concentração a ser utilizada no Immucillin-H, células mononucleares de indivíduos sadios foram estimuladas com o mitógeno PHA. Observou-se que redução significativa da produção de IFN-γ ocorreu tanto na concentração de 300nM, como 600nM. Embora esta supressão mediada pelo immucillinH fosse somente da ordem de 20-25%, é conhecida a dificuldade de se modular a resposta imunológica a um mitógeno. A capacidade do immucillin-H em modular a resposta imune foi avaliada em relação à produção das citocinas IFN-γ, TNF-α, IL-10 em culturas CMSPs de pacientes infectados pela Leishmania, estimuladas com SLA, tendo sido observada inibição 17 significativa somente com o IFN-γ. Esta ação seletiva indica a especificidade do efeito do immucillin-H sobre células T, uma vez que a IL-10 e TNF-α são citocinas predominantemente produzidas por monócitos. Embora a análise estatística tenha mostrado significância somente para a inibição da produção de IFN-γ nas amostras estimuladas com 1 µg/mL de SLA, esta redução também foi relevante no estímulo de SLA à 5 µg/mL. Este fato pode ser evidenciado pelo percentual inibitório alcançado por estas amostras – com média de 74,6% -, além de um valor de p bem próximo da significância estabelecida (p=0,06). Provavelmente a significância estatística será alcançada com o aumento do tamanho amostral. Os dados obtidos neste estudo indicam uma atividade inibitória do immucillin-H sobre células T de pacientes com leishmaniose cutânea. A importância desses achados reside no fato da patogênese da leishmaniose tegumentar causada pela L. braziliensis estar relacionada predominantemente à atividade de células T CD4+ e CD8+ (Da-Cruz et al., 1994; Da-Cruz et al., 2002; Uzonna et al., 2004). É bem documentada a existência de correlação entre ativação de células CD4+ e o tamanho da úlcera leishmaniótica (Antonelli et al., 2005), enquanto que o papel do CD8+ é observado através de uma correlação entre a frequência de células CD8+ e células CD8+ expressando granzima com a intensidade da resposta inflamatória tecidual (Da-Cruz et al., 1994). Esta resposta exacerbada e não modulada na leishmaniose tegumentar deve-se não só à ativação de células T, como à redução da capacidade dessas células de serem moduladas por citocinas regulatórias, como a IL-10 e o TGF-β (Bacelar et al., 2002). Existem evidências de que a modulação da resposta imune associada ao uso de drogas leishmanicidas é mais eficaz do que o antimonial pentavalente isolado, reduzindo o tempo de cura, além de aumentar a taxa de sucesso terapêutico em pacientes refratários ao tratamento da leishmaniose. Estas observações têm sido feitas tanto pela utilização do fator estimulante de colônias de granulócitos e macrófagos (granulocyte-macrophage colony-stimulating fator - GM-CSF), como da pentoxifilina (Santos et al., 2004; Almeida et al., 2005; Sadeghian G, Nilforoushzadeh MA, 2006; Lessa et al., 2011). Todavia, o GM-CSF deixou de ser fabricado para utilização em humanos e a pentoxifilina associada ao antimonial - que tem se revelado bastante eficaz no tratamento da leishmaniose mucosa em um estudo de fase III realizado no serviço de imunologia do COM-HUPES ainda não publicado - não se mostrou melhor que o antimonial isoladamente para tratamento da leishmaniose cutânea. 18 A capacidade do immucillin-H em modular a produção de IFN-γ em pacientes com leishmaniose tegumentar abre perspectivas para a realização de estudos avaliando a eficácia dessa molécula em combinação com antimonial pentavalente para tratamento da leishmaniose tegumentar. 19 VII. CONCLUSÕES 1. O immucillin-H exibe ação seletiva sobre a produção de IFN-γ, inibindo a produção desta citocina nas amostras estimuladas com SLA a 1 µg/mL e a 5 µg/mL. 2. A droga não exibe o mesmo efeito sobre a concentração das demais citocinas investigadas – TNF-α e IL-10. 3. O immucillin-H apresenta ação imunomoduladora específica sobre as células-T – principal fonte produtora de IFN-γ -, inibindo sua ativação em pacientes com leishmaniose cutânea. 20 VIII. SUMMARY BACKGROUND: Cutaneous leishmaniasis, which is caused by Leishmania braziliensis, has an extremely high prevalence in the Brazilian population. Welldemarcated cutaneous ulcers with raised edges characterize the disease. Immunologically, an over activation of T cells occurs in response to parasite’s antigens, leading to production of pro-inflammatory cytokines such as IFN-γ and TNF-α. This non-modulated inflammatory response is associated with the development of tissue lesion. Immucillin-H is a purine nucleoside phosphorylase (PNP) inhibitor and acts reducing T cell activation. Therefore, Imucillin-H is expected to modulate the immune response in cutaneous leishmaniasis. OBJECTIVE: Determine whether Immucillin-H is capable of modulating over activated immune response in cutaneous leishmaniasis. METHODOLOGY: This study was developed in Universitary Hospitalar Complex Professor Edgard Santos’ Immunology Service (SIM). Eight patients, diagnosed by positive PCR reaction or parasite isolation from lesion’s culture, were evaluated. These patients were from a leishmaniasis endemic are (Corte de Pedra, city of Tancredo Neves, state of Bahia, Brazil), where SIM’s researchers develop assistance services and research. Peripheral blood mononuclear cells were stimulated in vitro with Phitohemagglutinin (PHA) and soluble Leishmania antigen (SLA) isolated or associated whith Immucillin-H. The production of cytokines (IFN-γ, TNF-α and IL-10) in supernatant cultures was evaluated by ELISA technique. Statistical analysis was performed with non-parametric tests: MannWhitney Test and Wilcoxon Paired Test. RESULTS: Immucillin-H was able to inhibit IFN-γ production in samples stimulated by SLA. TNF-α and IL-10 inhibition was not significant. CONCLUSION: Immucillin-H was able to reduce cell T activation in patients with cutaneous leishmaniasis. Key words: 1. Leishmaniasis. 2. T cells. 3. Immucillin-H IX. REFERÊNCIAS BIBLIOGRÁFICAS 21 1. Almeida RP, Brito J, Machado PL, De Jesus AR, Schriefer A, Guimarães LH, et al. Successful treatment of refractory cutaneous leishmaniasis with GM-CSF and antimonials. Am J Trop Med Hyg 2005; 73(1):79-81. 2. Alvar J, Vélez I, Bern C, Herrero M, Desjeux P, Cano J, et al. Leishmaniasis Worldwide and Global Estimates of Its Incidence. PLoS ONE 2012;7(5). 3. Antonelli LR, Dutra WO, Almeida RP, Bacellar O, Carvalho EM, Gollob KJ. Activated inflammatory T cells correlate with lesion size in human cutaneous leishmaniasis. Immunol Let 2005;101(2):226-30. 4. Bacelar O, Lessa H, Schriefer A, Machado P, De Jesus AR, Dutra WO, et al. Upregulation of Th1-Type responses in mucosal leishmaniasis patients. Infect Immun 2002;70(12):6734-40. 5. Bantia S, Miller PJ, Parker CD, Ananth SL, Horn LL, Kilpatrick JM, et al. Purine nucleoside phosphorylase inhibitor BCX-1777 (Immucillin-H) —a novel potent and orally active immunosuppressive agent. International Immunopharmacology 2001;1(6):1199–210. 6. Bantia S, Kilpatrick JM. Purine nucleoside phosphorylase inhibitors in T-cell malignancies. Curr Opin Drug Discov Devel 2004;7(2):243-7. 7. Bittar RC, Nogueira RS, Vieira-Gonçalves R, Pinho-Ribeiro V, Mattos MS, Oliveira-Neto MP, Da-Cruz AM. T-cell responses associated with resistance to Leishmania infection in individuals from endemic areas for Leishmania (Viannia) braziliensis. Memórias do Instituto Oswaldo Cruz 2007;102(5):625-30. 8. Bittencourt AL, Barral A. Evaluation of the histopathological classifications of American cutaneous and mucocutaneous leishmaniasis. Mem Inst Oswaldo Cruz 1991;86(1): 51-6. 9. Brasil. Ministério da Saúde. Secretaria de Vigilância em Saúde. Manual de Vigilância da Leishmaniose Tegumentar Americana. 2 Ed. Brasília-DF; 2010. 10. Bzowska A, Kulikowska E, Shugar D. Purine nucleoside phosphorylases: properties, functions, and clinical aspects. Pharmacol Ther 2000;88(3):349-425. 11. Carvalho EM, Machado PRL, Rosa MEA, Jesus AR, Almeida RP. Immunopathogenesis and Immunotherapy in Tegumentary Leishmaniasis. Curr Res in Immunology 2007;1:91-126. 22 12. Da-Cruz AM, Conceição-Silva F, Bertho AL, Coutinho SG. Leishmania-Reactive CD4+ e CD8+ T Cells Associated with Cure of Human Cutaneous Leishmaniasis. Infect Immun 1994;62(6):2614-18. 13. Da-Cruz AM, Bittar R, Mattos M, Oliveira-Neto MP, Nogueira R, Pinho-Ribeiro V, Azeredo-Coutinho RB, et al. T-Cell-Mediated Immune Responses in Patients with Cutaneous or Mucosal Leishmaniasis. Long-Term Evaluation After Therapy. Clin and Diagn Lab Immunol 2002;9:251-56. 14. Da Silva R, Sacks DL. Metacyclogenesis is a major determinant of Leishmania promastigote virulence and attenuation. Infection and immunity 1987;55(11), 2802-806. 15. Darrah PA, Patel DT, De Luca PM, Lindsay RWB, Davey FD, et al. Multifunctional Th1 cells define a correlate of vaccine-mediated protection against Leishmania major. Nat Med 2007;13(7):843-50. 16. Deves C, de Assunção TM, Ducati RG, Campos MM, Basso LA, Santos DS, et al. The transition state analog inhibitor of Purine Nucleoside Phosphorylase (PNP) Immucillin-H arrests bone loss in rat periodontal disease models. Bone 2013;52(1):167–75. 17. Esfandiarpour I, Farajzadeh S, Rahnama Z, Fathabadi EA, Heshmatkhah A. Adverse effects of intralesional meglumine antimoniate and its influence on clinical laboratory parameters in the treatment of cutaneous leishmaniasis. Int J Dermatol 2012;51(10):1221-5. 18. Faria DR, Souza PEA, Duraes FV, Carvalho EM., Gollob KJ, Machado PR, et al. Recruitment of CD8+ T cells expressing granzyme A is associated with lesion progression in human cutaneous leishmaniasis. Parasite immunology 2009;31(8): 432-9. 19. Furtado T. Leishmaniose Tegumentar Americana. In: Machado-Pinto J(ed), Doenças infecciosas com manifestações dermatológicas. Rio de Janeiro, RJ: Editora Médica e Científica Ltda. 1994, p.319-328. 20. Galmarini CM. Drug evaluation: forodesine - PNP inhibitor for the treatment of leukemia, lymphoma and solid tumor. IDrugs 2006;9(10):712-22. 21. Giblett ER, Ammann AJ, Wara DW, Sandman R, Diamond LK. Nucleosidephosphorylase deficiency in a child with severely defective T-cell immunity and normal B-cell immunity. Lancet 1975; 1(7914):1010-3. 23 22. Giudice A, Vendrame C, Bezerra C, Carvalho LP, Delavechia T, Carvalho EM, Bacellar O. Macrophages participate in host protection and the disease pathology associated with Leishmania braziliensis infection. MC Infect Dis 2012;12:75. 23. Gramiccia M, Gradoni L. The current status of zoonotic leishmaniases and approaches to disease control. Int J Parasitol 2005;35:1169–80. 24. Grimaldi GJ, Tesh RB, McMahon-Pratt D. A review of the geographic distribution and epidemiology of leishmaniasis in the New World. Am J Trop Med Hyg 1989;41:687–725. 25. Guimarães LH, Machado PR, Lago EL, Morgan DJ, Schriefer A, Bacellar O, et al. Atypical manifestations of tegumentary leishmaniasis in a transmission area of Leishmania braziliensis in the state of Bahia, Brazil. Trans R Soc Trop Med Hyg 2009;103(7):712-5. 26. Holzmuller P, Bras-Gonçalves R, Lemesre JL. Phenotypical characteristics, biochemical pathways, molecular targets and putative role of nitric oxidemediated programmed cell death in Leishmania. Parasitology 2006;132:19-32. 27. Korycha A, Blonski JZ, Robak T. Forodesine (BCX-1777, Immucillin-H) – a new purine nucleoside analogue: mechanism of action and potential clinical application. Med Chem 2007;7:976-83. 28. Lessa HA, Machado P, Lima F, Cruz AA, Bacellar O, Guerreiro J, et al. Successful treatment of refractory mucosal leishmaniasis with pentoxifylline plus antimony. Am J Trop Med Hyg 2001;65(2):87-9. 29. Liew FY, Xu D, Chan WL. Immune effector mechanism in parasitic infections. Immunol Lett 1999;65:101-4 30. Lohoff M, Gessner A, Bogdan C, Röllinghoff M. Experimental murine leishmaniasis and the Th1/Th2 cell concept. Tokai J Exp and Clin Med 1998;23:347-50. 31. Marzochi MC. As leishmanioses no Brasil: as leishmanioses tegumentares. J Bras Med 1992;63;82-104. 32. Mayrink W, Botelho AC, Magalhães PA, Batista SM, Ade OL, Genaro O, et al. Immunotherapy, immunochemotherapy and chemotherapy for American cutaneous leishmaniasis treatment. Rev Soc Bras Med Trop 2006;39(1):14-21. 33. Montenegro J. Cutaneous reactions in leishmaniasis. Arch Derm Syphilol 1926;13:187. 34. Morris PE, Omura GA. Inhibitors of the enzyme purine nucleoside phosphorylase as potential therapy for psoriasis. Curr Pharm Des 2000;6(9):943-59. 24 35. Mougneau E, Bihl F, Glaichenhaus N. Cell biology and immunology of Leishmania. Immunol Rev 2011;240(1):286-96. 36. Ogura M, Tsukazaki K, Nagai H, Uchida T, Oyama T, et al. Phase I study of BCX1777 (forodesine) in patients with relapsed or refractory peripheral T/natural killer-cell malignancies. Cancer Sci 2012;103(7):1290-5. 37. Okwor I, Mou Z, Liu D, Uzonna J. Protective Immunity and Vaccination Against Cutaneous Leishmaniasis. Front Immunol 2012;3:128. 38. Oliveira LF, Schubach AO, Martins MM, Passos SL, Oliveira RV, Marzochi MC, et al. Systematic review of the adverse effects of cutaneous leishmaniasis treatment in the New World. Acta Trop 2011;118(2):87-96. 39. Queiroz A, Sousa R, Heine C, Cardoso M, Guimarães LH, Machado PR, et al. Association between an emerging disseminated form of leishmaniasis and Leishmania (Viannia) braziliensis strain polymorphisms. J Clin Microbiol 2012; 50(12):4028-34. 40. Reis LC. Caracterização da Resposta Imune Celular em Portadores de Leishmaniose Tegumentar Americana Antes e Depois do Tratamento Quimioterápico [Dissertação de Mestrado em Saúde Pública]. Recife: Centro de Pesquisas Aggeu Magalhães, Fundação Oswaldo Cruz; 2007. 41. Roberts MTM. Current understandings in the immunology of leishmaniasis and recent developments in prevention and treatment. Br Med Bull 2006;75:115-30. 42. Rogers KA, DeKrey GK, Mbow ML, Gillespie RD, Brodskyn CI, Titus RG. Type 1 and type 2 responses to Leishmania major. FEMS Microbiol Lett 2002;209(1):17. 43. Sadeghian G, Nilforoushzadeh MA. Effect of combination therapy with systemic glucantime and pentoxifylline in the treatment of cutaneous leishmaniasis. Int J Dermatol 2006;45(7):819-21. 44. Santos CD, Boaventura V, Cardoso CR, Tavares N, Lordelo MJ, Noronha A, et al. CD8(+) Granzyme B(+)-Mediated Tissue Injury Versus CD4(+)IFNγ(+)Mediated Parasite Killing in Human Cutaneous Leishmaniasis. J Invest Dermatol 2013. 133(6):1533-40. 45. Santos JB, De Jesus AR, Machado PR, Magalhães A, Salgado K, Carvalho EM, et al. J Infect Dis 2004;190:1793-6. 46. Schnorr D, Muniz AC, Passos S, Guimaraes LH, Lago EL, Bacellar O, et al. IFNγ production to leishmania antigen supplements the leishmania skin test in 25 identifying exposure to L. braziliensis infection. PLoS Negl Trop Dis 2012; 6(12):1947. 47. Sjölander A, Baldwin TM, Curtis JM, Handman E. Induction of a Th1 response and simultaneous lack of activation of a Th2 response are required for generation of immunity of leishmaniasis. J Immunol 1998;160:3949-57. 48. Soong L, Chang CH, Sun J, Longley BJ Jr, Ruddle NH, Flavell RA, McMahonPratt D. Role of CD4+ T cells in pathogenesis associated with Leishmania amazonensis infection. J Immunol 1997; 158(11):5374-83. 49. Sundar S, Reed SG, Sharma S, Mehrotra A, Murray HW. Circulating T Helper 1 (Th1) cell- and Th2 cell-associated cytokines in Indian patients with visceral leishmaniasis. Am J Trop Med Hyg 1997;56(5):522-5. 50. Sypek JP, Chung CL, Mayor SEH, Subramanyam JM, Goldman SJ, Sieburth DS, et al. Resolution of Cutaneous Leishmaniasis: Interleukin 12 Initiates a Protective T Helper Type 1 Immune Response. J Exp Med 1993;177:1797-802. 51. Uzonna JE, Joyce KL, Scott P. Low dose Leishmania major promotes a transient T helper cell type 2 response that is down-regulated by interferon gammaproducing CD8+ T cells. Immunol Rev 2004;201:318-38. 52. Xin L, Li Y, Soong L. Role of Interleukin-1β in Activating the CD11chigh CD45RB− Dendritic Cell Subset and Priming Leishmania amazonensis- Specific CD4+ T Cells In Vitro and In Vivo. Infect. Immun 2007;75(10):5018-26. X. ANEXOS: ANEXO I: Termo de Consentimento Livre e Esclarecido TERMO DE CONSENTIMENTO LIVRE E ESCLARECIDO 26 Nome do Projeto: Avaliação da Capacidade do Immucillin-H em Modular a Resposta Imune in vitro em Indivíduos com Leishmaniose Cutânea Nome do Participante: Investigador Principal: Edgar Marcelino de Carvalho Filho - Complexo Hospitalar Professor Edgard Santos (Com-HUPES), Rua João das Botas s/nº, Canela, 40110-160. Salvador, Bahia, Brasil. Tel.: (71) 3237-7353 CEP/FMB: Praça XV de novembro, s/nº, Largo do Terreiro de Jesus, 40025-010. Salvador, Bahia, Brasil. Tel.:(71) 3283-5564 No do Projeto: Convite e Objetivo: O (A) Senhor (a) está sendo convidado (a) a participar de uma pesquisa. Por favor, leia este documento com bastante atenção antes de assiná-lo. Caso haja alguma palavra ou frase que o (a) senhor (a) não consiga entender, converse com o pesquisador responsável pelo estudo ou com um membro da equipe desta pesquisa para explica-los. Caso o(a) senhor(a) não possa ler este documento, poderá contar com a ajuda de um familiar ou alguém de sua confiança para leitura do documento. A proposta deste termo de consentimento livre e esclarecido (TCLE) é explicar tudo sobre o estudo e solicitar a sua autorização para participar do mesmo. O objetivo principal deste estudo é determinar a capacidade da droga, chamada de Immucillin-H, em reduzir o crescimento acelerado de células do sistema de defesa do organismo em amostras de sangue de pacientes com leishmaniose cutânea. Dentre os objetivos específicos, este estudo avaliará a capacidade desta mesma droga em reduzir a produção de substâncias que aumentam o ritmo de crescimento dessas mesmas células. Participarão do estudo, aproximadamente, 15 pessoas com Leishmaniose Cutânea, e as análises serão feitas no Serviço de Imunologia do Complexo Hospitalar Universitário Professor Edgard Santos (COM-HUPES), em Salvador, Bahia. O (a) Senhor (a) foi escolhido (a) a participar do estudo porque vem sendo acompanhado no Posto de Saúde de Corte de Pedra, município de Tancredo Neves, Bahia, e possui ferida típica da leishmaniose cutânea com um a três meses de duração da doença, confirmada por exame laboratorial. Além das informações aqui prestadas você pode esclarecer dúvidas sobre o estudo com seu médico. Caso decida participar, você será solicitado a assinar este formulário de consentimento. 27 Participação Voluntária: Sua participação é totalmente voluntária, ou seja, você somente participa se quiser. A não participação no estudo não mudará seu acompanhamento médico. Você tem total liberdade de sair do estudo a qualquer momento, sem qualquer prejuízo à continuidade do acompanhamento na instituição. Finalidade: O estudo procura testar a capacidade da droga Immucillin-H em reduzir a resposta aumentada das células de defesa, encontrada em pacientes com leishmaniose cutânea. Procedimentos: Caso você concorde em participar do estudo, você será solicitado a fornecer 30 ml de sangue para realizar as avaliações acima citadas. Os resultados destes exames estarão disponíveis e você poderá consultar seu médico para obter informação sobre eles. Duração do estudo: A duração total do estudo é de 2 anos. Durante este período você será solicitado a fazer apenas uma coleta de sangue. Confidencialidade: Todas as informações colhidas e os resultados dos testes serão mantidos em segredo. Os resultados desta pesquisa serão apresentados em reuniões ou publicações científicas, mas não há por que se preocupar, pois sua identidade (nome e qualquer outra informação pessoal) jamais será revelada. Análise de riscos: Os riscos dos procedimentos são mínimos. Uma pequena dor no local da coleta de sangue poderá ocorrer. Em alguns casos, a coleta de sangue pode ser acompanhada por pequeno sangramento ou formação de área arroxeada (hematoma). Manteremos pressionada a área furada pela agulha por alguns minutos para evitá-los. Caso o paciente apresente algum desconforto ou tontura, deverá permanecer deitado. A equipe será responsável por providenciar tratamento médico e assegurar o bem estar dos participantes. Análise de benefícios: Não há benefício direto para o participante desse estudo. Porém, os resultados obtidos com este estudo poderão ajudar, no futuro, a desenvolver drogas que serão aplicadas aos pacientes para diminuir lesões causadas pela leishmaniose. Custos: Você não terá nenhum gasto e nem receberá qualquer pagamento pela sua participação. Em caso de danos relacionados à pesquisa: Em caso de dano pessoal, diretamente causado pelos procedimentos deste estudo, o participante tem direito a tratamento médico nas Instituições, bem como às indenizações estabelecidas em lei. 28 Esclarecimentos: Em qualquer etapa do estudo você terá acesso aos profissionais responsáveis pela pesquisa para esclarecimento de qualquer dúvida. Os responsáveis pelo estudo são os Dr. Edgar M. Carvalho e Rafael de Castro da Silva que poderão ser encontrados no Serviço de Imunologia do COM-HUPES, nos respectivos telefones: 71 3283-8114, 71 9101-6658. Consentimento: Se você leu o consentimento informado ou este lhe foi explicado e você aceita participar do estudo, favor assinar o nome abaixo. A você será entregue uma cópia deste formulário para guardar. Em caso de denúncia, o CEP-FMB/UFBA deve ser contatado através do telefone (71)3283-5575 ou (71)3283-5567 ou no endereço Largo do Terreiro de Jesus, s/n, Pelourinho – Salvador/BA. ____________________________ Assinatura do participante ____________ ____________ Data Hora Impressão digital do participante ____________________________ Assinatura do pesquisador ______________________________ Assinatura da testemunha ____________ ____________ Data ____________ Hora ____________ Data ANEXO II. Parecer consubstanciado do CEP PARECER CONSUBSTANCIADO DO CEP DADOS DO PROJETO DE PESQUISA Hora 29 Título da Pesquisa: Avaliação da Capacidade do Immucillin-H em Modular em Resposta Imune In Vitro em Indivíduos com Leishmaniose Cutânea Pesquisador: Edgar Marcelino de Carvalho Filho Área Temática: Versão: 2 CAAE: 24172214.7.0000.5577 Instituição Proponente:FACULDADE DE MEDICINA DA BAHIA Patrocinador Principal: MINISTERIO DA CIENCIA, TECNOLOGIA E INOVACAO DADOS DO PARECER Número do Parecer: 564.409 Data da Relatoria: 07/04/2014 Apresentação do Projeto: A leishmaniose cutânea (LC), causada pela Leishmania braziliensis, tem grande prevalência na população brasileira. A doença se caracteriza pela presença de úlcera(s) bem delimitadas, com bordas elevadas. Do ponto de vista imunológico, existe uma ativação exagerada de células T contra antígenos do parasita, com produção de citocinas pró-inflamatórias, como IFN-¿, TNF-¿ e IL-10. Esta resposta inflamatória não apropriadamente modulada se relaciona com o desenvolvimento da lesão tecidual. Alguns estudos in vitro, nos recentes anos, mostraram o efeito da inibição da enzima Purina Nucleosídeo Fosforilase (Purine nucleoside Phosphorylase - PNP) através do Immucillin-H, com direta ação sobre a proliferação celular, diminuindo-a acentuadamente. Como os efeitos do Immucillin-H se fazem somente em células T ativadas, não atingindo, portanto, outras células de defesa do hospedeiro, é importante avaliar a ação deste agente em atenuar a resposta imune de pacientes com leishmaniose cutânea, considerando o importante papel da exacerbação da resposta imune celular na patogênese dessa doença. Objetivo da Pesquisa: Geral Determinar a capacidade do Immucillin-H de modular negativamente a resposta imune mediadapor células em pacientes com leishmaniose cutânea. Continuação do Parecer: 564.409 Específicos: 30 Avaliar a capacidade do Immucillin-H de diminuir a resposta linfoproliferativa e a produção de citocinas em pacientes com leishmaniose cutânea. Avaliar a capacidade do Immucillin-H em diminuir a produção de citocinas pró-inflamatórias em pacientes com leishmaniose cutânea. Avaliação dos Riscos e Benefícios: Riscos: Os pesquisadores afirmam que os riscos dos procedimentos são mínimos. Uma pequena dor no local da coleta de sangue poderá ocorrer. Em alguns casos, a coleta de sangue pode ser acompanhada por pequeno sangramento ou formação de hematoma. A área de punção será pressionada por alguns minutos para evitálos. Caso o paciente apresente algum desconforto ou tontura, deverá permanecer deitado. A equipe será responsável por providenciar tratamento médico e assegurar o bem estar dos participantes. Benefícios: Não há benefício direto observado para o participante desse estudo. Porém, os resultados obtidos com este estudo poderão ajudar, no futuro, a desenvolver drogas que serão aplicadas aos pacientes para diminuir lesões decorrentes da doença em questão. Comentários e Considerações sobre a Pesquisa: Trata-se de pesquisa relevante na área de doenças negligenciadas, seguindo aspectos éticos e preceitos da Resolução CNS 466/12. Considerações sobre os Termos de apresentação obrigatória: Foi anexada a declaração de confidencialidade pelo pesquisador principal e demais pesquisadores. De igual forma, foi anexada a carta de anuência do Posto de saúde de Corte de Pedra e do HUPES. O calendário da pesquisa foi adequado para início somente após aprovação pelo CEP. O TCLE foi adequado de acordo com os preceitos da Resolução 466/12 do CNS. Recomendações: Cabe ao pesquisador principal a responsabilidade de enviar relatórios semestrais da pesquisa aprovada. Em caso de intercorrência o CEP FMB-UFBA deve ser comunicado. Continuação do Parecer: 564.409 Conclusões ou Pendências e Lista de Inadequações: 31 Não há Situação do Parecer: Aprovado Necessita Apreciação da CONEP: Não Considerações Finais a critério do CEP: SALVADOR, 23 de Março de 2014 Assinador por: Eduardo Martins Netto (Coordenador)
Baixar