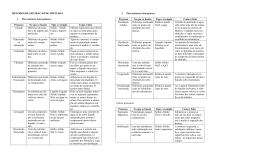
EXERCÍCIOS FINAIS Questões Objetivas CONCEITOS FUNDAMENTAIS 2. (Enem) Seguem a seguir alguns trechos de uma matéria da revista "Superinteressante", que descreve hábitos de um morador de Barcelona (Espanha), relacionando-os com o consumo de energia e efeitos sobre o ambiente. I. Apenas no banho matinal, por exemplo, um cidadão utiliza cerca de 50 litros de água, que depois terá que ser tratada. Além disso, a água é aquecida consumindo 1,5 quilowatt-hora (cerca de 1,3 milhões de calorias), e para gerar essa energia foi preciso perturbar o ambiente de alguma maneira... II. Na hora de ir para o trabalho, o percurso médio dos moradores de Barcelona mostra que o carro libera 90 gramas do venenoso monóxido de carbono e 25 gramas de óxidos de nitrogênio... Ao mesmo tempo, o carro consome combustível equivalente a 8,9kwh. III. Na hora de recolher o lixo doméstico... quase 1kg por dia. Em cada quilo há aproximadamente 240 gramas de papel, papelão e embalagens; 80 gramas de plástico; 55 gramas de metal, 40 gramas de material biodegradável e 80 gramas de vidro. 1) No trecho I, a matéria faz referência ao tratamento necessário à água resultante de um banho. As afirmações a seguir dizem respeito a tratamentos e destinos dessa água. Entre elas, a mais plausível é a de que a água: a) passa por peneiração, cloração, floculação, filtração e pós-cloração, e é canalizada para os rios. b) passa por cloração e destilação, sendo devolvida aos consumidores em condições adequadas para ser ingerida. c) é fervida e clorada em reservatórios, onde fica armazenada por algum tempo antes de retornar aos consumidores. d) passa por decantação, filtração, cloração e, em alguns casos, por fluoretação, retomando aos consumidores. e) não pode ser tratada devido à presença do sabão, por isso é canalizada e despejada em rios. 2) (Enem) Em nosso planeta a quantidade de água está estimada em 1,36×106 trilhões de toneladas. Desse total, calcula-se que cerca de 95% são de água salgada e dos 5% restantes, quase a metade está retida nos pólos e geleiras. O uso de água do mar para obtenção de água potável ainda não é realidade em largas escala. Isso porque, entre outras razões, a) o custo dos processos tecnológicos e desalinização é muito alto. b) não se sabe como separar adequadamente os sais nela dissolvidos. c) comprometeria muito a vida aquática dos oceanos. d) a água do mar possui materiais irremovíveis. e) a água salgada do mar tem temperatura de ebulição alta. 3) (Enem) Pelas normas vigentes, o litro do álcool hidratado que abastece os veículos deve ser constituído de 96% de álcool puro e 4% de água (em volume). As densidades desses componentes são dadas na tabela 1. Um técnico de um órgão de defesa do consumidor inspecionou cinco postos suspeitos de venderem álcool hidratado fora das normas. Colheu uma amostra do produto em cada posto, mediu a densidade de cada uma, obtendo a tabela A partir desses dados, o técnico pôde concluir que estavam com o combustível adequado somente os postos a) I e II. b) I e III. c) II e IV. d) III e V. e) IV e V. 4) (Ufrsg) Três amostras materiais designadas por I, II e III forma submetidas a diferentes processos de análise, sob presssão de 1 atm, obtendo os dados a seguir: Amostra I : É um gás incolor que liquefaz a uma temperatura de 183 oC. Quando submetido a processos usuais de decomposição, permanece a mesma substância. Amostra II: É um sólido branco que apresenta ponto defusão igual a 800 oC e ponto de ebulição igual a 1413 oC. Quando submetido a decomposição por eletrólise origina um sólido metálico e libera um gás. Amostra III: É um líquido límpido e incolor que não mantém uma temperatura constante durante a sua ebulição. Após a destilação observase a formação de cristais brancos no fundo do recipiente que o contém. As amostras I,II e III podem ser respectivamente: a) substância pura, mistura homogênea e mistura heterogênea b) substância simples, substância composta e solução c) substância simples, mistura homogênea e mistura homogênea d) solução gasosa, substância pura e substância composta e) mistura homogênea, mistura eutética e mistura azeotrópica 5) (Mackenzie) Assinalar a alternativa correta. a) Liquefação é o nome dado à passagem de sólido para líquido. b) Ocorre sublimação quando as gotas da chuva tocam o asfalto quente. c) Ocorre um fenômeno físico quando o peróxido de hidrogênio (H2O2), contido na água oxigenada, sofre decomposição (Fotólise). d) O sistema, constituído por dois cubos de gelo em um copo com água, é trifásico. e) Ocorrem reações químicas no processo da digestão dos alimentos. 6) (Ufba) Com base nos conhecimentos sobre os estados físicos da matéria, pode-se afirmar: (01) O processo de transformação de um sólido em um gás chama-se difusão. (02) Um sólido pode ser transformado num líquido, pelo processo de dissolução. (04) O vapor pode ser transformado num sólido, por resfriamento. (08) Pode-se transformar um líquido num sólido, através do processo de fusão. (16) A vaporização de um líquido puro, nas condições de equilíbrio, ocorre a pressão e temperatura constantes. Professor : Rogério Alves Professor : Rogério Alves (32) As interações das partículas de uma substância são mais fortes no estado sólido que no estado líquido. (64) Se os pontos de ebulição do éter etílico e do ácido acético são, a 1atm de pressão, respectivamente 34,6°C e 118,1°C, esse último composto é mais volátil que o éter. 7) (Ufba) As proposições a seguir foram formuladas por um estudante, após o estudo de substâncias puras e misturas. I. O leite puro não pode ser representado por fórmula molecular porque é uma mistura de várias substâncias. II. Como se trata de substância pura, o álcool anidro apresenta ponto de ebulição e densidade característicos. III. A água mineral é substância pura de composição definida. IV. O ar empoeirado é mistura heterogênea sólido + gás. V. Por ser substância pura, o café coado não pode ser submetido a processos de fracionamento de misturas. Quantas proposições estão corretas? a) 1 b) 2 c) 3 d) 4 Nesse processo, a energia solar cedida à água salgada e) 5 8) (Ufrrj) Com a adição de uma solução aquosa de açúcar a uma mistura contendo querosene e areia, são vistas claramente três fases. Para separar cada componente da mistura final, a melhor seqüência é: a) destilação, filtração e decantação. b) cristalização, decantação e destilação. c) filtração, cristalização e destilação. d) filtração, decantação e destilação. e) centrifugação, filtração e decantação. 9) (Ita) Qual das opções a seguir contém a associação CORRETA dos procedimentos de laboratório, listados na 1a coluna, com suas respectivas denominações, listadas na 2a coluna? 1. Adição de 20ml de água a uma solução aquosa saturada em cloreto de sódio e contendo um grande excesso de sal sedimentado, tal que ainda permaneça precipitado após a adição de mais solvente. 2. Adição de 20ml de água a uma solução aquosa não saturada em cloreto de sódio. 3. Retirada de fenol, solúvel em água e em éter etílico, de uma solução aquosa, por agitação com uma porção de éter etílico seguida por separação da fase orgânica da fase aquosa. 4. Dissolver glicose em água e a esta solução juntar etanol para que surjam novamente cristais de glicose. 5. Adição de 20ml água a nitrato de potássio cristalino. a. Dissolução. b. Extração. c. Diluição. d. Recristalização. a) 1a; 2c; 3b; 4d; 5a. c) 1a; 2a; 3a; 4d; 5c. e) 1a; 2a; 3c; 4d; 5c. a) fica retida na água doce que cai no copo, tonando-a, assim altamente energizada. b) fica armazenada na forma de energia potencial gravitacional contida na água doce c) é usada para provocar a reação química que transforma a água salgada em água doce. d) é cedida ao ambiente externo através do plástico, onde ocorre a condensação do vapor. e) é reemitida como calor para fora do tanque, no processo de evaporação da água salada Questões discursivas 11) (Fuvest) Proponha um procedimento de separação dos componentes de uma mistura de três substâncias, A, B e C, cujas solubilidades em água e acetona são indicadas a seguir: Substância A B C Solubilidade em água Solúvel Insolúvel insoúvel Solubilidade em acetona solúvel solúvel insolúvel 12) Evidências experimentais mostram que somos capazes, em média, de segurar por um certo tempo um frasco que esteja a uma temperatura de 60°C, sem nos queimarmos. Suponha uma situação em que dois béqueres contendo cada um deles um líquido diferente (X e Y) tenham sido colocados sobre uma chapa elétrica de aquecimento, que está à temperatura de 100°C. A temperatura normal de ebulição do líquido X é 50°C e a do líquido Y é 120°C. a) Após certo tempo de contato com esta chapa, qual dos frascos poderá ser tocado com a mão sem que se corra o risco de sofrer queimaduras? Justifique a sua resposta. b) Se a cada um desses frascos for adicionada quantidade igual de um soluto não volátil, mantendo-se a chapa de aquecimento a 100°C, o que acontecerá com a temperatura de cada um dos líquidos? Explique. b) 1c; 2c; 3a; 4b; 5a. d) 1c; 2a; 3b; 4b; 5c. 10) (Enem) Além de ser capaz de gerar eletricidade, a energia solar é usada para muitas outras finalidades. A figura a seguir mostra o uso da energia solar para dessalinizar a água. Nela, um tanque contendo água salgada é coberto por um plástico transparente e tem sua parte central abaixada pelo peso de uma pedra, sob a qual se coloca um recipiente (copo). A água evaporada se condensa no plástico e escorre até o ponto mais baixo, caindo dentro do copo. "É preciso ser mais virtuoso para suportar a prosperidade do que a adversidade." La Rochefoucauld
Baixar