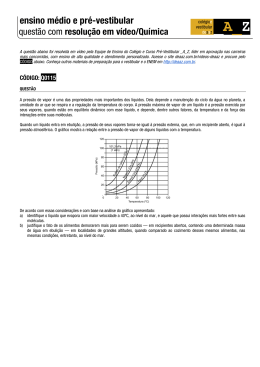
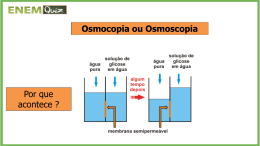
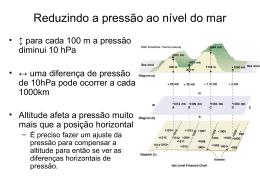
Aquecimento da Água: Análise do Efeito do Material Utilizado (inox ou alumínio) do Sistema de Aquecimento (recipiente aberto ou fechado) e da Solução Utilizada (água pura, água com sal ou água com açúcar), em seu Tempo de Ebulição Graziela Cristina Chaves de Castro Programa de Pós-Graduação em Engenharia Elétrica Universidade Federal de Minas Gerais Av. Antônio Carlos, 6627 - Belo Horizonte Email: [email protected] Resumo—Este trabalho apresenta um planejamento experimental, descreve suas etapas e realiza uma análise estatística dos dados obtidos para o experimento de aquecimento da água, com o objetivo de testar a influência dos fatores material, sistema de aquecimento e solução, no tempo de ebulição da água. Os fatores material e sistema de aquecimento, apresentam dois níveis cada, sendo eles: inox ou alumínio e recipiente aberto ou recipiente fechado, respectivamente. O fator solução, apresenta sete níveis: água pura, água 1cs sal, água 2cs sal, água 3cs sal, água 1cs açúcar, água 2cs açúcar, água 3cs açúcar, em que “cs” refere-se à medida do soluto utilizado, em colheres de sopa. Utilizou-se um planejamento fatorial generalizado, pois o fator solução apresentava sete níveis. Na análise estatística dos dados foi utilizado o teste ANOVA, que permite que vários grupos sejam comparados. O teste é paramétrico (a variável de interesse deve ter distribuição normal) e os grupos têm que ser independentes. Ao inferir sobre as características de uma população a partir da informação contida na amostra coletada, propondo um modelo para os dados coletados, houve a necessidade da execução de testes para validar este modelo e para visualizar a influência dos fatores e seus níveis na variável de resposta. Os resultados obtidos permitem concluir, considerando-se um nível de significância de 0.05, que somente os fatores “sistema” e “solução” podem influenciar no tempo de ebulição da água. I. I NTRODUÇÃO Quando aquecemos um líquido em um recipiente aberto, formam-se bolhas, geralmente no fundo, onde é aplicado calor. As primeiras pequenas bolhas que vemos são ar, expelido da solução pelo aumento de temperatura. A certa temperatura, grandes bolhas de vapor formam-se em todo o líquido. Essas bolhas de vapor sobem para a superfície e se quebram. Quando isso ocorre, o líquido está em ebulição. A temperatura na qual um líquido ferve depende da pressão exercida sobre ele. No caso da água, o valor tabelado é igual a 100oC, à pressão atmosférica de 1 atm, que é a pressão atmosférica ao nível do mar. É a temperatura de um líquido na qual sua pressão de vapor é igual à pressão aplicada. Para se formar uma bolha de vapor, a pressão no interior da bolha, Pb , deve ser ao menos igual à pressão acima dela, Ps . Como Pb é simplesmente a pressão de vapor do líquido, concluímos que um líquido entra em ebulição a uma temperatura na qual a pressão de vapor iguala-se à pressão exercida sobre sua superfície. Se esta pressão é 1 atm, nos referimos à essa temperatura como ponto de ebulição normal. O ponto de ebulição de um líquido pode ser reduzido pelo abaixamento da pressão exercida sobre ele (aplicando vácuo, por exemplo). Em altas altitudes (pressão reduzida) a temperatura de ebulição da água em um recipiente aberto é mais baixa. Uma solução é uma mistura homogênea de um soluto (substância sendo dissolvida) em um solvente (substância que efetua a dissolução). As soluções mais familiares estão no estado líquido, especialmente aquelas nas quais a água é o solvente. Uma solução de um soluto não volátil ferve a uma temperatura maior e congela a uma temperatura menor que o solvente puro. A elevação do ponto de ebulição é um resultado direto do abaixamento da pressão de vapor. A qualquer temperatura dada, uma solução tem pressão de vapor menor que a do solvente puro. Portanto, uma temperatura maior deve ser atingida antes de a solução ferver, isto é, antes que sua pressão de vapor se torne igual à pressão externa. Na evaporação, o movimento molecular ocorre predominantemente em um sentido: as moléculas, aos poucos, deixam o líquido e se difundem no ar. Em um recipiente fechado, o movimento das moléculas ocorre essencialmente em um sentido: de líquido para vapor. Nesse caso, as moléculas de vapor não podem escapar do recipiente. Algumas colidem com a superfície e retornam ao líquido. Com o passar do tempo, a concentração de moléculas no vapor cresce, como também a velocidade de condensação. Finalmente, ela se iguala à velocidade de vaporização e o líquido e o vapor estão em equilíbrio dinâmico. Uma vez atingido o equilíbrio, a concentração de moléculas na fase de vapor não varia com o tempo. Isto significa que a pressão exercida pelo vapor sobre o líquido permanece constante. A pressão do vapor em equilíbrio com o líquido é denominada pressão de vapor. A 100oC, a pressão de vapor da água chega a 1 atm (760 mmHg). O ponto de ebulição de um líquido é a temperatura na qual são formadas bolhas cheias de vapor no seu interior e depende da pressão exercida sobre o mesmo. O ponto de ebulição normal é a temperatura na qual um líquido ferve quando a pressão acima do líquido é 1 atm (760 mmHg). Para um líquido puro, a temperatura permanece constante durante a ebulição. Se o líquido é impuro, esperamos que a temperatura cresça continuamente durante a ebulição. A quantidade de calor absorvido no aumento de temperatura de uma substância depende de três fatores: • • • da massa da substância: quanto maior a massa, maior o calor absorvido. da variação de temperatura: quanto maior a variação de temperatura, maior o calor absorvido. do calor específico q = ce × m × ∆t = quantidade de calor absorvida pela água, em joules (J) ∆t = t f inal − tinicial cal = quantidade de calor necessária para elevar a temperatura de 1g de água em 1oC(1cal = 4,184J) ce = calor específico da água = 4,18J/gxoC m = massa da água = 1l = 1kg = 1x103 g • • • • • • • • Planejamento fatorial com análise de variância, para 03 (três) fatores (material, sistema e solução), sendo inox e alumínio; sistema aberto e sistema fechado; água pura, água com 1 colher de sopa de sal, água com 2 colheres de sopa sal, água com 3 colheres de sopa sal, água com 1 colher de sopa açúcar, água com 2 colheres de sopa de açúcar e água com 3 colheres de sopa açúcar, os diferentes níveis de cada fator, respectivamente. Para analisar o efeito individual de cada fator sobre o tempo de ebulição da água e os efeitos de interação entre eles, foram realizadas quatro replicações do experimento. Plano do experimento: Fatores: 3 Nível dos Fatores: 2, 2, 7 Classes: 28 Replicações: 4 por classe Observações totais: 112 Ordem das observações: aleatorizada (Minitab, versão 16) Temperatura ambiente e 0,89atm A ebulição é medida após o rompimento da 1a bolha na superfície da solução. Em temperatura ambiente (25oC) é esperado que a água ferva a 98oC. Nível de significância 0,05(5%): a hipótese nula será rejeitada se for detectada uma diferença significativa entre as médias dos 4 sistemas propostos. Variável de Resposta: tempo de ebulição da água A. Materiais e Métodos O abaixamento do ponto de congelamento, como a elevação do ponto de ebulição, é um resultado direto do abaixamento da pressão de vapor do solvente pelo soluto. O ponto de ebulição ou congelamento da solução é a temperatura na qual o solvente em solução tem a mesma pressão de vapor que a do solvente (líquido ou sólido) puro. A elevação do ponto de ebulição e o abaixamento do ponto de congelamento, como o abaixamento da pressão de vapor são propriedades coligativas. Elas são diretamente proporcionais à concentração de soluto, geralmente expressa em molalidade (m). [4] II. P LANEJAMENTO P RÉ -E XPERIMENTAL O objetivo deste experimento é inferir sobre as características de uma população a partir da informação contida na amostra obtida e propor um modelo para os dados coletados, verificando se existe diferença significativa entre as variações do tempo de ebulição da água, relativas aos diferentes fatores do experimento e suas interações, e se existir, estimar esta diferença. Para garantir as condições de identidade e independência dos dados coletados e evitar erros sistemáticos, optouse pela aleatorização na obtenção dos pontos experimentais, utilizando-se para este fim, o Minitab 16, que é uma ferramenta de análise estatística de dados. Este experimento foi realizado, tendo como base as seguintes considerações iniciais: A relação do material utilizado está listada abaixo: • • • • • • • • Recipiente graduado de 1000 ml Cronômetro Panelas de inox e de alumínio de mesmo tamanho Água (1l): não é totalmente pura (cloro) Açúcar (15g, 30g, 45g) Sal (15g, 30g, 45g) 3 queimadores de fogão de mesmo diâmetro - chama alta constante Termômetro químico Incoterm (vidro com mercúrio) – Escala: −10oC + 310oC – Divisão: 1oC (com grau de incerteza de uma unidade no último dígito) – Limite de erro: até 210oC, ±1oC / acima de 210oC, ±2oC 1) Protocolo do experimento: • • Colocar 1l de água à temperatura ambiente no recipiente graduado Medir a temperatura do sistema com um termômetro e anotá-la – O valor dessa temperatura corresponderá ao tempo inicial (zero minuto) – A leitura com o termômetro foi feita um pouco abaixo da superfície do líquido (nunca com o termômetro encostado no fundo do recipiente) • • • • • Colocar a água pura (ou uma das soluções) em uma das panelas e iniciar o aquecimento acendendo o queimador do fogão na temperatura mais alta e, ao mesmo tempo, acionando o cronômetro No caso das soluções, o sólido foi dissolvido por agitação até que fosse formada uma solução homogênea Quando a água ferver (entrar em ebulição), anotar a temperatura e o tempo indicados nos respectivos medidores No caso do recipiente tampado, esperar a temperatura alcançar 1 minuto a menos que a temperatura de ebulição do recipiente aberto e, então, abrir a tampa em 1 cm, para monitorar o tempo de ebulição Colocar o recipiente e os queimadores utilizados ainda quentes, em água fria, para o resfriamento dos mesmos 3) 4) B. Fatores, Níveis, Variáveis de Resposta Os fatores e os níveis definidos são detalhados na Tabela I. 5) Tabela I FATORES E N ÍVEIS D EFINIDOS Fator Material da Panela Sistema Termodinâmico Solução Aquosa Nível 1 Inox Aberto Água Pura Nível 2 Alumínio Fechado Água 1cs de sal ... ... Nível 7 Água 3cs de açúcar 6) C. Análise dos Resultados O modelo de efeitos é representado pela equação abaixo: yi jk = µ + τi + β j + γk + (τβ )i j + (τγ)ik + i = 1,...m j = 1,..n (β γ) jk + (τβ γ)i jk + εi jk k = 1,...l 7) (1) Em que: µ: é a média geral; τi : é o efeito do nível i do fator A; βj é o efeito do nível j do fator B; γj é o efeito do nível k do fator C; (τβ )i j é o efeito de interação entre os fatores A e B. (τγ)ik é o efeito de interação entre os fatores A e C. (β γ) jk é o efeito de interação entre os fatores B e C. (τβ γ)i jk é o efeito de interação entre os fatores A, B e C. εi jk : é o resíduo (erro aleatório com distribuição normal de média zero e variância σ 2 ); m,n,l são os níveis dos fatores A, B e C, respectivamente. D. Hipóteses As hipóteses de teste são: 1) Testar a influência do fator Material no tempo de ebulição da água. H0 = τi = 0 ∀i, significando que não existe influência do fator A no valor da variável de resposta considerada. H1 : ∃τi 6= 0, o que indica que existe influência deste fator no tempo de ebulição da água. 2) Testar a influência do fator Sistema no tempo de ebulição da água. H0 = β j = 0 ∀ j, significando que não existe influência do fator A no valor da variável de resposta considerada. H1 : ∃β j 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. Testar a influência do fator Solução no tempo de ebulição da água. H0 = γk = 0 ∀k, significando que não existe influência do fator A no valor da variável de resposta considerada. H1 : ∃γk 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. Testar a influência da interação entre os dois fatores (Material e Sistema) no tempo de ebulição da água. H0 = (τβ )i j = 0 ∀i, j, indicando a ausência de significância de interação entre esses fatores. H1 : ∃(τβ )i j 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. Testar a influência da interação entre os dois fatores (Material e Solução) no tempo de ebulição da água. H0 = (τγ)ik = 0 ∀i, j, indicando a ausência de significância de interação entre esses fatores. H1 : ∃(τγ)ik 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. Testar a influência da interação entre os dois fatores (Sistema e Solução) no tempo de ebulição da água. H0 = (β γ) jk = 0 ∀i, j, indicando a ausência de significância de interação entre esses fatores. H1 : ∃(β γ) jk 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. Testar a influência da interação entre os três fatores (Material, Sistema e Solução) no tempo de ebulição da água. H0 = (τβ γ)i jk = 0 ∀i, j, indicando a ausência de significância de interação entre esses fatores. H1 : ∃(τβ γ)i jk 6= 0, o que indica que existe influencia deste fator no tempo de ebulição da água. III. R ESULTADOS E D ISCUSSÃO Tabela II DADOS COLETADOS StdOrder 50 2 63 35 73 105 87 107 78 66 59 44 32 67 7 99 RunOrder 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 PtType 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Blocks 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 Material ALUMÍNIO INOX INOX INOX ALUMÍNIO ALUMÍNIO INOX ALUMÍNIO ALUMÍNIO INOX INOX ALUMÍNIO INOX INOX INOX ALUMÍNIO Sistema FECHADO ABERTO ABERTO ABERTO ABERTO ABERTO ABERTO FECHADO FECHADO FECHADO ABERTO ABERTO ABERTO FECHADO ABERTO ABERTO Solução ÁGUA PURA ÁGUA 1 SAL ÁGUA 3 AÇÚCAR ÁGUA 3 AÇÚCAR ÁGUA 2 SAL ÁGUA 3 AÇÚCAR ÁGUA 2 SAL ÁGUA 1 SAL ÁGUA PURA ÁGUA 2 SAL ÁGUA 2 SAL ÁGUA 1 SAL ÁGUA 3 SAL ÁGUA 3 SAL ÁGUA 3 AÇÚCAR ÁGUA PURA Tempo de Fervura 588 605 635 626 603 637 613 565 546 576 636 619 642 554 636 621 . . . . . . . . . . . . . . . . . . . . . . . . A. Análise de Variância A análise de variância, também conhecida como ANOVA (Analysis of Variance) é utilizada para comparar as médias de dois ou mais grupos simultaneamente, comparando as diferenças entre os grupos com as diferenças entre os indivíduos. Neste trabalho, como existem três fatores independentes e identicamente distribuídos, foi utilizado o teste ANOVA, com um nível de significância de α = 0.05. A Tabela III apresenta os resultados obtidos pelo software de análise estatística Minitab, versão 16. A primeira coluna indica a fonte de variação; a coluna DF (Degrres of Freedom) indica os graus de liberdade; a coluna SS (Sum os Squares) indica a soma de quadrados, a coluna MS (Mean Square) indica os quadrados médios, e F e P representam respectivamente o valor do teste estatístico tipo F e o p valor associado. O valor p é o menor nível de significância que levaria a não aceitação da hipótese nula para os dados disponíveis. Pvalores < 0.5 indicam diferenças significativas entre as médias analisadas. Os resultados indicados na Tabela III indicam que existe diferença significativa entre os níveis dos fatores Sistema e Solução (p = 0,000 e p = 0,003, respectivamente), indicando que os resultados são influenciados diretamente por estes fatores. Figura 2. Gráfico dos Efeitos dos Fatores Principais Figura 3. Gráfico dos Efeitos das Interações Tabela III R ESUMO DO TESTE DE HIPÓTESE REALIZADO ANOVA para o tempo de fervura Source MATERIAL SISTEMA SOLUÇÃO MATERIAL*SISTEMA MATERIAL*SOLUÇÃO SISTEMA*SOLUÇÃO MATERIAL*SISTEMA*SOLUÇÃO Error Total DF 1 1 6 1 6 6 6 84 111 Seq SS 135,1 125357,2 4122,8 182,6 1343,2 2370,6 2161,7 15950,2 151623,5 Adj SS 135,1 125357,2 4122,8 182,6 1343,2 2370,6 2161,7 15950,2 Adj MS 135,1 125357,2 687,1 182,6 223,9 395,1 360,3 189,9 F 0,71 660,18 3,62 0,96 1,18 2,08 1,90 Valor-p P 0,401 0,000 0,003 0,330 0,325 0,064 0,091 As figuras abaixo fornecem uma análise mais detalhada dos resultados obtidos. A Figura 3 indica os fatores que mais tem efeito na resposta. De acordo com a figura podemos ver que os fatores Sistema e Solução apresentam efeitos significativos. A Figura 1 indica que não existem distorções ou tendenciosidades na distribuição dos resíduos produzidos que invalidem a premissa de probabilidade normal do modelo. As Figuras 4 e 5 indicam respectivamente, a independência do modelo e a premissa de igualdade de variância. Figura 4. Figura 5. Figura 1. Independência Homoscedasticidade Gráfico dos Resíduos A Figura 6 apresenta o teste de homocedasticidade dos fatores analisados. De acordo com a figura, pode-se ver que as variâncias são homogêneas. Figura 6. Teste de homogeneidade de variâncias (homoscedasticidade) IV. C ONCLUSÃO Este trabalho descreveu um experimento com três fatores para a investigação da influência desses fatores em alterações no tempo de ebulição da água. Neste experimento foi utilizado um planejamento fatorial generalizado e o teste utilizado foi o ANOVA que utiliza internamente um teste estatístico do tipo F. Os resultados obtidos pela ANOVA, à uma taxa de significância de α = 0.05, confirmam que os fatores Sistema e Solução podem ser considerados significativamente influentes no tempo de ebulição da água. R EFERÊNCIAS [1] Campelo, F. Notas de aula da disciplina de planejamento e análise de experimentos, 2012, Programa de Pós Graduação em Engenharia Elétrica - UFMG. [2] MONTGOMERY, Douglas C. Design and analysis of experiments, John Wiley & Sons Inc, 2009. [3] MONTGOMERY, Douglas C.; RUNGER, George C; CALADO, Verônica. Estatística aplicada e probabilidade para engenheiros, 4.ed. Rio de Janeiro: LTC, 2009. [4] Masterton, Slowinski, Stanitski Princípios de Química, Sexta edição, Editora Guanabara Koogan S.A. ? Rio de Janeiro .
Download