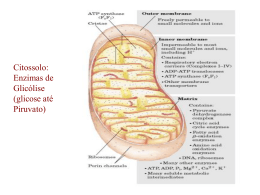
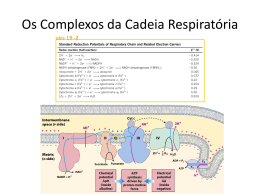
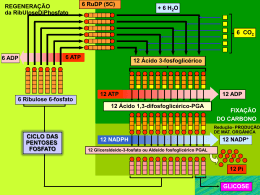
Fosforilação Oxidativa A respiração celular Fase aeróbica do catabolismo de carboidratos, lipideos, proteinas Ao nível macroscópico, a respiração se refere as trocas gasosas entre um organismo multicelular e seus meio ambiente (O2 consumido e CO2 produzido) 2 ADP 1 2 ATP 2 Piruvato Glicose HK Mitocôndria Citosol Rendimento de ATP pela oxidação incompleta da Glicose Apenas uma pequena parte da energia está aproveitada durante a glicólise (2ATP) Rendimento de ATP pela oxidação completa da Glicose O resto da energia (cerca de 90%) é obtida pela oxidação completa do piruvato pelo oxigênio via oxidação das coenzimas da cadeia respiratória. Nas três etapas de oxidação de glicose, os elétrons são poduzidos por desidrogenases que utilizam como coenzimas NAD+ ou FAD. “A oxidação de NADH está associada ao consumo de O2” Lehninger DPNH2 = NADH + H+ DPN = NAD+ Além disso há muito tempo era conhecido um pigmento que também estava associado ao consumo de O2 Inglaterra, Final do século XIX - MacMunn Reduzido – 4 bandas de absorção Oxidado – Nenhuma banda Pigmentos respiratórios Miohematina Histohematina em músculos e outros tecidos (hematina intracelular) Microespectrofotometro de Keilin 1889, Hop Seiler – pigmentos de MacMunn eram contaminantes derivados da hemoglobina … 1920 - David Keilin Presença ampla dos pigmentos de MacMunn na natureza Insetos (músculos torácicos de mosca (Gasterophilus) vermes, plantas, leveduras, tecidos humanos, etc … Citocromos ! Proteínas com heme como grupo prostético Evidências... Havia uma organela na célula que era capaz de oxidar os NADH’s e FADH2 do ciclo de Krebs. Nesta mesma fração celular existiam uns pigmentos (citocromos) que eram descritos como respiratórios. E que isso rendia ainda mais ATP que na via glicolítica. Rendimento de ATP pela oxidação completa da Glicose Potencial de redução (E°’) Permite prever o movimento de elétrons entre diferentes compostos. Quando as substâncias estão conectadas por um fio de metal em um circuito elétrico os elétrons fluem da substância com o potencial de redução mais baixo para o com o potencial de redução mais alto TABELA DE E°’ (Volts) Variação no potencial de redução e variação de energia livre A mitocôndria... Membrana interna Impermeável a maioria das pequenas moléculas e íons, incluindo H+. Componentes: Cadeia respiratória ADP-ATP trocador ATP sintase Outros transportadores Membrana externa Complexo piruvato desidrogenase Enzimas do ciclo de krebs Oxidação de ácidos graxos e aminoacidos ATP, ADP, Mg++, Ca++, K+ Permeável a íons e pequenas moléculas Mitocôndria de músculo de vôo de inseto Renata Gonçalves Mitocôndria de fígado de mamíferos Mecanismos de transporte – Translocadores e Sistemas de lançadeira A membrana interna da mitocôndria, ao contrário da membrana externa (10 – 15000 daltons), é impermeável a compostos com carga elétrica e íons inclusive a coenzima NADH/NAD+ e acetilCoA. Existem sistemas transportadores na membrana interna para garantir o transporte e o acesso de metabólitos à matriz mitocôndria. ADP ATP Pi Acidos dicarboxilicos (malato, succinato e fumarato, ...) Acidos tricarboxilicos (Citrato ou isocitrato) piruvato glutamato OHPi ou Acidos dicarboxilicos Malato Malato aspartato 2Na+ Ca++ Ca++ ATP/ADP translocase: a mais abondante na mb: representa 15% do conteudo proteico total da mb interna da mitocôndria Como a membrana interna da mitocôndria é impermeável a NADH e NAD+, a oxidação destes compostos não pode ser feita diretamente pela cadeia de transporte de elétrons. Os elétrons são transferidos para um composto citosólico, que transporta os elétrons na matriz mitocondrial, onde é oxidado. O composto oxidado retorna ao cistosol, permitindo a continuidade do processo. Sistema de Lançadeira. Existe diferente tipos de lançadeira. Existe assim um “pool” mitocondrial de NADH e um pool cistosólico de NADH Lançadeira Malato-Aspartato Lançadeira glicerol 3 fosfato Essência da fosforilação oxidativa 50 NADH 12,4 kcal/mol -0.2 Eo´ (volts) FMN 0.0 40 CoQ b 30 9,2 kcal/mol +0.2 c1 c a3 20 +0.4 +0.6 +0.8 24,8 kcal/mol 10 O2 0 Go´ (kcal/mol relative to O2) -0.4 As diferentes coenzimas da CR têm um E° que vai crescente durante o processo de transferência de elétrons, o O2 sendo o aceptor terminal de elétrons Complexo I NADH : ubiquinona oxidoredutase Complexo II Succinato desidrogenase Complexo III Ubiquinona:citocromo c oxidoredutase Complexo III e o ciclo Q Dois e- a partir de QH2 reduzem 2 moléculas de citocromo c.e 4 H+ são translocados para o espaço intermembranoso: dois do QH2 na primeira volta do ciclo e dois do QH2 na segunda volta Complexo IV ROS- Espécies reativas de oxigênio Doenças que podem ser vinculadas a lesão por ROS ATP sintase F1Fo-ATP sintase estator rotor Microscopia crioeletrônica Teoria quimiosmótica de Mitchell Transporte exergônico de H+ acoplado a síntese endergônica de ATP A F1Fo ATP sintase converte parte da energia quimiosmótica em trabalho mecânico Desacopladores O desacoplamento ocorre principalmente no tecido adiposo marrom Rato Inibidores da cadeia transportadora de elétrons Regulação da via de produção de ATP FO regulada pela disponilidade de Substratos
Baixar