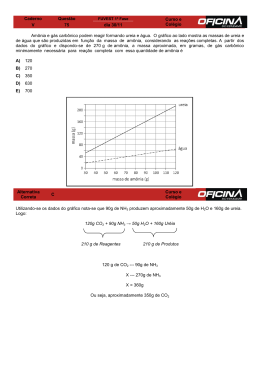
Comentários de Química UPE – Seriado 1.º ano Professores: Otávio Santos Jr. e Tatiana Marques. Apesar do extenso conteúdo de Química, a comissão decidiu por uma prova em que assuntos relacionados ao meio ambiente fossem priorizados, deixando à margem os clássicos: tabela periódica e funções inorgânicas, entre outros. Fica o registro da questão 27, sobre hibridação, cujo conteúdo não é especificado no programa, mesmo entendendo que o tópico possa ser abordado em ligações químicas. A total ausência de gráficos e tabelas também foi motivo de preocupação, haja vista que o domínio dessa habilidade é de extrema importância. Contestamos a questão 29, não no seu conteúdo, mas na ferramenta utilizada para sua resolução, pois exige do candidato o conhecimento do volume da esfera, tópico este que só será trabalhado na 2.ª série do ensino médio. Destacamos a questão 28 que conseguiu relacionar uma situação do cotidiano com a teoria da polaridade, número de oxidação (Nox) e reações químicas, além de abordar as propriedades e a aplicação da amônia (NH3). Resoluções Professores: Tatiana Marques e Otavio 25) Resposta: “c” “A destilação fracionada é um processo de separação de mistura homogênea de líquido com líquido. No caso da separação das frações do petróleo na torre de fracionamento, esta se fundamenta na diferença de temperatura de ebulição das frações separadas. 26) Resposta: “d” dA = 4 g/ml VA = 80 ml MA = dA.vA MA = 80.4 d mistura = 320g > dB = 5ml VB = 120 ml mB = dB.vB mB = 5.120 mB = 600g d mistura = 4,6 g/ml d = 7,8 g/ml logo, se a esfera for de: d = 2,7 g/ml flutuará na mistura d d = 1,7 g/ml = afundará na mistura flutuará na mistura = 8,9 g/ml afundará na mistura 27) Resposta: C2H4 + H2 H (2H6 (g) H | | H – C = C – H + H2 H H | | H–C–C–H | | H H sp3 Pd 150ºC 2 sp a) (Falsa) Sofrem alterações nos estados híbridos de sp2 para sp3. b) (Falso) Ambos os átomos de carbono sofrem alterações. No eteno (sp2), no etano (sp3) c) Verdadeiro. d) (Falso) Variam no estado de oxidação na hibridação, +1 +1 H H 2 | 2 +1 | +1 H–C=C–H (eteno) e) (Falso) eteno (sp2) etano (sp3) H+1 H+1 3 | 3 +1 +1 | H–C–C–H | | +1 +1 H H 28) Resposta: NH3 (amônia) a) “(Falsa) Apesar de ser uma substância gasosa como diz a afirmativa não é apolar e nem insolúvel em água, ao contrário é uma substância polar e solúvel em NH3 NH4OH” b) “(Falso) Apesar da amônia reagir com água formando o hidróxido de amônia não é uma substância de grande estabilidade como diz a afirmativa.” -3+1= +3 c) NH3 amônia +1 (NH4) (N03)-1 – sais de amônio -3+1= -14 (NH4) (Verdadeiro) em ambos os casos, ou seja, na amônia o nox do nitrogênio é (-3) e nos sais de amônio ele apresenta nox Υ(-3). d) (Falso) Nas condições citadas no texto, a NH3 reage com o gás oxigênio sendo dessa forma inflamável. Lembrar que para ser inflamável faz-se necessária a combustão e para isso é inevitável a presença do gás oxigênio. e) (Falso) Não é um solvente tão diferente, por exemplo, podemos afirmar que ambos são polares. 29) resposta: “e” Liga metálica (M) – MM = 40g lmol d = 5g/cm3 V = 68,1 m = d. Vesfera M = 160g m = 5.32 R = 2cm => V = V= . M (D) + 2 HC (aq) MC (aq) +VH=2(g) V =2 4.8 32cm3 160g 68,1 N= => n = 4 mols 3 mols N = 4 mols, logo existe 1 mol de exesso. 30) I II 0 0 Os países que utilizam combustíveis fósseis liberam CO2, gás do efeito estufa. 1 1 O principal poluente da indústria da celulose, utilizado no branqueamento do papel é o SO2, poluente secundário e incolor. Assim sendo, torna-se falsa a preposição. Processo kraft 2 2 O CO forma ligação estável com a hemoglobina impedindo que ela se combine com o gás oxigênio que será transportado para todo o corpo. Sendo assim, é possível a perda de reflexo e as tonturas como diz a afirmativa. 3 3 A decomposição anaeróbica de materiais orgânicos gera CH4, metano. E o H2S não influi na chuva ácida. 4 4 Os esgotos industriais são responsáveis pela poluição dos mananciais aquáticos e infelizmente, nos resíduos indesejáveis, não são 100% tratados pela indústria brasileira.
Baixar