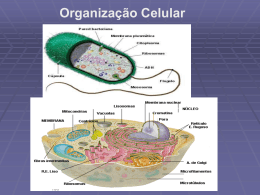
Controle e Regulação Princípios de feedback e Homeostase = constância de variáveis fisiológicas vitais. Variáveis reguladas = mantidas constantes ou quase constantes. Ex.: Tb nos homeotermos, glucose sangüínea etc Variáveis controladas = servem para manter a constância de uma variável regulada. Ex.: tx de sudorese, tx de glicogenólise, etc. Podem flutuar bastante. Mecanismos de regulação: 1. Feedback negativo: corrige na direção oposta do desvio do ponto de ajuste (os desvios são autocorretivos) 2. Feedforward ou alimentação antecipada= ação tomada para corrigir um desvio antes do desvio acontecer. Ex.:salivar antes de comer. Teoria do Controle a. 1. 2. 3. On-off termostato aquecedor ligado/ desligado temperatura oscila ao redor do ponto de ajuste b. 1. 2. 3. 4. Controle Proporcional muda em proporção ao tamanho do desvio muitas vezes em situações de fluxo tanque da descarga sanitária se o fluxo se modifica, o ponto de ajuste se modifica regulação da resp. pelo CO2 arterial 5. c. 1. 2. 3. d. 1. 2. Controle Derivado ou Controle de taxa muda em proporção à taxa do desvio pode responder a mudanças rápidas normalmente combinado com outros sistemas de controle Controle Integral muda em proporcão à integral do controle pode lidar com erros diminutos que surgem lentamente. Uso de Diagramas de Bloco Representações de uma junção de somação, mostrando a ação de variáveis controladas sobre uma variável regulada. Utilizados para se compreender circuitos complexos, quebrandos-os em blocos menores. Cada bloco realiza uma função particular e o diagrama mostra como estão conectados entre si. Ex.: O resultado Y é dado pela soma dos sinais de alimentação A, B e C( cada variável é uma seta) C ↓+ A+ + Y ↑+ B Modelo Simplificado da Regulação da [glucose]EC pelo controle da tx de secreção de insulina Regulação da [glucose] extracelular (Modelos para prever peformances do sistema biológico real em resposta a uma infusão constante de solução de glucose) Bloco 1 – junção de somação, na qual a taxa de entrada de glucose é subtraída da taxa de transporte de glucose para as células = taxa de mudança de [glucose]. Bloco 2 – integra esta taxa p/ dar a quantidade total de glucose extracelular. Bloco 3 – divide esta pelo volume do fluido extracelular a fim de obter a [glucose] extracelular. Bloco 4 – caixa de função, onde o gráfico mostra a relação entre a entrada, a [glucose] extracelular e a saída, taxa de secreção de insulina. Regulação da [glucose] extracelular- cont. Bloco 5 – calcula a taxa líquida de entrada da insulina no fluido extracelular = taxa de mudança da insulina = taxa de secreção de insulina – taxa de destruição da insulina. Bloco 6 – integra esta taxa líquida a fim de obter a quantidade total de insulina. A taxa de destruição da insulina é dada pela constante k x insulina total. Bloco 7 – realiza esse cálculo. Bloco 8 – calcula a [insulina], dividindo a insulina total pelo volume do fluido extracelular. Bloco 9 – completa o circuito; o gráfico dentro dessa caixa de função relaciona transporte de glucose para as células com a [insulina] extracelular. Regulação da [glucose] extracelular Regulação em Bactérias Nervos e Sistemas Nervosos Estrutura das células Nervosas 1. Neurônios: componentes básicos de todos os SN, variedade de formas e tamanhos porém c/ algumas características comuns = um corpo celular (ver., < 0,1mm diam) q contém o nu e mtas fibras finas (<0,01mm de espessura); ocorre no SNC formando agregados =gânglios, e nos órgãos sensoriais. 2. Cada neurônio tem um axônio (vários m no animal grande) + grande no. de fibras curtas (dendritos), altamente ramificados (< 1mm e compr.). 3. Um SN complexo tem imenso no. de neurônios. Ex.: cérebro humano: 10 Bilhões. Estrutura da Célula Nervosa Partes Funcionalmente mais importantes: 1.Axônio: principais linhas condutoras; maioria Mede de 1-10μm em diam; os da lula , 1000 μm. Um nervo consiste de 100’s ou 1000’s de ax, cada um se originando de um neurônio. 2. Sinapses: ponto onde neurônios e suas extensões fazem contato com outros neurônios. Um neurônio pode se conectar com 10’s de outros neurônos. Funcioa como uma válvula uniDirecional. Como os Neurônios funcionam Um impulso nervoso é uma correte elétrica que viaja ao longo de dentritos ou axônios devido ao movimento de íons através de canais com portões de voltagem na mambrana plasmática dos neurônios. Os canais de portão de voltagem abrem e fecham em resposta a uma voltagem elétrica, de tal maneira que são afetados por mudanças na carga elétrica ao redor deles. Quando um neurônio está “em repouso”, uma diferença de carga é mantida entre o lado de dentro e o lado de fora da célula. Esta diferença de carga é produzida e mantida amplamente por transporte ativo utilizando bombas de Na+ e K+. As bombas enviam Na+ para fora da célula e trazem íons K+ para dentro. Enquanto outros canais permitem algum fluxo de íons de K+ de volta para célula, os íons Na+ não podem voltar facilmente para dentro e assim, substituir as cargas positivas perdidas. O resultado final é que o exterior das células possui uma carga líquida positiva e o interior possui carga líquida negativa. Potencial de Repouso da Membrana Diferença de carga entre o interior e o exterior da célula Geração de um Impulso Nervoso Um impulso nervoso se inicia quando um estímulo perturba a membrana plasmática de um dendrito, fazendo os canais de Na+ se abrirem. Os íons de Na+ fluem para a célula, diminuindo a diferença de carga naquele local. Se a mudança for o suficiente, fará com que os canais de Na+ da vizinhança se abram. Vídeo: Potencial de ação Potencial de Ação da Membrana (PA) Isto permite muitos íons Na+ entrarem na célula naquele local, que a membrana lá fica “despolarizada” com a região local, o interior da célula com uma carga líquida positiva e o exterior com carga líquida negativa. Isto afeta os canais com portão de voltagem de Na+ da vizinhança, que, então se abrem, movendo a despolarização ao longo da membrana (PA) Repolarização da Membrana Mudanças na região antes do potencial de ação para restaurar o potencial de repouso (PR), os canais com portão de voltagem de sódio fecham e os canais com portão de voltagem do K+ se abrem. Isto permite um fluxo rápido de íons K para fora da célula, “repolarizando” a membrana de tal maneira que o interior fica novamente com carga líquida negativa e o exterior com carga líquida positiva. Seguem-se as bombas de Na-K para restaurar completamente o potencial de repouso da membrana e re-estabelecer a concentração apropriada dos íons Na+ e K+ dentro e fora da célula. Diagrama de um Neurônio Como calcular a diferença de potencial Usando as leis da físico-química. A diferença de potencial é causada pela distribuição desigual nos dois lados. Descrito pela Equação de Nernst E= RT/F loge [K]f / [K]d Em eletroquimica esta equação dá o potenial de eletrodo (E), em relação ao potencial de eletrodo padrão (Eo), das meias-células de uma bateria. Em fisiologia, esta equação é usada para descobrirmos o potencial elétrico da membana de uma célula em relação a um tipo de íon. E = Potencial elétrico R = constante universal dos gases [constante física que relaciona a quantidade de um gás (número de moléculas) com a pressão e a temperatura]. F = constante de Faraday = carga carreada por 1 equivalente de íons [K] = conc de K, dentro e fora da célula À temp ambiente, os valores de R e T são tais que: Ek = 25 loge [K]f / [K]d mV = 58 log10[K]f / [K]d= 75mV, com o lado de dentro negativo em relação ao de fora. [K]f / [K]d = 1:20 Como medir o Potencial de membrana • Inserindo um microeletrodo no axônio e lendo o potencial relativo ao lado de fora. • O valor assim observado é próximo daquele calculado, um pouco menor (-60 a -70mV). Como demonstrar que o PM é causado pelo gradiente de potássio Mudando a razão entre [K]d Qdo Kf é alto o pot responde como previsto pela equação de Nernst, porém qdo Kf é baixo, o potencial observado desvia daquele previsto pela Equação de Nernst. O que isso pode significar? Que a presença de outros íons deve ser considerada. Contribuição de Goldman para explicar essa diferença entre pot observado e pot calculado: E = RT/F ln PK [K]f + PNa[Na]f + PCl [Cl]f Se PNa fosse 0,01 da PK, a eq de Goldman prevê um PM a [K]f que corresponde aos pontos realmente observados. Experimento para demontrar que o elemento essencial era a integridade da membrana e não a composição do axoplasma 1. 2. Baker et al., 1962 – removeu o conteúdo do axoplasma e substituiu por solução salina artifiial (Fig. 11.7) o axônio se comportou como axônio normal; pôde ficar excitável por muits horase capaz de dar 100’de PA. Conclusões: O axoplasma não possui nenhum elemento estrutural necessário para gerar PM; pôde ser substituído por solução artificial; Se o Kd for diferente do normal, o PM muda como previsto pelas equações, e se Kd=Kf, o PR é abolido; o PM pode mesmo ser revertido fazendo a [K]d < [K]f O que aconteceria com o PM se a PNa fosse aumentada O grad de conc e o PM puxaria Na+ pra dentro tornando o lado de dentro positivo até que o potencial evite mais Na entrar. O PM seria de acordo com a eq de Nernst +55mV (dentro +). Assim, a membrana passou de um PM de 70mV (pot do K) para +55mV (pot do Na). O PM pode se alterar 125mV, meramente aterando-se as permeabilidades relativas ao Na e K = Pot Ação (PA) Vídeo Bomba de sódio Papel da Bomba de Sódio • O Na que entrou na célula qdo a PNa estava alta deve ser removido p/ manter o sistema funcionando Normalmente = TA. • Esta qt de Na pode ser calculada a partir de considerações teóricas ou medida experimentalmente: • o axônio é submerso em água do mar com 24Na estimula-se repetidamente o axônio p/ produzir PA Os Na+ entram no ax e o lado de dentro se torna radioativo após cessar o estímulo, o ax fica em repouso, o Na é removido lentamente do lado de dentro. Como demonstrar que a saída de Na é através de Transporte Ativo Envenena-se a bomba de sódio com dinitrofenol (DNP) cessa a saída do Na e a [Na]d pemanece constante após outra estimulação, mais Na entra, mostrando que o PA e a entrada de Na estão acoplados. Outra demonstração: Injeta-se 24Na em axônio gigante através de microtubos de vidro o ax é colocado em volume conhecido de água do mar a tx na qual o 24Na deixa o ax é medida se o ax for envenenado com DNP , a tx de saída do Na cai drasticamente DNP interfere com o proc de resp que fornece ATP, o requerimento da bomba de sódio Se ATP for adicionado ao ax, haverá aumento transitório na tx de saída do Na. Universalidade da Bomba de Sódio Todas as células possuem bomba de sódio Na-K-ATPase = grande proteína (120kDa com subuniades de 35kDa) Mantém a [Na]IC baixa e [K]IC alta É crucial para todos os órgãos, mas especialmente para o tecido nervoso e o cérebro. A hidrólise do ATP coloca o Na+ para fora da célula e o K+ para dentro. Localização da bomba de sódio Uso do glicosídeo ouabaína marcado com 3H. Este glicosídeo inibe a Na-K-ATPase, se ligando ao sítio ativo da bomba. Axônios de lula possui 1000’s de bombas/μm2. Na,K-ATPase Canais e Portões • Durante o PA os íons fluem através da membr. graças aos gradientes de concentração. • Esses movimentos são auxiliados por proteínas de transporte específicas da membr celular lipídica, q formam canais através dos quais solutos podem ser transportados por simples difusão. • Alguns canais ficam continuamente abertos; outros abrem transitoriamente = canais com portões (de voltagem, em resposta a mudanças no PM; portões ligantes, em resposta a um agente externo, um ligante. Canais de Na e K Baiacu Durante um PA, Na e K se movimentam em direções opostas, utilizando canais diferentes. Demonstração? Uso do veneno do peixe baiacu – alcalóide tetrodotoxina (TTX)- bloqueia o canal com portão de voltagem para o Na, enquanto deixa os de K inafetado. Tetrametil amônio (TEA) Um outro veneno- tetrametil amônio (TEA) bloqueia os canais de K enquanto deixa os de Na inafetados. É possível estudar experimentalmente o fluxo de íons Na, sem inteferência dos íons K, que se movimentam no sentido oposto. Pode-se medir a qt de Na que circula através da membrana pela medida da corrente elétrica gerada pelo fluxo iônico. Seqüência de Eventos na Propagação do PA 1. 2. 3. 4. 5. 6. Um ponto do axônio sofre despolarização Os portões de Na se abrem Entram na célula e mudam o PM A área adjacente se despolariza parcialmente Os canais se abrem e o Na entra e despolariza completamente a membrana. Os canais de K se abrem mais lentamente. Potencial de Ação A Função de Canais com Portões de Voltagem Insetos que se alimentam de plantas pobres em Sódio conseguem ter PA similares àqueles dos demais animais? O SN dos insetos é circundado por uma bainha nervosa, que separa o nervo do contato imediato com o FEC. Essa bainha consiste de uma camada não celular externa + membrana interna (perineurium)camada única de células especializadas. A bainha age como uma barreira que separa a superfície do axônio da hemolinfa e assim, restringe o movimento de materiais entre a hemolinfa e o fluido nas superfícies neuronais. O Na+ nessas superfícies pode ter uma ordem de magnitude maior do que aquela da hemolinfa. A [Na+] é mantida nas superf neuronais provavelmente através de uma bomba de Na+. Velocidade da Condução Nervosa Velocidade = k√ d o tamanho dos PA é similar entre os animais, porém, a velocidade de condução varia de nervo p/ nervo e de animal para animal. A constância de proporcionalidde k varia tb dentre os animais. Os axônios dos vertebrados possuem alta velocidade de condução porque são recobertos por uma fina camada de mielina (formada pelas células gliais de sustentação), que é interrompida a intervalos curtos, expondo a membrana nervosa (nódulos de Ranvier). Tabela. Velocidade de condução (m.s-1) em nervos de vários animais Fatores que interferem com a velocidade da condução nervosa Mielinização + grande diâmetro = a distância entre os nódulos de Ranvier aumenta com o diâmetro do axônio. Como o retardo da condução ocorre nesses nódulos, um menor número de nódulos nos axônios maiores permite ma propagação mais rápida do PA. Mielinização + Diâmetros muito pequenos (< 1μm) Fibras mielinizadas velocidade = k.d Fibras não-mielinizadas Velocidade = k√ d Importante consequência: para diam muito pequenos (<1μm), os axônios melinizados conduzem mais lentamente do que os nãomielinizados = coincide com o limite mínimo p/ o tamanho real das fbras mielinizadas no organismo, que nunca é menor do que 1μm em diam.(Fig.11.13). Velocidade de Condução x Mielinização x Diâmetro • Grande vantagem das fibras Mielinizadas: seu tamanho pequeno, que permite um SN complexo, com altas velocidades de condução, sem espaço indevidamente ocupado pelos condutores. • Se quiséssemos aumentar 10X a velocidade de condução em uma fibra NM necessitaríamos de um aumento de 100X no diam, e volume do nervo/unidade de compprimento seria aumentado 10.000X. Invertebrads com múltiplas camadas de Mielina Alguns invertebrados (insetos, minhocas, caranguejos e camarões) possuem fibras nervosas cobertas com múltiplas camadas de mielina similares à mielinização dos nervos dos vertebrados. A velocidade de condução dessas fibras é bem maior do que aquela das fibras não mielinizadas de diâmetro similar. Ex.: Palaemonetes vulgaris – diâm = 26µm v = 18-23 m s –1, bem mais rápida do que em outros nervos de diâm similar, porém não tão alta quanto a velocidade da condução nos nervos mielinizados dos vertebrados. Múltiplas Camadas de Mielina 1) 2) As camadas são arranjadas mais frouxamente Há um espaço EC entre a camada interna da bainha e o axônio. Assim, menos membranas estão presentes em uma bainha de camarão de uma dada espessura do que na bainha de mielina de fibras de vertebrados da mesma espessura. 3) Os espaços formam um reservatório para íons que aumenta a capacitância da bainha nervosa = Explicação para terem veloc menor do que a dos vertebrados. 4) O espaçamento entre os nódulos é menor e, como o retardo da veloc. da condução está nos nódulos, o maior número de nódulos explica a menor velocidade de condução. Sinapses: Inibição, Excitação e Computação Como a informação é transferida de um neurônio para outro? A transmissão de sinais nas sinapses é de dois tipos distintos: elétrica ou química. Sinapses Elétricas (menos difundidas que as sinapses químicas): demonstradas em lagostim, vários artrópodes, anelídeos, celenterados e moluscos. Nas SE a extremidade de um axônio fica tão próxima da membrana do próximo neurônio que há continuidade elétrica entre o interior do axônio e o próximo neurônio – junções gap (2nm) – esse espaço forma um caminho de baixa resistência que fornece um desvio para a corrente fluir do terminal do axônio para a próxima célula. Sinapses Elétricas Além da rota de baixa resistência entre o interior de um neurônio e o próximo, a transmissão elétrica também requer uma alta resistência que evita vazamento lateral da corrente no ponto de contato. Muitas sinapses elétricas permitem os impulsos serem conduzidos em ambas as direções, porém outras permitem a corrente fluir somente do ponto présináptico para o pós-sináptico, como as sinapses químicas. Sinapse Química Os potenciais de ação ao chegar no terminal présináptico fazem com que os canais com portão de voltagem de Ca++ se abram. Os íons Ca++ se difundem para dentro da célula e fazem com que as vesículas liberem acetilcolina (neurotransmissor) As moléculas de Acetilcolina se difundem do terminal pré-sináptico para a fenda sináptica e se ligam aos sítios receptores nos canais de Na+ com portão de ligante. Os canais de Na+ com portões ligantes se abrem e os íons Na+ se difundem para o interior da célula, tornando o potencial de membrana mais positivo. Se o potencial de membrana atingir o nível , um potencial de ação será produzido. Sinapses Químicas O terminal do axônio forma o botão sináptico (estrutura pré-sináptica), que faz contato com um dendrito ou corpo celular de outro neurônio (estrutura póssináptica) fenda sináptica (20nm). Botão sináptico: contém um grande número de vesículas (20-100nm de diâmetro). Exceto quando a velocidade for muito importante a transmissão química parece ser superior. A grande vantagem está na duração = permite integração por períodos mais longos. A transmissão de um impulso do botão présináptico para o neurônio pós-sináptico ocorre através da liberação de neurotransmissores armazenados nas vesículas [adrenalina, dopamina, acetil-colina, GABA, serotonina, ácido glutâmico, noradrenalina]. Sinapse Quimica Transmissão de um Impulso O impulso chega no botão pre-sináptico a mudança no PM permite os íons Ca++ fluir para o terminal (passam por canais de Ca normalmente fechados, mas que se abrem em resposta a mudança na voltagem) a elevação na [Ca] (extremamente breve) afeta as vesículas, que se fundem com a membrana pré-sináptica e libera o neurotransmissor [na junção NM cerca de 300 vesículas são liberadas para cada impulso nervoso]. Transmissão de impulso na junção NM Cada vesícula contém cerca de 10.000 moléculas de acetilcolina, que rapidamente se difunde através da fenda sináptica para a membrana pós-sináptica [pequena distância – pequena fração do milisegundo = mais lento que a sinapse elétrica]. Na membrana pós-sináptica as moléculas de acetilcolina se ligam a receptores [proteínas constituintes da membrana pós-sináptica que formam canais normalmente fechados, mas abertos em resposta à acetilcolina e assim permitem Na e K fluir]. Cada canal requer 2 moléculas de acetilcolina para abrir; fica aberto por curto período qdo 20.000 Na e K fluem através do canal antes de fechar. Como resultado do movimento de íons, a diferença de potencial através da membrana é reduzida, aproximando-se de zero. Tem sido estimado que um único neurônio possui 10.000 conexões sinápticas Há mais sinapses no cérebro humano do que estrelas no Universo conhecido. Sinapses no Cérebro As sinapses no cérebro diferem de tal maneira que a ação da mesma substância pode ser excitatória em algumas sinapses e inibitória em outras. Métodos de registros elétricos permitiram a compreensão da transmissão sináptica – pipetas finíssimas de vidro (<1 µm de diâmetro) são preenchidas com solução salina, fazendo microeletrodos que podem ser usados para registrar qlqr mudança de potencial. Qdo 1 impulso chega na membrana présináptica, há um retardo de 1 fração de ms antes de ocorrer mudança no potencial da membrana pós-sináptica = potencial póssináptico = PSP sobe rapidamente decai a uma velocidade menor. Sinapses no Cérebro (cont.) a) b) a) Os PSP diferem dos PA em 2 aspectos: são menores em amplitude duram mais (10 a 100x). Conseqüências: um único PSP raramente é suficiente para causar um PA no neurônio pós-sináptico. b) a longa duração permite interações com outros PSPs no mesmo neurônio, na mesma sinapse e em sinapses vizinhas. O que causa o Potencial PósSináptico (PSP)? Liberação do NT na membrana pré-sináptica, e o atraso corresponde à liberação do NT e o tempo de difusão através da fenda. Qdo o NT é degradado (enzimas) o PSP decai gradualmente. Se um segundo impulso chega no mesmo terminal do axônio antes do PSP precedente ter decaído, a qt do NT é aumentada e o PSP é maior = somação temporal. Sinapses no Cérebro (cont.) Se um impulso chega agora em outra sinapse dentro da mesma área, o novo PSP é adicionado ao potencial existente = somação espacial. Esses 2 tipos de somação formam a base da computações em cada neurônio e em todo o SN. Se muitos impulsos estimulatórios chegam em várias sinapses em um neurônio, uma combinação de somação temporal e espacial pode levar a PSP suficientemente grande para causar PA no axônio. Se o potencial de membrana póssináptico for ligeiramente diminuído ou despolarizado pelo PSP, a mudança é na direção de um PA = EPSP = potencial pós-sináptico excitatório. Sinapses no Cérebro (Cont.) Se o PSP causa um aumento no PM normal (hiperpolarização), seu efeito é na direção oposta= IPSP = potencial pós-sináptico inibitório (inibe a geração de um PA). O NT pode ser estimulatório ou inibitório (Figura 11.19) – um EPSP sozinho causa uma despolarização parcial na membrana póssináptica, e se a despolarização alcança o limiar, um PA completo é iniciado. Se um IPSP também chegar, a somação dos 2 impede a membrana de atingir o limiar para acontecer o PA. Figura 11.19 Inibição Pré-Sináptica Ocorre qdo uma fibra inibitória se conecta com um botão terminal de uma fibra excitatória (Figura 11.20). Um impulso na fibra inibitória causa hiperpolarização do botão excitatório. Como resultado, um impulso que agora chega no axônio excitatório causa menos liberação de NT e um PSP reduzido. As inibições pré-sinápticas são altamente seletivas, pois afetam somente sinais chegando em uma determinada sinapse. Já a inibição póssináptica trabalha subtraindo de todos os PSPs excitatórios que chegam no neurônio. Inibição Pré-Sináptica Fórmulas estruturais de alguns compostos conhecidos como neurotransmissores ou candidatos Noradrenalina Adrenalina Serotonina Dopamine Ácido Glutâmico GABA Estudar: A resposta a uma determinada substância depende do órgão-alvo e não da natureza da substância neurotransmissora.Ex. acetilcolina no músculo esquelético vs no coração. Figura 12.4-Principais aspectos da ação de NT no SN periférico de vertebrados. Dificuldades em se determinar se uma determinada substância é um NT Função normal dos receptores opiáceos específicos
Baixar