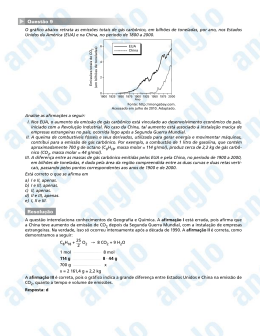
Questões / PAS 1a Etapa UnB PAS-1ª Etapa-2014 O problema da disponibilidade da água no Brasil ganha, mais uma vez, as manchetes. No início de 2014, após inundações catastróficas em parte do Sudeste e na área central do país, além da inundação secular que atingiu, por alguns meses, Rondônia, Acre e partes de Mato Grosso, a seca se abateu não no Nordeste, como historicamente acontece, mas no Sudeste. A escassez de água no sistema de represas da Cantareira, em São Paulo, criou cenários alarmantes para o abastecimento da capital e de sua região metropolitana. W. J. Junk, M. T. F. Piedade, E. Candotti. Água no Brasil, excesso, escassez e problemas crescentes. In: Revista Ciência Hoje, n.º 315, vol. 53, jun./2014 59. Na água, substância composta pelos elementos químicos oxigênio e hidrogênio, a proporção em massa do oxigênio é superior a 93%. Massa Molar da água, H2O: 18 g/mol Massa Molar do oxigênio, O: 16 g/mol 18 g --------- 100 % 16 g --------- x % x = 88,9 % (é inferior a 93%) ERRADO Considere a situação em que uma pessoa percorra, de bicicleta, uma distância em que seriam gastos, de automóvel, 3,0 L de gasolina constituída exclusivamente por iso-octano, cuja fórmula molecular é C8H18 e a densidade é igual a 0,69 g/mL. Considere, ainda, que a combustão completa desse combustível seja representada pela equação química abaixo, em que a, b, c e d são os coeficientes estequiométricos das espécies envolvidas. a C8H18(l) + b O2(g) c H2O(l) + d CO2(g) Com base nessas informações, julgue os itens subsequentes. 81. A menor soma de a, b, c e d que permite balancear corretamente a reação de combustão completa do iso-octano com números inteiros é igual a 30. 1 C8H18(l) + 25/2 O2(g) 9 H2O(l) + 8 CO2(g) 2 C8H18(l) + 25 O2(g) 18 H2O(l) + 16 CO2(g) ERRADO 80. Com a utilização da bicicleta, em vez do automóvel, e, portanto, sem queima da gasolina, deixa-se de emitir, para a atmosfera, mais de 5.000 g de CO2. Texto: V = 3,0 L C8H18 e a densidade é igual a 0,69 g/mL. 0,69 g ---------- 1 mL x g ---------- 3000 mL (3,0 L) x = 2.070 g Massa Molar C8H18 = 114 g/mol Massa Molar CO2 = 44 g/mol 2 C8H18(l) + 25 O2(g) 18 H2O(l) + 16 CO2(g) 2.114 g ----- 16.44 g (Massa Molar) 2070 g ------ x g x = 6.391,57 g CORRETO A elevação da temperatura média da Terra usualmente é atribuída ao aumento, na atmosfera terrestre, da concentração de CO2 decorrente da queima de combustíveis fósseis. Entretanto, alguns especialistas argumentam que a Terra já experimentou muitos ciclos de aquecimento (um a cada 100.000 anos, aproximadamente, todos acompanhados por aumento da concentração de CO2 na atmosfera. Controvérsias à parte, não se pode descartar a hipótese de que o CO2 produzido pelo homem contribua para intensificar o aquecimento global e o fato de que a emissão de CO2 é apenas um dos fatores negativos associados ao emprego dos combustíveis fósseis, o que torna necessário o estímulo ao emprego de fontes alternativas de energia. Considerando essas informações e o gráfico acima, julgue os itens a seguir 93. Considere um recipiente cúbico com arestas de 1,0 m e completamente preenchido por água. Considere, ainda, que a água contida nesse recipiente esteja sempre saturada com CO2, cujo comportamento da solubilidade é mostrado na figura apresentada. Nessas condições, se a temperatura da água contida no recipiente for aumentada de 10 ºC para 20 ºC, a massa de CO2 liberada para a atmosfera será superior a 1,0 kg. E 1,0 m3 = 1000 dm3 = 1000 L = 106 mL 10ºC: 0,22 g CO2 em 100 mL H2O 20ºC: 0,16 g CO2 em 100 mL H2O Diferença: 0,06 g CO2 em 100 mL H2O x g CO2 em 106 mL H2O x = 600 g CO2 Menor que 1,0 Kg CO2 ERRADO 94. Um dos efeitos nocivos ao meio ambiente causados pela queima dos combustíveis fósseis é o fenômeno conhecido como chuva ácida, que deriva, principalmente, da emissão de compostos de enxofre e nitrogênio, facilmente convertidos em ácidos quando em contato com a umidade do ar. CORRETO SO2 + H2O H2SO4 2 NO2 + H2O HNO2 + HNO3 Nos últimos anos, tem-se falado muito em “sequestro de carbono”, expressão que se refere à remoção de CO2 a partir de misturas de gases. Na natureza, a remoção do CO2 contido no ar atmosférico ocorre naturalmente, por meio da fotossíntese. Entretanto, metodologias têm sido desenvolvidas pelo homem para a separação do CO2 contido em misturas gasosas, para posterior reconversão do gás, por exemplo, em combustíveis líquidos. Essa separação pode ocorrer por criogenia ou por adsorção. Na criogenia, a mistura de gases, normalmente pressurizada, é resfriada gradativamente, de forma que os constituintes são separados com base na propriedade de condensarem em diferentes temperaturas. No processo por adsorção, utiliza-se um adsorvente (frequentemente, carvão ativado) que tenha a capacidade de adsorver seletivamente o CO2 em seus sítios ativos. Considerando essas informações, julgue os itens de 95 a 97, assinale a opção correta nos itens 98 e 99, que são do tipo C, e faça o que se pede no item 100 que é do tipo B. 95. Considere que, à pressão p, a temperatura de ebulição do CH4 e a do CO2 sejam iguais a -120 ºC e -40 ºC, respectivamente. Nessas condições, se uma amostra de gás natural constituída por CH4 e CO2, à pressão p, for gradualmente resfriada a partir da temperatura ambiente, o CH4 se condensará antes do CO2. E ERRADO - 40º C CO2 - 120º C CH4 96. Na separação de misturas gasosas, além dos métodos de separação por criogenia e por adsorção, pode ser utilizada a decantação. ERRADO Decantação: separa misturas heterogêneas e toda mistura gasosa é homogênea. 97. A soma das massas de CO2 e H2O consumidas durante o processo de fotossíntese é igual à soma das massas de O2 e de matéria orgânica produzidas no mesmo processo. CORRETO Está de acordo com a Lei da conservação de massa, de Lavoisier. 98. A reconversão do CO2 em combustíveis líquidos é um processo A. exotérmico, ou seja, com liberação de calor. B. endotérmico, ou seja, com liberação de calor. C. exotérmico, ou seja, com absorção de calor. D. endotérmico, ou seja, com absorção de calor. Como a queima de um combustível fóssil é exotérmica, a sua reação inversa será endotérmica, ou seja, trata-se de uma reação com absorção de energia. 99. A separação de gases por criogenia ou por adsorção são exemplos de processo A. físico, pois envolve a criação de novas substâncias. B. químico, pois envolve a criação de novas substâncias. C. físico, pois não envolve a criação de novas substâncias. D. químico, pois não envolve a criação de novas substâncias. Técnicas de separação de materiais são processos físicos, pois não há alteração da natureza da matéria (estrutura molecular). 100. Considerando que cada sítio ativo do carvão ativado seja responsável pela adsorção de uma molécula de CO2 e assumindo 6,0 × 1023 como o número de Avogadro, calcule o número de sítios ativos necessários para a adsorção de 88,0 g de CO2. Divida o valor obtido por 1023. Após efetuados todos os cálculos solicitados, despreze, para marcação no Caderno de Resposta, a parte fracionária do resultado final obtido, caso exista. Massa Molar do CO2 = 44g/mol 1 mol ------- 44 g ------- 6,0 x 1023 moléculas 88 g ------- x x = 12 x 1023 moléculas Multiplicando por 1023 resposta = 12 0 1 2 PAS-1ª Etapa-2013 O emprego da biomassa como fonte de energia gera um ciclo fechado de carbono, conforme ilustra a figura acima. Na fotossíntese, CO2 e H2O da atmosfera são convertidos em moléculas orgânicas constituintes da biomassa. A reação pode ser representada pela equação a seguir, que não está balanceada. CO2 + H2O + energia C6H12O6 + O2 Com base nessas informações e considerando que a densidade da água seja igual a 1,0 g/mL, julgue os itens de 53 a 59 e assinale a opção correta no item 60, que é do tipo C. 53. O emprego do carvão mineral e o da energia solar são formas de se obter energia sem afetar o ciclo do carbono. ERRADO. O carvão mineral utilizado como energia produz CO2. Somente do da energia solar. 55. É transferida entre os seres vivos na cadeia alimentar a energia que foi liberada na queima de petróleo ou de carvão mineral e ficou, por milhões de anos, fora de circulação. ERRADO. Não aumenta a captação e sim a produção do CO2. 58. Considere que os compostos CO2, H2O e C6H12O6 estejam, a 25ºC, nos estados gasoso, líquido e sólido, respectivamente. Nesse caso, apenas o C6H12O6 tem temperatura de fusão superior a 25 ºC e apenas o CO2 tem temperatura de ebulição inferior a 25ºC. CORRETO. 59. O volume de água necessário para a formação de 1,0 kg de C6H12O6 é superior a 700 mL. ERRADO. Massa molar: H2O = 18 g/mol Massa molar: C6H12O6 = 180 g/mol Reação: 6 CO2 + 6 H2O C6H12O6 + 6 O2 6 mols 1 mol 6.18 g x 1.180 g 1000g (1kg) x = 600 g d = 1,0 g/mL 1,0 g ----- 1mL 600 g ----- x x = 600 mL 60. Diferentemente do ciclo geológico, o ciclo biológico do carbono é relativamente rápido; estima-se que a renovação de carbono atmosférico ocorra de vinte em vinte anos. No ciclo biológico, o carbono é devolvido à atmosfera por meio da A. erupção de vulcões. B. produção de biomassa. orgânica. C. decomposição orgânica D. queima de combustíveis fósseis. Considere que o gás natural seja constituído exclusivamente de metano (CH4), e a gasolina, de isooctano (C8H18). Em condições padrão, o calor liberado na combustão de 1,0 mol de metano e na de 1,0 mol de gasolina, cujas equações estão representadas abaixo, é igual, respectivamente, a 75 kJ/mol e 255 kJ/mol. CH4(g) + 2 O2(g) CO2(g) + 2 H2O(l) C8H18(l) + 12,5 O2(g) 8 CO2(g) + 9 H2O(l) A partir dessas informações, julgue os itens subsequentes. 61. De acordo com o princípio de Avogadro, na combustão do metano, o volume de CO2(g) formado é superior ao volume de CH4(g) queimado, porque a massa molar do CO2 é maior que a massa molar do CH4. CH4(g) + 2 O2(g) CO2(g) + 2 H2O(l) 1 mol CH4 forma 1 mol de CO2 1 Volume de CH4 formam 1 Volumes de CO2 Independe da massa e sim do nº de mol ERRADO 62. Do ponto de vista ambiental, não é recomendada a conversão de um automóvel originalmente movido a gasolina em veículo movido a gás natural, porque ela resultará em aumento da liberação de CO2 por unidade de energia gerada. CH4 + 2 O2 CO2 + 2 H2O 1 mol CH4 forma 1 mols de CO2 -------- LIBERA 75 kcal C8H18 + 12,5 O2 8 CO2 + 9 H2O 1 mol C8H18 forma 8 mols de CO2 -------- LIBERA 255 kcal x mol CO2 ------------ 75 kcal x = 2,35 mols de CO2 Utilizando gasolina, forma-se mais quantidade de CO2 para liberar a mesma quantidade de energia. ERRADO O óleo pode ser separado da parte proteica da semente de girassol pela extração com solvente. O óleo bruto é submetido, posteriormente, ao processo de refino, por meio do qual se removem os ácidos graxos livres. Para isso, o óleo bruto é tratado com uma base, conforme indicado na equação química abaixo, em que RCOOH representa um ácido carboxílico de cadeia hidrocarbônica R. Como resultado dessa reação, são gerados sal e água, que formam, com o óleo, uma emulsão. RCOOH + NaOH RCOONa + H2O ácido sal A partir dessas informações e considerando que o ácido oleico e o sal resultante de sua neutralização (oleato de sódio) possuam massas molares iguais a 282,5 g/mol e 304,5 g/mol, respectivamente, e que a densidade do óleo bruto de girassol seja 0,90 g/mL, julgue o item 66, assinale a opção correta no item 67, que é do tipo C, e faça o que se pede no item 68, que é do tipo B. 66. Dado que a neutralização de um ácido é uma reação exotérmica, é conveniente, para serem minimizadas as variações de temperatura no interior da câmara de reação, envolver o sistema com uma resistência elétrica, o que possibilita a reposição da energia envolvida na reação. ERRADO Sendo a neutralização exotérmica, ao envolver o sistema com uma resistência elétrica, dificultará. 67. Para a separação do óleo bruto a partir do solvente utilizado na extração do girassol e para a separação do óleo a partir da emulsão formada durante seu refino, são, respectivamente, apropriadas A. a destilação e a centrifugação. centrifugação B. a filtração e a decantação. C. a decantação e a filtração. D. a centrifugação e a destilação. 68. Considerando a neutralização, com NaOH, de 1.000 L de uma amostra de óleo bruto de girassol que contém 0,020% em massa de ácido oleico, calcule, para a conversão de 100% do óleo, a massa do sal oleato de sódio, em gramas, que será obtida. Após efetuados todos os cálculos, despreze, para marcação no Caderno de Respostas, a parte fracionária do resultado final obtido, caso exista. Do texto: massas molares = 282,5 g/mol (ác. Oleico) e 304,5 g/mol (sal), densidade do óleo bruto de girassol = 0,90 g/mL, Cálculo da massa do óleo: densidade: 0,9 g ----- 1 mL x g ----- 106 mL (1000L) x = 9.105 g Cálculo da massa do óleo oleico: 9.105 g ----- 100 % x g ----- 0,02 % x = 180 g Cálculo da massa do sal formado: RCOOH + NaOH RCOONa + H2O 282,5 g -------------- 304,5 g 180 g ---------------- x g x = 194,01 g 194 A temperatura é um dos fatores que afetam o nível de oxigênio das águas, conforme mostra o gráfico acima, no qual está representada a curva da solubilidade do gás oxigênio (O2) na água, em função da temperatura. Considerando que, no intervalo de temperatura apresentado no gráfico, a densidade da água seja igual a 1,0 g/mL e que a concentração mínima de oxigênio que permite a vida de determinado organismo seja 1,3 × 10-4 mol/L, julgue os próximos itens. 69. Com o efeito estufa, a temperatura média na superfície terrestre aumenta e, portanto, a solubilidade do oxigênio na água diminui, o que pode ocasionar redução do nível de oxigenação de rios, lagos e oceanos. CERTO Pela análise do gráfico, verifica-se que a solubilidade do O2 diminui com o aumento da temperatura. 70. O número de moléculas em 1,8 mL de água pura, nas condições de temperatura indicadas no gráfico, é superior a 1,0 × 1022. Texto: Considerando que, no intervalo de temperatura apresentado no gráfico, a densidade da água seja igual a 1,0 g/mL e que a concentração mínima de oxigênio que permite a vida de determinado organismo seja 1,3 × 10-4 mol/L... 1,3.10-4 mol O2------- 1000 mL H2O (1 L) x mol O2 ------- 1,8 mL H2O x = 2,34 . 10-7 mol O2 1 mol O2 ------- 6.1023 moléculas 2,34 . 10-7 mols O2 ------- x x = 14,04 . 1016 moléculas O2 14,04 . 1016 > 1,0 . 1022 errado 72. Para uma solução aquosa saturada em oxigênio, a 40 ºC, a concentração de oxigênio é suficiente para permitir a vida do organismo em questão. À 40ºC, a solubilidade é 6,5 mg/L 6,5 mg O2 --------- 1 L H2O Transformando 6,5 mg em mols: 1 mol O2 --------- 32 g (Massa Molar) x ---------- 0,0065 g (6,5 mg) x = 0,208 mols O2 TEXTO: [...]a concentração mínima de oxigênio que permite a vida de determinado organismo seja 1,3 × 10-4 mol/L,[...] CERTO PAS-1ª Etapa-2012 Os processos I e II, indicados na figura acima, são necessários quando a biomassa é utilizada na geração de energia. Nos dois processos, a etapa de combustão resulta em pelo menos dois produtos: gás carbônico (CO2) e vapor de agua (H2O). Considerando esses dados e a fórmula do etanol (C2H5OH), julgue os itens a seguir. A massa molar do etanol corresponde a 46 g/mol. C2H5OH C = 12 x 2 = 24 H=1x6=6 O = 16 x 1 = 16 24 + 6 + 16 = 46 • No caso de combustão completa do etanol, a seguinte equação está de acordo com a lei de conservação das massas: C2H5OH(l) + O2(g) 2CO2(g) + 3H2O(g). Resposta: Errado Fazendo o balanceamento, temos: C2H5OH(l) + 3 O2(g) 2CO2(g) + 3H2O(g). Considere que, a partir de determinada biomassa, foram obtidas duas amostras de igual massa, uma pulverizada e outra em cavacos, as quais serão submetidas a etapa de combustão no processo I, representado na figura. Nessa situação, se ambas as amostras forem submetidas a combustão nas mesmas condições, a reação mais rápida ocorrera com a amostra em cavacos. Resposta: Errado Quanto maior a área de contato, maior será a velocidade da reação, logo, a pulverizada será maior rápido. Na agroindústria da cana-de-açúcar, o principal açúcar obtido pela evaporação do caldo da cana e a sacarose, um sólido branco cuja formula e C12H22O11. Em 100 mL de água à 15 °C, a solubilidade da sacarose é de, no máximo, 197 g e, à 100 °C, é de, no máximo, 487 g. A partir de 160 ºC, temperatura aproximada de fusão desse açúcar, iniciase a formação de caramelo de cor escura e parda, em processo cinético que não pode ser revertido. Originado do caldo de cana, o açúcar bruto, de cor escura é fabricado em engenhos com equipamentos simples e rústicos, apresenta de 65% a 84% de sacarose. O açúcar de usinas, produzido em instalações de grande capacidade, apresenta 99% de sacarose, na forma de cristais brancos. No engenho ou na usina, a cana é moída, e o caldo, evaporado. Nas usinas, a evaporação é realizada em várias etapas e sob vácuo. O primeiro vaso evaporador trabalha a pressão aproximada da atmosfera, em temperatura de 101 ºC; nos três evaporadores seguintes, a pressão é inferior à da atmosfera e as temperaturas são respectivamente de 92 ºC, 75 ºC e 56 ºC. Após a etapa de evaporação, ocorre a cristalização, obtendo-se o açúcar na forma sólida e branca. Na obtenção de 1 kg de açúcar bruto, de engenho, o rendimento não ultrapassa 2,5 mols de sacarose. Resposta: Correto Massa molar da sacarose: C12H22O11: C = 12 x 12 = 144 H = 1 x 22 = 22 O = 16 x 11 = 176 144 + 22 + 176 = 342 g/mol Massa sacarose = 1 kg = 1000 g 1 mol ---- 342 g x ---- 1000 g x = 2,9 mol No texto: ... fabricado em engenhos com equipamentos simples e rústicos, apresenta de 65% a 84% de sacarose Considerando um rendimento de pelo menos 65%: 2,9 mol --- 100% x ---- 84 % x = 2,436 mol No item: Na obtenção de 1 kg de açúcar bruto, de engenho, o rendimento não ultrapassa 2,5 mols de sacarose Logo, está correto, pois 2,436 mol < 2,5 mol Na obtenção do açúcar por eliminação da água, a solução vai-se tornando mais concentrada, o que exige temperaturas cada vez mais altas para a vaporização do solvente. No processo de evaporação realizado em usina, a temperatura de ebulição depende da pressão, e a sacarose não se decompõe. Resposta: Correto • Quanto mais concentrada a solução, maior a temperatura de ebulição, pois quanto mais partículas dissolvidas, mais difícil a saída da água na evaporação. • A pressão afeta na temperatura de ebulição, pois, quanto maior a pressão, mais difícil a evaporação, logo, aumenta a temperatura de ebulição. Considere que 420 g de sacarose sejam dissolvidos em 100 mL de água fervente e que, a seguir, o sistema seja resfriado até a temperatura de 15 ºC. Nesse caso, ocorrerá a deposição de massa de açúcar cristalizado superior a metade da massa inicialmente dissolvida. Resposta: Correto No texto: Em 100 mL de água à 15 °C, a solubilidade da sacarose é de, no máximo, 197 g e, à 100 °C, é de, no máximo, 487 g. Solubilidade à 15ºC: 197 g / 100 mL H2O Solubilidade à 100ºC: 487 g / 100 mL H2O No item: 420 g de sacarose sejam dissolvidos em 100 mL de água fervente e que, a seguir, o sistema seja resfriado até a temperatura de 15 ºC. Solubilidade à 15ºC: 197 g / 100 mL H2O 420 g – 197 g = 223 g não dissolvem No item: ... Nesse caso, ocorrerá a deposição de massa de açúcar cristalizado superior à metade da massa inicialmente dissolvida. Massa inicial: 420 g Massa depositada: 223 g metade = 210 g Superior à metade: 223 > 210 g Considerando que uma pessoa ingeriu uma bebida a que havia adicionado um sache de 6 g de açúcar com 95% em massa de sacarose, conclui-se que a quantidade de moléculas de sacarose ingeridas por essa pessoa foi igual a A. 1,0 × 1022. B. 6,0 × 1022. C. 1,0 × 1023. D. 6,0 × 1023. Cálculo de 95% da massa (6 g): 6 g --- 100 % x --- 95 % x = 5,7 g Cálculo do número de moléculas: 1 mol --- 342 g --- 6.1023 moléculas 5,7 g --- x 23 x = 5,7 . 6.10 342 = 0,1 . 1023 = 1022 moléculas letra A Um atleta resolveu perder peso subindo e descendo, tão rápido quanto possível, uma escada de 100 degraus, medindo cada um deles 0,15 m de altura. Ele estabeleceu a meta de subir a escada em 80 segundos. O atleta tem massa igual a 80 kg, e a eficiência de seus músculos e de 20%, ou seja, de 100 J de gordura metabolizada, dos quais 20 J são utilizados para realizar o trabalho mecânico de subir a escada, sendo o restante eliminado na forma de calor. A evaporação do suor no resfriamento do corpo do atleta e um processo exotérmico, o qual envolve transferência de energia. Resposta: Errado O corpo resfria porque a água (do suor) para evaporar precisa de calor (cedido pelo corpo). Logo, a água absorve calor do corpo para evaporar, então é um processo endotérmico. PAS-1ª Etapa-2011 O petróleo bruto é um material fluido, de fácil transporte, que apresenta principalmente compostos de carbono e hidrogênio. Na figura acima, são apresentados diversos tipos de combustíveis e produtos extraídos do petróleo bruto. Considerando a figura e a tabela apresentadas, julgue os itens a seguir. Os combustíveis derivados do petróleo são obtidos pelo processo de decantação fracionada do petróleo bruto. Errado. Os combustíveis derivados do petróleo são obtidos pelo processo de destilação fracionada do petróleo bruto. A destilação fracionada serve para separar uma mistura homogênea composta por dois líquidos, com ponto deebulição diferentes. Destilação fracionada Destilação fracionada do petróleo Considere que a transformação de querosene em gasolina seja representada pela equação a seguir, em que m e n são números inteiros positivos. Nesse caso, o processo é químico, diferentemente do processo que ocorre na torre de separação, que é físico. Correto. Toda transformação química existe a formação de novas substâncias e, a físicas, não. Na torre de separação, a temperatura deve ser heterogênea, com intensidade que aumente de cima para baixo, uma vez que, quanto maior for a faixa de massa molecular e de quantidade de carbonos, maior será a faixa de ebulição da fração de moléculas. Correto. Na figura acima, uma ilustração da molécula de ácido ascórbico — vitamina C —, as esferas pretas, vermelhas e cinza representam, respectivamente, átomos de carbono, oxigênio e hidrogênio. Considerando essas informações, julgue os itens que se seguem. Um indivíduo que ingerir diariamente 60 mg de vitamina C consumirá, em 300 dias, menos de 20 g de ácido ascórbico. 1 dia ------ 60 mg x = 300 x 60 = 18.000 mg = 18 g 300 dias ------ x Correto. Em 352 g de ácido ascórbico, existem mais de 1024 moléculas desse composto Pretas – C – 12 u Vermelha – O – 16 u Cinza – H – 1 u C6H8O6 Massa Molar = 12x6 + 1x8 + 16x6 = 176 1 mol ------ 176 g ------ 6.1023 moleculas 352 g ------ x x = 12 . 1023 moleculas Correto. x = 1,2 . 1024 moleculas Na composição centesimal em massa do ácido ascórbico, a contribuição do oxigênio é menor que 50%. C6H8O6 Massa da molécula = 12x6 + 1x8 + 16x6 = 176 u Massa do O = 16x6 = 96 u 176 --- 100 % 96 --- x Errado. x = 54 % 54,5 % > 50 % PAS - 2010 Na tabela periódica, os elementos químicos são dispostos de maneira sistemática em função de suas propriedades. Recentemente, essa sistemática foi usada no projeto Printmaking, que envolveu 96 artistas de vários países — Austrália, Canadá, Inglaterra, Alemanha, Itália, Japão, Escócia e Estados Unidos da América —, na promoção da integração entre ciência e arte, por meio da releitura da tabela periódica. Foram utilizadas várias técnicas, como gravura, litografia e serigrafia na produção de 118 obras de arte, uma para cada um dos elementos químicos conhecidos. Os modelos de tabela periódica de Mendeleyev e Moseley têm em comum a sugestão de que as propriedades físicas e químicas dos elementos variam periodicamente em função das suas massas atômicas crescentes. Errado. Mendeleev e Meyer listaram os elementos químicos conhecidos em ordem crescente de massa atômica. Entretanto, tal classificação conferia alguns problemas à tabela de Mendeleev. Moseley chegou-se à conclusão que os elementos ficariam em um padrão ainda mais regular quando arranjados em uma tabela em ordem crescente de seu número atômico, ao invés da massa atômica. Os gases nobres apresentam altos pontos de fusão e ebulição, uma vez que, nesses gases, as forças interatômicas de atração são muito intensas. Errado. Os gases têm forças intermoleculares muito fracas, por isso têm baixo pontos de fusão e de ebulição. Considerando-se que o lítio se combina com o flúor para formar um composto iônico de fórmula LiF, é correto afirmar que, na formação da ligação iônica desse composto, há transferência de um elétron do elemento com maior número de elétrons para o elemento com menor número de elétrons. Errado. Lítio – Metal alcalino – Família 1 ou 1A Flúor – Halogênio – Família 17 ou 7A LiF Li menor número de elétron F 1 elétron no último nível 7 elétron no último nível maior número de elétron Da combinação do cálcio com o oxigênio forma-se o composto molecular CaO, que apresenta propriedades alcalinas, tal como o CO2. Errado. O CaO é um óxido básico, por ser formado por um metal. Reage com água, formando uma BASE: CaO + H2O Ca(OH)2 O CO2 é um óxido ácido, por ser formado por um ametal. Reage com água, formando um ÁCIDO: CO2 + H2O H2CO3 O termo “afinidade eletrônica” pode ser corretamente definido como a propriedade periódica que mede a tendência de um átomo, em uma ligação química, em atrair elétrons. B. a propriedade periódica que mede a tendência de um átomo, em uma ligação química, em doar elétrons. C. a variação de energia que ocorre quando um elétron é adicionado a um átomo isolado, na fase gasosa, em seu estado fundamental. D. a energia necessária para que um elétron seja removido de um átomo isolado, na fase gasosa, em seu estado fundamental. A. Letra C. A. B. C. D. a propriedade periódica que mede a tendência de um átomo, em uma ligação química, em atrair elétrons. (ELETRONEGATIVIDADE) a propriedade periódica que mede a tendência de um átomo, em uma ligação química, em doar elétrons. (ELETROPOSITIVIDADE) a variação de energia que ocorre quando um elétron é adicionado a um átomo isolado, na fase gasosa, em seu estado fundamental.(ELETROAFINIDADE ou AFINIDADE ELETRÔNICA) a energia necessária para que um elétron seja removido de um átomo isolado, na fase gasosa, em seu estado fundamental. (POTENCIAL DE IONIZAÇÃO) Letra C.
Download