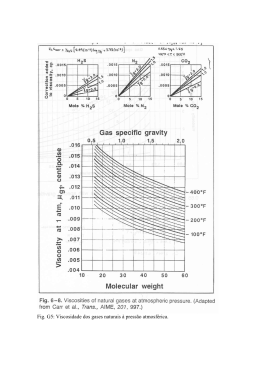
Estrutura da Matéria Lista-3 2 de novembro de 2006 Prof. Rômulo Rodrigues da Silva 1) O experimento de Rutherford, Fig.(1), mostrou pela primeira vez como deve ser a estrutura atômica. Figura 1: Para explicar a observação experimental, Rutherford propôs o modelo, Fig.(2), onde toda a carga positiva do átomo está confinada no núcleo, Ze. Dada a força de interação entre partı́cula α, ze, e o núcleo, F (r) = zZe2 , r2 (1) (a) nesse modelo, como você definiria o raio, R, de um núcleo. (b) Encontre a solução da hipérbole, Fig.(2), r(θ) = 1/u(θ), onde u(θ) obedece a equação da trajetória: d2 u m + u = − 2 2 F (1/u), (2) 2 dθ Lu onde m é a massa da partı́cula α e L o seu momento angular. (c) Utilize a condição u(π − φ) = 0 e mostre que: b(φ) = R cotg(φ/2), 2 1 (3) onde R é o raio nuclear obtido no ı́tem (a). (d) Considerando um grande número de colisões de partı́culas α em um único núcleo, Fig.(3), determine o número de partı́culas α, dN, que atravessam o anel de raio b ao redor do núcleo. (e) Mostre que a fração de partı́culas α que atravessam esse anel é: 2πbdb dN = = ρt2πbdb, Ntot Aatom (4) e determine através das Eqs.(3) e (4), a relação para a fração de partı́culas α por unidade de área do anel do detector, Fig.(1). Figura 2: Figura 3: 2) (a) Obtenha os autoestados de energia do hidrogenóide, usando os postulados de Bohr. (b) Considere uma transição entre um estado inicial i para um estado final f , obtenha a frequência da radiação emitida e o número de onda. (c) Como você explicaria através do ı́tem (b), a observação das séries de Lyman, Balmer e Paschen. (d) Considere uma estrela que contém hidrogênio em sua atmosfera e que é observado em seu espectro uma boa fração de linhas que obedece a série de Paschen. Estime a temperatura da estrela. 3) (Eisberg, pg-123) Deduza a relação que liga a frequência da radiação emitida em uma transição entre dois estados de um átomo de Bohr e a frequência orbital dos elétrons nesses dois estados. Estude essa relação no limite de n grande e comente acerca de sua correspondência com as predições da fı́sica clássica. 4) Sommerfeld considerou um átomo mais realı́stico que o de Bohr, pois considerava que os elétrons poderiam descrever elipses. Ao adicionar essa possibilidade de movimento, Sommerfeld teve que trabalhar com a sua recém 2 descoberta mecânica quântica, baseada nas regras de quantização de WilsonSommerfeld. Para o movimento do elétron orbtitando ao redor do núcleo, temos as seguintes regras de quantização: Jθ = I Ldθ = nθ h, (5) Jr = I pr dr = nr h. (6) A Eq.(5) fornece facilmente a quantização do momento angular de Bohr (ver lista2). Por outro lado, a obtenção da integral da Eq.(6) não é tão simples. (a) Mostre que usando a mecânica não-relativı́stica, pr = mṙ, e que a trajetória dos elétrons é dada por: A , (7) r= 1 − cos(θ) podemos escrever a integral Jr , na forma: 2 Jr = L Z 2π dθ 0 sen2 (θ) . [1 − cos(θ)]2 (8) (b) Use o valor da integral obtido por resı́duos (Rômulo), √ 1 − 2 − 1 Jr = −2πL √ , 1 − 2 e a relação entre os parâmetros da elipse, Fig.(4), b √ = 1 − 2 , a para obter a relação: nθ b = , (9) a n onde n = nr + nθ . (c) Use o fato que os autoestados de energia do átomo de Sommerfeld não-relativı́stico depende apenas do número quântico n (Rômulo), mostre quantas trajetórias distintas podemos construir para um elétron com energia n = 3. (d) Explique por que essa situação constitui um estado degenerado. (e) Como Sommerfeld conseguiu eliminar esses estados degenerados? 3 Figura 4: boa sorte !! 4
Baixar