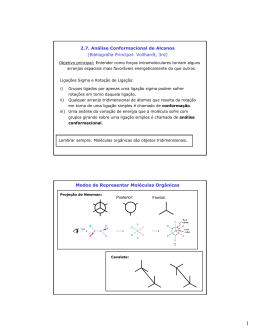
DISCIPLINA: QUÍMICA ORGÂNICA II CURSO: Farmácia Prof. Hermes Cerqueira ANÁLISE CONFORMACIONAL Salvador ESQUELETO DAS MOLÉCULAS ORGÂNICAS - ALCANOS Por ser a molécula orgânica (C-H) mais simples, são úteis para introdução de assuntos importantes como: - Nomenclatura – regra para nomear moléculas orgânicas; - Isomerismo – moléculas com a mesma fórmula molecular, mas com estruturas diferentes; - Conformação – diversas formas como os átomos podem se dobrar e flexionar; - Estereoquímica – orientação dos átomos no espaço tridimensional. Prof. Hermes Cerqueira – Farmácia - FTC DESENHO DE ESTRUTURAS - Estrutura de Lewis – ligações simples, dupla e tripla; - Estrutura de Lewis Condensada; - Estrutura Bastão; - cada ponto em uma linha dentada é tido como átomo de carbono; - as extremidades das linhas são consideradas átomos de carbono; - todos os H unidos aos elementos não carbônicos, devem ser exibidos; - Presume-se que todos os átomos sejam neutros a menos que uma carga seja exibida. - Estrutura de Ressonância. Uso de Flexas - flecha de ressonância - flecha de equilíbrio - flecha de reação - flecha de ponta dupla - flecha de ponta simples FALANDO EM GREGO – SIGMA E PI - Ligações covalentes ocorrem onde orbitais dos átomos ligantes de sobrepõem; - Ligação sigma: sobreposição orbital ocorre entre os dois núcleos ligantes; - s-s , sp – sp, sp - s - Ligação Pi: sobreposição orbital ocorre acima e abaixo dos núcleos; -p–p Prof. Hermes Cerqueira – Farmácia - FTC NOMENCLATURA DOS ALCANOS - Nomes com raízes históricas – metano, etano, propano e butano - Nomes com prefixos gregos – pent, hex, hept, oct, non, dec Fórmula Geral: Cn H2n+2 C4H10 pode ser representado de quantas formas? - linear: butano - ramificado: isobutano Nomenclatura - encontrando a cadeia mais longa - numerando a cadeia - encontrando os substituintes - ordenando os substituintes ISÔMEROS Você é capaz de desenhar todos os isômeros possíveis em uma determinada fórmula molecular ? C6H14 - desenhe a cadeia linear principal; - pense no desenho dos isômeros ramificados; - desenhe a cadeia principal com um carbono a menos; - redesenhe a estrutura colocando esse carbono como grupo metila; - agora repita os passos anteriores para quatro, três, dois e um carbono. - escreva o nome para cada cadeia e treine nomenclatura; Prof. Hermes Cerqueira – Farmácia - FTC CONFORMAÇÃO DOS ALCANOS DE CADEIA LINEAR - Ligações simples carbono-carbono são capazes de GIRAR. Isso permite que os alcanos existam em conformações diferentes. - Imagine seu corpo em seu dia.... - Deitado lendo um livro - Sentado assistindo aula - Alongando-se em uma ginástica … cada atividade coloca seu corpo em conformações diferentes e o gasto de energia pode ser baixo ou alto. Qual você prefere? CONFORMAÇÃO DOS ALCANOS DE CADEIA LINEAR - Os alcanos podem existir em conformações diferentes – diferentes arranjos espaciais dos átomos; - Nem todas as conformações têm energia igual; - As moléculas preferem estar em conformações de baixa energia em vez das de alta energia. - Conformações individuais são chamadas de confôrmeros; Prof. Hermes Cerqueira – Farmácia - FTC REPRESENTAÇÃO TRIDIMENSIONAL UTILIZANDO O PAPEL BIDIMENSIONAL - Fórmulas em Perspectiva - Projeção em Cavalete - Projeção de Newman Tensão Torsional: é o nome dado à repulsão sentida pelos elétrons ligantes de um substituinte quando passam perto dos elétrons de outro substituinte ANÁLISE CONFORMACIONAL E PROJEÇÃO DE NEWMAN - Cunhas sólidas nas estruturas de Lewis indicam uma ligação saindo do papel e cunha pontilhada indicam uma ligação que está entrando no papel. - As três linhas em formato de Y representam as três ligações do primeiro carbono que está sendo observado; - O ponto de conexão entre as linhas é o carbono da frente; - O círculo desenhado atrás do carbono frontal, representa o carbono de trás; - As três linhas saindo do círculo representa as três ligações que saem daquele carbono. PROJEÇÃO DE NEWMAN PODE AJUDAR A ANALISAR AS ROTAÇÕES EM TORNO DE UMA LIGAÇÃO CARBONO-CARBONO ESPECÍFICA. Prof. Hermes Cerqueira – Farmácia - FTC FÓRMULA CAVALETE CONFORMAÇÕES IMPORTANTES - Conformação Eclipsada: resulta quando as ligações do carbono frontal e do carbono de trás se alinham e o ângulo diedral é 0. - Conformação Alternada: resulta quando as ligações do carbono frontal e as ligações do carbono de trás têm um ângulo diedral de 60o. Tensão Torsional: repulsão elétron-elétron entre as ligações - Conformação alternada → Tensão Torsional Menor → menor energia → mais estáveis. - Conformação eclipsada → Tensão Torsional Maior → maior energia → menos estável. Prof. Hermes Cerqueira – Farmácia - FTC CONFORMAÇÕES DO BUTANO - Projeção de Newman observa-se pelos carbonos C2-C3; - Nem todas as eclipsadas e nem todas as alternadas têm a mesma energia; - Antialternada – os dois grupos Metila estão a 180o - Eclipsada – os grupos Metila estão a 120o - Gauche Alternada – os dois grupos Metila ficam lado a lado - Totalmente Eclipsada – os grupos Metila estão a 0o DIAGRAMA DE ENERGIA PARA CONFÔRMEROS DE BUTANO Totalmente Eclipsada Energia Eclipsada Gauche Alternada Anti Alternada 0 60 120 Graus Girados 180
Baixar