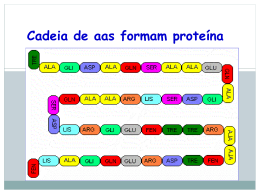
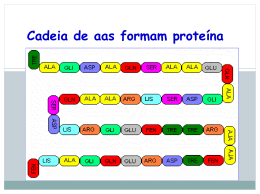
PROTEÍNAS 1 - Definição - ComposiçãO - Ocorrência -I M P O R T Â N C I A - Propriedades Físicas -E s T R U T U R A Necessidades diárias de proteína •10 a 15% das necessidades energéticas; •1g/Kg de peso por dia; •Atletas e gestantes: necessidade de ingestão aumentada PROTEÍNAS PROTEÍNAS •Compostos orgânicos complexos de alto peso molecular; •Contêm C, H, O, N e S; •São polímeros de 100 ou mais aminoácidos (aas). COMPOSIÇÃO 5 Profa. Denise Esteves Moritz - UNISUL Ligação Peptídica • Professora Dra Rosi Bio-quimica.blogspot.com BIO-QUIMICA Cadeia de aas formam proteína 9 Profa. Denise Esteves Moritz - UNISUL Classificação:Estrutura • 1 - Primária • 2 - Secundária • 3 - Terciária • 4 - Quaternária BIO-QUIMICA Estrutura a) b) c) d) Primária ou nível primário. Secundária ou nível secundário ou helicoidal Terciária ou nível terciário Quaternária ou nível quaternário Profa. Denise Esteves Moritz - UNISUL Estrutura a) Estrutura Primária ou Nível Primário É a seqüência em número de aminoácidos (cadeia peptídica). A ligação estabilizante é a ligação peptídica (covalente). Se imaginarmos os aminoácidos representados por letras: A, B, C, D, ... teremos uma esquematização da estrutura primária de uma proteína: ........A – B – C – D – A – D – A -.............. É importante salientar que o número de aminoácidos determina o número de proteínas. [Fatorial (!) do nº de aa]. Uma variação na seqüência conduz a uma proteína diferente e com ação bioquímica diferente. Ex: a ocitocina e a vasopressina diferem entre si na seqüência de apenas dois aa; a ocitocina provoca as contrações uterinas e a vasopressina provoca aumento da pressão sangüínea. Profa. Denise Esteves Moritz - UNISUL Estrutura Primária Estrutura b) Estrutura secundária ou nível secundário (helicoidal) É o enrolamento da estrutura primária em torno de um eixo imaginário, originando uma hélice chamada de hélice. Assim, esta estrutura está relacionada com a disposição espacial das estruturas primárias, e pode ser em forma de um hélice ou uma folha pregueada. Profa. Denise Esteves Moritz - UNISUL Estrutura As ligações estabilizantes dessa estrutura secundária são: Ligação ou Ponte de Hidrogênio: formada pela interação ou atração entre: oxigênio da carboxila de um aa e hidrogênio do grupo amino de outro/ - oxigênio da carboxila de um aa e hidrogênio do grupo carboxila de outro. 2. Ligação Iônica: formada pela atração entre as cadeias laterais dos aa ácidos e aa básicos. 3. Ligação hidrófoba ou apolar: formada pela interação de radicais apolares como: metil, etil, metileno, etc; dos aa constituintes da molécula. 4. Ligação ou ponte dissulfeto: formada pela união de grupos –SH dos aa chamados de cisteína. OBS: - As ligações estabilizantes em maior número são as pontes de H. - A ligação estabilizante mais forte é a ligação dissulfeto. 1. Profa. Denise Esteves Moritz - UNISUL Estrutura Secundária Hélice Laminar BIO-QUIMICA Estrutura c) Estrutura terciária ou nível terciário É a sua forma tridimensional ocasionada pelo enrolamento da espiral sobre si mesma (novelo). As ligações estabilizantes são as mesmas da estrutura secundária. Profa. Denise Esteves Moritz - UNISUL Estrutura Terciária Estrutura Terciária Estrutura d) Estrutura Quaternária ou Nível Quaternário É a que resulta da reunião de várias estruturas terciárias que, em conjunto, assumem formas espaciais bem definidas. As ligações estabilizantes são as mesmas da estrutura secundária. OBS: nem todas as proteínas apresentam esta estrutura, mas de uma maneira geral, todas as enzimas as apresentam. Profa. Denise Esteves Moritz - UNISUL Estrutura Quaternária Estrutura Quaternária Desnaturação A desnaturação de uma proteína é a desorganização das estruturas quaternárias, terciárias e secundárias. Agentes desnaturantes são os que provocam a desorganização. São eles: - agentes físicos (calor, radiações UV, alta pressão e ultra som) - agentes químicos (ácidos fortes, bases fortes, metais pesados e uréia) A proteína desnaturada apresenta as seguintes alterações: a) Físicas: aumento da viscosidade; não podem ser cristalizadas ou auto-organizadas. Químicas: maior reatividade: devido a exposição de grupos químicos que estavam encobertos por estruturas; diminuição da solubilidade do PHi e, conseqüente precipitação. Biológicas: perda de suas propriedades enzimáticas, antigênicas e hormonais; facilmente digeridas por enzimas hidrolíticas. b) c) Profa. Denise Esteves Moritz - UNISUL 25 Muitas proteínas apresentam-se firmemente enrolada em seu estado natural, como um novelo de lã. Porém, se alguma destas interações forem quebradas, sua forma será alterada e sua conformação – perdida! Chamamos isso de DESNATURAÇÃO DE UMA PROTEÍNA. SÃO AGENTES DESNATURANTES: •pH – abaixo de 5,0 •Temperatura – acima de 50 0C Profa. Denise Esteves Moritz - UNISUL FUNÇÃO DAS PROTEÍNAS ANABÓLICA blocos formadores para material celular CATABÓLICA combustível energético proteínas musculares e hepáticas FUNÇÃO ESPECÍFICA Tipos Exemplos Localização e Função Enzimas Catalisa a síntese de ácidos Ácido – graxo sintetase graxos Reserva Albumina Clara de ovo Transportadoras Hemoglobina Transporta O2 no sangue Protetoras no sangue Anticorpos Bloqueiam substâncias estranhas Hormonais Insulina Regula metabolismo da glicose Estruturais Colágeno Tendões, cartilagens, pelos Contráteis Miosina Constituíntes fibras musculares DIGESTÃO E ABSORÇÃO Inicia estômago PEPSINA meio ácido Pepsina PROTEÍNA POLIPEPTÍDEOS ABSORÇÃO dipeptidases e aminotripeptidases jejuno e íleo transporte passivo não existe depósito de aminoácidos proteínas Destino dos aas na célula • Após absorção os aas caem na corrente sanguínea • Síntese de peptídeos e proteínas • Oxidação para formação de energia (fígado e músculo) 30 FIM! Profa. Denise Esteves Moritz - UNISUL
Baixar