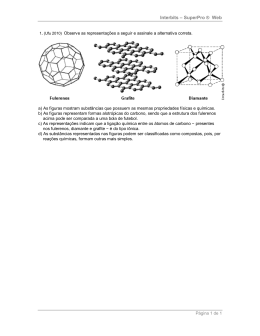
Roteiro de Estudo RO de Química – 2ª Série EM - 2° Bimestre 1. (F1 M14) Pilhas de Ni-Cd são muito utilizadas em eletrodomésticos caseiros, como em rádios portáteis, controles remotos, telefones sem fio e aparelhos de barbear. A reação de oxirredução desse tipo de pilha é: Cd(s) NiO2(s) 2H2O( ) Cd(OH)2(s) Ni(OH)2(s). Considere as seguintes afirmações a respeito dessa reação: I. O cádmio se oxida. II. O dióxido de níquel é o agente redutor. III. O cádmio é o agente oxidante. IV. O número de oxidação do níquel varia de +4 para +2. Está correto o que se afirma em a) I, II e III apenas. b) III e IV apenas. c) I, II, III e IV. d) I e IV apenas. e) NDA. 2. (F1 M15) O silício é o segundo elemento mais abundante, depois do oxigênio, na crosta da Terra. Ele ocorre como SiO2 em uma enorme variedade de minerais silicatos. O elemento é obtido pela reação do SiO2 fundido em presença de carbono a altas temperaturas, liberando um gás, conforme reação a seguir: SiO2 2C s Si ______ g Considerando a reação acima, assinale a alternativa que completa corretamente a equação. a) É gerado 1 mol do gás CO, devido à reação de oxirredução. b) São gerados 2 moles do gás CO, devido à redução do carbono. c) São gerados 2 moles do gás CO2 , devido à oxidação do carbono. d) São gerados 2 moles do gás CO, devido à oxidação do carbono. e) São gerados 2 moles do gás CO2 , devido à redução do carbono. 3. (F1 M16) O gás hidrogênio (H2) é uma excelente alternativa para substituir combustíveis de origem fóssil ou qualquer outro que produza CO2. Uma forma bastante simples de produzir gás hidrogênio em pequena escala é adicionando alumínio a ácido clorídrico, de acordo com a equação a seguir: j A q HC xAC 3 y H2 Após o balanceamento correto, a soma dos menores coeficientes estequiométricos inteiros j, q, x e y será: a) 4. b) 9. c) 11. d) 13. e) 15. 4. (F2 M26) Para a produção de energia, os mamíferos oxidam compostos de carbono nos tecidos, produzindo dióxido de carbono gasoso, CO2 (g), como principal subproduto. O principal meio de remoção do CO2 (g) gerado nos tecidos envolve sua dissolução em água, seguida da reação do gás dissolvido com a água, sob a ação de um catalisador biológico, a enzima anidrase carbônica, como representado a seguir. H O 2 CO2 (g) CO2 (aq) calor catalisador biológico HCO3 (aq) H (aq) CO2 (aq) H2O( ) (etapa 1) (etapa 2) A respeito desse processo, é correto afirmar que a) a reação de formação de HCO3 (aq) na etapa 2 só ocorre na presença do catalisador biológico. b) a concentração de CO2 (aq) não influi na acidez do meio. c) a concentração de H+ (aq) aumenta com a elevação da temperatura. d) a concentração de H+ (aq) não varia com a elevação da temperatura. e) o aumento da concentração de CO2 (aq) aumenta a acidez do meio. 5. (F2 M27) O dióxido de nitrogênio, proveniente da queima de combustíveis fósseis, é uma das espécies que mais contribui para o efeito da chuva ácida. A reação COLÉGIO OBJETIVO 1 química que provoca a diminuição do pH da água da chuva é representada pelo equilíbrio a seguir: 2NO2 + H2O ↔ H+ + NO3- + HNO2 ∆H < 0 Num ensaio em laboratório, foram acondicionados num sistema fechado N2(g), O2(g), NO2(g) e vapor de água que está em equilíbrio com água líquida. A partir desses dados, considere as seguintes afirmações: 1. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema. 2. Um aquecimento brando tenderá a aumentar o pH da solução dentro do sistema. 3. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, diminuindo o pH da solução dentro do sistema. 4. A contribuição do ácido nitroso (HNO 2) para o pH da solução dentro do sistema é desprezível. Em relação à xilocaína, é INCORRETO afirmar que: a) apresenta fórmula molecular C14H22ON. b) apresenta sete átomos de primários. c) tem quatro átomos de carbono primário. d) tem quatro ligações covalentes. e) possui cadeia carbônica homogênea. 8. (F2 M30) Observe a fórmula Assinale a alternativa correta. a) Somente as afirmativas 1 e 3 são verdadeiras. b) Somente as afirmativas 2, 3 e 4 são verdadeiras. c) Somente as afirmativas 1 e 4 são verdadeiras. d) Somente as afirmativas 2 e 3 são verdadeiras. e) Somente as afirmativas 1, 2 e 4 são verdadeiras. 6. (F2 M28) Uma solução aquosa, à temperatura de 25 C, apresenta um potencial hidrogeniônico (pH) igual a 6 (seis). A concentração em mol L1 de íons OH1 , e seu potencial hidroxiliônico (pOH) nesta solução são, respectivamente: Dados: K w 1014 mol L1 2 a) 106 , 8 b) 108 , 8 c) 107 , 7 As quantidades totais de átomos de carbono primário, secundário e terciário são, respectivamente: a) 5, 2 e 2. b) 3, 2 e 2. c) 3, 3 e 2. d) 2, 3 e 4. e) 5, 1 e 3. 9. (F2 M31) A charge a seguir retrata o preparo de um alimento em uma cozinha. d) 105 , 9 e) 1010 , 4 7. (F2 M29) TEXTO PARA A PRÓXIMA QUESTÃO: As funções orgânicas oxigenadas constituem uma grande família de compostos orgânicos, uma vez que, depois do carbono e do hidrogênio, o oxigênio é o elemento químico de maior presença nesses compostos. O comportamento químico e demais propriedades desses compostos estão diretamente relacionados à maneira como os elementos químicos citados se apresentam nas moléculas das diferentes substâncias. A xilocaína, ou lidocaína, é um composto oxigenado que apresenta a propriedade de atuar como anestésico local. A fórmula estrutural desse anestésico é representada a seguir. Sobre o contexto da charge, é CORRETO afirmar que se trata de a) um exagero, pois fritar alimentos não causa poluição nos ambientes internos. b) um excesso de cuidados, pois os gases produzidos durante a fritura são inertes. COLÉGIO OBJETIVO 2 c) uma crítica, pois as panelas utilizam PVC e liberam ácido clorídrico durante as frituras. d) uma recomendação, pois a combustão completa do GLP durante o processo de fritura produz muita fuligem e material particulado. e) um alerta, pois, durante a fritura, podem ser produzidos gases, que são nocivos à saúde, como o monóxido de carbono e o dióxido de nitrogênio. 10. (F2 M32) TEXTO PARA A PRÓXIMA QUESTÃO: Futebol é emoção no ar, ou melhor, no campo. É um espetáculo que mexe com todos e quase tudo, inclusive com a Química, que forma uma “verdadeira equipe” de produtos presentes nos estádios e sem a qual o espetáculo certamente seria menos colorido. Por exemplo, no gramado, podem estar os fertilizantes agrícolas como o cloreto de potássio e o sulfato de amônio, que, em conjunto com a água, mantêm verde, firme e uniforme a base em que rola a polêmica “jabulani”. Mas há outros integrantes na equipe química: para os pés dos jogadores, está escalado o ABS utilizado na fabricação das travas das chuteiras, que permitem dribles e passes que encantam (ou desencantam) a torcida; para os uniformes, estão escalados tecidos mais leves e confortáveis, porém, mais resistentes a puxões; para segurar a bola, evitar dúvidas e liberar o grito de gol, está escalado o náilon da rede que cobre a meta. Na equipe química, também estão presentes as tintas especiais que pintam os rostos dos torcedores e os materiais sintéticos dos barulhentos tambores e “vuvuzelas”. E para completar a festa, a Química, é claro, também vai saudar as equipes com o nitrato de potássio, empregado na fabricação de fogos de artifício. Como se pode ver, a Química tem participação garantida em qualquer campeonato. Disponível em: <http://www.abiquim.org.br/vceaquim/tododia/14.asp>. Acesso em: 05 jul. 2010. (Adaptado) O ABS é um termoplástico formado pelas três diferentes unidades moleculares: (A) acrilonitrila, (B) buta1,3-dieno ou 1,3-butadieno e (S) estireno (S, do inglês styrene), cuja fórmula estrutural é dada abaixo: Gabarito: Resposta da questão 1: [D] Teremos: Agente redutor Agente oxidante Cd(s) NiO2(s) 2H2O( ) Cd(OH)2(s) Ni(OH)2(s) 0 2 (oxidação) 4 2 (redução) Resposta da questão 2: [D] A equação balanceada é a seguinte: Pela variação de nox, observamos que o carbono sofreu oxidação. Resposta da questão 3: [D] 2 A 6HC 2A C 3 3H2 2 6 2 3 13 Resposta da questão 4: [E] Um aumento na temperatura diminui a concentração de gás carbônico na água (a solubilidade de um gás diminui com a elevação da temperatura). O aumento da concentração de CO2 (aq) aumenta a acidez do meio, pois desloca o equilíbrio da etapa 2 para a direita, consequentemente elevando a concentração de cátions H (aq). Deslocamento para a direita HCO3 (aq) H (aq) CO2 (aq) H2O( ) (etapa 2) Elevação da concentração Sobre o estireno, é correto afirmar: a) Não é um hidrocarboneto saturado. b) É classificado como hidrocarboneto. c) É um ácido. d) Apresenta cadeia heterogênea. e) Apresenta fórmula molecular é C8H6. Resposta da questão 5: [E] Análise das afirmações: [1] Verdadeira. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema, COLÉGIO OBJETIVO 3 pois o equilíbrio será deslocado para a direita, no sentido do menor número de mols dos participantes gasosos. 2NO2 (g) H2O( ) H (aq) NO3 (aq) HNO2 (aq) C4H10 2 mols de gás zero mols de gás C4H10 [2] Verdadeira. Um aquecimento brando (processo endotérmico) tenderá a aumentar o pH da solução dentro do sistema, pois o equilíbrio será deslocado para esquerda. 13 O2 4CO2 5H2O (queima completa) 2 9 O2 4CO 5H2O (queima incompleta) 2 5 O2 4C 5H2O (queima incompleta) 2 C4H10 Resposta da questão 10: [B] O estireno é um hidrocarboneto aromático, pois apre H (aq) NO3 (aq) HNO2 (aq) ΔH 0 senta núcleo benzênico. 2NO2 (g) H2O( ) exotérmico ΔH 0 0 endotérmico ΔH 0 [3] Falsa. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, aumentando o pH da solução dentro do sistema, pois ocorrerá diluição do sistema e consequentemente diminuição da concentração de cátions H+ (aumento do pH). n V Aumento de volume : n [H ] pH aumenta. V [H ] [4] Verdadeira. A contribuição do ácido nitroso (HNO2; fraco) para o pH da solução dentro do sistema é desprezível. Resposta da questão 6: [B] Teremos: pH 6 pH pOH 14 6 pOH 14 pOH 8 [OH ] 10 pOH [OH ] 10 8 mol / L Resposta da questão 7: [A] Resposta da questão 8: [E] Resposta da questão 9: [E] O gás de cozinha é composto por uma mistura de butano e propano, que podem originar gases nocivos com a queima incompleta, como o CO e o NO 2. COLÉGIO OBJETIVO 4
Baixar