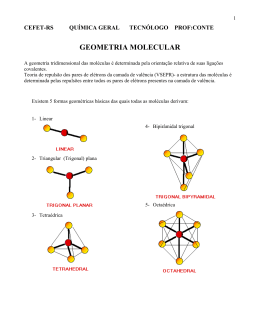
51. Um dos efeitos do tsunami de Sendai, ocorrido em 11 de março de 2011, foi a explosão ocorrida no dia 12 de março na Central Nuclear de Fukushima I. O tsunami atingiu-a e provocou uma avaria no sistema de refrigeração. O corte de eletricidade impediu a recuperação desse sistema, permitindo que os bastões do combustível continuassem a aquecer, aumentando a pressão e originando a explosão. No dia anterior, fora declarado estado de emergência na central nuclear e, apesar da informação de que não havia fugas radioativas, evacuaram-se cerca de 3000 residentes num raio de 3 km do reator. Horas depois, o raio de evacuação tinha sido elevado para 10 km, afetando já 45 000 pessoas. Em agosto de 2013, quase dois anos e meio após o acidente nuclear, verificaram-se vários vazamentos de material radioativo e, ainda, a possibilidade de um grande transbordamento de água contaminada com material radioativo para o oceano Pacífico, co- 16 locando em estado de emergência o complexo nuclear de Fukushima e acirrando as pressões sobre a Tepco (Tokyo Eletric Power), empresa que administra o complexo. O governo do Japão acredita que os vazamentos de água estejam ocorrendo há dois anos. A Tepco também informou que os níveis de césio-134 na água do poço estavam em 9.000 becquerels por litro, ou seja, 150 vezes o nível máximo permitido. Já o nível de césio-137 atingira 18.000 becquerels 200 vezes o nível permitido. Foram os mais altos níveis de césio apresentados desde o desastre de março de 2011. Relativamente aos isótopos césio-134 e césio137 podemos afirmar que a soma do número de nêutrons das duas espécies vale (A) (B) (C) (D) (E) 55. 110. 161. 189. 271. Química 52. O monóxido de carbono, formado na combustão incompleta em motores automotivos, é um gás extremamente tóxico. A fim de reduzir sua descarga na atmosfera, as fábricas de automóveis passaram a instalar catalisadores contendo metais de transição, como o níquel, na saída dos motores. Observe a equação química que descreve o processo de degradação catalítica do monóxido de carbono: 2 CO(g) + O2(g) → 2 CO2(g) ∆H = –283 kJ.mol–1 Com o objetivo de deslocar o equilíbrio dessa reação, visando a intensificar a degradação catalítica do monóxido de carbono, a alteração mais eficiente é (A) (B) (C) (D) (E) reduzir a quantidade de catalisador. reduzir a concentração de oxigênio. aumentar a temperatura. aumentar a pressão. adicionar um sólido. 53. Um laboratório realiza a análise de células utilizando uma solução fisiológica salina com pH neutro. O laboratório dispõe de apenas quatro substâncias que poderiam ser usadas no preparo dessa solução: HC, NaC, NaOH e NaHCO3. Entre elas, a que deve ser escolhida para uso na análise está indicada em (A) (B) (C) (D) (E) HCl. NaCl. NaOH. NaHCO3. CH3 - COOH. 54. Homens que começam a perder cabelo na faixa dos 20 anos podem ter maior risco de câncer de próstata no futuro. A finasterida – medicamento usado no tratamento da calvície – bloqueia a conversão da testosterona em um androgênio chamado dihidrotestosterona (DHT), que se estima estar envolvido na queda de cabelos. O medicamento também é usado para tratar câncer de próstata. (www.agencia.fapesp.br. Adaptado.) Simulado Interno 2013 - II Sobre a DHT, cuja fórmula está representada, é correto afirmar que (A) é um hidrocarboneto aromático de fórmula molecular C19H30O2. (B) é insolúvel em água e tem fórmula molecular C17H26O2. (C) apresenta as funções fenol e cetona e fórmula molecular C19H30O2. (D) é apolar e apresenta fórmula molecular C17H29O2. (E) apresenta as funções álcool e cetona e fórmula molecular C19H30O2. 55. As tatuagens podem ter vários significados, depende do ponto de vista: em alguns grupos sociais, elas funcionam como forma de comunicação não verbal e servem para identificar os membros de um mesmo grupo, tribo ou sociedade. A técnica utilizada nas tatuagens permanentes consiste em introduzir na derme, com o auxílio de agulhas, pigmentos que ficam retidos nas células da pele. Os pigmentos mais comuns e suas cores específicas estão relacionados a seguir: PIGMENTO COR Sais de cádmio Amarelo ou vermelho Sais de crômio Verde Sais de ferro Castanho, rosa e amarelo Sais de cobalto Azul Sulfeto de Mercúrio Preto Carbono (carvão) Preto Óxido de Titânio Branco Entre os metais de transição que possuem quatro níveis de energia na configuração do seu 17 estado fundamental, o de maior raio atômico éo (A) (B) (C) (D) (E) Cádmio. Crômio. Ferro. Cobalto. Titânio. Cd ( s ) + NiO2 ( s ) + 2 H2O ( ) → Cd ( OH)2 ( s ) + Ni ( OH)2 ( s ) 56. Quando átomos do elemento X, o qual está presente no terceiro período e no grupo 17 da moderna classificação periódica, se combinam com átomos do elemento Y, o qual está presente no terceiro período e grupo 2, forma-se um composto (A) (B) (C) (D) (E) molecular de fórmula XY2. iônico de fórmula X2Y. molecular de fórmula XY. iônico de fórmula YX2. iônico de fórmula Y2X. 57. Associe a coluna I (fenômenos) com a coluna II (descrição). Coluna I I. II. III. IV. V. Tamisação ou peneiração. Levigação. Filtração. Decantação. Evaporação. Coluna II ( ) Obtenção de sal a partir da água do mar. ( ) Separação da areia grossa da fina. ( ) Separação de substâncias de maior densidade de outras de menor densidade utilizando água corrente (ou outro líquido). ( ) Obtenção do café a partir do pó e água quente. ( ) Remoção das impurezas sólidas da água em estações de tratamento de água deixando a mistura em repouso por algum tempo. Assinale a alternativa que apresenta a sequência correta. (A) (B) (C) (D) (E) 18 58. A bateria de níquel-cádmio (pilha seca), usada rotineiramente em dispositivos eletrônicos, apresenta a seguinte reação de oxirredução: III - I - II - IV - V. I - III - II - V - IV. V - I - II - III - IV. I - II - III - IV - V. I - V - III - IV - II. O agente oxidante e o agente redutor dessa reação, respectivamente, são (A) H2 O ( ) , Cd ( OH)2 ( s ) . (B) NiO2 ( s ) , Cd ( OH)2 ( s ) . (C) NiO2 ( s ) , Cd ( s ) . (D) Cd ( s ) , Cd ( OH)2 ( s ) . (E) NiO2 ( s ) , Ni ( OH)2 ( s ) . 59. Observe com atenção a tabela a seguir. Composto p.e (ºC) (1atm) Solubilidade em água (g 100mL–1) CH3CHOHCH2OH 187 infinita CH3CH2CH2CH2OH 117,7 8,3 O propilenoglicol (CH3CHOHCH2OH) tem ponto de ebulição maior que o butanol (CH3CH2CH2CH2OH) e é mais solúvel em água. Assinale a explicação correta para a informação dada. (A) O propilenoglicol tem massa molar muito maior que o butanol. (B) As forças intermoleculares que atuam no butanol são mais fortes que aquelas presentes no propilenoglicol. (C) A cadeia carbônica maior do butanol é responsável por sua maior solubilidade em água. (D) O propilenoglicol faz um maior número de ligações de hidrogênio entre suas moléculas e também com a água do que o butanol. (E) O maior ponto de ebulição do propilenoglicol se deve ao maior número de interações por focas de van der Walls realizadas por suas mioléculas. Química 60. Os automóveis modernos movidos a gasolina são equipados com dispositivos antipoluição, popularmente conhecidos como “catalisadores”. Os gases que saem do motor são forçados a passar pelo conversor catalítico (catalisador), que contém metais apropriados como Pt e Rh, os quais aumentam a velocidade de uma série de reações. Dessa forma, alguns gases tóxicos são transformados em gases não tóxicos (ou menos tóxicos), o que diminui a poluição atmosférica. Abaixo se tem a representação de reações químicas numeradas de I a V: I. 2NH3(g) + 2O2(g) → N2O( g ) + 3H2 O ( g ) II. 2CO( g ) + 2NO( g ) → 2CO2( g ) + N2( g ) III. CO2 ( g ) + 2NO2( g ) → C( s ) + 2NO( g ) + 2O2( g ) IV. 2NO( g ) → N2( g ) + O2( g ) II. Pessoas ansiosas respiram rapidamente, eliminando muito CO2 com o que a reação deste com H2O se desloca para a esquerda. III. Pessoas com diarreia sofrem grande perda de íons bicarbonato, com o que a reação do CO2 com H2O se desloca para a direita. É correto o que se afirma em (A) (B) (C) (D) (E) I, apenas. III, apenas. I e III, apenas. II e III, apenas. I, II e III. 62. A influenza é uma virose respiratória aguda que ocorre durante todo ano, sendo popularmente conhecida como gripe. A estrutura química a seguir representa o Oseltamivir, um componente dos antigripais atualmente utilizado. V. 2CO( g ) + O2( g ) → 2CO2( g ) Dessas reações, as que são catalisadas em um conversor catalítico automotivo são as de número (A) (B) (C) (D) (E) I, II e IV. I, III e IV. II, III e V. II, IV e V. I, III, IV e V. 61. No corpo humano, 70% do transporte de CO2 para os pulmões, por meio das hemácias e do plasma, ocorre sob a forma de íons bicarbonato. Estes são produzidos pela reação do dióxido de carbono com água, representada pela seguinte reação química: Sobre a estrutura acima, é incorreto afirmar que (A) (B) (C) (D) (E) apresenta fórmula molecular C16H28N2O4. apresenta os grupos funcionais amina e éter. é um composto aromático. é um composto insaturado. apresenta os grupos funcionais amida e éster. 63. Considere as interações que podem ocorrer entre duas substâncias quaisquer entre as representadas na tabela. I. II. III. IV. CO2(aq) + H2O(l) → H+(aq) + HCO3–(aq) A diminuição do pH do sangue constitui a acidose, que provoca náusea, vômito e cansaço. O aumento do pH do sangue corresponde à alcalose, que provoca distúrbios respiratórios, cãibras e convulsões. Considere as seguintes afirmações. I. Pessoas com deficiência respiratória não exalam CO2 suficientemente, com o que a reação deste com H2O se desloca para a esquerda. Simulado Interno 2013 - II iodo água etanol ciclo-hexano Forças intermoleculares do tipo ligações de hidrogênio podem ocorrer na interação das substâncias (A) (B) (C) (D) (E) I e II. I e III. II e III. II e IV. III e IV. 19 64. Considere que a massa de uma gota de água é de 0,05 g. Calcule a quantidade de mols (n) que existe nessa gota de água. Dado: massa molecular da água é igual a 18 u. (A) (B) (C) (D) (E) 0,28 mol 0,0028 mol 0,056 mol 1,27·1021 mol 2,8·1023 mol 65. A atividade física intensa e prolongada causa a transpiração do corpo e, assim, a perda de sais minerais, principalmente sais de sódio, importantes para o equilíbrio orgânico, que tecnicamente chamam-se hidro-eletrolíticos. Isso ocorre porque minerais como sódio, potássio, magnésio e cálcio são importantes para a maioria das funções de contração muscular do nosso corpo. Esses minerais, perdidos pelo suor - cuja densidade média é 1,004 g/L - durante a transpiração, podem ser repostos pela ingestão de bebidas isotônicas, melhorando o desempenho esportivo. Considerando as informações do texto, têmse as seguintes afirmativas. I. II. III. IV. V. O suor é uma mistura heterogênea do tipo suspensão. A densidade do suor é a razão entre seu volume e sua massa e representa uma propriedade química. O suor sobre a pele desaparece quando o atleta para de jogar, porque retira energia térmica do corpo para transformar seu estado físico de líquido para gasoso. Os íons sódio e potássio, contidos no suor, são metais alcalinos e pertencem ao primeiro grupo da tabela periódica. Os íons sódio, potássio e magnésio, liberados durante a transpiração, possuem cargas iguais a +1, +1 e +2, respectivamente. Assinale a alternativa que reúne somente afirmativas corretas. (A) (B) (C) (D) (E) 20 II - III - IV - V. I - II - IV - V. III - IV - V. I - II - IV. II - IV - V. 66. A água do mar possui uma concentração ideal de sais (30 g/L) que permite a sobrevivência dos seres vivos. Para reproduzir o ambiente marinho, em um aquário contendo 2 x 106 cm3 de água, devemse adicionar (A) (B) (C) (D) (E) 6 x 101 kg de sais. 1,5 x 102 kg de sais. 2 x 106 kg de sais. 6 x 104 kg de sais. 2 x 104 kg de sais. 67. As medalhas olímpicas não são de ouro, prata ou bronze maciços, mas sim peças de metal submetidas a processos de galvanoplastia que lhes conferem as aparências características, graças ao revestimento com metais nobres. Sobre o processo de galvanoplastia, assinale a alternativa correta. (A) O processo é espontâneo e gera energia elétrica no revestimento das peças metálicas. (B) Consiste em revestir a superfície de uma peça metálica com uma fina camada de outro metal, por meio de eletrólise aquosa de seu sal. (C) É um fenômeno físico, pois, no revestimento da peça metálica, ocorrem fenômenos que alteram a estrutura do material. (D) A peça submetida ao revestimento metálico atuará como ânodo e será o eletrodo de sinal positivo. (E) Só ocorre quando a ddp for superior a 100V. 68. A chuva ácida é um problema dos grandes centros urbanos e das metrópoles industriais. Nesses locais, certas atividades humanas lançam na atmosfera grandes quantidades de ENXOFRE, o qual, reagindo com o OXIGÊNIO do ar, forma compostos como o TRIÓXIDO DE ENXOFRE. Este, por sua vez, reage com a ÁGUA da chuva, formando o ÁCIDO SULFÚRICO, que se precipita na forma de chuva ácida, causando danos ao meio ambiente e ao organismo humano. O texto faz referência a cinco espécies de matéria, as quais podem ser classificadas, respectivamente, como substâncias Química (A) simples, composta, simples, composta, simples. (B) simples, composta, simples, composta, composta. (C) composta, simples, simples, composta, composta. (D) composta, composta, composta, simples, simples. (E) simples, simples, composta, composta, composta. 69. Em 1923, Brönsted (Dinamarca) e Lowry (Inglaterra) apresentaram um novo conceito para ácidos e bases. Nesse conceito, as reações entre um ácido e uma base envolvem transferência de H+ (o ácido doa e a base recebe) e, no equilíbrio, identifica-se a presença de dois pares ácido-base conjugados de maneira que, para cada par, o ácido tem um próton (H+) a mais do que a sua base conjugada. Considere o equilíbrio ácido-base a seguir. → H2NO 3+ (aq) + HSO −4 (aq) HNO3(aq) + H2SO4(aq) ← De acordo com esse conceito, assinale a opção correta. (A) HNO3 e H2SO4 são os ácidos conjugados de um sistema. (B) H2NO 3+ e HSO −4 são as bases conjugadas de um sistema. (C) H2SO4 e HSO −4 são o ácido e a base conjugados de um sistema. (D) HNO3 e H2NO 3+ são o ácido e a base conjugados de um sistema. (E) H2SO4 e H2NO 3+ são o ácido e a base conjugados de um sistema. 70. Sejam dadas as seguintes moléculas: H2O, BeH2, BC 3 , CC 4 e NH3. As configurações espaciais dessas moléculas são, respectivamente, (A) angular, linear, trigonal, tetraédrica, piramidal. (B) angular, trigonal, linear, tetraédrica, angular. (C) angular, linear, piramidal, tetraédrica, piramidal. (D) trigonal, linear, angular, tetraédrica, tetraédrica. (E) linear, linear, angular, piramidal, trigonal. Simulado Interno 2013 - II 71. A incorporação de saberes e de tecnologias populares como, por exemplo, a obtenção do sabão de cinzas, a partir de uma mistura de lixívia de madeira queimada com grandes quantidades de gordura animal sob aquecimento, demonstra que já se sabia como controlar uma reação química, cuja finalidade, nesse caso, era produzir sabão. De acordo com o conhecimento químico, o sabão de cinzas se forma mediante a ocorrência de reações químicas entre a potassa, que é obtida das cinzas, e os ácidos graxos presentes na gordura animal. (www.if.ufrgs.br/ienci/artigos/Artigo_ID241/ v15_n2_a2010.pdf. Acesso em 21.09.2012. Adaptado) A palavra potassa é usada em geral para indicar o carbonato de potássio (K2CO3), que, em meio aquoso, sofre hidrólise. A produção do sabão é possível porque a hidrólise da potassa leva à formação de um meio fortemente (A) (B) (C) (D) (E) ácido, promovendo a esterificação. ácido, promovendo a saponificação. alcalino, promovendo a esterificação alcalino, promovendo a saponificação. ácido, promovendo a hidrólise da gordura. 72. Em cinco frascos de 250ml providos de rolha e numerados de I a V, são colocados 100ml de tetracloreto de carbono, 100ml de água e 2g da substância indicada a seguir. I. II. III. IV. V. Iodo. Cloreto de sódio. Benzeno. Açúcar. Cloreto de prata. Essas misturas, agora com três componentes, são agitadas. Uma vez estabelecido o equilíbrio, é falso afirmar que (A) em I a maior parte do iodo estará dissolvida na fase orgânica. (B) em II praticamente todo cloreto de sódio estará dissolvido na fase aquosa. (C) em III praticamente todo o benzeno estará dissolvido no tetracloreto de carbono. (D) em IV praticamente todo o açúcar estará dissolvido na fase orgânica. (E) em V praticamente todo o cloreto de prata estará na forma de uma terceira fase sólida. 21 73. Os fulerenos são constituídos por uma rede formada por pentágonos e hexágonos, fechando assim a “esfera”. Os fulerenos são formas alotrópicas do elemento químico carbono que apresentam a estrutura abaixo. (A) somente às propriedades hidrófilas do radical hidroxila. (B) às propriedades hidrófilas de R, qualquer que seja seu tamanho. (C) às propriedades hidrófobas de R, qualquer que seja seu tamanho. (D) ao fato de o aumento de R corresponder ao aumento da parte apolar hidrofóbica. (E) ao fato de à diminuição de R corresponder uma diminuição na polaridade da molécula. 75. Os elementos que I. Outras formas alotrópicas do carbono são (A) (B) (C) (D) (E) isótopos de carbono-13. calcário e mármore. silício e germânico. monóxido e dióxido de carbono. diamante e grafite. 74. Determina-se experimentalmente que, num álcool R-OH, a solubilidade em água varia inversamente com o tamanho de R. Esse fato se deve 22 formam óxidos que em água produzem soluções básicas, II. têm a primeira energia de ionização pequena e a segunda muito maior, III. em água liberam hidrogênio gasoso são (A) (B) (C) (D) (E) halogênios. calcogênios. semimetais. metais de transição. metais alcalinos. Química
Baixar