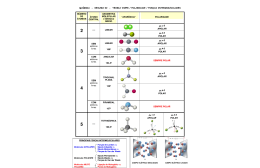
EXERCÍCIOS RESOLVIDOS Disciplina: Métodos cromatográficos Docente: Daniele Cristina Adão 1) As misturas de amirinas ( e β-amirina) e de dióis (breína e maniladiol) aparecem no cromatograma obtido em CCD, revelado com solução sulfato cérico, inicialmente como manchas de cor alaranjada, que após um período de 15 min se tornam rosa (Rf=0,46) e verde (Rf=0,29), respectivamente. O cromatograma em camada delgada de gel de sílica foi desenvolvido utilizando o eluente hexano-acetato de etila (8:2). Justifique a ordem de eluição, conhecendo as estruturas. R: A mistura de dióis apresenta Rf menor pois apresenta uma polaridade maior que as amirinas, e com isso tem maior interação com a FE, sílica. A FM é apolar, logo, tem maior interação com a mistura de amiras apresentando um Rf maior (0,46). Os compostos breína e maniladiol apresentam em sua estrutura uma hidroxila a mais que as amirinas, ou seja, maior polaridade e ligações de hidrogênio com a FE. 2) Em uma placa de sílica encontra-se um composto com fator de retenção (Rf = 0,2 – representado na figura como dS1) quando a fase móvel é hexano. Qual solvente, tolueno ou acetonitrila, aparentemente aumentaria o fator de retenção (representado na figura como dS2)? R: A FM, hexano, é apolar e a FE, a sílica, polar. Sendo assim, para aumentar o fator de retenção, é necessário que o composto tenha menor interação com a FE e maior com a FM. Nesse caso, supõe-se que o composto seja polar, por interagir com a FE e permanecendo próximo ao ponto de injeção. Se for utilizada uma FM mais polar o composto irá interagir com o solvente se distanciando do ponto de injeção. Entre a acetonitrila e o tolueno, a acetonitrila é mais polar e esse seria o solvente ideal para aumentar o fator de retenção (distância percorrida pela mancha). 3) Em uma coluna de sílica encontra-se um composto com tempo de retenção de 5,5 minutos quando a fase móvel é hexano. Qual solvente, tolueno ou acetonitrila, aparentemente reduziria o tempo de retenção (para o tempo de retenção igual a 1,8 min – identificados na figura)? R: A FM, hexano, é apolar e a FE, a sílica, polar. Sendo assim, considerando o tempo de retenção elevado, podemos supor que o composto permanece mais tempo dentro da coluna, ou seja, interage mais com a FE, o composto seria então pouco-polar ou polar. Para reduzir o tempo de retenção (tempo de eluição) o ideal, nesse caso, seria utilizar uma FM mais polar porque desta forma o composto irá interagir com a fase móvel permanecendo menos tempo na coluna. Entre a acetonitrila e o tolueno, a acetonitrila é mais polar e esse seria o solvente ideal para reduzir o tempo de retenção, o tempo que o composto leva para passar pela coluna e ser identificado. 4) Uma coluna cromatográfica utilizando sílica como fase estacionária, foi utilizada para separar os pigmentos do pó de pápica. Inicialmente foi percolado pela coluna uma fase móvel de éter de petróleo que promoveu a remoção do caroteno (1), na sequência passando-se então a éter de petróleo-acetona (1:1) e acetona para a remoção da Capsantina (2). Discuta a ordem de eluição e o uso de diferentes fases móvel. R: Verifique que o composto 1 (-caroteno) é apolar (cadeia longa de carbonos) e o composto 2 (Capsantina) pouco-polar (presença de grupamentos hidroxilas). A FE, sílica, é polar, desta forma a eluição com um solvente apolar, éter de petróleo, promove a separação do composto 1 uma vez que retém o composto 2 na fase estacionária. O composto 2 só é eluído quando uma fase móvel mais polar, acetona, é percolada pela coluna.
Baixar