REVISÃO QUÍMICA
Profº JURANDIR
QUÍMICA
01- O despejo de dejetos de esgotos
domésticos e industriais vem causando
sérios problemas aos rios brasileiros.
Esses poluentes são ricos em substâncias
que contribuem para a eutrofização de
ecossistemas, que é um enriquecimento da
água por nutrientes, o que provoca um
grande crescimento bacteriano e, por fim,
pode promover escassez de oxigênio
Uma maneira de evitar a diminuição da
concentração de oxigênio no ambiente é:
A) Aquecer as águas dos rios para aumentar a
velocidade de decomposição dos dejetos.
B) Retirar do esgoto os materiais ricos em
nutrientes para diminuir a sua concentração nos
rios.
C) Adicionar bactérias anaeróbicas às águas dos
rios para que elas sobrevivam mesmo sem
oxigênio.
D) Substituir produtos não degradáveis por
biodegradáveis para que as bactérias possa utilizar
os
nutrientes.
E)Aumentar a solubilidade dos dejetos no esgoto
para que os nutrientes fiquem mais acessíveis às
bactérias.
O processo de eutrofização do ambiente é
decorrente do aporte de esgotos causando a
proliferação de bactérias decompositoras
de matéria orgânica. A proliferação dessas
bactérias impede a penetração de luz solar para
a fotossíntese dos seres aeróbios e o alto
consumo de O2 leva a morte dos animais
heterotróficos. Com isso, uma das medidas que
pode ser adotada é a redução da concentração
de matéria orgânica que é jogada nos rios para
evitar o aparecimento inicial das bactérias
aeróbicas.
Letra: b
DESEQULÍBRIO ECOLÓGICO DO RIO POTI EM TERESINA
02. A tabela abaixo mostra os valores máximos permitidos para
algumas espécies iônicas e elementos químicos em águas de
abastecimento público.
Analisando 10mL da água de um poço, foram encontrados os
seguintes resultados:
Bário
10-2mg
Ferro
2 . 10-3mg
Manganês
2 . 10-3mg
Comparando com a tabela fornecida, assinale a alternativa correta em
relação aos três metais acima:
a) A água do poço está própria para o consumo.
b) A água está imprópria para o consumo apenas em relação ao
manganês.
c) A água está imprópria para o consumo em relação ao ferro e ao
manganês.
d) A água está imprópria para o consumo em relação ao Bário e ao
manganês.
e) A água está imprópria para o consumo em relação aos três metais.
BÁRIO
FERRO
10-2mg .................10 ml
Xmg ................... 1000ml
2.10-3mg .........10 ml
Xmg ...............1000ml
X=1mg/L
X= 0,2mg/L
MANGANÊS 2.10-3mg........10ml
Xmg .............1000ml X=0,2mg/L
A CONCENTRAÇÃO DE MANGANÊS ESTÁ
ACIMA DO VALOR MÁXIMO PERMITIDO
LETRA: B
LIXO ELETRÔNICO (e-waste)
03-(ENEM) Em 2006, foi realizada uma conferência das
Nações Unidas em que se discutiu o problema do lixo
eletrônico,também denominado e-waste. Nessa ocasião,
destacou-se a necessidade de os países em
desenvolvimento serem protegidos das doações nem
sempre bem-intencionadas dos países mais ricos. Uma
vez descartados ou doados, equipamentos eletrônicos
chegam a países em desenvolvimento com o rótulo de
“mercadorias
recondicionadas”,
mas
acabam
deteriorando-se em lixões, liberando chumbo, cádmio,
mercúrio e outros materiais tóxicos.
Internet: <g1.globo.com> (com adaptações).
A discussão dos problemas associados ao e-waste leva à
conclusão de que:
A - os países que se encontram em processo de industrialização
necessitam de matérias-primas recicladas oriundas dos países
mais ricos.
B - o objetivo dos países ricos, ao enviarem mercadorias
recondicionadas para os países em desenvolvimento,é o de
conquistar mercados consumidores para seus produtos.
C - o avanço rápido do desenvolvimento tecnológico, que torna os
produtos obsoletos em pouco tempo, é um fator que deve ser
considerado em políticas ambientais
D - o excesso de mercadorias recondicionadas enviadas para os
países em desenvolvimento é armazenado em lixões apropriados.
E - as mercadorias recondicionadas oriundas de países ricos
melhoram muito o padrão de vida da população dos países em
desenvolvimento.
COMENTÁRIO
Devido ao acelerado volume de inovações
tecnológicas que são dispostas no mercado,
os produtos se tornam ultrapassados em um
curto espaço de tempo, havendo assim um
elevado fluxo de consumo de mercadorias
desse segmento. Diante deste fato, as
políticas ambientais devem analisar esse
fator de maneira mais aprofundada.
LETRA C
4 Rs DA RECICLAGEM
REDUZIR
REUTILIZAR
RECUPERAR
RECICLAR
Minimização de resíduos
• 4Rs :
• Reduzir o lixo evitando o
desperdício,
• Reaproveitar tudo o que for
possível antes de jogar fora
• e só então enviar para Reciclar.
• Reutilizar
04. Muita informação errônea vem circulando na internet brasileira sobre bicarbonato de sódio, consistindo
num grande desserviço às pessoas que poderiam se beneficiar dos poderes terapeuticos desta substância.
Andou circulando um email propagando os benefícios do bicarbonato para a cura do câncer. O problema é
que este email, num tom completamente sensacionalista e carecendo de referências científicas, gerou reações
negativas de muitas pessoas tanto da área de saúde convencional quanto alternativa, que, sem pesquisar os
fatos e se baseando apenas em tal email, passaram a pregar contra o uso do bicarbonato.
(http://caminhosparaasaude.blogspot.com.br/2013/03/bicarbonato-de-sodio.html)
Sobre o bicarbonato de sódio (NaHCO3), podemos afirmar que:
a) Usa-se como antiácido, para tratar a acidez do estômago porque ele tem o poder de neutralizar os excessos
do ácido nítrico do suco gástrico.
b) É empregado na extinção de pequenas chamas, pelo CO2, resultante da sua decomposição térmica de
acordo com a reação: 2 NaHCO3 → Na2CO3 + CO2 + H2O →
c) Na higienização bucal, na forma de bochecho o bicarbonato de sódio atua na neutralização dos ácidos que
atacam o esmalte dentário, também para o combate de aftas.Sendo que sua solução aquosa permanece incolor
em presença do indicador fenolftaleína.
d) Devido à capacidade do bicarbonato de sódio libertar um óxido neutro gasoso, também é muito usado nas
receitas de culinária como agente levedante ("fermentos químicos"), para ser utilizado no crescimento das
massas de pães, bolos e biscoitos
e) A decomposição térmica de um mol do sal produz 22,4litros de CO2 nas CNTP.
2 mols DE NaHCO3 ........................ 22,4 litros de CO2
1 mol ................................................. X
X = 11,2 LITROS DE CO2
LETRA: B
05.(ENEM) O ferro pode ser obtido a partir da hematita, minério rico
em óxido de ferro, pela reação com carvão e oxigênio. A tabela a seguir
apresenta dados da análise de minério de ferro (hematita) obtido de
várias regiões da Serra de Carajás.
Minério da
região
Teor de enxofre (S) / % em massa
Teor de ferro (Fe) / % em massa
Teor de sílica (SiO2) / % em massa
1
0,019
63,5
0,97
2
0,020
68,1
0,47
3
0,003
67,6
0,61
Fonte: ABREU, S . F. Recursos minerais do Brasil, vol. 2. São Paulo: Edusp, 1973
No processo de produção do ferro, a sílica é removida do minério por reação com
calcário (CaCO3). Sabe-se, teoricamente (cálculo estequiométrico), que são
necessários 100 g de calcário para reagir com 60 g de sílica.
Dessa forma, pode-se prever que, para a remoção de toda a sílica presente em 200
toneladas do minério na região 1, a massa de calcário necessária é, aproximadamente,
em toneladas, igual a:
a) 1,9.
b) 3,2.
c) 5,1.
d) 6,4.
e) 8,0.
200 TON ------------100%
X
----------------0,97%
CaCO3---------------
SiO2
X= 1,94 TON DE SiO2
100g
Y
60g
1,94Ton
-------------------------------
Y = 3,2 TON
LETRA:B
06. (ENEM ) Ao colocar um pouco de açúcar na água e mexer até
a obtenção de uma só fase, prepara-se uma solução. O mesmo
acontece ao se adicionar um pouquinho de sal à água e misturar
bem. Uma substância capaz de dissolver o soluto é denominada
solvente; por exemplo, a água é um solvente para o açúcar, para
o sal e para várias outras substâncias. A figura a seguir ilustra
essa citação.
Suponha que uma pessoa, para adoçar seu cafezinho, tenha
utilizado 3,42 g de sacarose (massa molar igual a 342 g/mol) para
uma xicara de 50 mL do líquido. Qual a concentração final, em
mol/L, de sacarose nesse cafezinho?
a) 0,02
b) 0,2
c) 2 d) 200
e) 2000
CÁLCULO DO Nº DE MOLS DE SACAROSE
342g ---------- 1MOL
3,42g---------- X
X= 0,01 mol
CÁLCULO DA CONCENTRAÇÃO EM MOL/L
50mL ---------- 0,01MOL
1000mL-------- X
X= 0,2 mol/L
07. (C7H26) Julgue os itens abaixo colocando
verdadeiro ou falso
( ) O alcatrão da hulha obtido através da destilação
seca da hulha constitui-se numa excelente fonte de
composto aromático para industria petroquímica
( ) Tanto o Metil-Terc-Butil-Eter (MTBE) quanto o
Chumbo Tretaetila-Pb(C2H5)4 são considerados
antidetonantes da gasolina, bastante utilizados
atualmente no Brasil.
( ) O petróleo de base naftênica é de superior
qualidade ao de base parafínica.
( ) O petróleo é uma substância originada a partir do
soterramento de animais e vegetais ocorridos há
milhares de anos.
Carvão Mineral
A destilação seca da hulha à 1 000º C
A destilação seca da hulha à 1 000º C fornece:
fornece:
gásda
dahulha:
hulha: mistura
mistura de
2, CH
4, CO;
gás
deHH
,
CH
2
4, CO;
águas amoniacais: solução de NH4OH e seus
águas
amoniacais:
Utilizada
para
a
sais;
produção de adubo orgânico.
alcatrão da hulha: líquido oleoso, escuro,
alcatrão
da hulha: líquido
oleoso, escuro,
formado principalmente
por aromáticos;
formado principalmente por aromáticos;
carvão coque: principal produto, usado com
redutor coque:
em metalurgia.
carvão
principal produto, usado para
aquecer fornos siderúrgico.
DIVISÃO:
- Base Parafínica (90% de alcanos).
- Base Naftênica (Rico em ciclanos).
- Base Aromática (Rico em
compostos aromáticos).
- Base Asfáltica (Hidrocarboneto de
massa molar elevada).
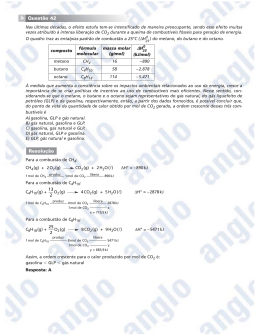
03. (C5H17) (ENEM) Nas últimas décadas, o efeito estufa tem-se intensificado de maneira
preocupante, sendo esse efeito muitas vezes atribuído à intensa liberação de CO2 durante a
queima de combustíveis fósseis para geração de energia. O quadro traz as entalpias-padrão de
combustão a 25 °C (∆H) do metano, do butano e do octano.
À medida que aumenta a consciência sobre os impactos
ambientais relacionados ao uso da energia, cresce a
importância de se criar políticas de incentivo ao uso de
combustíveis mais eficientes. Nesse sentido considerandose que o metano, o butano e o octano sejam representativos
do gás natural, do gás liquefeito de petróleo (GLP) e da
gasolina, respectivamente, então, a partir dos dados
fornecidos, é possível concluir que, do ponto de vista da
quantidade de calor obtido por mol de CO2 gerado, a ordem
crescente desses três combustíveis é:
a) gasolina, GLP e gás natural.
b) gás natural, gasolina e GLP.
c) gasolina, gás natural e GLP.
d) gás natural, GLP e gasolina.
e) GLP, gás natural e gasolina.
GÁS
NATURAL
GLP
GASOLINA
CH4 + 2 O2 → 1CO2 + 2H2O
1 mol CO2 ............890 KJ
C4H10 + 13/2 O2 → 4CO2 + 5H2O
4 mol CO2 ............2878 KJ
1 mol CO2 ............X KJ
X = 719,5 KJ
C8H18 + 25/2 O2 → 8CO2 + 9H2O
8 mols CO2 ............5471 KJ
1 mol CO2 ............X KJ
X = 683,97 KJ
09. “(...) Plásticos foram descobertos no século passado,
mas o primeiro completamente sintético a ser
comercializado foi a baquelite, inventado em 1910. (...) Foi
em 1922 que o alemão Hermann Staudinger descobriu que
substâncias como a borracha eram formadas por cadeias de
moléculas, chamadas por ele de macromoléculas. Estava
descoberto o polímero (...)”
(Texto extraído do jornal Folha de S. Paulo, 11/12/94.)
Assinale a alternativa que relaciona polímeros que
contenham halogênios em sua estrutura:
a) polietileno e polipropileno.
b) nylon e lycra.
c) baquelite e borracha.
d) PVC e teflon®.
e) amido e proteínas.
10. O poliestireno, o nylon e o policloreto de
vinila(PVC), são substâncias poliméricas obtidas
respectivamente por:
a) polimerização em cadeia, copolimerização e
policondensação.
b) copolimerização, policondensação e polimerização
em cadeia.
c) polimerização em cadeia, policondensação e
policondensação.
d) polimerização em cadeia, policondensação e
polimerização em cadeia.
e) polimerização em cadeia, polimerização em cadeia e
policondensação.
POLIMEROS DE ADIÇÃO COMUM OU HOMOPOLÍMEROS
MONÔMERO
POLÍMERO
APLICAÇÃO
ETILENO
POLIETILENO
SACOS PLÁSTICOS
CLORETO DE
VINILA
POLICLORETO DE VINILA
(PVC)
TUBOS E CONEXÕES
TETRAFLÚORETIL TEFLON
ENO
REVESTRIMENTO DE
PANELAS
ESTIRENO
POLIESTIRENO
ISOPOR
PROPILENO
POLIPROPILENO
CORDAS
METACRILATO DE ACRÍLICO
METILA
LENTES DE AUTOMÓVEL
ACETATO DE
VINILA
POLIACETATO DE VINILA
(PVA)
TINTAS
CIANETO DE
VINILA
POLICIANETO DE VINILA
(ORLON)
LÂ SINTÉTICA, CARPETE
POLIMEROS DE ADIÇÃO 1,4
MONÔMERO
POLÍMERO
APLICAÇÃO
ISOPRENO
POLIISOPRENO
BORRACHA
NATURAL
CLOROPRENO
OU NEOPRENO
POLICLOROPRENO
BORRACHA
SINTÉTICA
Vulcanização da borracha é a adição de enxofre (entre 5% e 8%)
às ligações duplas do polímero, feita sob aquecimento,
formando uma estrutura tridimensional (termofixa), com o
enxofre servindo de ponte entre as cadeias carbônicas.
POLIMEROS DE CONDENSAÇÃO
POLÍMERO
APLICAÇÃO
BAQUELITE
CABOS DE PANELAS
NYLON
FIOS DE PESCA
KEVLAR
POLIÉSTER
COLETE A PROVA DE
BALA
FIBRA TÊXTIL
POLICARBONATO
VIDRO BLINDADO
RESINAS EPÓXI
DUREPÓXI
EU VOU
PASSAR!!!
EU VOU
PASSAR!!!
Nós que fazemos o
estamos muito satisfeitos de termos conseguido
conquistar a sua confiança, e é essa confiança que nos
motiva a prosseguir nesta caminhada árdua, no
entanto, gratificante. Temos absoluta certeza de que a
sua vitória depende principalmente da sua vontade de
vencer; contamos com ela neste Vestibular, pois, o
nosso sucesso enquanto escola é motivado pelo seu,
então, acredite em você, seja um Vencedor.
Prof. Jurandir.
EU VOU
PASSAR!!!
Não esqueçam: “Tudo posso Naquele que me fortalece”
Que Deus ilumine VOCÊS rumo a sua aprovação.
REVISÕES PARA VESTIBULARES
Prof. Jurandir
Baixar