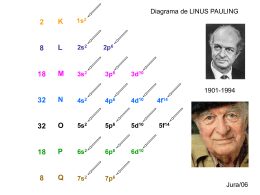
24/03/2015 Direitos Exclusivos para o autor: Prof. Gil Renato Ribeiro Gonçalves CMB- Colégio Militar de Brasília [email protected] Reservados todos os direitos. É proibida a duplicação ou reprodução desta aula, com ou sem modificações (plágio) no todo ou em parte, sob quaisquer formas ou por quaisquer meios (eletrônico, mecânico, gravação, fotocópias ou outros) sem permissão expressa do autor. Obs.: Algumas figuras foram copiadas do banco de figuras do www.google.com Os Elementos Químicos Física – CFB – 90ANO Prof. Gil Renato Ribeiro Gonçalves Prof. Gyl Renato 2 1 24/03/2015 Definições Os Elementos Químicos: São formados por um conjunto de átomos com o mesmo número atômico (isótopos) e, por isso, quimicamente idênticos. Prof. Gyl Renato 3 Os Elementos Químicos Pouco mais de 110 elementos são conhecidos, mas somente 90 ocorrem naturalmente na Terra. Alguns elementos foram produzidos em laboratório, em aceleradores de partículas. Prof. Gyl Renato 4 2 24/03/2015 Os Símbolos dos Elementos nº de massa Au 197 79 Símbolo químico do elemento Ouro (Aurium) nº atômico Prof. Gyl Renato 5 Átomos Todo átomo é neutro, logo possuem o mesmo número de prótons e elétrons. Au Na C 197 79 22 11 12 6 79 prótons e 79 elétrons 11 prótons e 11elétrons 6 prótons e 6 elétrons Prof. Gyl Renato 6 3 24/03/2015 Átomos Todo átomo é neutro, logo possuem o mesmo número de prótons e elétrons. Quando um átomo eletricamente neutro perde ou recebe elétrons, ele se transforma em um íon. Íon negativo é chamado de ânion. Íon positivo é chamado de Câtion. Prof. Gyl Renato 7 Átomos 37 Cl 2 8 7 Na 2 8 Perdendo 1 um elétron 17 23 11 Ganhando um elétron Prof. Gyl Renato 37 Cl 17 23 11 - 28 8 +2 Na 8 8 4 24/03/2015 Massa Atômica O átomo do carbono-12 foi escolhido como padrão. Uma unidade de massa atômica (1 u.m.a.) vale um doze avos (1/12) da massa atômica do carbono-12. Exemplo 1: a massa atômica do hélio é 4 u.m.a., ou seja, 4 vezes 1/12 a massa do carbono-12. Exemplo 2: a massa atômica do cloro é 35,453 u.m.a., ou seja, 35,453 vezes 1/12 a massa do carbono-12. 9 Isótopos São os elementos químicos que possuem o mesmo número de prótons, ou seja, mesmo número atômico, porém se diferem pelo número de nêutrons. + 1 1 H HIDROGÊNIO + 2 1 H DEUTÊRIO + 3 1 H TRÍTIO 10 5 24/03/2015 Isótopos Os isótopos possuem suas propriedades químicas iguais, pois este fator está relacionado com a estrutura de sua eletrosfera; mas têm suas propriedades físicas diferentes, já que este fator depende da massa do átomo, que no caso, são diferentes. 1 1 2 H 1 HIDROGÊNIO H DEUTÊRIO 11 Isóbaros São átomos de diferentes números de próton, mas que possuem o mesmo número de massa (A). Assim, são átomos de elementos químicos diferentes, mas que têm mesma massa, já que um maior número de prótons será compensado por um menor número de nêutrons, e assim por diante. Desse modo, terão propriedades físicas e químicas diferentes. 14 14 6 7 C CARBONO N NITROGÊNIO 12 6 24/03/2015 Isótonos São átomos de diferentes números de prótons e de massa, mas que possuem mesmo número de nêutrons. Ou seja, são elementos diferentes, com propriedades físicas e químicas diferentes. 11 10 5 4 B BORO N=A- Z N = 11 - 5 N=6 Be BERÍLIO N =A- Z N = 10 - 4 N=6 13 Exercício 3 do livro texto (pág. 65): Um átomo X possui 8 elétrons e seu número atômico é igual a 8. Sabendo que esse átomo é isótopo de Y, que possui número de massa 18, responda: qual o número de nêutrons do átomo Y?. ? 8 X 18 8 Y N =A- Z N = 18 - 8 N = 10 14 7 24/03/2015 Exercício de Fixação nº 4, da lista: As letras A, B, C, D e E, representam átomos aleatórios, e possuem os seguintes nº atômicos e nº de massa: 36 37 40 38 e 40 18A , 19B , 18C , 20D 19E . Verifique quais são isótopos, isóbaros e isótonos entre si. Isótopos 36 18 A 40 18 Isóbaros 40 18 C 40 19 C E 15 Exercício de Fixação nº 4, da lista: As letras A, B, C, D e E, representam átomos aleatórios, e possuem os seguintes nº atômicos e nº de massa: 18A36, 19B37, 40 38 e 19E40. Verifique quais são isótopos, 18C , 20D isóbaros e isótonos entre si. Isótonos 36 18 A N=A- Z N = 36 - 18 N = 18 36 18 36 18 38 20 A B D 40 38 37 40 18 C 20 D 19 E 19 B N = 18 N = 22 N = 18 N = 21 16 8 24/03/2015 Exercício de Fixação nº 5, da lista: Considere os seguintes íons: Cr2+ e Cr3+. Qual o número de prótons, elétrons e nêutrons de cada um dos íons? 52 prótons= 24 2+ elétrons =(24-2)= 22 Cr 24 N =A- Z N = 52 - 24 N = 28 nêutrons =28 52 24 prótons= 24 Cr3+ elétrons =(24-3)= 21 N=A- Z N = 52 - 24 N = 28 nêutrons =28 17 TABELA PERIÓDICA Prof. Gyl Renato 18 9 24/03/2015 TABELA PERIÓDICA Metais alcalinos Metais alcalinos-terrosos Metais de transição Outros metais Não-metais Gases nobres Lantanídeos Prof. Gyl Renato Actinídeos 19 Relação da T. P. com a dist. Eletrônica S p d f Prof. Gyl Renato 20 10 24/03/2015 2 8 18 32 32 18 2 K L M N O P Q 1s2 2s2 3s2 4s2 5s2 6s2 7s2 2p6 3p6 4p6 5p6 6p6 3d10 4d10 4f14 5d10 5f14 6d10 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 216d10 10 20 38 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 54 70 86 102 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 118 7p6 ... 22 11 24/03/2015 Relação da T. P. com a dist. Eletrônica 1 133 55 Cs 1 2 55 elétrons p 3 4 5 S d 6 Cs 7 Dist. Elet.: 55 elétrons 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s1 Prof. Gyl Renato 23 Relação da T. P. com a dist. Eletrônica 1 1 2 2 40 20 Ca 20 elétrons p 3 4 5 6 S Ca 7 Dist. Elet.: 20 elétrons d 1s2 2s2 2p6 3s2 3p6 4s2 Prof. Gyl Renato 24 12 24/03/2015 Relação da T. P. com a dist. Eletrônica 1 1 6 2 2 3 4 5 6 19 9 1 F S 9 e- Dist. Elet.: 9 elétrons 4 p d 7 2 3 5 F 1s2 2s2 2p5 Prof. Gyl Renato 25 Relação da T. P. com a dist. Eletrônica 1 1 2 2 3 4 5 6 6 Antimônio 122 51 S 7 Dist. Elet.: 51 elétrons Sb 1 2 3 51 e- d Sb 4 5 p 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p3 Prof. Gyl Renato 26 13 24/03/2015 Relação da T. P. com a dist. Eletrônica 1 1 65 30 2 2 3 4 5 6 1 S 6 Zn 2 3 4 30 e5 6 7 8 1 2 3 5 p 9 10 Zn d 7 4 1s2 2s2 2p6 3s2 3p6 4s2 3d10 Dist. Elet.: 30 elétrons Prof. Gyl Renato 27 Relação da T. P. com a dist. Eletrônica 1 1 2 3 4 5 6 7 6 165 68 Er 2 68 e- 1 2 3 4 5 6 7 8 9 10 d S 1 2 3 4 5 6 7 8 p 9 10 11 12 13 14 f D. E. : 68 e- 1 2 3 4 5 Er 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f12 28 Prof. Gyl Renato 14 24/03/2015 Relação da T. P. com a dist. Eletrônica 1A 1 8A 2A 2 3 4 5 6 19 9 3A 4A 5A 6A 7A F S 9 e- d 7 Dist. Elet.: 9 elétrons p F Família 7A 1s2 2s2 2p5 Prof. Gyl Renato 29 Relação da T. P. com a dist. Eletrônica 1A 1 Antimônio 2A 2 3 4 5 6 122 51 S 7 Dist. Elet.: 51 elétrons Sb d 8A 3A 4A 5A 6A 7A 51 e- Sb p Família 5A 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p3 15 24/03/2015 Descubra a família e o período dos elementos com nº atômico: 19, 32, 36, 38, 52 e 83. Exercício de fixação nº1: Período=4 (N) Família=1A Z=19= 1s2 2s2 2p6 3s2 3p6 4s1 Família=4A Z=32= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p2 Período=4 (N) Família=8A Z=36= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 Período=4 (N) 31 Exercício de fixação nº1: Descubra a família e o período dos elementos com nº atômico: 19, 32, 36, 38, 52 e 83. Z=38= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 Família=2A Período=5 (O) Z=52= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p4 Período=5 (O) Família=6A Z=52= 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p3 Período=6 (P) Família=5A 32 16 24/03/2015 LINKS DE TABELA PERIÓDICA http://www.portalsae.com.br/includes/objetoAprendizagem/Ta belaPeriodica.swf http://www.ptable.com/?lang=pt Fim da apresentação. Obrigado. 17
Baixar