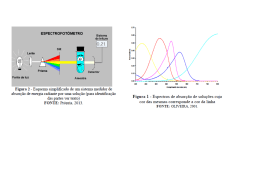
MF-605.R-3 - MÉTODO DE PARARROSANILINA (determinação SO2 no ar) Notas: Aprovada pela Deliberação CECA nº 027, de 06 de julho de 1978 Publicada no DOERJ de 27 de julho de 1978 1. OBJETIVO O objetivo deste documento é definir o Método de Pararrosanilina para determinação de Dióxido de Enxofre (SO2) no ar, a ser adotado nas atividades de controle de poluição do ar ambiente, como parte integrante do Sistema de Licenciamento de Atividades Poluidoras. 2. CARACTERÍSTICAS GERAIS DO MÉTODO: 2.1 Descrição Geral: O dióxido de enxofre é absorvido do ar numa solução de tetracloromercurato de potássio (TCM). É formado um complexo de diclorossulfitomercurato, resistente à oxidação pelo oxigênio do ar. Uma vez formado, este complexo é estável a oxidantes fortes (ex: ozônio, óxidos de nitrogênio). O complexo reage com pararrosanilina e formaldeído formando o ácido pararrosanilina metil sulfônico, intensamente colorido. A absorbância da solução é medida espectrofotometricamente. 2.2 Condições Gerais de Emprego do Método: O método é utilizado para medição de dióxido de enxofre no ar ambiente usando períodos de amostragem de até 24 horas. 2. 3 Concentrações Limite de Dióxido de Enxofre Concentrações de dióxido de enxofre na faixa de 25 a 1050 g/m3 (0,01 a 0,40 ppm) podem ser medidas sob dadas condições. Pode-se medir concentrações abaixo de 25 g /m3 por amostragem de maiores volumes de ar, somente se a eficiência de absorção do sistema for previamente determinada. Maiores concentrações podem ser analisadas usando amostras menores, uma maior coleta de volume, ou uma alíquota adequada da amostra coletada. A lei de Beer é seguida dentro da faixa de trabalho de 0,03 a 1,0 unidade de absorbância (0,8 a 27 g de íon sulfito num volume final de 25 ml, computado como SO 2). 2.4 Sensibilidade do Método: O limite inferior de detecção de dióxido de enxofre em 10 ml de TCM é O,75 g (baseado em duas vezes o desvio padrão), representando uma concentração de 35 gSO2 /m3(0,0l ppm) numa amostra de ar de 30 litros. 2.5 Interferências: 2.5.1 Os efeitos das principais minimizados ou eliminados. 2.5.2 Interferências por óxidos de nitrogênio são eliminados por ácido sulfâmico; ozônio por tempo de espera e metais pesados por EDTA (ácido etileno diaminotetracético, sal dissódico) e ácido fosfórico. 2.5.3 Até 60 g de Fe (III), 10 g de Mn (II), e 10 g de Cr(III) em 10 ml de reagente de absorção podem ser toleradas no procedimento. Nenhuma interferência foi observada com 10 g de Cr (II) e 22 g de V (V). 2.6 Precisão, Exatidão e Estabilidade: 2.6.1 O desvio padrão relativo, em 95% do nível de confiança, é de 4,6% para o procedimento analítico usando amostras padrão. 2.6.2 Após a coleta da amostra as soluções são relativamente estáveis. A 22 ºC perdas de dióxido de enxofre ocorrem numa taxa de 1% por dia. Quando as amostras são guardadas a 5 ºC por 30 dias, perdas detectáveis de dióxido de enxofre não ocorrem. A presença de EDTA aumenta a estabilidade do SO2 na solução, e a taxa de decomposição é independente da concentração de SO2. 3. APARELHAGEM 3.1 Aparelhagem para Amostragem: 3.1.1 Borbulhador 3.1.1.1 São aceitos borbulhadores normalmente usados em amostragem de poluição do ar para concentrações acima de 25 g/m3 (0,01 ppm). Um borbulhador de vidro (impinger midget), mostrado na figura 1, é recomendado para amostras de 30 minutos e 1 hora. interferências conhecidas têm sido 3.1.1.2 Para amostragem de 24 horas, montar um borbulhador que pode ser um tubo de polipropileno de 164 por 32 mm, ou um tubo de polipropileno com tampa de 2 saídas, de fabricação especial, ou ainda um borbulhador de vidro com diâmetro de 6 mm e 6 polegadas de comprimento. 3.1.2 Bomba Deve ser usada uma bomba capaz de manter uma pressão diferencial de ar maior que 0,7 atmosferas na vazão desejada. 3.1.3 Medidor de Vazão de Ar ou Orifício Crítico 3.1.3.1 Empregar um rotâmetro calibrado ou um orifício crítico capaz de medir a vazão de ar dentro de ± 2%. 3.1.3.2 Para amostragem de 30 minutos, uma agulha hipodérmica de calibre 22 e 1 polegada de comprimento pode ser usada como sendo um orifício crítico para dar uma vazão de cerca de 1 litro/minuto. 3.1.3.3 Para amostragem de 1 hora, uma agulha hipodérmica de calibre 23 e de 5/8 de polegada de comprimento, pode ser usada para fornecer uma vazão, em torno de 0,5 litro/minuto. 3.1.3.4 Para amostragem de 24 horas pode-se usar uma agulha hipodérmica de calibre 27 e 3/8 de polegada de comprimento para dar uma vazão em torno de 0,2 litro/minuto. 3.1.3.5 Usar um filtro de membrana para proteger a agulha (ver figura 2a). 3.2 Aparelhagem para Análise: ESPECTROFOTÔMETRO 3.2.1 Será empregado espectrofotômetro adequado para medir absorbância em 548 nm com uma banda espectral efetiva de largura menor que 15 nm. 3.2.2 Problemas com o branco podem ocorrer com espectrofotômetros que tenham largura da banda espectral maior. 3.2.3 A calibração do comprimento da onda do instrumento deve ser verificada. 3.2.4 Se medirmos transmitância, esta pode ser convertida para absorbância através da fórmula: A = log10 (1/T), onde: A = absorbância (nm) T = transmitância 4. REAGENTES: 4.1 Reagentes a Empregar na Amostragem: 4.1.1 Água destilada Deve ser livre de oxidantes. 4.1.2 Reagente de Absorção: Tetracloromercurato de potássio (TCM) 0,044 M Dissolver 10,86 g de cloreto mercúrico, 0,06 g de EDTA (ácido etilenodiamino tetracítico, sal dissódico), e 6,0 g de cloreto de potássio em água e completar até a marca, em balão volumétrico de 1 000 ml. (Cuidado: altamente venoso. Se cair na pele, lavar imediatamente com água). O pH deste reagente deve ser aproximadamente 4,0 mas tem sido notado que não há diferença apreciável na eficiência da coleta na faixa de pH 5 a pH 3. O reagente da absorção e normalmente estável por 6 meses. Não utilizar o reagente se um precipitado se formar. 4.2 Reagentes a Empregar na Análise: 4.2.1 Acido Sulfâmico 0,6% Dissolver 0,6 g de ácido sulfâmico em 100 ml de água destilada. Preparar diariamente. 4.2.2 Formaldeído 0,2% Diluir 5 ml de formaldeído (36 -38%) para 1 000 ml com água destilada. Preparar diariamente. 4.2.3 Solução estoque de iodo (0,1 N) Colocar 12,7 g de iodo em becher de 250 ml, adicionar 40 g de iodeto de potássio e 25 ml da água. Agitar até completar dissolução e então completar o volume a 1 000 ml com água destilada. 4.2.4 Solução de iodo (0,01 N) Diluir 50 ml de solução de iodo 0,1 N para 500 ml com água destilada. 4.2.5 Solução de Amido Indicador Misturar 0,4 g de amido solúvel é 0,002 g de iodeto mercúrico (preservativo) com um pouco de água. Adicionar a pasta lentamente em 200 ml de água fervendo. Continuar fervendo até que a solução fique clara. Esfriar e transferir a solução para um vidro de tampa esmerilhada. 4.2.6 Solução estoque de Tiosulfato de sódio (0,1 N) 4.2.6.1 Dissolver 25 g de tiosulfato de sódio (Na2S2O3.5 H2O) em 1000 ml de água destilada, fervida antes de usar e depois resfriada. Adicionar 0,1 g de carbonato de sódio à solução. Deixar a solução em repouso por um dia antes da padronização. 4.2.6.2 Para fazer a padronização, pesar, com precisão de 0,1 mg, 1,5 g de iodato de potássio, seco a 180 ºC, e diluir até a marca em um balão volumétrico de 500 ml. Pipetar 50 ml da solução de iodato para um erlenmeyer de 500 ml com tampa esmerilhada. Adicionar 2 g de iodeto de potássio e 10 ml com tampa esmerilhada. Adicionar 2 g de iodeto de potássio e 10 ml de ácido clorídrico 1 N. Fechar o erlenmeyer. Depois de 5 minutos, titular com solução estoque de tiosulfato 0,1 N até amarelo-pálido. Então adicionar 5 ml de solução de amido e continuar a titulação até o desaparecimento da cor azul. 4.2.6.3 Calcular a normalidade da solução estoque de tiosulfato através da fórmula: N = Normalidade da solução de tiosulfato; V = Volume de tiosulfato gasto (ml); M = Massa de iodato de potássio; em g 4.2.7 Solução titulante de tiosulfato de sódio (0,01 N) Diluir 100 ml de solução estoque de tiosulfato para 1 000 ml com água destilada recentemente fervida, obtendo-se desta forma: (Normalidade) = (Normalidade da Solução Estoque) x 0,100 4.2.8 Solução padrão de sulfito para a preparação da solução de sulfito -TCM Dissolver 0,3 g de metabisulfito de sódio (Na2 S2 O5) ou 0,40 g de sulfito de sódio (Na2 SO3) em 500 ml de água destilada recentemente fervida e esfriada (solução de sulfito é instável: sendo assim, é importante o uso de água com o mais alto grau de pureza para minimizar essa instabilidade). Essa solução contém o equivalente de 320 a 400 g/ml de SO2. A concentração da solução é determinada adicionando-se excesso de iodo e titulando-se com solução padrão de tiosulfato de sódio. Para titular, pipetar 50 ml de iodo 0,01 N em cada um dos dois frascos de iodo de 500 ml. (A e B) .Ao frasco A (branco) adicionar 25 ml de água destilada, e ao frasco B (amostra) pipetar 25 ml da solução de sulfito. Repousar os frascos e deixar reagir por cinco minutos. Preparar a solução padrão de sulfito TCM (item 4.2.9) ao mesmo tempo que a solução de iodo é adicionada aos frascos. Utilizando-se uma bureta contendo tiosulfato 0,01N, titular cada frasco até atingir uma coloração amarelo pálido. Adicionar 5 ml de solução de amido e continuar a titulação até a cor azul desaparecer. 4.2.9 Solução padrão de sulfito TCM 4.2.9.1 Pipetar precisamente 2 ml de solução padrão em um balão volumétrico de 100 ml e completar com TCM 0,04 M. 4.2.9.2 Calcular a concentração de dióxido de enxofe na solução padrão, com o emprego de fórmula, gSO2 /ml = ( A B ).(N ).(32.000) .0,02 onde: 25 A = Volume de tiosulfato gasto no branco (ml), B = Volume de tiosulfato gasto na amostra (ml); N = Normalidade da solução titulante de tiosulfato; 32.000 = Miliequivalente de SO2 (g); 25 = Volume da solução padrão de sulfito (ml); 0,02 = Fator de diluição. 4.2.9.3 Essa solução é estável por 30 dias se for mantida a uma temperatura de 5 ºC. Se a solução não for mantida nesta temperatura, preparar diariamente. 4.2.10 Solução estoque de Pararrosanilina purificada (percentual nominal 0,2) 4.2.10.1 Especificações do corante O corante deve apresentar as seguintes especificações: a) Deve ter absorbância máxima em 540 nm quando ensaiada numa solução tampão de acetato de sódio - ácido acético 0,1 M; b) A absorbância do reagente branco, sensível à temperatura (0,015 unidades de absorbância/ºC), não deve exceder 0,170 unidades de absorbância a 22 ºC, com 1 cm, de faixa de passagem ótica, quando o branco é preparado de acordo com o procedimento analítico. c) A curva de calibração (item 6.2) deve ter um coeficiente angular de 0,030 ± 0,002 unidades de absorbância/ g SO2, quando o corante está puro e a solução de sulfito foi padronizada corretamente. 4.2.10.2 Preparo da solução estoque Uma solução especialmente purificada de pararrosanilina (99-l00% pura), apresentando as especificações do subitem anterior pode ser utilizada no preparo da solução 0,2%. Porém, o corante pode ser purificado, uma solução estoque preparada e ensaiada de acordo com o procedimento de Scaringelli. 4.2.11 Reagente pararrosanilina Em um balão volumétrico de 250 ml adicionar 20 ml da solução estoque (4.2.10). Para cada um por cento da solução estoque ensaiada abaixo de 100%, adicionar 0,2 ml. Juntar 25 ml de ácido fosfórico 3 M e completar o volume com água destilada. Este reagente é estável pelo menos por 9 meses. 5 PROCEDIMENTO: 5.1 PROCEDIMENTO PARA AMOSTRAGEM: 5.1.1 O procedimento é descrito para amostragem de curta duração (30 minutos e l hora) e para amostragem de longa duração (24 horas). Pode-se fazer diferentes combinações de vazão e tempo de amostragem para atender as especificações do método. 5.1.2 Amostragem de curta duração (30 minutos e 1 hora) 5.1.2.1 Colocar um borbulhador no sistema como mostra a figura 2. Colocar 10 ml da solução de TCM no borbulhador. Coletar amostra a uma vazão de 1 litro/minuto por 30 minutos ou a 0,5 litros/minuto por 1 hora, usando um rotâmetro, como mostra a figura 2, ou um orifício crítico, como mostra a figura 2a, para controlar a vazão. 5.1.2.2 Proteger o reagente de absorção da incidência direta do sol, durante e após a amostragem, cobrindo o borbulhador com folha de alumínio. Determinar o volume de ar amostrado, multiplicando-se a taxa de vazão pelo tempo em minutos e anotar a pressão atmosférica e a temperatura. Guardar a amostra a 5 ºC se esta (ver item 2.6.2) for estocada por mais de um dia antes da análise. 5.1.3 Amostragem de longa duração (24 horas) Colocar 50 ml da solução de TCM no tubo de absorção e coletar a amostra a 0,2 litros/minuto por 24 horas de 0 a 24 horas. Durante a coleta e a estocagem proteger contra os raios solares. Determinar o volume total de ar multiplicando-se a taxa de vazão pelo tempo em minutos. A correção da temperatura e pressão para amostragem de 24 horas é extremamente difícil e normalmente não é feita. Entretanto, a exatidão do resultado será maior se uma correção média puder ser feita. Se for necessário estocar a solução a 5 ºC. 5.2 PROCEDIMENTO PARA ANÁLISE: 5.2.1 Preparo da amostra: Após a coleta, se um precipitado se formar, centrifugar a solução. 5.2.1.1 Amostragem de 30 minutos e 1 hora - transferir a amostra quantitativamente para um balão volumétrico de 25 ml, usar cerca de 5 ml de água destilada para lavagem. Deixar em repouso por 20 minutos para que haja decomposição do ozônio. 5.2.1.2 Amostragem de 24 horas - diluir a amostra para 50 ml com solução absorvente. Pipetar 5 ml da amostra em um frasco volumétrico de 25 ml. Levar a 10 ml com reagente de absorção. Repousar por 20 minutos para que haja decomposição do ozônio. 5.2.2 Determinação: 5.2.2.1 Para uma batelada de amostras preparar um reagente branco, adicionando-se 10 ml da solução absorvente (TCM) em um balão volumétrico de 25 ml. 5.2.2.2 Preparar uma solução de controle adicionando-se 2 ml da solução padrão de sulfito - TCM e 8 ml da solução de TCM em um balão volumétrico de 25 ml. Para cada balão contendo a amostra, solução de controle ou reagente branco, pipetar 1 ml de ácido sulfâmico 0,6% e deixar que se efetue a reação durante 10 minutos para eliminar o nitrito proveniente dos óxidos de nitrogênio. Pipetar precisamente 2 ml de solução de formaldeído 0,2% e a seguir 5 ml da solução de pararrosanilina. Completar todos os balões com água destilada e fervida a 25 ml e agitar. 5.2.2.3 Após um intervalo de 30 minutos e antes de completar 60 minutos, determinar as absorbâncias da amostra (denominada A), do reagente branco (denominado A0 ) e da solução de controle em 548 nm, usandose uma cubeta de 1 cm. 5.2.2.4 Usar como referência água destilada e não o reagente branco (NOTA: Isto é importante por causa da sensibilidade da cor do reagente branco com mudanças de temperatura que podem ser induzidas no compartimento da célula do espectrofotômetro). 5.2.2.5 Não permitir que a solução colorida permaneça nas células de absorbância durante muito tempo porque há formação de uma película. Limpar as células com álcool após o uso. 5.2.2.6 Se a temperatura das determinações não diferir mais do que 2 ºC da temperatura de calibração (item 6.2), o reagente branco deve estar dentro de uma faixa de 0,03 unidades de absorbância na interseção da curva de calibração com eixo - Y. Se o reagente branco variar mais do que 0,03 unidades de absorbância do valor encontrado na curva de calibração, fazer uma nova curva. 5.2.3 Faixa de Absorbância: 5.2.3.1 Se a faixa de absorbância da amostra estiver entre 1,0 e 2,0, a amostra pode ser diluída de 1 : 1 com o reagente branco e a leitura efetuada dentro de poucos minutos. 5.2.3.2 Soluções com absorbância mais alta podem ser diluídas em até seis vezes como reagente branco, a fim de obter leituras dentro de 10% do valor da absorbância real. 6 CALIBRAÇÃO E EFICIÊNCIA: 6.1 MEDIDOR DE VAZÃO E AGULHA HIPODÉRMICA Calibrar o medidor de vazão (flowmeter) e a agulha hipodérmica contra um medidor de vazão padrão (Wet Test Meter). 6.2 Curvas de Calibração 6.2.1 Procedimento com a solução de sulfito - TCM Pipetar, com precisão, volumes da solução de sulfito - TCM (item 4.2.9) correspondentes a 0: 0,5; 1,0; 2,0; 3,0 e 4,0 ml em uma série de balões volumétricos de 25 ml. Adicionar aproximadamente 10 ml da solução de TCM. Então adicionar os reagentes de acordo com o descrito no item 5.2.2. 6.2.1.2 Para uma maior precisão usar um banho a temperatura constante. A temperatura de calibração deve ser mantida dentro de ± 1 ºC e na faixa de 20 ºC a 30 ºC. A variação entre a temperatura de calibração e a temperatura de análise deve ser de dois graus aproximadamente. 6.2.1.3 Plotar absorbância contra a massa total em gSO2. A massa total em gSO2 é igual a concentração da solução padrão (item 4.2.9) em gSO2/ml multiplicada pelo volume de sulfito adicionado ( gSO2 total = gSO2/ml x ml adicionado). 6.2.1.4 Uma relação linear deve ser obtida e a interseção no eixo - y estaria a ± 0,03 unidades de absorbância padrão. 6.2.1.5 Para uma maior precisão determinar a melhor reta usando análise regressiva pelo método dos mínimos quadrados. Determinar o coeficiente angular através da seleção dos melhores pontos, calcular o seu inverso e denominá-lo como fator de calibração Bs (ver item 4.2.10.1 as especificações sobre o coeficiente angular da curva de calibração). Este fator de calibração pode ser usado para calcular os resultados das amostras onde não haja uma variação de temperatura ou pH. Finalmente, uma solução de controle contendo uma concentração conhecida de SO2 é recomendada para assegurar uma maior confiabilidade deste fator. 6.2.2 Procedimento com os tubos de Permeação de SO2: 6.2.2.1 6.2.2.2 Considerações Gerais: a)- Atmosferas contendo concentrações conhecidas de dióxido de enxofre em níveis desejados podem ser preparadas usando tubos de permeação. O tubo de permeação emite SO 2 em uma faixa de concentração baixa e constante, quando a temperatura do mesmo é mantida numa variação de ± 0,1 ºC desde que o tubo seja precisamente calibrado à temperatura de uso. b)- O gás de permeação do tubo é arrastado por um baixo fluxo de gás inerte para uma câmara de mistura onde é diluído com ar livre de SO2. c)- Estes sistemas são mostrados esquematicamente nas figuras 3 e 4 e são descritos detalhadamente por O'Keeffe o Ortman, Scaringelli, Frey, Saltzman, Rosenberg e Bell. Preparação de Atmosfera Padrão: a) Os tubos de permeação podem ser preparados ou comprados. Podem ser utilizados tubos com uma permeação certificada do National Bureau of Standards. Tubos com taxas de permeação de 0,2 a 0,4 g/min, vazões do gás inerte de cerca de 50 ml/min e vazões de ar de diluição de 1 litro a 15 litros/minuto fornecem atmosferas padrão contendo os níveis desejados de SO 2 (25 a 390 g/m3; 0,01 a 0,15 ppm SO2). b) A concentração de SO2 em qualquer atmosfera padrão pode ser calculada da seguinte maneira: C = Concentração de SO2 ( g/m3) nas condições de referência; P = Taxa de permeação do tubo; Qd = Vazão do ar de diluição (l/min) nas condições de referência; Qi = Vazão do gás inerte (l/min) nas condições de referência. 6.2.2.3 6.3 Amostragem e Preparação da Curva de Calibração a) Preparar uma série de atmosferas padrão (geralmente 6) contendo níveis de SO2 de 25 a 390 gSO2/m3. Amostrar cada atmosfera usando aparelhagem semelhante e tomando exatamente o mesmo volume de ar como será feito em amostragem do ar. b) Determinar as absorbâncias como descrito no item 5.2. c) Plotar a concentração de SO2 em g/m3 (eixo - X) contra valores de absorbância (A – A0) (eixo - Y). Traçar a melhor reta e determinar o coeficiente angular. Pode ser usada alternativamente, análise de regressão pelo método dos mínimos quadrados para calcular o coeficiente angular da curva. d) Calcular o inverso do coeficiente angular e chamar de Bg. EFICIÊNCIA DA AMOSTRAGEM A eficiência da coleta está acima de 98%; a eficiência pode cair, entretanto, para concentrações abaixo de 25 g SO2 /m3. 7 CÁLCULOS: 7.1 Conversão de Volume: Converter o volume de ar amostrado para as condições de referência, 25 ºC e 760 mm Hg (NOTA: em amostras de 24 horas isto pode não ser possível), lançando mão de expressão: onde: Vr = Volume de Ar a 25 ºC e 760 mm Hg (litros); V = Volume de Ar amostrado (litro); P = Pressão barométrica (mm Hg) t = Temperatura relativa do ar (ºC) 7.2 CONCENTRAÇÃO DE DIÓXIDO DE ENXOFRE 7.2.1 Quando soluções de sulfito são usadas para preparar curvas de calibração, computar a concentração de dióxido de enxofre na amostra através da seguinte fórmula: gSO2 / m3 = (A A0 ).(10 3 ).Bs .D Vr A = Absorbância da amostra; A0 = Absorbância do branco; 103 = Conversão de litros para metro cúbico; Vr = Volume de ar corrigido para 25 ºC e 760 mm Hg (litros); Bs = Fator de calibração (g/unid. de absorbância); D = Fator de diluição, sendo que: para amostras de 30 minutos e 1 hora, temos: D = 1, e para amostras de 24 horas, temos: D = 10 7.2.2 Quando atmosferas padrão de SO2 são usadas para preparar curvas de calibração, computar o dióxido de enxofre na amostra pela seguinte fórmula: gSO2 /m3 =(A-A0) x Bg onde: A = Absorbância da amostra; A0 = Absorbância do branco; Bg = Coeficiente angular da curva. 7.2.3 Conversão de g/m3 para ppm - se desejada, a concentração de dióxido de enxofre pode ser calculada em ppm SO2 nas condições de referência como se segue: ppmSO2 = gSO2/m3 x 3,82 x 10-4 8. BIBLIOGRAFIA DE REFERÊNCIA: 8.1 West, P.W., and Gaeke, G.C., "Fixation of Sulfur Dioxide as Sulfitomercurate III and Subsequent Colorimetric Determination", Anal. Chem., 28, 1816 (1956). 8.2 Ephralms, F. "Inorganic Chemistry", p.562, Edited by P.C.L. Thorne and E. R. Roberts , 5th Edition, Interscience. (1948). 8.3 Lyles, G. R., Dowling, F. B., and Blanchard, V. J., "Quantitative Determination of Formaldehyde in Parts Per Hundred Million Concentration Level". J. Air Poll Cont. Assoc. 15, 106 (1965). 8.4 Scaringelli, F. P., Saltzman, B. E., and .Frey, S.A., "Spectrophotometric Determination of Atmospheric Sulfur Dioxide", Anal. Chem. 39,1709 (1967). 8.5 Pate, J. B. Ammons,. B. E., Swanson, G. A., Lodge, J.P., "Nitrite Interference in Spectrophometric Determination of: Atmospheric Sufur Dioxide,", Anal. Chem. 37, 942 (l965). 8.6 Zurlo, N. and Griffini, A.M., "Meausurement of the SO2 Content of Air in the Presence of Oxides of Nitrogen and Heavy Metais", Med. Lavoro, 53, 230 (1962). 8.7 Scarinigelli, F. P. Elfers, L. Norris, D., and Hochheiser, S., "Enhanced Stability of Sulfur Dioxide in Solution", Anal. Chem. 42, 1818 (197O). 8.8 Lodge, J.P. Jr., Pate, J.B., Ammons, B.E. and Swanson, G.A., "Use Of Hypodermic Needles as Critical Orifices in Air Sampling". J. Air Poll Cont. Assoc. 16, 197 (1966). 8.9 O'Keeffe A.E., and Ortman, G.C." Primary Standards for Trace Gas Analysis", Anal. Chem. 38, 760 (1966). 8.10 Scaringelli, F.P., Frey, S.A., and Saltzman, B.E., "Evolution of Teflon Permeation Tubes for Use With Sulfur Doxide", Amer. Ind. Hygiene Assoc. J. 28, 260 (1970). 8.11 Scaringelli, F. P., O'Keeffe, A. E., Rosenberg. E., and Bell, J. P., "Preparation of Know Concentrations of Gases and Vapors with Permeation Devices Calibrated Gravimetrically", Anal. Chem, 42, 871 (1970) 8.12 Urone, P., Evans, J. B., and Noyes, C. M., "Tracer Techniques in Sulfur Dioxide Colorimetric and Conductiometric Methods", Anal Chem. 37, 1104 (1965) 8.13 Bostrom, C. E., "The Absorption of Sulfur Dioxide at Low Concentrations. (p.p.m.) Studie by an Isotopic Tracer Method", Intern. J. Air Water Poll. 9. 33 (1965).
Baixar