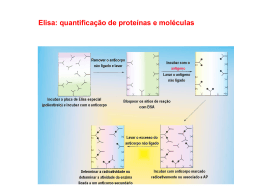
UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA ELÉTRICA E INFORMÁTICA INDUSTRIAL – CPGEI LUCIANA MARTINS PEREIRA DE ARAÚJO Análise de Detecção de Fluorescência para Aplicação em Sistemas de Diagnóstico em Saúde DISSERTAÇÃO CURITIBA 2010 LUCIANA MARTINS PEREIRA DE ARAÚJO Análise de Detecção de Fluorescência para Aplicação em Sistemas de Diagnóstico em Saúde . Dissertação apresentada ao Programa de PósGraduação em Engenharia Elétrica e Informática Industrial da Universidade Tecnológica Federal do Paraná, como requisito parcial para a obtenção do grau de Mestre em Ciências – Área de Concentração: Engenharia Biomédica. Orientador: Prof. Dr. Fábio Kurt Schneider Coorientador: Prof. Dr. Gilberto Branco CURITIBA 2010 Ficha catalográfica elaborada pela Biblioteca da UTFPR – Campus Curitiba A663 Araújo, Luciana Martins Pereira de Análise de detecção de fluorescência para aplicação em sistemas de diagnóstico em saúde / Luciana Martins Pereira de Araújo. — 2010. 93 f. : il. ; 30 cm Orientador: Fábio Kurt Schneider Co-orientador: Gilberto Branco Dissertação (Mestrado) – Universidade Tecnológica Federal do Paraná. Programa de Pós-graduação em Engenharia Elétrica e Informática Industrial. Área de concentração: Engenharia biomédica, Curitiba, 2010. Bibliografia: f. 82-9 1. Espectroscopia fluorescente. 2. Európio. 3. Agentes luminescentes – Uso em diagnóstico. 4. Corantes fluorescentes – Uso em diagnóstico. 5. Engenharia elétrica – Dissertações. I. Schneider, Fábio Kurt, orient. II. Branco, Gilberto, co-orient. III. Universidade Tecnológica Federal do Paraná. Programa de Pósgraduação em Engenharia Elétrica e Informática Industrial. III. Título. CDD (22. ed.) 621.3 Dedico esta dissertação a Deus, pois sem Ele, nada seria possível. À minha família pelo incentivo e confiança. Ao meu esposo e minha filha, pelo apoio incondicional, compreensão e motivação. Enfim, a todos que de alguma forma tornaram este caminho mais fácil de ser percorrido. AGRADECIMENTOS À Coordenação de Aperfeiçoamento de Pessoal de Nível Superior - CAPES, pelo suporte e apoio financeiro a esse projeto. Ao Professor Dr. Fábio Kurt Schneider, pela orientação e confiança. Ao Professor Dr. Arandi Ginane Bezerra Junior e o Dr. Gilberto Branco, pela coorientação, apoio, dedicação e partilha. Aos colegas do CPGEI pelo companheirismo, convívio, estímulo e partilha, em especial, Claúdio Marquetto, Joyce Klock, Terezinha Strapasson, Leonardo Zanin, Neusa Grando e Joaquim de Mira. Aos alunos de Iniciação Científica, Vinícius Oliveira e Eduardo Almeida dos Santos, pelo apoio e aprendizado partilhado. Ao colega Wellington Celestino dos Santos, pelo apoio e pela partilha de aprendizado. Aos professores, pelo conhecimento compartilhado. Ao meu esposo Walter Duarte e minha filha Lívia Helena que colaboraram em todos os momentos, pela paciência, incentivo e amor. Agradeço a Deus que me deu força e sempre esteve presente em minha vida. Aos meus pais Evandro Reis Pereira (in memorian) e Maria da Piedade Martins que sempre me deram força para continuar perseverando rumo ao objetivo a ser alcançado. RESUMO ARAÚJO, Luciana M. P. Análise de detecção de Fluorescência para Aplicação em Sistemas de Diagnóstico em Saúde 2010. Dissertação (Programa de PósGraduação em Engenharia Elétrica e Informática Industrial da Universidade Tecnológica Federal do Paraná). Curitiba, 2010. A técnica de espectroscopia de emissão de fluorescência tem sido utilizada para caracterizar moléculas e compostos moleculares, pois propicia que fluoróforos sejam usados como elementos de marcação de antígenos e/ou anticorpos, que servirão para a identificação de doenças. Assim, o objetivo desta dissertação é analisar a emissão de fluorescência a partir de um novo composto molecular, desenvolvido pelo Laboratório de Polímeros Paulo Scarpa (LaPPS/UFPR) em função do elemento químico európio, denominado complexo LaPPS34M, por meio de um sistema de detecção em estado sólido resolvido no tempo. As características ópticas como: o espectro de absorção, o espectro de fluorescência, o deslocamento de Stokes e os tempos de vida de luminescência resultaram nos parâmetros importantes do complexo para potenciais aplicações em sistemas biomédicos através do projeto INDISAÚDE/PR. Palavras-Chave: Fluorescência, Fluoróforo, Espectroscopia, Diagnóstico, Saúde Pública. ABSTRACT ARAÚJO, Luciana M. P. Fluorescence detection analysis for Application in Diagnostic Systems in Health. 2010. Graduate Program in Electrical Engineering and Computer Science Industrial of the Federal Technological University of Parana). Curitiba. 2010. The technique of fluorescence emission spectroscopy has been used to characterize molecules and molecular compounds. Fluorophores can be used as markup elements of antigens and / or antibodies for identification of disease. Thus, the objective of this dissertation is to analysis the fluorescence emission from a new molecular compound, developed by the Laboratory of Polymers Paulo Scarpa (Lapps / UFPR) according to the chemical element europium, called complex LaPPS34M, through a solid state detection system resolved in time. The optical characteristics as: absorption spectrum, fluorescence spectrum, the Stokes shift and the lifetime of luminescence have resulted in importants parameters of the complex for potential applications in biomedical systems by designing INDI-SAÚDE/PR. Keywords: Fluorescence, Fluorophore, Spectroscopy, Diagnosis, Public Health. LISTA DE FIGURAS Figura 1 - Esquema representativo da marcação do complexo antígenoanticorpo por fluoróforo. ................................................................................... 25 Figura 2 - Apresentação do diagrama de Jablonski. ........................................ 26 Figura 3 - Ilustração do deslocamento de Stokes entre o pico de absorção máxima e o pico de emissão máxima. ............................................................. 32 Figura 4 - Ilustração da estrutura molecular do fluoróforo comercial Cy3. O N+ é o símbolo do íon nitrogênio e o I- é o símbolo do íon iodo. .............................. 38 Figura 5 - Estrutura molecular do complexo LaPPS34M, com os elementos N (nitrogênio) e O ( oxigênio), as cadeias aromáticas (representada pelos hexágonos)....................................................................................................... 39 Figura 6 - Dimensões, formas e tamanhos das nanopartículas metálicas. ...... 42 Figura 7 - Esquema do processo de FRET entre dois fluoróforos, a fluoresceína doadora) e a rodamina (receptora), onde r é a distância de mínima de FRET. 44 Figura 8 - Descrição do processo de FRET pelo de diagrama de Jablonski. ... 45 Figura 9 - Desenho esquemático do espectrofotômetro de duplo feixe ........... 49 Figura 10 - Espectro de absorção do fluoroforo Cy3 obtido pelo espectrofotômetro. ........................................................................................... 51 Figura 11 - Espectro de absorção do complexo LaPPS34M obtido pelo espectrofotômetro ............................................................................................ 51 Figura 12 - Representação esquemática do sistema de detecção proposto .... 52 Figura 13 - Desenho esquemático do sistema experimental por válvula fotomultiplicadora R928 (de alta sensibilidade) ................................................ 53 Figura 14 - Desenho esquemático do sistema com o uso da válvula fotomultiplicadora miniatura (R5600U-01). ....................................................... 54 Figura 15 - Desenho esquemático do sistema experimental por fotodiodo ...... 55 Figura 16 - (a) Dispositivo OPT 301 apresenta um fotodiodo integrado com amplificador conversor corrente-tensão, (b) resposta espectral do OPT 301, (i) emissão de luminescência do indicador (LAPPS34M ~ 615 nm) (ii) excitação do indicador (LAPPS34M ~ 350 nm). .................................................................... 56 Figura 17 – Espectro de emissão da lâmpada xenon ...................................... 58 Figura 18 - Espectro de emissão de led azul, com comprimento de onda do pico é 440 nm. .................................................................................................. 59 Figura 19 - Espectro de emissão de led ultravioleta, com comprimento de onda do pico é 400 nm. ............................................................................................. 59 Figura 20 - Espectro de transmitância do filtro de interferência na região do vermelho........................................................................................................... 61 Figura 21 - Diagrama representativo da transmitância de luz pela amostra na cubeta .............................................................................................................. 63 Figura 22 - llustração do espectro de transmitância da cubeta de quartzo ...... 63 Figura 23 - Representação do processo de geração e multiplicação de elétrons em uma válvula fotomultiplicadora ................................................................... 64 Figura 24 - Circuito de Implementação do Amplificador de Transimpedância . 65 Figura 25 - Espectro de fluorescência do fluoróforo Cy3 obtido pela FASE I (válvula fotomultiplicadora R928) ..................................................................... 68 Figura 26 - Espectro de absorção e emissão de fluoróforo Cy3 demonstrando o deslocamento de Stokes obtido pela FASE I. .................................................. 68 Figura 27 - Espectro de fluorescência do complexo LaPPS34M obtido pela FASE I. ............................................................................................................. 69 Figura 28 - Espectro de absorção e emissão de LaPPS34M demonstrando o deslocamento de Stokes obtido pela FASE I ................................................... 70 Figura 29 - a)Espectro de Fluorescência do fluoróforo Cy3 e b) o espectro de fluorescência do Fluoróforo Cy3 conjugado com Nanopartícula de Ouro obtido pela FASE I. ..................................................................................................... 71 Figura 30 - Espectro de fluorescência (em preto) do complexo LaPPS34M e o espectro de fluorescência do LaPPS34M ( em verde) conjugado com nanopartículas de prata obtido pela FASE I. .................................................... 72 Figura 31 - Decaimento de Fluorescência do Complexo LaPPS34M com o uso da válvula fotomultiplicadora R928 obtido pela FASE I .................................... 74 Figura 32 - Decaimento exponencial de emissão de luminescência do indicador LaPPS34M pela válvula fotomultiplicadora miniatura R5600U-01 obtido pela FASE II. ............................................................................................................ 75 Figura 33 - Sinal elétrico aplicado ao led para excitação do indicador (linha contínua), sinal de saída do detector na ausência do fluoróforo (linha tracejada) e sinal de luminescência na presença do fluoróforo (linha contínua) obtido pela FASE III. ........................................................................................................... 76 Figura 34 - Exponencial de decaimento de emissão de luminescência do indicador LaPPS34M pelo uso detectores de fotodiodo obtido pela FASE III .. 77 Figura 35 - A) Tamanho das nanopartículas de ouro por DLS, B) Espectro de absorção das nanopartículas de ouro e C) Espectro de absorção linear para o colóide de prata ................................................................................................ 95 LISTA DE TABELAS Tabela 1 - Características dos Fluoróforos Comerciais em relação aos comprimentos de onda de absorção e de emissão de fluorescência ............... 31 Tabela 2 - Características ópticas relevantes para um fluoróforo da família Cycorante ............................................................................................................. 39 Tabela 3 - Relação entre as fases da pesquisa e os resultados do tempo de vida de Luminescência ..................................................................................... 77 LISTA DE FOTOGRAFIAS Fotografia 1 - Espectrofotômetro de Duplo Feixe UV-Vis. ................................ 50 Fotografia 2 - Montagem do uso das lentes convergentes no experimento de fluorescência. ................................................................................................... 60 Fotografia 3 - Monocromador do tipo Czerny-Turner. ...................................... 62 LISTA DE ABREVIATURAS E SIGLAS INDI-SAÚDE Instituto Nacional de Inovação em Saúde Pública NAT Teste de Ácido Nucléico DNA Ácido Desoxirribonucléico HIV Human Immunodeficiency Virus Ē Intensidade do Campo Elétrico [V/m] H Intensidade do Campo Magnético [A/m] RNA Ácido Ribonucléico ELISA Enzyme Linked Immuno Sorbent Assay Cy3 Fluoróforo Comercial Cianina (Cyanine) Cy4 Fluoróforo Comercial Cianina (Cyanine) Cy7 Fluoróforo Comercial Cianina (Cyanine) LaPPS34M Complexo de Európio/ Bipiridina/ Dibenzoílmetano PH Pontecial Hidrogeniônico NADH Quinona Oxidorredutase FAD Dinucleotídeo Flavina Adenina NP Nanopartículas DLS Espalhamento Dinâmico da Luz FRET Transferência de Energia de Ressonância Fluorescência Ln Familia dos elementos quimicos dos Lantanídeos Lu Elemento Químico Lutécio Y Elemento Químico Ítrio Sc Elemento Químico Escândio Na Elemento Químico Sódio K Elemento Químico Potássio Sb Elemento Químico Antimônio Cs Elemento Químico Césio de Eu Elemento Químico Európio Eu3+ Representação do Elemento Európio Tb3+ Representação do Elemento Térbio C Elemento Químico Carbono H Elemento Químico Hidrogênio O Elemento Químico Oxigênio Au Elemento Químico Ouro Ag Elemento Químico Prata Ni Elemento Químico Níquel Cu Elemento Químico Cobre La Família dos lantanídeos N Elemento Químico Nitrogênio Z Número Atômico dos Elementos Químicos RMN Ressonância Magnética Nuclear led Light Emitting Diode π Orbital pi Ligante e Antiligante π* Orbital pi Antiligante λ Comprimento de Onda S Estado Singleto S S S 1 2 0 Primeiro Estado Singleto Excitado Segundo Estado Singleto Excitado Estado Singleto Fundamental THF Tetrahidrofurano UV-Vis Espectroscopia na Região do Ultravioleta-Visível OEM Onda Eletromagnética PCR Polimerase Chain Reaction PMT Photo Multiplier Tube USB Universal Serial Bus Gap Fosfeto de Gálio DC-DC Conversor de Corrente Contínua UFPR Universidade Federal do Paraná PR Estado do Paraná CI Conversões Internas CSI Cruzamento Interno LASER Light Amplification by Stimulated Emission of Radiation UTFPR Universidade Tecnológica Federal do Paraná DMSO Dimetilsulfóxido RMSE Quadrado Médio do Erro LaPPS Laboratório de Polímeros Paulo Scarpa DO Densidade Óptica FITC Isotiocianato de Fluoresceína RITC Rodamina AT Amplificador de Transimpêdancia a.u Arbitraries Unites (Unidades Arbitrárias) A ZX Representação do elemento químico (Z é o número atômico e A o número de massa) SUMÁRIO 1. INTRODUÇÃO ........................................................................................... 19 1.1. MOTIVAÇÃO ............................................................................................. 19 1.2. JUSTIFICATIVA ......................................................................................... 20 1.3. OBJETIVOS ............................................................................................... 21 1.3.1. Objetivo Geral ...................................................................................... 21 1.3.2. Objetivos Específicos .......................................................................... 21 1.4. ESTRUTURA DA DISSERTAÇÃO ............................................................ 23 2. FLUORESCÊNCIA E FLUORÓFORO ....................................................... 24 2.1. INTRODUÇÃO ........................................................................................... 24 2.2. COMPLEXO ANTÍGENO- ANTICORPO.................................................... 24 2.3. O FENÔMENO DE FLUORESCÊNCIA ..................................................... 25 2.4. FLUORÓFOROS ....................................................................................... 29 2.4.1. Características Ópticas dos Fluoróforos .............................................. 29 2.4.2. Propriedades dos Fluoróforos Comerciais e dos Complexos Biomarcadores ................................................................................................. 34 2.4.2.1. Fluoróforo Comercial Cy3 .................................................................... 37 2.4.2.2. Complexo LaPPS34M ......................................................................... 39 2.5. NANOPARTÍCULA .................................................................................... 41 2.5.1. Fluoróforo na Presença de Nanopartículas ......................................... 43 2.6. RESUMO ................................................................................................... 46 3. SISTEMAS DE AQUISIÇÃO DE LUMINESCÊNCIA.................................. 47 3.1. INTRODUÇÃO ........................................................................................... 47 3.2. DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DO CY3 E DO COMPLEXO LaPPS34M .................................................................................. 47 3.2.1. Espectrofotômetro de Duplo Feixe ...................................................... 48 3.2.1.1. Espectro de Absorção ......................................................................... 50 3.3. SISTEMA DE AQUISIÇÃO DE SINAL DE FLUORESCÊNCIA .................. 52 3.4. SISTEMA DE DETECÇÃO DE FLUORESCÊNCIA ................................... 57 3.4.1. Fonte Óptica ........................................................................................ 57 3.4.2. Lentes Convergentes e Filtros ............................................................. 59 3.4.3. Monocromador .................................................................................... 61 3.4.4. Cubeta ................................................................................................. 62 3.4.5. Válvulas Fotomultiplicadoras ( PMTs) ................................................. 63 3.4.6. Amplificador de Transimpedância........................................................ 65 3.4.7. Aquisição do Processamento do Sinal ................................................ 66 3.5. RESUMO ................................................................................................... 66 4. RESULTADOS .......................................................................................... 67 4.1. INTRODUÇÃO ........................................................................................... 67 4.2. ESPECTROS DE FLUORESCÊNCIA........................................................ 67 4.3. ESPECTROS DE FLUORESCÊNCIA COM NANOPARTÍCULAS METÁLICAS ..................................................................................................... 71 4.4. TEMPOS DE VIDA DE LUMINESCÊNCIA DO FLUORÓFORO E DO COMPLEXO LaPPS34M .................................................................................. 73 5. DISCUSSÃO E CONCLUSÃO................................................................... 78 5.1. INTRODUÇÃO ........................................................................................... 78 5.2. CARACTERIZAÇÃO DE BIOMARCADORES ........................................... 78 5.3. SISTEMAS DE CUSTO REDUZIDO .......................................................... 80 5.4. LIMITAÇÕES DO ESTUDO ....................................................................... 81 5.5. TRABALHOS FUTUROS ........................................................................... 81 5.6. PUBLICAÇÕES ......................................................................................... 83 6. REFERÊNCIAS BIBLIOGRÁFICAS .......................................................... 84 7. ANEXOS .................................................................................................... 92 19 1. INTRODUÇÃO 1.1. MOTIVAÇÃO Muitas doenças infecciosas, comuns em diversas regioes de países em desenvolvimento, são tratáveis por meio de medicações apropriadas. Isto tem prevenido e diminuído, significativamente, a mortalidade e a morbidade das populações infectadas residentes nestas áreas de risco (MABEY, 2004). Os métodos de diagnósticos mais rápidos certamente auxiliarão para que as doenças infecciosas, que apresenta significantes consequências para a saúde pública, sejam eficientemente controladas se identificadas precocemente (NICHOL, 2000). As técnicas tradicionais de diagnóstico laboratorial incluem os métodos diretos: como a identificação direta do microrganismo por meio da microscopia óptica, e métodos indiretos: como a inoculação de amostras potencialmente infectadas em animais e meios de cultura. Além destes, nos últimos vinte anos, também houve o desenvolvimento de métodos rápidos de diagnóstico, que proporcionaram um avanço importante, pois os resultados podem ser obtidos em poucas horas ou até mesmo em minutos (PERUSK, 2003). Atualmente, várias doenças infecciosas e parasitárias são pesquisadas pelos métodos imunológicos. Graças à sua simplicidade, o método ELISA (Enzyme LinkedImmuno Sorbent Assay) permite reconhecer e quantificar antígenos através de uma reação enzimática (ENGVALL, 1971). Este método é usado para analisar grande número de indivíduos com um volume pequeno de amostra (PERUSK, 2003). Os testes moleculares como o PCR (Polimerase Chain Reaction) em tempo real e os microarranjos líquidos possibilitaram a marcação do complexo antígeno-anticorpo por sondas fluorescentes com diferentes espectros de emissão (YANG, 2004). Ao aplicar os fluoróforos nos estudos diagnósticos, recorre-se a uma área que está em franca expansão. Novas tecnologias estão sendo empregadas à procura de diagnósticos mais rápidos e precisos. Neste sentido, a utilização conjunta da fluorescência através dos fluoróforos levou a criação 20 de outra área de pesquisa, chamada de imunofluorescência, que é a ligação do antígeno e anticorpo através da marcação do anticorpo marcado com uma molécula fluorescente (VALEUR, 2002),(LAKOWICZ,1999). 1.2. JUSTIFICATIVA O esforço do sistema nacional de saúde em ampliar o setor de diagnósticos e conjuntamente integrar a produção acadêmica com o setor produtivo possibilitou a criação do Instituto Nacional de Inovação em Saúde Pública (INDI-SAÚDE), que se situa no Instituto Carlos Chagas – Curitiba/PR (2008). Assim sendo, o objetivo do INDI-SAÚDE, consiste na implantação de novas tecnologias para a produção de sistemas de diagnóstico centrados em doenças causadas por microrganismos importantes para a saúde pública no Brasil. Uma das metas do Instituto é a nacionalização de insumos e sistemas de diagnóstico relevantes para a saúde pública, envolvendo métodos rápidos para utilização no local de tratamento (point of care) (INDI, 2008). Adicionalmente, pretende-se obter procedimentos de multitestes para o diagnóstico e controle do sangue, ou seja, aqueles capazes de detectar mais de uma doença simultaneamente. Os sistemas de diagnósticos desenvolvidos pela Instituto terão seu alicerce no diagnóstico molecular, como os microarranjos líquidos, por ser o método moderno para detecção e quantificação de doenças por microrganismos, como por exemplo doença de chagas e dengue (INDI, 2008). Um dos estudos do Instituto Nacional de Inovação em Saúde Pública é a marcação do complexo antígeno-anticorpo através de fluoróforos para detectar doenças por meio de fluorescência. Essa dissertação representa um dos projetos a serem desenvolvidos pelo INDI-SAÚDE através do complexo LaPPS34M, desenvolvido pelo laboratório de polímeros Paulo Scarpa da UFPR será realizado um estudo de comparação com um fluoróforo comercial Cy3, amplamente utilizado na tecnologia de microarranjos. Algumas características ópticas tais como deslocamento de Stokes e o tempo de vida de luminescência 21 são avaliados para o estudo do potencial de aplicação do complexo LaPPS34M como fluoróforo. 1.3. OBJETIVOS 1.3.1. Objetivo Geral O objetivo principal deste trabalho é analisar a detecção de fluorescência para aplicação em sistemas de diagnósticos com ênfase em um novo composto molecular - desenvolvido em função do elemento químico európio (Eu - grupo dos lantanídeos) - denominado complexo LaPPS34M por meio de um sistema de excitação e detecção em estado sólido resolvido no tempo. 1.3.2. Objetivos Específicos Os objetivos específicos são: 1. Determinar os espectros de absorção do fluoróforo Cy3 e do complexo LaPPS34M e a relação entre os picos máximos de absorção para as amostras. 2. Determinar a relação entre os espectros de fluorescência do fluoróforo Cy3 e do complexo LaPPS34M e os picos máximos de emissão das amostras 3. Avaliar a relação entre a fluorescência de Cy3 e de LaPPS34M na presença de nanopartículas e suas implicações na intensidade de fluorescência. 4. Analisar a detecção de fluorescência com o uso de fotodetectores (válvula fotomultiplicadora R928, válvula fotomultiplicadora miniatura 22 R5600U-01 e de detector optoeletrônico OPT301) e utilizando uma instrumentação de baixo custo. 5. Determinar o tempo de vida de luminescência do complexo LaPPS34M. 23 1.4. ESTRUTURA DA DISSERTAÇÃO O trabalho está dividido em 5 capítulos, onde neste capítulo 1 são expressas as motivações, as justificativas e os objetivos gerais e específicos desta dissertação. O capítulo 2, apresenta uma revisão sobre a luminescência, com ênfase para a fluorescência e suas propriedades físicas. Descreve-se ainda alguns fluoróforos e os fatores que afetam o desempenho dos fluoróforos. O capítulo 3 apresenta o uso do sistema para a identificação de emissão fluorescente; com fonte óptica composta de diodos emissores de luz violeta, chaveados (e controlados) para excitar substâncias fluorescentes em solução aquosas; e detecção com sensor optoeletrônico. O capítulo 4 apresenta os resultados usando a instrumentação implementada quanto à detecção da fluorescência para atingir os objetivos específicos previamente listados. Finalmente, o capítulo 5 apresenta uma discussão e as principais conclusões do trabalho. 24 2. FLUORESCÊNCIA E FLUORÓFORO 2.1. INTRODUÇÃO O capítulo versará sobre a espectroscopia de fluorescência, os fluoróforos e as propriedades ópticas dos fluoróforos comerciais e do complexo LaPPS34M. 2.2. COMPLEXO ANTÍGENO- ANTICORPO Na descricao de imunologia, a interação do antígeno com o anticorpo é fundamental. Essa relação é denominada de complexo antígeno-anticorpo ou complexo imune (ALBERTS et al ,1995). A maior parte dos métodos de diagnósticos baseia-se na detecção do complexo antígeno-anticorpo, ou seja, quando um antígeno, que é definido como uma substância estranha que induz uma resposta imune, causa uma produção de anticorpos e/ou linfócitos sensibilizados que reagem especificamente com a substância ingressa num organismo (VOET, 1995). O sistema imunológico do corpo inicia a produção de anticorpos, que são proteínas que reconhecem um antígeno de forma específica e com alta afinidade e são produzidos pelos linfócitos B, que se originam na medula óssea. Os anticorpos são então distribuídos pelo organismo inteiro através do sistema linfático para neutralizar a ação do antígeno (VOET, 1995). Para que haja detecção do complexo antígeno-anticorpo é necessário que este esteja conjugado com um indicador, conforme apresentado na Figura 1. Os fluoróforos são compostos que emitem luz em certo comprimento de onda quando excitados por uma radiação luminosa de outro comprimento de onda, e podem atuar como biomarcadores, quando conjugados com o complexo antígeno-anticorpo ou estruturas internas de células. 25 A marcação descrita na Figura 1 descreve a ligação entre um anticorpo específico, geralmente de uma espécie diferente da célula, e outro anticorpo, que seja “anti” o anticorpo utilizado anteriormente, sendo este novo anticorpo de uma terceira espécie e tendo sido também previamente marcado por algum fluoróforo, desta maneira, formam-se complexos antígeno-anticorpo marcados, de forma que esta estrutura é bem mais eficiente na detecção de doenças por fluorescência e seu uso em diagnósticos. Figura 1 - Esquema representativo da marcação do complexo antígeno-anticorpo por fluoróforo. Fonte: Modificado de FERREIRA, 2001 2.3. O FENÔMENO DE FLUORESCÊNCIA Quando os fótons são absorvidos por uma molécula, a mesma é levada a um estado excitado. Após um determinado tempo, há o retorno da molécula ao estado fundamental (ou estado não excitado) com a possível emissão de parte da energia absorvida na forma de energia radiante (WILLARD, 1988). Uma forma mais clara de visualização dos estados de excitação das moléculas é apresentada pelo diagrama de Jablonski (Erro! Fonte de referência não 26 encontrada.), que relaciona as transições que ocorrem entre os níveis básicos de energia e os níveis excitados, bem como as reemissões de energia radiante (ATVARS, 2002). Inicialmente, a partir da absorção de radiação, a molécula é promovida para um estado excitado singleto Sn (Erro! Fonte de referência não encontrada.). Posteriormente, a molécula se desativa por relaxamento, através dos níveis vibracionais de estados eletrônicos, até atingir o primeiro nível vibracional do estado excitado singleto de menor energia S1. Este processo de relaxamento recebe o nome de conversão interna (EISBERG, 1988). Figura 2 - Apresentação do diagrama de Jablonski. Fonte: Própria A partir do estado singleto S1, existem alguns caminhos possíveis para a molécula retornar ao estado fundamental: (a) se não há diferença de energia entre o estado excitado e estado fundamental existi a possibilidade de sobreposição de níveis vibracionais, a molécula pode ser levada ao mais baixo nível vibracional do estado excitado por relaxamento vibracional sem emissão de radiação eletromagnética, ou seja, ocorre um cruzamento interno. (b) se, no entanto, a diferença energética entre o estado excitado e estado fundamental for relativamente grande, a desativação para o estado fundamental se dá com emissão de radiação na forma de fluorescência 27 (VALEUR, 2002). Isto quer dizer que o spin1 do estado excitado mantém sua orientação original e há uma maior probabilidade de acontecer essa configuração. Corresponde a um fenômeno rápido, na ordem de 10-9 a 10-7 segundos (EISBERG, 1988). (c) se ocorrer um cruzamento entre sistemas, que é a transferência de elétrons entre estados de diferentes multiplicidades de spins. Outro fenômeno de desativação se faz presente é a fosforescência. Esta representa emissão de fótons após as transições do estado singleto para o estado tripleto, isto é, neste tipo de fenômeno o spin se mantém de forma contrária da sua posição inicial e o tempo de duração é maior, na ordem de 10-3 s a 10 s (AMANDO,2004). O uso da fluorescência é um dos métodos para aplicação em sistemas de diagnósticos, utilizados pelo Instituto Nacional de Inovação para Diagnósticos em Saúde Pública do Paraná (INDI-SAÚDE/PR), que busca sondas fluorescentes de baixo custo que possam ser utilizadas em kits diagnósticos para a detecção de doenças por microorganismos demandas do sistema de saúde pública nacional. O complexo LaPPS34M faz parte das sondas fluorescentes compostas de Európio (Eu3 +) ou Térbio (Tb3 +) que estão sendo estudados para aplicação em sistemas biomédicos (ALBANI, 2007). Os tempos de vida dos fluoróforos destes elementos estão na escala de tempo de milisegundos e surgem de transições entre os orbitais f dos átomos. Possuem características ópticas relevantes na marcação de doenças, pois têm grande fotoestabilidade. a) Fatores que afetam a fluorescência Há uma grande variedade de fluoróforos e, consequentemente, uma gama de espectros de absorção e emissão, além de uma diferenciação dos 1 O spin corresponde a um grau de liberdade interno do elétron,e, embora seja descrito como de forma aproximada com o movimento do elétron em torno do seu próprio eixo, é uma propriedade intrínseca da partícula (CARUSO, 2006). 28 tempos de vida de luminescência para cada biomarcador. A detecção de fluorescência pode então sofrer modificações na sua intensidade com as mudanças de temperatura, pH, a possibilidade de interação com solvente, viscosidade, polarização, pressão e suas interações com os solutos (VALEUR,2002),(LAKOWICZ,1999). O aumento da temperatura tem como consequência um aumento na eficiência dos processos de conversões internas (CI) na desativação do estado excitado (Figura 02). No entanto, por ser um fenômeno de tempo de vida relativamente curto, esse fator é menos crítico no caso da fluorescência, o que permite fácil observação do fenômeno na temperatura ambiente (BASSI, 2001). Para o caso do pH, a fluorescência de compostos aromáticos com funcionalidades ácidas ou básicas apresentam forte dependência com o pH, desta forma, é importante manter o pH das amostras sempre constante. A presença de outros grupos químicos, como o oxigênio dissolvido, pode levar a uma diminuição da fluorescência pelo aumento do cruzamento inter sistemas (CSI), conforme Erro! Fonte de referência não encontrada.. O decréscimo na viscosidade da solução que possui o fluoróforo leva a diminuição da taxa de colisões moleculares levando a uma diminuição da difusão dos fótons de fluorescência Os solventes contendo átomos pesados acarretam na diminuição da energia relativa do estado excitado. Essa diminuição de energia pode levar a um aumento da eficiência das conversões internas (CI) e em contrapartida a diminuição da fluorescência (BASSI, 2001). Todos os fatores acima mencionados contribuem para que a fluorescência seja atenuada. Os testes foram realizados a temperatura ambiente, com o pH 7 fixo, a viscosidade é mantida constante e a diluição foi realizada para manter a razão entre solvente e soluto sempre a mesma. Nesta dissertação as condições acima elencadas foram necessárias para manter o sistema constante ao longo das experiências ora realizadas 29 2.4. FLUORÓFOROS Os fluoróforos formam um grupo químico que fluoresce quando exposto a luz de um determinado comprimento de onda. Cada fluoróforo tem um espectro de emissão e de excitação característico. Prasad (2003) classifica os fluoróforos em duas categorias, os fluoróforos intrínsecos ou naturais, e os fluoróforos biomarcadores, não naturais. Os fluoróforos intrínsecos são aqueles que ocorrem naturalmente. As proteínas como triptofano, tirosina e a fenilalamina, e algumas enzimas NADH, FAD e Ribofavin encontrados dentro das células e dos tecidos são caracterizados como fluoróforos intrínsecos, alguns destes fluoróforos encontram-se ilustrados no anexo A. Eles podem ser usados para estudar as estruturas dinâmicas das células e das proteínas. Também servem como parâmetros para os estudos de autofluorescência (LAKOWICZ,1999). Os fluoróforos extrínsecos são aqueles que são adicionados a uma amostra e chamados também de biomarcadores. Os fluoróforos comerciais como a família das sondas cyanines são representativas desse grupo, representados no anexo B. As fluorescências advindas de sondas fluorescentes apresentam alta intensidade, são estáveis durante iluminação contínua e não perturbam o processo ou a biomolécula onde está sendo estudada (LAKOWICZ,1999). O fluoróforo comercial Cy3 e o complexo LaPPS34M são sintetizados em laboratórios e classificam-se como fluoróforos extrínsecos, sendo caracterizados como biomarcadores. 2.4.1. Características Ópticas dos Fluoróforos Algumas propriedades, como os espectros de absorção e de emissão, o deslocamento de Stokes e o tempo de vida de luminescência, fazem com que os fluoróforos tenham grande aplicação na biologia molecular, medicina e 30 engenharia biomédica principalmente relacionada aos diagnósticos e tratamentos de várias doenças, tais como doença de chagas, dengue e hepatite (HAUGLAND,1996). a) Absorção e Emissão A intensidade do feixe luminoso diminui ao atravessar qualquer meio absorvente, de acordo com a seguinte lei exponencial geral. (Eq.1) em que e são respectivamente as intensidades do feixe incidente e do feixe transmitido, é o coeficiente de absorção (cm-1), dependente do comprimento de onda e é o comprimento do meio absorvente (cm). Define-se a transmitância como: (Eq. 2) e absorbância (Abs) ou densidade óptica (DO) como: (Eq. 3) Quando o meio absorvente é uma solução com uma dada concentração c, é comum relacionar com a concentração, sendo: (Eq. 4) 31 Onde se designa por coeficiente de extinção molar ou absortividade molar e c é a concentração da solução em estudo. Se a concentração for expressa em M (mol-1), será expresso em M-1 cm-1. Usando as relações anteriores pode-se então escrever: (Eq. 5) Esta relação representa a forma usual da Lei de Beer, que prevê para soluções diluídas em apenas uma espécie de absorvente, uma proporcionalidade direta entre a concentração e a absorbância. A constante de proporcionalidade é o coeficiente de extinção molar, , que é a medida da intensidade da banda de absorção, ou seja, a intensidade de energia da transição para cada comprimento de onda. Na Tabela 1 estão listados os comprimentos de onda de absorção e emissão de fluorescência para alguns fluoróforos encontrados comercialmente. Tabela 1 - Características dos Fluoróforos Comerciais em relação aos comprimentos de onda de absorção e de emissão de fluorescência Fluoróforos Acridime Orange 502 526 Alexa Fluor 532 532 553 Cy3 548 562 Cy7 710 805 FITC 490 520 RITC 570 595 FDA 495 520 Fonte: Modificado de HAUGLAND, 1996 b) Deslocamento de Stokes A natureza do solvente e o ambiente local produzem profundos efeitos sobre o espectro eletrônico das moléculas. Esses efeitos são a origem do 32 deslocamento de Stokes (Δλ), que é a diferença do comprimento de onda entre as posições do máximo dos espectros de excitação e emissão, da mesma transição eletrônica. Esta foi uma das primeiras observações do fenômeno conhecido como fluorescência, descrito pelo físico irlândes G. G. Stokes, em 1852 (LAKOWICZ, 1999), (ABBYAD et al, 2007). Uma causa comum para o deslocamento de Stokes é a rápida relaxação da estrutura para níveis vibracionais mais baixos a partir de S1 demonstrado na Figura 2. A Figura 3 representa um desenho esquemático de um exemplo dos espectros típicos de fluorescência para moléculas, onde podemos ver representado o deslocamento de Stokes (Stokes Shift). Essa característica óptica é importante para diferenciar os espectros de absorção e emissão para cada molécula estudada. No caso específico desta dissertação o complexo LaPPS34M será responsável por um deslocamento de Stokes de aproximadamente 200 nm. Figura 3 - Ilustração do deslocamento de Stokes entre o pico de absorção máxima e o pico de emissão máxima. Fonte: Modificado de MGUILBAULT, 1990 Para aplicações em sistemas biomédicos e biológicos é necessário que os espectros de absorção e emissão sejam localizados em comprimentos de onda distintos no espectro eletromagnético para que haja uma facilidade na detecção de fluorescência por parte da instrumentação. No caso do complexo 33 LaPPS34M a absorção se dá na região do azul (350 nm) e a emissão se dá na região do vermelho (615 nm). A equação 6 descreve as transições possíveis para que ocorra o deslocamento de Stokes. O comprimento de onda de absorção (ou o espectro de absorção da molécula) descreve a variação de energia entre dois estados. (Eq. 6) Onde: E1 corresponde ao nível de energia fundamental [J]; E2 é o nível de energia do estado excitado [J] ħ a constante de Planck [6,62 x 10-34 J.s] c a velocidade de propagação da luz [ km/s] é o comprimento de onda de emissão [nm] c) Tempos de Vida de Luminescência A fluorescência tem sido usada para estudar vários sistemas químicos, físicos e biológicos (LAKOWICZ,1991), (JAMESON,1991). Apesar da grande quantidade de informações que se consegue com medidas estáticas, é interessante examinar também a fluorescência resolvida no tempo, ou seja, através da análise do tempo de vida é possível verificar se uma amostra contém vários fluoróforos distintos, pois neste caso o que se espera é mais de um tempo de vida. No caso de um único tipo de fluoróforo, os dados resolvidos no tempo podem indicar a influência do meio em que se encontra o fluoróforo uma vez que isto pode alterar o tempo de vida de luminescência. Há duas técnicas para se obter dados de fluorescência resolvidos no tempo. Na primeira, uma amostra é excitada com um pulso de luz e observa-se a fluorescência em função do tempo. Na segunda técnica, a amostra é excitada 34 com luz modulada e a fluorescência em função do tempo é obtida da resposta em frequência da emissão. Nos dois casos o objetivo é obter os parâmetros que descrevem a fluorescência em função do tempo. Os tempos de vida de luminescência dos fluoróforos podem variar de 10 -12 a centenas de 10-9 s. Este tempo corresponde ao intervalo temporal para que haja um decaimento exponencial partindo do valor máximo até 36,8%. (isto é, 1/e). A equação a seguir relaciona os parâmetros para a obtenção dos valores do tempo de vida de luminescência dos fluoróforos. (Eq. 7) Onde é a intensidade de luminescência inicial no instante de t igual a 0, e seguido de variável que é o tempo de vida de luminescência do fluoróforo. Esta pode também ser descrita como Γ + krn)–1. (Eq. 8) Onde Γ representa à taxa de emissão do fluoróforo e krn a taxa de decaimento não radiativa do estado fundamental. Geralmente, para os fluoróforos comerciais os tempos de vida estão em torno de 10-9 s. O Cy3 tem o tempo de vida de luminescência em torno de 0,3 ns e é utilizado na marcação de complexos imunes, pois é invariável ao pH (entre 3 a 7) e a temperatura, mantendo sua estabilidade perante outros fluoróforos, tais como a fluoresceína (MUJUMDAR et al, 1996). 2.4.2. Propriedades dos Fluoróforos Comerciais e dos Complexos Biomarcadores 35 A seleção de um marcador ou de um complexo biomarcador, é influenciada por fatores tais como as características espectrais. As características do instrumento de detecção são fundamentais para que haja precisão na coleta dos dados. Os parâmetros dos instrumentos a serem considerados incluem o tipo de fonte de excitação, os filtros ópticos utilizados para a discriminação do sinal e de sensibilidade, e os detectores, ou seja, a forma como será adquirido os dados. As características importantes dos marcadores na otimização são o espectro de excitação, o deslocamento de Stokes, a emissão espectral e o tempo de vida de luminescência. Outros fatores, incluindo o coeficiente de extinção, o rendimento quântico de fluorescência, fotoestabilidade e a sensibilidade ambiental, determinam a intensidade de luminescência de biomoléculas marcadas. Além disso, os efeitos das características físicas do marcador sobre a rotulagem influenciam na eficiência e estrutura biológica das moléculas (HAUGLAND,1996). Uma abordagem utilizada amplamente é determinar qual o marcador ou quais os marcadores que são mais adequados para uma determinada aplicação. O desempenho de um fluoróforo está diretamente relacionado com as propriedades químicas e seus conjugados de ácidos nucléicos (HAUGLAND,1996). O rendimento quântico de fluorescência é uma medida da eficiência com que a molécula excitada é capaz de converter a radiação luminosa absorvida em emitida. É definida como a fração de fótons absorvidos que são convertidos em emissão de fluorescência. O rendimento quântico é muito sensível ao ambiente, ao pH, a temperatura e a estrutura do fluoróforo (PRASAD, 2003). Fotoestabilidade é a capacidade que tem um fluoróforo de sofrer repetidos ciclos de excitação e de emissão sem ser destruído, enquanto no estado excitado. O ambiente tem um forte efeito em alguns fluoróforos e mínimos sobre outros. Os mais fortes fatores ambientais que afetam o rendimento de fluorescência são o pH e a escolha do solvente. 36 O coeficiente de extinção molar (ε) é a capacidade que um mol2 de uma substância tem em absorver luz num dado comprimento de onda, ou o quão fortemente uma substância absorve radiação a uma determinada frequência. Esta capacidade é muito importante na determinação da quantidade de radiação luminosa que pode gerar uma molécula através da emissão de fluorescência (PRASAD, 2003). A maioria dos fluoróforos de uso comercial ou complexos biomarcadores têm coeficientes de extinção molar em seu comprimento de onda de absorção máxima variando entre 5.000 e 200.000 L mol−1cm−1 (HAUGLAND, 1996). Em geral, marcadores, com grandes deslocamentos de Stokes tendem a ter coeficientes de extinção relativamente pequenos, enquanto que os marcadores com pequenas mudanças no deslocamento de Stokes tendem a ter coeficientes de extinção relativamente grandes. Algumas características dos fluoróforos para que se possa ter biomarcadores de qualidade, são: 1) Os marcadores devem produzir sinais luminosos, que são espectralmente distinguíveis da excitação e da emissão; 2) Fluoróforos devem ser compatíveis com a instrumentação disponível; 3) Os marcadores e seus conjugados devem ser estáveis em relação ao pH, temperatura e condições de iluminação necessária para a análise. Além disso, alguns dos fatores que influenciam no desempenho dos fluoróforos, são: 1) Os espectros de excitação e emissão de acordo com a fonte de excitação e filtro de comprimentos de onda de emissão; 2) O rendimento quântico de fluorescência do marcador; 3) A fotoestabilidade do marcador; 4) O meio onde o marcador se encontra, e 2 O mol é definido como sendo a quantidade de matéria de um sistema que contém tantas entidades elementares quantos são os átomos contidos em 0,012 kg de carbono 12 (SOLOMONS, 2009). 37 5) O coeficiente de extinção molar. A banda espectral e a pureza do corante também são fatores importantes que afetam a análise do fluoróforo. A importância da largura de banda espectral, especialmente no espectro de emissão, concentra-se na capacidade dos instrumentos em distinguir um marcador do outro (PRASAD, 2003). O uso dos fluoróforos como biomarcadores abre a possibilidade de pesquisas de como novos fluoróforos podem se enquadrar nas características necessárias para aplicação em sistemas biomédicos. Nesta dissertação analisa-se o complexo LaPPS34M em comparação com o fluoróforo Cy3 para demonstrar as possíveis aplicações deste novo complexo em biomédica e também nos projetos desenvolvidos pelo Instituto Nacional de Inovação em Saúde Pública (INDI-SAÚDE). 2.4.2.1. Fluoróforo Comercial Cy3 Há uma grande quantidade de marcadores ou fluoróforos. A família Cyanine (Cy) são marcadores fluorescentes. Esta família de fluoróforos tem grande intensidade de fluorescência em relação à emissão de cores, possuindo faixas espectrais distintas e estão disponíveis em diferentes composições químicas permitindo rotulagem via amina ou grupos tiol. O fluoróforo Cyanine proporciona alta sensibilidade e é fotoestável (ERNST,1989). O marcador Cy3 tem emissão na região do verde e pode ser sintetizado com grupos reativos em cada um dos radicais [R] ou ambas as cadeias laterais, de modo que o fluoróforo pode ser quimicamente ligado a qualquer ácido nucléico ou moléculas de proteínas (ERNST,1989). Na Figura 4 apresenta-se a estrutura molecular do Cy3. Os Radicais [R] representam os grupos aminas ou tiol aos quais a molécula pode se ligar. Os números 1, 2 e 3 representam as posições das ramificações que compõem a estrutura molecular do fluoróforo. 38 + Figura 4 - Ilustração da estrutura molecular do fluoróforo comercial Cy3. O N é o - símbolo do íon nitrogênio e o I é o símbolo do íon iodo. Fonte: Modificado de LAUREN et al,1988 O Cy3 constitui uma família molecular com solubilidade em água, e tolerância ao Dimetilsulfóxido (DMSO), com comprimento de onda de excitação da ordem de 550 nm e de emissão da ordem de 570 nm (ambos na faixa de emissão do verde). A marcação em sistemas médicos e biológicos é direcionada para identificação e quantificação do complexo antígeno-anticorpo ou de estruturas internas da célula. Os Cy3 são usados em uma ampla variedade de aplicações. Para rotulagem de proteínas e ácidos núcleicos tal como descrito pelos trabalhos de WILTSHIRE, 2000, e para localização de DNA e RNA (XIAO, 2007). Esta classe de marcadores é insensível ao pH na faixa entre 3-10 e é fotoestável. A fluorescência advinda desse marcador permanece por mais tempo, caracterizado pela fotoestabilidade. As características ópticas da família de Cy’s, que refletem a qualidade de um fluoróforo, são apresentadas na Tabela 2. 39 Tabela 2 - Características ópticas relevantes para um fluoróforo da família Cy-corante Cy- Peso Molecular [u] λABS [nm] λEm [nm] Rendimento Quântico Coeficiente de extinção molar -1 -1 [M .cm ] Tempo de vida [ns] Cy3 765,9 548 562 <0,3 0.04 0,30 Cy4 791,9 646 664 1.0 0.24 0,25 Cy5 792,1 649 670 0,28 0,15 1,0 corante Fonte: adaptada de Mujumdar, R.B., et al,1993 2.4.2.2. Complexo LaPPS34M O complexo tem a estrutura molecular composta por európio/bipiridina/dibenzoílmetano na concentração de 1:1:3. A estrutura molecular é demonstrada na Figura 5, e apresenta a faixa de comprimento de onda de absorção na região do azul e emissão de fluorescência na região do vermelho (AKCELRUD, 2010).. Figura 5 - Estrutura molecular do complexo LaPPS34M, com os elementos N (nitrogênio) e O ( oxigênio), as cadeias aromáticas (representada pelos hexágonos). Fonte : Lapps/UFPR,(2010) O elemento químico európio (63Eu152) pertence à família dos lantanídeos que compreende os elementos do lantânio (57La138,9) ao lutécio 40 (71Lu), entre os quais se incluem o ítrio (39Y89) e o escândio (21Sc45),(LEE, 1999). Esses elementos são aplicados na investigação das propriedades e funções de sistemas biomédicos e na identificação de substâncias biológicas. Eles são usados principalmente como sondas espectroscópicas no estudo de biomoléculas e suas funções, por exemplo em marcadores biológicos para acompanhar o caminho percorrido pelos medicamentos no homem e em animais; também como marcadores em imunologia e, como agentes de contraste em diagnóstico não invasivo de patologias em tecidos por imagem de ressonância magnética nuclear (MARTINS, 2005). A semelhança entre as características físicas e químicas dos elementos lantanídeos (SÁ, 2000) faz com que eles sejam mais estáveis. LUI (1997) descreve o estudo de fluorescência resolvida no tempo onde se encontrou os tempos de vida de luminescência dos sistemas contendo európio em torno de microsegundos. A presença do elemento európio em alguns complexos ou polímeros faz com que a luminescência esteja presente (LIMA, 2005). Há uma transferência de energia intramolecular do íon metálico central e esse efeito é chamado de efeito antena3 . Dentre os lantanídeos, os íons Eu(III) e Tb(III), são os mais utilizados como sondas espectroscópicas, nas quais os elementos considerados quelatos 4 destes elementos são os mais convenientes como sondas luminescentes para sistemas biológicos. Isto se deve ao fato de os mesmos serem estáveis e a transferência de energia do quelato para o íon Ln poder atingir eficiência de aproximadamente 100% (BÜNZLI, 1989), fazendo com que a luminescência seja intensa, apresentando assim, alto rendimento quântico. Os tempos de vida de luminescência destes complexos são longos (100 a 1000 µs); a diferença de energia entre a absorção do ligante e a emissão do íon (deslocamento de Stokes) é muito grande, acima de 200 nm; possuem alta 3 O processo de conversão de luz, chamado de efeito antena, envolve a absorção de radiação ultravioleta através dos ligantes, que atuam como antenas, a transferência de energia do estado excitado do ligante para os níveis 4f do íon metálico e a emissão de radiação se dá no visível, característica do íon metálico ( LIMA, 2005) 4 Quando, em uma molécula, o átomo de metal possui ligantes coordenados a ele,sendo que, cada um desses ligantes efetua duas ligações ou mais com este metal, essa molécula é considerada um quelato ( SALIBA,2009) 41 sensibilidade de detecção; têm facilidade de se ligarem ao reagente bioanalítico para marcação de antígenos e/ou anticorpos (BÜNZLI, 1989). O complexo LaPPS34M que é estudado em relação ao fluoróforo comercial Cy3, apresenta maior tempo de luminescência, em torno de 110 μs a 114,5 μs, como está demonstrado nas figuras 30 e 32. 2.5. NANOPARTÍCULA A nanotecnologia refere-se à técnica utilizada para manipular estruturas na ordem de 10-9 m, tornando possível a criação de estruturas funcionais em nano escala. Elas podem ser produzidas a partir de diferentes materiais e formas (LIU, 2006). As nanopartículas são utilizadas em uma grande variedade de áreas, incluindo materiais biomedicina, avançados, fármacos e eletrônica, cosméticos (ZUO magnetismo, et optoeletrônica, al, 2007). Há várias nanopartículas como as de materiais metálicos, por exemplo: ouro (Au), prata (Ag), níquel (Ni), cobre (Cu), semicondutores e os polímeros. A Figura 6 apresenta as nanopartículas metálicas em diferentes dimensões, formas e composições e produzem materiais com distintas propriedades de dispersão da luz. Outra característica visível na figura é a variação na cor das nanopartículas metálicas (ROSI et al, 2005). 42 Figura 6 - Dimensões, formas e tamanhos das nanopartículas metálicas. Fonte: Modificado de ROSI et al, (2005) A utilização conjuntamente com de nanopartículas fluoróforos, há um possibilita aumento que da ao conjugá-las intensidade de fluorescência (LAKOWICZ, 2001). A intensificação do sinal permite que a detecção de fluorescência seja ampliada por causa da transferência de energia de ressonância. As aplicações dessa tecnologia são a caracterização e o aprimoramento de novos biomarcadores, como por exemplo, para o diagnóstico de câncer e a detecção de doenças infecciosas por microorganismos (SOKOLOV, 1998) e (SIWACH, 2009). O aumento da intensidade de fluorescência do fluoróforo Cy3 e do complexo LaPPS34M foi realizado com o uso de nanopartículas de ouro e prata e servirão de parâmetros para a otimização do sistema de instrumentação desenvolvido com a finalidade de obter as características ópticas das amostras. As nanopartículas utilizadas foram produzidas pela UFPR e sua produção e caracterização estão apresentadas no anexo C. 43 2.5.1. Fluoróforo na Presença de Nanopartículas A transferência de energia de ressonância de fluorescência (Fluorescence Resonance Energy Transfer - FRET) é uma técnica para a caracterização de interações à distância. É uma das poucas ferramentas disponíveis que é capaz de medir as interações intermoleculares e a distância intramolecular tanto in vivo quanto in vitro (SELVIN, 2000). É um processo pelo qual um doador não radiativo do estado excitado (e.g., um fluoróforo) transfere energia para um estado receptor através de interações de longo alcance dipolo-dipolo (LAKOWICZ, 1999). A FRET envolve a excitação de um fluoróforo doador por incidência de luz dentro do seu espectro de absorção. Essa absorção de radiação eleva o fluoróforo a uma maior energia, estado excitado, que normalmente decai (retorno ao estado fundamental) com um espectro de emissão característico. Se, no entanto, outro fluoróforo ou nanopartículas (o receptor) existe nas proximidades do doador há uma sobreposição do espectro de absorção do receptor ao espectro de emissão do doador e, em seguida a possibilidade de transferência de energia não-radiativa entre o doador e o receptor (PRASAD, 2003). A Figura 7 mostra a sobreposição do espectro de absorção da proteína fluorescente fluoresceína e do espectro de emissão da proteína fluorescente rodamina possibilitando uma forte interação FRET. 44 Figura 7 - Esquema do processo de FRET entre dois fluoróforos, a fluoresceína doadora) e a rodamina (receptora), onde r é a distância de mínima de FRET. Fonte: Modificado de SAPSFORD et al, 2006. Em geral, o doador e o receptor são diferentes. O FRET é detectado pelo aparecimento de fluorescência do receptor ou por extinção de fluorescência do doador. Em uma molécula os elétrons migram do estado fundamental (So) para um nível de vibração mais elevada, de forma rápida com tempos da ordem de pico segundos. Estes elétrons decaem para o nível mais baixo de vibração (S1) e, eventualmente, dentro de nanosegundos, voltam para o estado (So) e um fóton de luz é emitido (LAKOWICZ et al, 2008). Na transferência de energia de ressonância o fóton não é emitido, mas a energia é transferida para a molécula receptora, cujos elétrons por sua vez, tornam-se excitados. Isto está apresentado na Figura 6, por meio de um diagrama de Jablonski para o processo de FRET. 45 Figura 8 - Descrição do processo de FRET pelo de diagrama de Jablonski. Fonte: Própria O FRET pode resultar em uma diminuição da fluorescência da molécula doadora como em um aumento da fluorescência do receptor. O método estabelece a medida da interação entre o fluoróforo e a superfície das nanopartículas A taxa de transferência de energia é dependente de muitos fatores, tais como o grau de sobreposição espectral entre o doador e o receptor, a orientação relativa dos dipolos de transição, e mais importante, a distância entre o doador e receptor nas moléculas. Geralmente o FRET ocorre nos sistemas biomédicos em dimensões (r) em torno de 2 a 10 nm (CHEN, 2007). Quando se conjuga as nanoparticulas com fluoróforos ou complexos há um aumento da intensidade de fluorescência. A Figura 30 representa o resultado do fenômeno de FRET para o caso de nanopartículas de prata conjugadas com o bioindicador LaPPS34M. 46 2.6. RESUMO Neste capítulo, apresentou-se que a medição de fluorescência apresenta potencialidade para sistemas de diagnósticos rápidos utilizando um biomarcador fluorescente. Para a caracterização óptica deste indicador fluorescente utilizou-se os espectros de absorção e emissão da substância ou complexo, o deslocamento de Stokes entre a absorção e emissão e o tempo de vida do emissão de luminescência. Normalmente, o Cy3 é o indicador mais utlizado para a marcação do complexo antígeno-anticorpo, entretanto, este trabalho utililizará o novo complexo LaPPS34M (Lapps/UFPR) para a emissão de fluorescência devido ao maior tempo de emissão (na ordem de 100s) e deslocamento de Stokes (em torno de 200 nm). Adicionalmente, o uso de nanopartículas possibilitará a intensificação do sinal de fluorescência quando houver a conjugação de fluoróforos com as nanopartículas. No capítulo a seguir, apresenta-se uma descrição dos elementos utilizados na implementação de um sistema de aquisição de fluorescência. 47 3. SISTEMAS DE AQUISIÇÃO DE LUMINESCÊNCIA 3.1. INTRODUÇÃO Neste capítulo é apresentado o sistema implementado para a detecção da emissão de fluorescência dos fluoróforos Cy3 e LaPPS34M. Dentro deste sistema, utilizou-se para a detecção de fluorescência, a válvula fotomultiplicadora R928 e a válvula fotomultiplicadora miniatura R5600U-01 e, posteriormente, por um componente optoeletrônico OPT 301. 3.2. DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DO CY3 E DO COMPLEXO LaPPS34M A análise de elementos químicos, as estruturas internas dos compostos e o levantamento de dados físico-químicos da absorção, emissão e dispersão da interação da luz com as amostras são essenciais para descrever o comportamento e natureza dos compostos orgânicos (LEE, 1999). A absorção de radiação eletromagnética que acontece na região do ultravioleta e também do visível, é estudada através da espectroscopia de absorção. Se o objeto de interesse é a emissão, obtém-se tal espectro pela espectroscopia de emissão. Há outros tipos de espectroscopia como de infravermelho, de microondas, Raman, de fluorescência, de raios x, de plasma, fotoacústica e de ressonância magnética (OKUNO, 1982). Para que haja interação entre a luz incidente e a amostra deve haver ressonância. A radiação eletromagnética e as partículas da amostra devem ter a mesma frequência, e isto só é possível se a energia de excitação for maior que a fundamental levando às transições eletrônicas entre os níveis de energia (EISBERG, 1988). A absorção molecular se dá através da soma das contribuições de vários níveis de energia, a rotacional, vibracional e eletrônica. O movimento de translação da molécula como um todo não modifica as posições relativas das 48 partículas que a constituem, entretanto as ligações intermoleculares e os ângulos entre as ligações vibram, enquanto que a estrutura nuclear gira como um todo. Podemos desprezar os movimentos de rotação e vibração das moléculas, pois as velocidades eletrônicas são pelo menos mil vezes maiores que as nucleares (BASSI, 2001). 3.2.1. Espectrofotômetro de Duplo Feixe Para a determinação o espectro de absorção e emissao dos fluoróforos Cy3 e LaPPS34M, utilizou-se um espectrofotômetro para as regiões do ultravioleta, do visível e do infravermelho. O espectrofotômetro apresenta uma fonte de radiação eletromagnética de espectro contínuo, um porta amostra, um monocromador e um detector (Figura 9). Nos espectrofotômetros de feixe simples a radiação só atravessa a amostra e nos espectrofotômetros de feixe duplo mede-se simultaneamente a intensidade transmitida pela amostra e a transmitida por um padrão de referência, a diferença das duas intensidades é aquela absorvida pela amostra. 49 Figura 9 - Desenho esquemático do espectrofotômetro de duplo feixe Fonte: Própria O equipamento disponível no laboratório de óptica da UTFPR consiste em um espectrofotômetro de duplo feixe UV-VIS, modelo DB – 1880S, composto de duas fontes óticas, uma lâmpada de tungstênio – halogênio ( para a região do visível) e outra de deutério (para a região do ultravioleta). Tem-se internamente dois monocromadores que permitem a passagem de uma faixa estreita do espectro da energia incidente com um comprimento de onda específico, que varia de 190 nm a 1100 nm. A cubeta onde se coloca a amostra é de quartzo com volume de 3,5 ml e o comprimento do caminho óptico, pelo qual se dará a interação da radiação e a substância da amostra, é definido pelo diâmetro interno da cubeta na ordem de 10 mm. A fotografia 1 representa o equipamento disponível no laboratório de óptica da UTFPR. 50 Fotografia 1 - Espectrofotômetro de Duplo Feixe UV-Vis. Fonte: Própria O sistema descrito foi utilizado para se obter os espectros de absorção do fluoróforo comercial Cy3, o espectro de absorção do complexo LaPPS34M, e a resposta espectral dos filtros utilizados no experimento. 3.2.1.1. Espectro de Absorção Os espectros de absorção do fluoróforo comercial Cy3 e o do complexo LaPPS34M foram obtidos pelo espectrofotômetro descrito no item 3.2.1. O fluoróforo Cy3 foi diluído em uma solução tampão na proporção 1:1, isto é, 1 ml de soluto em 1 ml de solvente e colocado na cubeta de quartzo e transportada ao espectrofotômetro. Observa-se que a absorção do fluoróforo Cy3 acontece na região compreendida entre 530nm e 560nm, com um pico máximo em 550 nm, conforme vizualiza-se na Figura 6. O espectro de absorção do complexo LaPPS34M foi obtido diluindo a amostra em solução de tetrahidrofurano (THF), seguindo o mesmo procedimento no qual foi obtido o espectro de absorção do fluoróforo Cy3. A Figura 6 representa o gráfico do complexo LaPPS34M com um pico máximo (principal) em 400nm e outro secundário em 300nm. 51 Figura 10 - Espectro de absorção do fluoroforo Cy3 obtido pelo espectrofotômetro. Fonte: Própria Figura 11 - Espectro de absorção do complexo LaPPS34M obtido pelo espectrofotômetro Fonte: Própria Os resultados indicam que no caso do fluoróforo Cy3, os dados coletados no laboratório da UTFPR correspondem ao disponível na literatura, pois o pico máximo de absorção se encontra em 550 nm, conforme apresentado na Erro! Fonte de referência não encontrada.. Para o estudo do complexo LaPPS34M percebe-se a presença de dois picos, sendo que a maior 52 absorbância se encontra em 400 nm, como demonstrado na Erro! Fonte de referência não encontrada.. 3.3. SISTEMA DE AQUISIÇÃO DE SINAL DE FLUORESCÊNCIA Para a detecção da luminescência, foi implementado um sistema de detecção de acordo com a Figura 12. O sistema é composto por (a) uma fonte óptica acoplada a um gerador de sinais utilizado para a excitação do fluoróforo, (b) um fluoróforo em uma cubeta posicionada de forma que o caminho óptico de excitação e de detecção formem um ângulo de 90 graus para minimizar a energia de excitação que incide no sensor de luminescência, (c) lente convergente para orientar o feixe incidente d) Monocromador ou filtro óptico para emissão, (e) um fotodetector de estado sólido, (f) um amplificador de transimpedância, (g) e (h) representam o sistema de aquisição e processamento de sinais através do osciloscópio e computador padrão. Figura 12 - Representação esquemática do sistema de detecção proposto Fonte: Própria O método proposto será dividido em três fases devido a utilização de três distintos optodetectores (válvula fotomultiplicadora R928, válvula fotomultiplicadora miniatura R5600U-01 e detector optoletrônico OPT301): 53 A fase I é constituída da coleta de dados a partir da instrumentação com o uso da válvula fotomultiplicadora R928, conforme pode ser visto na Figura 13 Figura 13 - Desenho esquemático do sistema experimental por válvula fotomultiplicadora R928 (de alta sensibilidade) Fonte: Própria A instrumentação descrita na Figura 13 possibilita a obtenção do espectro de fluorescência e o tempo de vida de luminescência da amostra LaPPS34M na fase 1, bem como o espectro de fluorescência do fluoróforo comercial Cy3, cujo sistema de detecção baseia-se na utilização da válvula fotomultiplicadora grande. O sistema é composto por (a) uma fonte óptica acoplada a um gerador de sinais utilizado, neste caso led´s ultravioleta e azul (b) uma cubeta de quartzo contendo a amostra, (c) uma lente convergente d) um monocromador para selecionar o comprimento de onda de emissão modelo SpectraPro 275 (Acton Research Co., U.S.A) com distância focal de 275 mm, sistema óptico do tipo Czerny-Turner, (d) uma válvula fotomultiplicadora grande tipo janela lateral R928 (Hamamatsu Co.,U.S.A), (e) um amplificador de transimpedância, (f) e (g) um sistema de aquisição e processamento de sinais. A fase II é constituída de (a) uma fonte óptica composta de um diodo emissor de luz ultravioleta,(b) uma câmara de amostra que contém saída que direcionam o feixe de luz do diodo emissor de luz para o filtro, (c) um filtro que 54 serve para selecionar o comprimento de onda de emissão de fluorescência, (d) uma válvula fotomultiplicadora miniatura em modelo R5600U-01 ultra compacto com 10 mm de comprimento, 15 mm de diâmetro e janela óptica (fotocatodo) de 8 mm de diâmetro. São ainda componentes da fase II, (e) um amplificador de transimpedância usado para converte o sinal luminoso em tensão elétrica (f) um osciloscópio que permite a captação dos sinais e (g) um computador padrão para realizar o tratamento dos dados. O tamanho reduzido da válvula e do filtro de interferência permitiu a acomodação deste conjunto em uma das saídas da câmara de amostras, configurando um sistema compacto conforme o esquema apresentado na Figura 14. Figura 14 - Desenho esquemático do sistema com o uso da válvula fotomultiplicadora miniatura (R5600U-01). Fonte: Própria No caso específico do sistema com o uso da válvula fotomultiplicadora miniatura (R5600U-01), a câmara de amostra é adaptada para que a amostra seja utilizada em um tubo de ensaio, tamanho de 2 cm de diâmetro e 10 cm de altura. O complexo LaPPS34M foi diluído em tetrahidrofurano (THF) colocado no tubo de ensaio e posteriormente na câmara de amostra. Através da configuração descrita na Figura 14, permite-se obter o tempo de vida de luminescência. 55 A fase III corresponderá pelo uso da mesma instrumentação com detector optoleletrônico, a ilustração do desenho esquemático do sistema é apresentada na Erro! Fonte de referência não encontrada.. Figura 15 - Desenho esquemático do sistema experimental por fotodiodo Fonte: Própria A instrumentação descrita na Erro! Fonte de referência não encontrada. possibilita a obtenção do tempo de vida de luminescência da amostra LaPPS34M na fase 3, cujo sistema de detecção baseia-se na utilização do fotodiodo OPT301. O sistema é composto por (a) uma fonte óptica acoplada a um gerador de sinais utilizado para a excitação do indicador, (b) um indicador em uma cubeta posicionada de forma que o caminho óptico de excitação e de detecção formam um ângulo de 90 graus, (c) filtro óptico para permitir a emissão, (d) um fotodetector de estado sólido, (e) amplificador de transimpedância é utilizado para converter o sinal luminoso em sinal elétrico (f) um sistema de aquisição e processamento de sinais. A fonte óptica corresponde ao diodo emissor de luz na faixa do violeta com comprimento de onda para o pico de emissão em 400 nm. Aplica-se um sinal com frequência de 100Hz (periodo de 10 ms) e duty cicle de aproximadamente 15%, isto é, pulso de 1.5 ms. Esse sinal foi aplicado utilizando-se o gerador de sinais AFG3000 da Tektronix. A amostra LaPPS34M. foi diluída em uma solução de tetrahidrofurano (THF) na proporção 1:1, isto é, 10 ml de soluto em 10 ml de solvente e colocada num tubo de ensaio de 2 mm de diâmetro. 56 No caminho óptico da emissão foi acrescido um filtro de interferência com o espectro de transmitância apresentado na Figura 20. Observa-se que a resposta desse filtro apresenta elevada transmitância na região de emissão do complexo LAPPS34M. O filtro foi adicionado ao sistema com a intenção de minimizar qualquer interferência da energia de excitação no fotodetector permitindo a passagem da energia emitida pelo indicador. A detecção do sinal de fluorescência foi obtida por um fotodiodo OPT301, com janela fotosensível de 2,29 mm x 2,29 mm (OPT301, 1994). O fotodetector tem um amplificador conversor corrente-tensão integrado no mesmo encapsulamento. A Erro! Fonte de referência não encontrada.a apresenta o circuito interno do OPT301 e a Erro! Fonte de referência não encontrada.b é a resposta espectral do sensor. (i) (ii) Figura 16 - (a) Dispositivo OPT 301 apresenta um fotodiodo integrado com amplificador conversor corrente-tensão, (b) resposta espectral do OPT 301, (i) emissão de luminescência do indicador (LAPPS34M ~ 615 nm) (ii) excitação do indicador (LAPPS34M ~ 350 nm). Fonte: Burr-Brown Corporation, 1994 Da figura 16(b), a resposta espectral do detector optoreletrônico apresenta: (a) uma boa resposta para a emissão de luminescência do indicador (LAPPS34M ~ 615 nm) e (b) uma resposta inferior para a excitação do indicador (LAPPS34M ~ 350 nm). Os sinais foram adquiridos com um osciloscópio digital modelo TDS2002B (Tektronix, Beaverton, OR, U.S.A.). Os sinais são digitalizados e 57 armazenados em um dispositivo via interface serial USB. Após transferidos para um computador os dados são processados utilizando uma função Dynamic Fit Wizard do programa Sigmaplot 11.0 para determinação dos parâmetros de uma ou mais exponenciais. O parâmetro de tempo de decaimento da exponencial corresponde ao tempo de vida de luminescência do indicador LaPPS34M. Na fase I, II e III com a utilização dos sistemas descritos nas figuras 13, 14 e 15 foram coletadas as características ópticas necessárias para caracterizar o fluoróforo estudado, ou seja, o complexo LaPPS34M. O levantamento dos espectros de absorção, de emissão de fluorescência e os tempos de vida de luminescência são os parâmetros relevantes para a consolidação das características ópticas de um fluoróforo. A descrição do uso de nanopartículas de ouro e prata servirão para demonstrar a possibilidade de intensificar o sinal de intensidade de fluorescência nos sistemas utilizados. 3.4. SISTEMA DE DETECÇÃO DE FLUORESCÊNCIA Em um sistema de detecção de luminescência típico, um feixe de luz de alta intensidade passa através de lentes convergentes para orientar o feixe a passar pela cubeta. O feixe de luz de excitação passa através de uma cubeta contendo a amostra (Figura 12). Para evitar a detecção do feixe incidente, pode-se fazer a observação da fluorescência em ângulo reto com o feixe incidente, pois a amostra irá emitir em todas as direções. A luz emitida (luminescência) passa através de um monocromador para a análise do comprimento de onda e depois vai para um detector fotossensível (válvula fotomultiplicadora). Os comprimentos de onda são detectados e apresentam a intensidade de emissão como uma função do comprimento de onda da luz emitida (WILLARD, 1988). 3.4.1. Fonte Óptica 58 A fonte óptica deve ceder energia radiante para a faixa de comprimento de onda de absorção do estudo. Há vários tipos de fontes ópticas que podem ser utilizadas para obter a fluorescência como: diodos emissores de luz LightEmitting Diodes (led) e os dispositivos de Light Amplification by Stimulated Emission of Radiation (LASER). A excitação advinda dos marcadores fluorescentes gera pulsos na faixa de nano segundos. A fonte óptica deve ser capaz de fornecer um espectro de energia abrangente. Os diodos representam a fonte óptica escolhida por apresentarem um baixo custo e grande diversidade de comprimentos de onda. Para a obtenção do tempo de vida de luminescência da molécula LaPPS34M utilizou-se uma lâmpada xênon de arco curto (1,5 mm) para excitação pulsada tipo FX-249 (EG&G ELETRO-OPTICS, U.S.A). A Figura 17 representa o espectro de emissão. Esta lâmpada possibilita excitações na faixa de 7J e potência média de 20 W e trabalha com tensões de até 1500 V com taxas de repetições de até 500 Hz. A faixa espectral está entre 310 a 1100 nm. 100 90 Emissão Relativa [a.u] 80 70 60 50 40 30 20 10 0 300 400 500 600 700 800 Comprimento de Onda [nm] Figura 17 – Espectro de emissão da lâmpada xenon Fonte: Própria Utilizou-se conjuntamente uma fonte de disparo da lâmpada tipo PS302 (EG&G ELETRO-OPTICS, U.S.A), a tensão de saída pode ser regulada entre 400 e 1500 V, com pulsos com tensão de 3V com duração de 1 a 100 μs. 59 As figuras 18 e 19 representam os espectros de emissão dos dois leds utilizados no experimento, os espectros de emissão do led azul e do ultravioleta foram obtidos utilizando o sistema descrito pela Figura 12. Figura 18 - Espectro de emissão de led azul, com comprimento de onda do pico é 440 nm. Fonte: Própria Figura 19 - Espectro de emissão de led ultravioleta, com comprimento de onda do pico é 400 nm. Fonte: Própria 3.4.2. Lentes Convergentes e Filtros 60 A lente convergente utilizada no experimento de fluorescência serviu para redirecionar a luz que vem da fonte óptica, neste caso do diodo emissor de luz (led) para o foco. A amostra era colocada na posição focal em relação à lente. Foram utilizadas duas lentes convergentes de 15 cm e 5 cm de distância focal respectivamente, como mostra o esquema de montagem do sistema de detecção representado na Fotografia 2. Fotografia 2 - Montagem do uso das lentes convergentes no experimento de fluorescência. Fonte: Própria Os filtros em geral selecionam os comprimentos de onda que são transmitidos através de absorção, pela interação da energia radiante incidente com o material do filtro. Eles possibilitam a passagem de comprimentos de onda acima ou abaixo de um valor específico; caracterizam-se por não serem sensíveis ao ângulo de incidência da radiação e são muito utilizados em sistemas óticos para selecionar as faixas de frequência desejáveis. No experimento de fluorescência, para a obtenção do tempo de vida do complexo LaPPS34M foram utilizado filtros de 614 nm e 640 nm. A Figura 20 61 representa o espectro de transmissão de um filtro de interferência na região do vermelho. 1,0 Transmitância [%] 0,9 0,8 0,7 0,6 600 700 800 900 1000 1100 Comprimento de Onda [nm] Figura 20 - Espectro de transmitância do filtro de interferência na região do vermelho Fonte: Própria 3.4.3. Monocromador A função de um monocromador é permitir a passagem de uma faixa estreita do espectro da energia radiante centrada em um comprimento de onda específico. O monocromador utilizado no experimento de detecção de fluorescência foi o SpectraPro 275 (Acton Research Co., U.S.A) com distância focal de 275 mm, sistema óptico do tipo Czerny-Turner, conforme mostra a Fotografia 3. O equipamento permite o controle local ou remoto da velocidade de varredura, comprimentos de onda inicial e final, avanço passo a passo, para uma das duas grades possíveis de serem acopladas. A 1ª Grade possui 1200 ranhuras/mm, comprimento de onda de transmissão de 300nm, e a 2ª Grade possui 1200 ranhuras/mm, comprimento de onda de 500 nm (Acton Research Co., 1992). As fendas foram fixadas em 3,0 mm, tanto na entrada com na saída, possibilitando um controle da faixa de passagem do comprimento de onda e da resolução. A resolução máxima está em torno de 0,1 nm medido para um comprimento de onda a 435,8 nm com uma grade difratora de 1200 ranhuras/mm. 62 Para o experimento foi escolhida a grade 1 por estar de acordo com a região do espectro do de fluorescência desejado com a largura da fenda mantida constante em 3 mm. Fotografia 3 - Monocromador do tipo Czerny-Turner. Fonte: Própria 3.4.4. Cubeta A cubeta do tipo 111–OS (Hellmasulamericana Ltda) para os estudos de fluorescência possui todas as laterais polidas de quartzo, possibilitando que a transmitância seja alta para a faixa de comprimento de onda de excitação e emissão, permitindo que a luz de excitação entre em uma direção e possa ser detectada em outra direção, perpendicular a da excitação, diminuindo assim a incidência de radiação de excitação no detector. A câmara de amostra utilizada possui um caminho óptico de 10 mm, conforme ilustrado na Figura 21. Na Figura 22 é representado o espectro de transmitância da cubeta de quartzo. Na faixa correspondente a absorção da amostra LaPPS34M, a cubeta de quartzo é apropriada, pois tem pouca absorção no ultravioleta. 63 Figura 21 - Diagrama representativo da transmitância de luz pela amostra na cubeta Fonte: Modificado de BRANCO, 1997 Figura 22 - llustração do espectro de transmitância da cubeta de quartzo Fonte: BRANCO, 1997 3.4.5. Válvulas Fotomultiplicadoras ( PMTs) 64 A detecção é realizada através da transformação dos sinais ópticos em sinais elétricos com o uso de sensores opto-eletrônicos. Um dos sensores utilizados foi uma válvula fotomultiplicadora tipo janela lateral R928 (Hamamatsu Co.,U.S.A) com sensibilidade do catodo de 352 μA/lúmen, com corrente de anodo na ausência de energia radiante incidente de 4,5 nA. O tempo de subida do sinal é de 2,2 ns e a resposta espectral óptica varia de 190 a 900 nm. Utilizou-se uma fonte de alta tensão para a polarização da válvula, conversor DC-DC tipo C1309-04 ( Hamamatsu Co., U.S.A) com tensão de entrada de 13 a 24 V e corrente de 160 mA. A tensão de saída regulada foi de 190 a 1100 V. As válvulas fotomultiplicadoras (PMT - photo multiplier tube) combinam uma camada fotosensível de metais alcalinos (multialkali: Na-K-Sb-Cs) denominada de fotocatodo, e um multiplicador de elétrons que consiste em uma série de dinodos cobertos com um material de alta emissão secundária (metal channel dynode). O fotocatodo converte fótons incidentes em fotoelétrons e estes são multiplicados de dinodo para dinodo atingir o anodo, conforme a Figura 23. Figura 23 - Representação do processo de geração e multiplicação de elétrons em uma válvula fotomultiplicadora Fonte: BRANCO,1997 Um conjunto de resistores divide a tensão de polarização para os diversos dinodos. O ganho total (G) da válvula corresponde ao número de estágios n multiplicado pelo fator de emissão secundária por estágio f , sendo dado por: 65 G fn (Eq.12) Os valores assumidos por f apresentam-se na faixa de 3 a 10, sendo que para dinodos recobertos com GaP (Fosfeto de Gálio), o fator de emissão secundária pode alcançar 50. Esta larga capacidade de amplificação interna, permite a utilização das PMTs na medição de sinais luminosos com baixos níveis de intensidade, na faixa de 10-14 a 10-4 lúmens, sendo que 1 lúmen corresponde a 1,47 mW (BRANCO, 1997). 3.4.6. Amplificador de Transimpedância Para converter a corrente do sensor optoeletrônico em um nível de tensão, utiliza-se um amplificador de transimpedância. O circuito apresentado na Figura 24 foi montado em circuito impresso e introduzido numa caixa metálica. O circuito possui capacitores para estabilizar a tensão de alimentação, diodos (1N4148) de proteção na entrada e diodo para alimentação da tensão de saída. O amplificador operacional foi o OP 627 com baixa corrente de fuga e offset e alta impedância de entrada com baixo valor capacitivo, alto ganho de malha aberta, ampla largura de banda de 16 MHz assim como variação da tensão de saída. Figura 24 - Circuito de Implementação do Amplificador de Transimpedância Fonte: SCHNEIDER, 1995 66 3.4.7. Aquisição do Processamento do Sinal Os sinais foram adquiridos com um osciloscópio digital modelo TDS2002B (Tektronix, Beaverton, OR, U.S.A.). Os sinais são digitalizados e armazenados em um dispositivo via interface serial USB. Depois de transferidos para um computador os dados são processados. Utilizou-se uma função Dynamic Fit Wizard do programa Sigmaplot 11.0 para determinação dos parâmetros de uma exponencial 3.5. RESUMO Implementou-se um sistema de detecção de fluorescência com 3 distintos detectores ópticos, denominados de fases I (válvula fotomultiplicadora R928), II (válvula fotomultiplicadora miniatura R5600U-01) e III (detector optoeletrônico OPT301). De acordo com os detectores e as suas medidas dos tempo de emissão de fluorescência, estes servirão de referência para a construção de equipamentos de baixo custo e maior resistência mecânica. O capítulo 4 a seguir apresenta os ensaios realizados para a determinação dos tempos de vida da fluorescência com a instrumentação implementada e o marcador LaPPS34M. 67 4. RESULTADOS 4.1. INTRODUÇÃO No sistema desenvolvido, a detecção de fluorescência foi feita por meio de (a) válvulas fotomultiplicadoras e (b) um detector optoeletrônico. Os resultados deste trabalho são apresentados neste capítulo na seguinte sequência: a) Os espectros de emissão de Fluorescência do Cy3 e do complexo LaPPS34M; b) Os espectros de emissão de fluorescência conjugados com nanopartículas do Cy3 e do complexo LaPPS34M; c) O tempos de vida de luminescência do complexo LaPPS34M. 4.2. ESPECTROS DE FLUORESCÊNCIA a) Fluoróforo Cy3 Os espectros de fluorescência de Cy3 foram obtidos através da fase I descrita no item 3.3. A amostra de fluoróforo comercial Cy3 foi diluída em solução tampão na proporção de 1:1 e colocada na cubeta de quartzo. A Figura 25 representa o gráfico da região do espectro de emissão. O fluoróforo Cy3 apresenta excitação na região do azul e região espectral de emissão variando de 530 nm a 580 nm, com um pico máximo em 564 nm. Os dados experimentais foram obtidos com pulsos de 75 μs com frequência de 147,3 Hz. A válvula fotomultiplicadora R928 foi mantida a 800 V e as fendas do monocromador mantidas com abertura de 3 mm. O deslocamento de Stokes do fluoróforo Cy3 é pequeno entre a excitação e a emissão, em torno de aproximadamente 15 nm, indicando a aproximação entre os picos do espectro de excitação e emissão concentrando- 68 se na região do verde, com a excitação na região do azul, isto dificultaria, no filtro óptico, separar emissão de recepção. Emissão de Fluorescência [a.u] 1,0 0,9 0,8 0,7 0,6 0,5 520 540 560 580 600 620 Comprimento de Onda [nm] Figura 25 - Espectro de fluorescência do fluoróforo Cy3 obtido pela FASE I (válvula fotomultiplicadora R928) Fonte: Própria A Figura 26 representa o deslocamento de Stokes do fluoróforo Cy3 demonstrando a variação para o complexo em torno de 20 a 50 nm. Figura 26 - Espectro de absorção e emissão de fluoróforo Cy3 demonstrando o deslocamento de Stokes obtido pela FASE I. Fonte: Própria 69 b) Complexo LaPPS34M Na Fase I descrita no item 3.3 o complexo LaPPS34M foi diluído em solução de tetrahidrofurano (THF) cuja a fórmula molecular é representada por C4 H8 O, na proporção de 1:1. Pulsos ópticos de 3 ms com frequência de 114 Hz foram obtidos de forma experimental. A válvula fotomultiplicadora R928 foi mantida em 700 V e a abertura das fendas do monocromador em 3 mm. A região espectral de emissão acontece entre 600 nm e 630 nm, com um pico máximo em 615 nm conforme a Figura 27. Essa caracterização óptica indica que a molécula tem um grande O deslocamento de Stokes entre os picos do espectro de excitação e emissão, e esta variação ocorre entre a região do azul (excitação) e a região do vermelho (emissão). 1,0 Emissão de Fluorescência [a.u] 0,9 0,8 0,7 0,6 0,5 0,4 0,3 0,2 0,1 0,0 580 590 600 610 620 630 640 Comprimento de onda [nm] Figura 27 - Espectro de fluorescência do complexo LaPPS34M obtido pela FASE I. Fonte: Própria A Figura 28 representa o deslocamento de Stokes do complexo LaPPS34M demonstrando a variação para o complexo em torno de 200 a 250 nm. 70 Figura 28 - Espectro de absorção e emissão de LaPPS34M demonstrando o deslocamento de Stokes obtido pela FASE I Fonte: Própria 71 4.3. ESPECTROS DE FLUORESCÊNCIA COM NANOPARTÍCULAS METÁLICAS a) Fluoróforo Cy3 O fluoróforo Cy3 foi conjugado com nanopartículas de ouro e a Figura 29 representa os espectros de fluorescência. No anexo C segue a descrição da formação e caracterização das nanopartículas. Segundo a teoria de FRET descrita na seção 2.7.1 quando um fluoróforo se encontra na presença de nanopartículas pode haver um aumento da intensidade de fluorescência e um decréscimo do tempo de vida. O gráfico da Figura 29 demonstra que o fluoróforo comercial Cy3 na presença de nanopartículas de ouro apresenta um deslocamento espectral, no sentido de menores comprimentos de onda, com um aumento de aproximadamente 170% no valor da intensidade de fluorescência, demonstrada pelo aumento da intensidade de sinal do sistema, confirmando a teoria de que a presença de nanopartículas modifica a fluorescência. 26 100 90 Intensidade de Fluorescência [a.u] Emissão de Fluorescência [a.u] 24 22 20 18 16 14 80 70 60 50 40 30 20 10 12 520 540 560 580 Comprimento de Onda [nm] 600 620 0 500 520 540 560 580 600 Comprimento de Onda [nm] Figura 29 - a)Espectro de Fluorescência do fluoróforo Cy3 e b) o espectro de fluorescência do Fluoróforo Cy3 conjugado com Nanopartícula de Ouro obtido pela FASE I. Fonte: Própria 72 b) Complexo LaPPS34M No estudo do complexo LaPPS34M, a escolha das nanopartículas de prata se deu em virtude de que o espectro de absorção destas nanopartículas ocorre na região do espectro de absorção do complexo, o que segundo a teoria de FRET (seção 2.5.1) ocasiona uma intensificação da fluorescência. Neste caso, a absorção das nanopartículas de prata acontece em 400 nm e a absorção do complexo está na faixa de 350 nm a 400 nm. A Erro! Fonte de referência não encontrada. representa o gráfico do espectro de fluorescência do complexo LaPPS34M, demonstrando que há uma modificação do sistema com a introdução das nanopartículas de prata. A amostra foi diluída em etanol na proporção de 1:1, isto é, 10 ml de soluto em 10 ml de solvente. E posteriormente a colocação de nanopartículas de prata na proporção de 1 ml para 2 ml da solução de LaPPS+Etanol numa cubeta de quartzo de 3.5 ml. O sistema foi iluminado com diodo ultravioleta usando a instrumentação descrita na seção 3.4.1. Observa-se um aumento da intensidade de fluorescência com a conjugação do LaPPS34M com nanopartículas de prata, em torno de 15% do valor inicial. Esta constatação condiz perfeitamente com o esperado pela teoria descrita por LAKOWICZ, 1999. 1,2 Intensidade de Fluorescência [a.u] LaPPS34M 1,0 LaPPS34M com Ag 0,8 0,6 0,4 0,2 0,0 740 760 780 800 820 840 860 880 900 Comprimento de Onda [nm] Figura 30 - Espectro de fluorescência (em preto) do complexo LaPPS34M e o espectro de fluorescência do LaPPS34M ( em verde) conjugado com nanopartículas de prata obtido pela FASE I. 73 Fonte: Própria 4.4. TEMPOS DE VIDA DE LUMINESCÊNCIA DO FLUORÓFORO E DO COMPLEXO LaPPS34M a) Fluoróforo Cy3 Geralmente para os fluoróforos comerciais os tempos de vida estão em torno de 10-9 s. O Cy3 tem o tempo de vida de 0.3 ns (HAHN, 2000). A medida do tempo de vida do fluoróforo comercial Cy3 não foi possível de ser realizada pela instrumentação construída para a detecção de fluorescência, uma vez que o sistema de detecção não é capaz de observar eventos tão rápidos em função da resposta em frequência do circuito optoeletrônico. b) O complexo LaPPS34M O complexo LaPPS34M utilizado para estudar a fluorescência permite uma estabilidade maior e também, como visto anteriormente, possui o tempo de vida de luminescência em torno de 100 a 1000 µs (BÜNZLI, 1989). A instrumentação descrita na fase I (seção 3.2) desta dissertação possibilitou a medida do tempo de vida do complexo e confirmou o dado que consta na literatura. Na Figura 31 está apresentado o gráfico de decaimento de fluorescência do complexo LaPPS34M observado com o sistema de aquisição com a válvula fotomultiplicadora R928 descrita na Figura 13. O tempo de vida de luminescência obtido é de 110 μs. 74 1,0 Intensidade de Sinal [a.u.] 0,8 0,6 0,4 0,2 0,0 0,0000 0,0002 0,0004 0,0006 0,0008 0,0010 Tempo [s] Figura 31 - Decaimento de Fluorescência do Complexo LaPPS34M com o uso da válvula fotomultiplicadora R928 obtido pela FASE I Fonte: Própria Para o caso da fase II com o uso de uma válvula fotomultiplicadora miniatura, conforme descrita na figura 15, o valor do tempo de vida de luminescência é dado por 109,5 μs, confirmando os dados relatados nas fases I anterioremente mencionada e também descrito por BÜNZLI, 1989, que o tempo de vida de luminescência é longo para composto na presença de európio em sua estrutura molecular. A Figura 32 ilustra o decaimento exponencial de emissão de luminescência do indicador LaPPS34M pela válvula fotomultiplicadora miniatura R5600U-01. O valor do tempo de vida foi obtido através da composição duas funções exponenciais (tempo de vida de fluorescência e resposta temporal da Val/vula fotomultiplicadora miniatura). 75 Intensidade Relativa de Sinal [a.u] 1,0 0,8 0,6 0,4 0,2 0,0 0,0002 0,0004 0,0006 0,0008 0,0010 Tempo [s] Figura 32 - Decaimento exponencial de emissão de luminescência do indicador LaPPS34M pela válvula fotomultiplicadora miniatura R5600U-01 obtido pela FASE II. Fonte: Própria A partir da fase III a Erro! Fonte de referência não encontrada. apresenta o sinal elétrico aplicado ao diodo emissor de luz (led) para excitação do indicador (linha contínua), o sinal de saída do detector na ausência do fluoróforo (linha tracejada) e o sinal de luminescência na presença do fluoróforo (linha contínua). Todos os sinais foram normalizados para apresentarem valor igual a 1 antes do início do decaimento. 76 Figura 33 - Sinal elétrico aplicado ao led para excitação do indicador (linha contínua), sinal de saída do detector na ausência do fluoróforo (linha tracejada) e sinal de luminescência na presença do fluoróforo (linha contínua) obtido pela FASE III. Fonte: Própria Na Erro! Fonte de referência não encontrada. é possível observar que a resposta do circuito detector não é tão rápida quanto a que seria observada utilizando detectores de maior velocidade (e.g., válvula fotomultiplicadora). É possível observar a resposta temporal referente à luminescência do complexo LaPPS34M destacada da resposta do sistema sensor na ausência do complexo. Sabe-se, portanto, que a luminescência desse complexo pode ser observada por detectores de estado sólido de baixo custo que tenham sensibilidade aproximada a do fotodetector utilizado (i.e., 0.47A/W para comprimento de onda de 650nm) mas que tenham uma resposta temporal mais rápida que a do OPT301 (i.e., típico “rise time” de 90 μs, tempo para transição de 10% a 90% do sinal). Após o tratamento dos dados obteve-se o tempo de vida de fluorescência do complexo LaPPS34M, correspondendo ao valor de 114,5 μs. A Erro! Fonte de referência não encontrada. apresenta os detalhes dos pontos amostrados para o decaimento de luminescência e a curva exponencial ajustada (linha contínua). O valor do tempo de vida foi obtido através da 77 composição duas funções exponenciais (tempo de vida de fluorescência e resposta temporal do fotodiodo). Figura 34 - Exponencial de decaimento de emissão de luminescência do indicador LaPPS34M pelo uso detectores de fotodiodo obtido pela FASE III Fonte: Própria Por fim é possível estabelecer que há uma correlação entre os tempos de vida de luminescência para as três fases estudadas ao longo dessa dissertação. A Tabela 3 representa os resultados encontrados. Tabela 3 - Relação entre as fases da pesquisa e os resultados do tempo de vida de Luminescência Método de Medição Tempo de Vida de Luminescência [μs] FASE I (válvula fotomultiplicadora R928) 110,0 FASE II (válvula fotomultiplicadora R5600U-01) 109,5 FASE III (detector optoeletrônico OPT301) 114,5 Fonte : Própria 78 5. DISCUSSÃO E CONCLUSÃO 5.1. INTRODUÇÃO A detecção usando válvula fotomultiplicadora e fotodiodo possibilitou a medição de parâmetros para avaliar a utilização de novas moléculas e/ou complexo em sistemas biológicos ou médicos. A obtenção dos espectros de absorção, de emissão de fluorescências, de emissão de fluorescências na presença de nanopartículas e os tempos de vida de luminescência demonstram que o complexo LaPPS34M assim como o fluoróforo comercial Cy3 possuem características ópticas necessárias para serem biomarcadores. 5.2. CARACTERIZAÇÃO DE BIOMARCADORES a) Fluoróforo Cy3 A fase I possibilitou fazer a caracterização de possíveis fluoróforos para aplicação em sistemas biomédicos e de diagnósticos em saúde. O estudo do fluoróforo Cy3 e também do complexo LaPPS34M demonstra a necessidade de obter as características ópticas que são importantes para a utilização de biomarcadores. Os espectros de absorção e de emissão do fluoróforo comercial Cy3 demonstram que há um deslocamento de Stokes pequeno, correspondente a um deslocamento de 20 a 50 nm. Essa variação é muito pequena e dificulta a detecção quando a instrumentação é de baixa resolução. Adicionalmente, a proximidade dos espectros de absorção e de emissão dificulta até mesmo diferenciar o espectro de emissão do diodo utilizado, escolhido para emitir na região de absorção do marcador, do espectro de fluorescência do fluoróforo Cy3. 79 Os espectros de fluorescência do marcador conjugado com nanopartículas metálicas, sejam elas de prata ou de ouro, sinalizou uma variável para caracterizar os candidatos a novos fluoróforos. A utilização de nanopartículas, que pode resultar no aumento de intensidade de fluorescência, possibilita que o sistema de detecção de fluorescência possa ser mais simples permitindo que um fotosensor com uma menor sensibilidade seja utilizado. Pode-se observar que o fluoróforo comercial Cy3 conjugado com nanopartícula de ouro propicia um aumento da intensidade de fluorescência de aproximadamente 170% em relação ao espectro de fluorescência na ausência de nanopartícula. b) Complexo LaPPS34M O grande deslocamento de Stokes do complexo LaPPS34M garante que a absorção e a emissão se darão em regiões distantes do espectro. Essa variação espectral permite uma precisão do sinal de fluorescência que é fundamental para sistemas de detecção que utilizam detectores por válvulas fotomultiplicadoras, válvulas fotomultiplicadoras miniaturas ou fotodiodos. Um dos erros associados à detecção de fluorescência é o mascaramento do sinal de fluorescência pelo sinal advindo dos diodos, impossibilitando a confiabilidade na instrumentação desenvolvida. Outro aspecto verificado no caso do complexo LaPPS34M é o deslocamento do comprimento de onda de 615 nm para 820 nm na presença de diferentes solventes conforme observa-se nas figuras 27 (espectro de fluorescência em tetrahidrofurano) e a figura 30 (espectro na presença de etanol). Alguns fatores devem ter contribuído para tal mudança, como: a diluição do complexo em diferentes solventes e a presença de nanopartículas de prata. O tempo de vida de luminescência fornece informações que possibilitam identificar e quantificar o tempo médio que a molécula passa no estado excitado antes de retornar ao estado fundamental. No caso do 80 fluoróforo comercial Cy3, o tempo de vida de luminescência se encontra em torno de 0,3 ns, o que representa um tempo de luminescência curto. No caso do complexo LaPPS34M verificou-se através do gráfico do tempo de vida de luminescência, demonstrado na figura 31, 32 e 34, que o tempo de decaimento da amostra varia entre 110 μs ( com o uso de válvula fotomultiplicadora R928), 109,5 μs ( com o uso da válvula fotomultiplicadora miniatura R5600U-01) e 114,5 μs (com uso do detector optoeletrônico OPT301) Esse tempo elevado de luminescência é adequado para aplicações biomédicas, onde é interessante o uso de moléculas com tempos de vida de luminescência maiores, caracterizando uma nova classe interessante de fluoróforos. 5.3. SISTEMAS DE CUSTO REDUZIDO As fases I, II e III evidenciam a busca por um sistema de detecção de fluorescência que reduza os custos de aquisição e processamento de dados. Na fase I o uso da válvula fotomultiplicadora R928 encarece o sistema proposto, tendo em vista a necessidade futura de se projetar equipamentos de detecção de fluorescência que sejam compactos e tenha um custo reduzido. Na fase II com o uso da válvula fotomultiplicadora miniatura R5600U-01 que é mais barata que a anteriormente mencionada, é possível obter dados confiáveis com uma redução de custo em torno de 30%. A fase III demonstra a possibilidade de redução ainda maior dos custos utilizando detectores optoeletrônicos. Nos três casos o estudo da fluorescência resolvida no tempo, garante a escolha de um sistema eficiente pra a detecção de fluorescência. Concluiu-se que a identificação de fluorescência por meio do uso do complexo LaPPS34M possibilita a indicação da amostra estudada para aplicações em sistemas biomédicos que necessitem de biomarcadores, pois as características ópticas relevantes como espectro de absorção e emissão, o deslocamento de Stokes e o tempo de vida de luminescência apresentam superioridade nas características ópticas em relação aos fluoróforos comerciais 81 já em uso, como o Cy3. O complexo apresenta características ópticas importantes para estudos de identificação e quantificação de microorganismos. Assim, desta maneira, sinalizamos o uso do complexo de európio – LaPPS34M para utilização nos projetos do Instituto Nacional de Inovação em Saúde Pública (INDI-Saúde), que se situa no Instituto Carlos Chagas – Curitiba/PR. 5.4. LIMITAÇÕES DO ESTUDO Um dos fatores limitantes observado neste estudo foi à necessidade de contornar obstáculos referentes à detecção do sinal de fluorescência utilizando um equipamento de baixo custo. O sistema utilizado, baseado na válvula fotomultiplicadora encarece o processo e inviabiliza equipamentos de leitura do tipo point-of-care. A necessidade de se testar a emissão de fluorescência para outros detectores, como fotodiodos, se tornam fundamentais quando estamos interessados em sistemas de leituras ópticas de baixo custo, e que possam ser colocados em equipamentos que façam interpretações de diagnósticos nos locais de atendimento do paciente. Outra limitação é que os fluoróforos utilizados devem apresentar grandes deslocamentos de Stokes para que os sistemas de detecção de fluorescência dos equipamentos possam com precisão distinguir os espectros de absorção e emissão sem a necessidade de uso de componentes especiais e de custo elevado. 5.5. TRABALHOS FUTUROS Os resultados deste estudo sugerem novos trabalhos que incorporem a necessidade de testar novos complexos, aproveitando que o laboratório de Polímeros Paulo Scarpa – LaPPS, da Universidade Federal do Paraná, possui um acervo de complexos e polímeros que podem desempenhar o papel de 82 possíveis biomarcadores, tanto nos processos industriais como em processos biológicos e médicos. Essa interação entre as instituições faz com que novos estudos possam ser direcionados na busca de efetivar a participação desses novos complexos em estudos que priorizem o diagnóstico e tratamento de doenças. Salienta-se também que a inserção dessa dissertação nos estudos do Instituto Nacional de Inovação em Saúde Pública (INDI-Saúde), possibilita contribuir com novos trabalhos relacionados ao tema e também servir de alicerce para o desenvolvimento de equipamentos de detecção de fluorescência de baixo custo, condição primordial para o avanço tecnológico do país visando a independência externa relacionada aos sistemas de identificação e tratamento de doenças. 83 5.6. PUBLICAÇÕES 1 - Araújo, L.M.P.; Oliveira. S.V.; Schneider, F.K.; Bezerra-Jr, A.G.; Gewehr, P.M; Turchett D.A.; Akcelrud, L.C. Optical Characterization of the Molecule Lapps34m for use as a New Fluorophore. Latin America Optics and Photonics Conference (LAOP), September 27-30, 2010, Recife, Brasil. 2- Oliveira, V. S. ; Araújo, L.M.P; Schneider, F.K.; Bezerra-Jr, A.G. Sistema para Estudo da Fluorescência de Marcadores para Diagnósticos em Saúde Pública. I CICPG - I Congresso de Iniciação Científica e PósGraduação, 13 a 16 de setembro de 2010, Florianópolis, Santa Catarina, Brasil. 3- Araújo, L.M.P.; dos Santos, E. A. ; Schneider, F.K.; Branco,G.; Turchett D.A.; Akcelrud, L.C.; Bezerra-Jr, A.G. Sistema de Detecção de Fluorescência para Aplicação em Sistemas de Diagnóstico em Saúde. XXII Congresso Brasileiro de Engenharia Biomédica, 21 a 25 de novembro de 2010, Tiradentes, MG. 4- Dos Santos, E. A.; Schneider, F.K.; Araújo, L.M.P.; Branco,G.; Simas, A. G.; Branco,G.; Sistema de Detecção de Fluorescência para Análise de Complexo Antígeno-Anticorpo com Indicadores Fluorescentes. Seminário de Iniciação Científica e Tecnológica (SICITE 2010), realizado de 06 a 08 de Outubro, no Campus de Cornélio Procópio/ UTFPR, Paraná, 2010. 84 6. REFERÊNCIAS BIBLIOGRÁFICAS ALBANI, J. R. Principles and applications of fluorescence spectroscopy. Blackwell Science, a Blackwell Publishing company, 2007. ALBERTS, B, DENNIS, B., LEWIS, J., RAFF, M., ROBERTS, K., WATSON, J. D., Molecular Biology of the Cell, 3rd Ed. Garland Publ. New York,1995. ABBYAD,P.; CHILDS,W.; SHI,X. and BOXER,S. G. Dynamic Stokes shift in green fluorescent protein variants, PNAS, vol. 104, no. 51, p.p. 20189– 20194. , December 18, 2007. ALCANTARA, P.Jr. Espectroscopia Molecular. Departamento de Física, UFPA Curso Física Moderna II , março 2002. An Introduction to fluorescence spectroscopy . PerkinElmer Life and Analytical Sciences. PerkinElmer Ltd, 2000. ANDRADE, C. Compêndio de Nomenclatura Macromolecular, UNLZ, Zamora, 1995 ARAÚJO, L.M.P.; OLIVEIRA. S.V.; SCHNEIDER, F.K.; BEZERRA-JR, A.G.; GEWEHR, P.M; TURCHETT, D.A.; AKCELRUD, L.C. (2010), Optical Characterization of the Molecule LaPPS34M for use as a New Fluorophore. Latin America Optics and Photonics Conference (LAOP), September 27 -30, Recife, Brasil. ATVARS, T.D.Z.; MARTINELLI, C. Espectroscopia de Luminescência . Chemkeys, 2002. AKCELRUD, L. C. Cartilha do Laboratório de Polímeros Paulo Scarpa. Curitiba, 34 p, 2010. BASSI, A.B.M.S. Conceitos Fundamentais em Espectroscopia .Chemkeys, 2001. BRANCO, G. Novo Instrumento para Monitorização de O2 Gasoso através de Fosforescência Resolvida no Tempo. Curitiba, 1997. Dissertação 85 ( Mestrado em Ciências, Engenharia Biomédica) – Centro Federal de Educação Tecnológica do Paraná. BRASIL. Ação Civil Pública n.º 200500761820, de outubro de 2005, o Juízo da 9.ª Vara Cível da Comarca de Goiânia. Ministério Público Federal, Goiânia, GO, 10 Julho de 2006. BioProbes 23, 1996, p. 01 Disponivel em: 16 de maio de 2010. www.invitrogen.com •.Acesso em BÜNZLI, J.-C. G.; Choppin, G. R.; Lanthanide Probes in Life, Chemical and Earth Sciences, Theory and Practice, Elsevier: New York, 1989. CARUSO, F; OGURI, V. Física Moderna: Origens Clássicas e Fundamentos Quânticos. Rio de Janeiro: Editora Campus, 2006. 606 p. Dependence of Fluorescence Intensity on the Spectral Overlap between Fluorophores and Plasmon Resonant Single Silver Nanoparticles. Nano Lett., Vol. 7, No. 3, 2007. CHEN,Y.; MUNECHIKA,K.; GINGER, D.S. DUNBAR, S.A; JACOBSON, J.W. (2000), Application of the Luminex LabMAP in rapid screening for mutations in the cystic fibrosis transmembrane conductance regulator gene: A pilot study. Clin Chem.Sep, 46(9): 1498-500. EISBERG, R & RESNICK, R. Física Quântica. Tradução: Paulo Costa Ribeiro e Enio Frota da Silveira. Editora Campus. Rio de Janeiro. 1988. ENGVALL, E.; PERLMANN, P. Enzime-linked immunosorbent assay (ELISA). Quantitative assay of immunoglobulin G. Immunochemistry 8: 871874, 1971. Espectroscopia de Fluorescência. Disponível em: http://espectrometriadefluorescencia/espectrometria_com.mht. Acesso em 10 de junho de 2009. Espectro de Fluorescência do Triptofano. www.chemkeys.com, acesso 16 de Maio de 2010. Disponível em: 86 ERNST, L. A.; GUPTA, R.K. ; MUJUMDAR, R. B. and WAGGONELR, A. S. Cyanine Dye Labeling Reagents for Sulfhydryl Groups, Cytometry 10:3-10 (1989). Estrutura Molecular de Fluoróforo Comercial Cy3. Disponível em: www.visaoportal.com.br/blog/.../For_as%20intermoleculares.pdf, acesso em 10 de Junho de 2010. FERREIRA, A.W.; ÁVILA, S.L.M. Diagnóstico imunológico das principais doenças infecciosas e parasitárias. 2. ed., Rio de Janeiro: Guanabara Koogan, 2001. FULTON, R.J. et al ( 1997), Advanced multiplexed analysis with the FlowMetrix system. Clin Chem. Sep,43(9): 1749 -56. GALO, A. L.; COLOMBO, M. F. Espectrofotometria de longo caminho óptico em espectrofotômetro de duplo-feixe convencional: uma alternativa simples para investigações de amostras com densidade óptica muito baixa. Quim. Nova, Vol. 32, No. 2, 488-492 (2009). GUILBAULT, G.G. Practical Fluorescence, Second Edition, Marcel Dekker, Inc., New York, 1990. HAHN, C.D.; RIENER, C. K.; GRUBER, H.J. Labeling of Antibodies with Cy3-, Cy3.5-, Cy5-, and Cy5.5-monofunctional Dyes at Defined Dye/Protein Ratios. Bioconjugate Chem., 11, 696-704, 2000. HAUGLAND, R.P. Molecular Probes Handbook for Fluorescent Probes and Research Chemicals, 6th Edition (1996). INSTITUTO NACIONAL DE INOVAÇÃO EM DIAGNÓSTICOS PARA A SAÚDE PÚBLICA, INDI-SAÚDE , projeto apresentado ao edital 015/2008. ITO, J.A. Técnicas Espectroscópicas em Biofísica .Caderno de Física UEFS, 03(01): 21-28, 2004. JAMESON, D. M.; Hazlett, T. L.; In Biophysical and Biochemical Aspects of fluorescence Spectroscopy; Dewey, T. G.; Ed.; Plenum Press; New York 1991; p 105. 87 JACKSON IMMUNORESEARCH. Disponível em: "Cyanine Dyes (Cy2, Cy3, and Cy5)". http://www.jacksonimmuno.com/technical/f-cy3-5.asp. Acesso em 11 de Agosto de 2010. KRENKE, B.E et al. Development of a novel, fluorescent, two primers approach to quantitative PCR. Profiles in DNA, Promega Corporation, Vol.8, Nº.1, pp.3-5, 2005. LAKOWICZ, J. R. Principles of Fluorescence Spectroscopy. Chapter 3: Fluorophores. Kluwer Academic/Plenum Publishers, New York, 1999. _________. Radiative Decay Engineering: Biophysical and Biomedical Applications, Analytical Biochemistry 298, 1–24 (2001). LAKOWICZ, J. R.; RAY,K.; CHOWDHUR, M.;, SZMACINSKI,H.; YI FU, J. Z. and NOWACZYK,K. Plasmon-controlled fluorescence: a new paradigm in fluorescence spectroscopy, Analyst. 2008 October ; 133(10): 1308–1346. LAKOWICZ, J. R.; Gryczynski, I. In Topics in Fluorescence Spectroscopy Vol 1; Lakowicz, J. R.; Ed.; Plenum Press; New York 1991; p 293. LAWSON, C. L. and Hanson, R. J. Solving Least Squares Problems, Prentice-Hall,1974, Chapter 23. LEE, J. D.; Química Inorgânica não tão Concisa; Tradução: Toma, H. E.; Rocha, R. C.; Edgard Blücher Ltda.: São Paulo, 1999, cap. 29. Lei de Beer-Lambert. Disponível em:http://pt.wikipedia.org/wiki/Lei_de_BeerLambert.Acesso em 08 de Junho de 2010. LIMA, Patrícia P.; MALTA, Oscar L. and ALVES, Severino J. Estudo spectroscópico de complexos de Eu3+, Tb3+ E Gd3+ com ligantes derivados de ácidos dicarboxílicos. Quím. Nova [online]. 2005, vol.28, n.5, pp. 805-808. LIU, W.T. Nanoparticles and Their Biological and Environmental Applications, Journal of bioscience and bioengineering, vol. 102, no. 1, 1–7, 2006. 88 LIU, X.J., LI, Y.Z., CI, Y.X. Time-resolved Fluorescence Studies of the interation of the Eu3+ complexes of Tetracycline Analogues with DNA. Analytica Chimica Acta 345, 213-217, 1997. MABEY, D.; PEELING, R.W.; UOWSKI, A.; PERKINS, M.D. Diagnostics for the developing world. Nat Ver Microbiol 2: 231-240, 2004. MARTINS, T. S.; ISOLANI, P. C. Terras raras: aplicações industriais e biológicas.Química Nova, São Paulo, v. 28, n 1, p. 111-117, 2005. MUJUMDAR, R. B. et al. Cyanine labelling reagents: sulfobenzindocyanine succinimidyl esters. Bioconjug. Chem. 4, 105-111, 1993. _________________. Cyanine labelling reagents: sulfobenzindocyanine succinimidyl esters, Bioconjugate Chem. 3(7), 365-36, 1996. MULLIS, K.B. The unusual origin of the polymerase chain reaction. Sci Am 262: 56-65, 1990. NOVAIS, M. C., ALVES, M.P. PCR em Tempo Real. Revista Biotecnologia Ciência & Desenvolvimento, Edição 33, 2004. NICHOL, S.T.; ARIKAWA, J.; KAWAOKA, Y. Emerging viral diseases. Proc Natl Acad Sci USA 97:12411-12412, 2000. OKUNO, E. et al .Física para Ciências Biológicas e Biomédicas. Editora Harbra, São Paulo, 1982. OPT301, Burr-Brown Corporation, U.S.A. January, 1994. PERUSK ,A.H.; PERUSKI, L.F. Immunological methods for detection and Identification of Infectious disease and biological warfare agents. Clin Diag Lab Immunol 10: 506-513, 2003. PRASAD, Paras N., “ Introduction to Biophotonics,” Wiley- Interscience, (2003). 89 RAOULT, D.; FOURNIER, P.E.; DRANCOURT, M. (2004),What does the Future hold for Clinical Microbiology?. Nat Rev.Microbiol 2: 151-159. RICHARDSON, F. S.(1982), Terbium(III) and Europium(III) ions as Luminescent Probes and Stains for Biomolecular Systems, Chem. Rev., 82 (5), pp 541–552. REITZ, J. R.; MILFORD, F. J. e CRISTY, R. W. Fundamentos de Teoria Eletromagnética, Editora Campus, Rio de Janeiro, 1991. RIFFITHS et al. Introdução à genética, 8º Edição, Guanabara Koogan, 2006. ROSI, N. L. and MIRKIN, C. A. Nanostructures in Biodiagnostics, Chem. Rev. 2005, 105, 1547-1562. SÁ,G.F; MALTA, O.L.; DONEGA, C.. M.; SIMAS, A.M.; LONGO, R.L;SANTACRUZ, P.A. e SILVA, E.F. Spectroscopic properties and design of highly luminescent lanthanide coordination complexes. Coordination Chemistry Reviews. 196. 165–195. 2000. SALIBA, Lucas. F. Interação do complexo luminescente [Eu(tta)3] com sílica mesoporosa”. Dissertação ( Mestrado em Ciências de Materiais) – Universidade Estadual Paulista. “ Júlio de Mesquita Filho”., Faculdade de Engenharia UNESP, Ilha Solteira, 2009. SANCHEZ, M.C.A. Testes sorológicos. In: Diagnóstico laboratorial das principais doenças infecciosas e auto-imunes 2. ed., Rio de Janeiro: Guanabara Koogan, 2001. SANTOS, Wellington C. Produção e Caracterização de nanopartículas por ablação a laser em meio líquido. 2010. Dissertação (Mestrado em Física) – Instituto de Física, Universidade Federal do Paraná, Curitiba, 2010. SAPSFORD ,K. E. ; BERTIL. and MEDINTZ ,I. L. Materials for Fluorescence Resonance Energy Transfer Analysis: Beyond Traditional Donor– Acceptor Combinations, Angew. Chem. Int. Ed. 2006, 45, 4562 – 4588. SELVIN, P. R. “The Renaissance of Fluorescence Resonance Energy Transfer,” Nature Structural Biology, Vol. 7, No. 9, pp. 730-734 (2000). 90 SIERRA, M.M.S.; GIOVANEL, M.; DONARD, F.X. e BELIN, C. A utilização da Espectroscopia de fluorescência no Estudo da Matéria Orgânica dissolvida nas águas naturais: Evolução e Perspectivas .Química Nova, 19(3), 1996. SIWACH, O.P.; SEN,P. Fluorescence properties of Ag nanoparticles in water, methanol and hexane. Journal of Luminescence 129 (2009) 6–11. SKOOG, D.A.; Leary J.J. Análisis Instrumental, 4° ed.; Ed. McGraw-Hill (1994), págs. 201-219. SOKOLOV,K.; CHUMANOV,G.; COTTON, M.T. Enhancement of Molecular Fluorescence near theSurface of Colloidal Metal Films. Anal. Chem. 1998, 70, 3898-3905 SPECTOR, N. Manual para a redação de teses, dissertações e projetos de pesquisa. Rio de Janeiro : Guanabara Koogan, 1997. ULLMANN, M.; FRIEDLANDER, S.K.; SCHMIDT-OTT, A. Nanoparticle formation by laser ablation. Journal of Nanoparticle Research 4: 499–509, 2002. VALEUR,B. Molecular Fluorescence: Principles and Applications,. Chapter 3: Characteristics of Fluorescence Emission, Wiley-VCH, Weinheim, Germany, 2002. VOET, D. VOET, J., Biochemistry, 2nd Ed. John Wiley & Sons, New York, (1995). XIAO, M.; PHONG A.; HA, C.; CHAN, T.F.; CAI, D.; LEUNG, L.; WAN, E.; KISTLER, A.L.; DERISI, J.L.; SELVIN, P.R.; KWOK, P.Y. Rapid DNA mapping by fluorescent single molecule detection. Nucleic Acids Research 2007 35(3). YAGER P.; EDWARDS T.; FU E.; HELTON K.; NELSON K.; TAM M. R. & WEIGL B. H. Microfluidic diagnostic technologies for global public health. Nature, vol. 442, july 2006. 91 ZHANG, J.; LAKOWICZ, J. R. Metal-enhanced fluorescence of an organic fluorophore using gold particles. OPTICS EXPRESS, Vol. 15, No. 5, 2007. ZUO, L.; WEI, W.; MORRIS,M.; WEI,J.; GORBOUNOV. M. New Technology and Clinical Applications of Nanomedicine, Med Clin N Am 91, 845– 862(2007). YANG, S.; ROTHMAN, R. PCR-based diagnostics for infections diseases: uses, limitations and future applications in acute-care settings. Lancet 4: 337-348, 2004. WANG, D.; COSCOY, L.; ZYLBERBERG, M.; AVILA, P. C.; BOUSHEY, H.A.; GANEM, D.; DERISI, J.L.(2002), Microarray-based detection and genotyping of viral pathogens. Proc Natl Acad Sci U.S.A . Nov 26,99(24): 15687-92. WILLARD, H.H., MERRIT Jr., L.L., DEAN, J. A. & SETTLE Jr.,F. A. Instrumental Methods of Analysis, 7th. Edn. Belmont: Wadsworth, ( 1988). WILSON, D. Hiv Epidemiology: A Review of Recent Trends and Lessons. Global HIV/AIDS Program.The World Bank. 2006. WILTSHIRE, S.; O’MALLEY, S.; LAMBERT,J.; KUKANSKIS, K.; EDGA, D.; KINGSMORE,S.F.; SCHWEITZER,B. Detection of Multiple Allergen-specific IgEs on Microarrays by Immunoassay with Rolling Circle Amplification. Clinical Chemistry 46, No. 12, 2000. 92 7. ANEXOS ANEXO A FLUORÓFOROS INTRÍNSECOS 93 ANEXO B FLUORÓFOROS EXTRÍNSECOS OU BIOMARCADORES FLUORESCEÍNA Rodamina B 94 ANEXO C PRODUÇÃO E CARACTERIZAÇÃO DAS NANOPARTÍCULAS A produção e caracterização das nanoparticulas (NP) se deram por ablação a laser em meio líquido utilizando alvos metálicos (ULLMANN, 2002). Os alvos utilizados foram de Au, e Ag. A ablação foi realizada usando a linha de emissão 1064 nm de um laser Nd:YAG Quantronix Model 117 operando em modo Q-switched, com duração de pulso de 150 ns e taxa de repetição de 300 Hz. O feixe laser foi guiado para a amostra através de dois espelhos e focalizado por uma lente de 50 mm de distância focal formando um spot de 40 µm. Para todos os alvos foi utilizada água bidestilada como meio liquido. A coluna de água formada sobre a superfície dos alvos era de 2 mm, exceto para o alvo de ouro onde a coluna era de 3 mm. A caracterização das partículas foi realizada utilizando as técnicas de espalhamento dinâmico de luz (DLS) para obtenção da distribuição de tamanho das partículas, e por absorção linear de luz (UV-VIS) para estudo das atividades ópticas. O DLS foi realizado com o equipamento BI-200SM ver. 2.0 da Brookhaven utilizando como fonte de luz a emissão de 632.8 nm de um laser de HeNe com potência de 75 mW máxima. em modo continuo (CW). A obtenção da distribuição de tamanho foi através do modelo NNLS5. Os gráficos abaixo representam os resultados dos espectros de absorção das nanopartículas de ouro e prata, e também a caracterização por DLS do tamanho das nanopartículas de ouro, que fazendo aproximação para as nanopartículas de prata o tamanho se mantém constante. 5 O modelo NNLS (Non-Negative Least-Squares) constitui em uma distribuição não negativa dos mínimos quadrados para mostrar a distribuição do tamanho das nanopartículas, função do MATLAB, construído por CL Lawson, RJ Hanson, 1974. (LAWSON, 1974) 95 (A) (B) (C) Figura 35 - A) Tamanho das nanopartículas de ouro por DLS, B) Espectro de absorção das nanopartículas de ouro e C) Espectro de absorção linear para o colóide de prata Fonte: (SANTOS, 2010)
Download