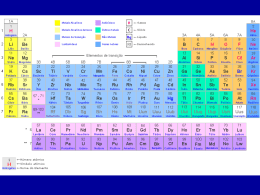
Classificação Periódica dos Elementos Químicos Classificação periódica de Dimitri Mendeleyev Colocou os elementos por ordem crescente das suas massa atômicas, distribuindo-os em 8 colunas verticais e 12 linhas horizontais; Verificou que as propriedades variavam periodicamente à medida que aumentava a sua massa atômica; • Admitiu que o peso atômico de alguns elementos não estava correto; • Deixou lugares vagos para os elementos que ainda estavam por descobrir. Lei periódica de Moseley Demonstrou que a carga do núcleo do átomo é característica de um elemento químico; Reordenou os elementos químicos por ordem crescente dos seus números atômicos; Tabela Periódica H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Fr Ra Ac Un q Un p Un h Un s Un o Un e Uu n Uu u “Quando os elementos são agrupados por ordem crescente de número atômico (Z) observa-se a repetição periódica de várias propriedades.” TABELA PERIÓDICA PERÍODOS São as LINHAS HORIZONTAIS da tabela periódica 1º Período 2º Período 3º Período 4º Período 5º Período 6º Período 7º Período 6º Período Série dos Lantanídeos 7º Período Série dos Actinídeos O número de ordem do período de um elemento químico é igual ao número de níveis eletrônicos que este elemento possui. Fe F 9 26 1s²1s² 2s²2s² 2p52p6ou 3s² K3p =624s² L =3d 76 ou Possui DOIS NÍVEIS DE ENERGIA, então, localiza-se K = 2 L =da 8 tabela M = 14periódica N=2 no 2º PERÍODO Possui QUATRO NÍVEIS DE ENERGIA, então, localiza-se no 4º PERÍODO da tabela periódica TABELA PERIÓDICA GRUPOS OU FAMÍLIAS São as LINHAS VERTICAIS da Tabela Periódica. Elementos Nível de Valência H 1s1 Li 2s1 Na 3s1 K 4s1 Rb 5s1 Cs 6s1 Fr 7s1 Agrupa os elementos químicos que em geral possuem a mesma configuração eletrônica no último nível de energia e por isso propriedades químicas semelhantes. TABELA PERIÓDICA ELEMENTOS REPRESENTATIVOS(A) E DE TRANSIÇÃO(B) Os elementos representativos possuem o elétron DIFERENCIAL (mais energético) em um subnível “s” ou “p” da última camada 19 K 1s² 2s² 2p6 3s² 3p6 4s1 9 F 1s² 2s² 2p5 TABELA PERIÓDICA ELEMENTOS REPRESENTATIVOS(A) E DE TRANSIÇÃO(B) Os elementos de transição possuem o elétron DIFERENCIAL (mais energético) em um subnível “ d ” (transição externa) da penúltima camada ou“ f ” (transição interna) da antepenúltima camada 26 Fe 57 La 1s² 2s² 2p6 3s² 3p6 4s² 3d6 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f 1 Para os elementos REPRESENTATIVOS a sua família é identificada pelo TOTAL DE ELÉTRONS NA CAMADA DE VALÊNCIA (última camada). 20Ca 1s² 2s² 2p6 3s² 3p6 4s² Família II A 17 Cl 1s² 2s² 2p6 3s² 3p5 33As 1s² 2s² 2p6 3s² 3p6 4s² 3d10 4p3 Família VII A Família V A TABELA PERIÓDICA As famílias dos elementos REPRESENTATIVOS possuem nomes especiais Famílias Nome Especial Elementos da Família Metais Alcalinos 1 ou 1A 2 ou 2A 13 ou 3A Li, Na, K, Rb, Cs, Fr Metais Alcalinos Terrosos Be, Mg, Ca, Sr, Ba, Ra Família do Boro B, Al, Ga, In, Tl 14 ou 4A 15 ou 5A Família do Carbono 16 ou 6A 17 ou 7A 18 ou 8A Família do Nitrogênio Calcogênio Halogênio Gases Nobres C, Si, Ge, Sn, Pb N, P, As, Sb, Bi O,S,Se,Te,Po F, Cl, Br, I, At He, Ne, Ar, Kr, Xe, Rn TABELA PERIÓDICA CLASSIFICAÇÃO DOS ELEMENTOS QUÍMICOS Quanto às Características Físicas a) Metais : são os elementos situados a esquerda na tabela periódica. Geralmente eles brilham quando polidos, conduzem eletricidade e calor, possuem alto ponto de fusão, podem ser transformados em fios e são maleáveis. b) Ametais ou Não – Metais : São os elementos situados a direita na tabela periódica. Não possuem brilho, não conduzem calor nem eletricidade e possuem baixo ponto de fusão. (exceção do carbono que possue ponto de fusão de 3.500º C) Quanto à Natureza a) Naturais ou Cisurânicos : são os elementos químicos que podem ser encontrados na natureza. Com exceção do Tecnécio (Z = 43), todos os outros possuem número atômico menor do que o Urânio (Z ≤ 92). b) Artificiais ou Transurânicos : são os elementos químicos obtidos em laboratórios e que possuem número atômico maior do que o do Urânio (Z > 92). TABELA PERIÓDICA CLASSIFICAÇÃO DOS ELEMENTOS QUÍMICOS Quanto ao Elétron de Diferenciação a) Representativos : O elétron de diferenciação está no subnível s ou p. Famílias 1, 2, 13, 14, 15, 16, 17 e 18 b) Transição Externa : O elétron de diferenciação está no subnível d. Famílias 3, 4, 5, 6, 7, 8, 9, 10, 11, 12. c) Transição Interna : O elétron de diferenciação está no subnível f. Série dos Lantanídeos e dos Actinídeos. TABELA PERIÓDICA CLASSIFICAÇÃO DOS ELEMENTOS QUÍMICOS Quanto ao Estado Físico QUESTÃO 01 Nos metais de transição interna, o elétron de diferenciação (o mais energético) se localiza no: a) subnível “s”, da última camada. b) subnível “p”, da penúltima camada. c) subnível “f”, da antepenúltima camada. d) subnível “d”, da antepenúltima camada. e) subnível “g”, da penúltima camada. QUESTÃO 02 1 2 3 4 5 6 7 A configuração eletrônica de um átomo é 1s² 2s² 2p6 3s² 3p6 4s² 3d5. Para este elemento podemos afirmar: F I) É elemento representativo II) É elemento de transição. III) Seu número atômico é 25. IV) Possui 7 subníveis de energia. a) somente I é correta. b) somente II e III são corretas. c) somente II, III e IV são corretas. d) todas são corretas. e) todas são falsas. Elétron diferencial V em subnível “d” V elemento de transição V 2 + 2 + 6 + 2 + 6 + 2 + 5 = 25 QUESTÃO 03 Um elemento configuração químico tem número atômico 33. A sua eletrônica indica que está localizado na: a) família 5 A do período 3. b) família 3 A do período 3. c) família 5 A do período 4. d) família 7 A do período 4. e) família 4 A do período 7. 1s² 2s² 2p6 3s² 3p6 4s² 3d10 4p3 Família 5A ou 15 Período 4 QUESTÃO 04 Na classificação periódica, os elementos químicos situados nas colunas 1A e 7A são denominados, respectivamente: 1A ou 1 alcalinos 7A ou 17 halogênio a) halogênios e alcalinos. b) alcalinos e alcalinos terrosos. c) halogênios e calcogênios. d) alcalinos e halogênios. e) halogênios e gases nobres. QUESTÃO 05 (UFAM – AM) Na classificação periódica, os elementos Ba (grupo 2), Se (grupo 16) e Cl (grupo conhecidos,respectivamente, como: Ba alcalino terroso Se calcogênio Cl halogênio a) alcalino, halogênio e calcogênio b) alcalino terroso, halogênio e calcogênio c) alcalino terroso, calcogênio e halogênio d) alcalino, halogênio e gás nobre e) alcalino terroso, calcogênio e gás nobre 17) são LISTA DE EXERCÍCIO 01) No início do século XIX, com a descoberta e o isolamento de diversos elementos químicos, tornou-se necessário classifica-los racionalmente para a realização de estudos sistemáticos. Muitas contribuições foram somadas até se chegar à atual classificação periódica dos elementos químicos. Em relação à classificação periódica atual, responda: a) Como são classificados os elementos de acordo com sua natureza? b) Como são classificados os elementos de acordo com as suas características físicas? c) Como são classificados os elementos químicos com relação ao elétron de diferenciação? d) Qual o critério utilizado para listar os elementos de forma seqüencial na tabela periódica? e) Qual a relação entre os elementos de um mesmo grupo ou família? f) Qual a relação entre os elementos de um mesmo período? LISTA DE EXERCÍCIO 02) (UEG GO) Analise as configurações eletrônicas dos elementos representados em I, II e III e, em seguida, marque a alternativa CORRETA: I. 1s22s22p63s23p5 II. 1s22s22p63s1 III. 1s22s22p63s23p64s23d10 a) O número de elétrons da camada de valência dos elemento I e III são respectivamente 7 e 10. b) Os elementos II e III são classificados como elementos de transição. c) O número de prótons do elemento II é igual a 12. d) O elemento I pertence à família dos halogênios (família 17) e, ao reagir com sódio metálico, forma um composto com alto ponto de fusão. LISTA DE EXERCÍCIO 03) (UFAM) Dadas as configurações abaixo, associe com a classificação periódica correspondente I. 1s2 2s2 2p6 3s2 3p5 II. 1s2 2s2 2p6 3s2 3p6 4s2 3d1 III. 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 IV. 1s2 2s2 2p6 3s2 3p6 ( ( ( ( ) ) ) ) Metal Alcalino Terroso Halogênio Gás Nobre Metal de Transição A numeração correta, de cima para baixo, é: a) I, III, II, IV b) I, IV, III, II c) III, I, IV, II d) III, II, IV, I e) IV, III, II, I LISTA DE EXERCÍCIO 04 (UDESC) Os elementos X e Y apresentam as seguintes configurações eletrônicas 1s22s22p63s23p64s23d104p3 e 1s22s22p63s23p64s1, respectivamente. O período e a família em que se encontram estes elementos são: a) Os elementos X e Y pertencem ao quarto período, sendo que o elemento X pertence à família V A, enquanto e elemento Y pertence à família I A. b) Os elementos X e Y pertencem ao quarto período, sendo que o elemento X pertence à família III A, enquanto e elemento Y pertence à família I A. c) Os elementos X e Y pertencem à mesma família e ao mesmo período. d) Os elementos X e Y pertencem ao terceiro e primeiro períodos respectivamente. Quanto à família os dois elementos pertencem à família IV A. e) O elemento X é um elemento alcalino e o elemento Y é um halogênio.
Baixar