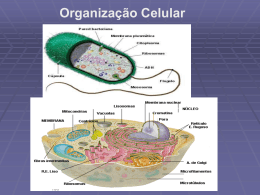
PATOLOGIA GERAL È literalmente, o estudo (logos) do sofrimento (pathos). •Saúde: estado de perfeita adaptação do organismo ao ambiente físico, psíquico ou social em que se vive, sentindo-se bem e sem apresentar sinais ou alterações orgânicas evidentes. •Doença: é um estado de falta de adaptação ao ambiente físico, psíquico ou social, no qual o indivíduo sente-se mal (apresentando sintomas) e explicita alterações orgânicas evidenciais. •Adaptação - Homeostasia: prioridade geral dos organismos que se relaciona com a capacidade de ser sensível às variações do meio ambiente e de produzir respostas capazes de adaptá-lo. •Síndrome: reunião de sinais e sintomas ou uma combinação de lesões sem os quais a doença não pode ser diagnosticada. Patologia Geral • Ciência básica/prática clínica, • Estudo das alterações estruturais e funcionais nas células, tecidos e órgãos que dão origem ás doenças. • Tenta explicar os “porquês” e as causas dos sinais e sintomas manifestados por pacientes, fornecendo fundamentações sólidas para assistência clínica e tratamento. Rudolf Virchow (1821-1905). Patologista em Berlim. Uma das figuras mais importantes da Medicina européia na segunda metade do século XIX. Defendeu que as alterações fundamentais nas doenças seriam traçáveis às células, e cada doença provocaria alterações microscópicas características. Livro: Patologia Celular, 1858. Patologia • Patologia Geral – aborda as reações básicas das células e tecidos a estímulos anormais que geram doenças. • Patologia Sistêmica (especial) – examina as respostas específicas de órgãos e tecidos especializados a estímulos bem definidos. Aspectos Básicos de um Processo Mórbido que formam o Cerne da Patologia: • Causa – Etiologia, • Patogenia – Os mecanismos do seu desenvolvimento, • Alterações Morfológicas – Alterações estruturais induzidas nas células e órgãos do corpo, • Importância Clínica – Conseqüências funcionais das alterações morfológicas. Etiologia ou Causa • Fatores etiológicos: intrínsecos ou genéticos e adquiridos (p.ex., infecciosos, nutricionais, químicos, físicos). • Causa – Diagnóstico – Enfermidade – Tratamento. • Fatores genéticos – afecções – induzidas pelo ambiente – exerce influências – doenças genéticas. Patogenia • É a seqüência de eventos nas respostas das células ou tecidos ao agente etiológico, do estímulo inicial á expressão final da doença. Alterações Morfológicas • Alterações estruturais nas células ou tecidos que são típicas da doença ou diagnóstica do processo etiológico. Perturbações Funcionais e Importância Clínica • A natureza das alterações morfológicas e sua distribuição em diferentes órgãos ou tecidos determinam as manifestações clínicas ( sinais e sintomas), evolução e prognóstico da doença. Célula Normal • É confinada dentro de uma faixa razoavelmente estreita de função e estrutura por seus programas genéticos de metabolismo, diferenciação e especialização; por limitações das células vizinhas; e pela disponibilidade de substratos metabólicos. Entretanto, é capaz de dar conta das demandas fisiológicas normais – homeostase normal. A UNIDADE DA VIDA Se os limites da resposta adaptativa a um estímulo forem ultrapassados ou, em certos casos, quando a adaptação é impossível lesão celular A lesão celular é reversível até um certo ponto, mas, se o estímulo persistir ou for intenso, a célula atinge um ponto sem retorno e sofre lesão celular irreversível e morte. Morte Celular • É o resultado final da lesão celular, • Maior conseqüência da isquemia, infecção, toxinas e reações imunes. • Padrões morfológicos: necrose ( necrose de coagulação), apoptose. Necrose/Necrose de Coagulação • É o tipo mais comum de morte celular após estímulos exógenos ( isquemia, lesão química). • Manifesta-se por tumefação intensa ou ruptura da célula, desnaturação e coagulação das proteínas citoplasmáticas e degradação das organelas celulares. Necrose de Coagulação Necrose de Coagulação – Músculo Cardíaco Anatpat-unicamp. Normal – Músculo Cardíaco Anatpat-unicamp. Apoptose • Ocorre quando a célula morre mediante ativação de um programa de suicídio controlado internamente. • É um processo destinado a eliminar células indesejáveis durante a embriogênese e em diversos processos fisiológicos. • Características morfológicas - condensação e fragmentação da cromatina. NECROSE X APOPTOSE Respostas Celulares á Lesão Alterações Subcelulares •Lesão Celular Aguda •Lesão Reversível •Morte Celular Necrose / Apoptose •Adaptações Celulares •Acúmulos Intracelulares •Calcificações Patológicas •Envelhecimento Celular Causas de Lesão Celular • • • • • • • • Oxigênio, Agentes Físicos, Agentes Químicos, Agentes Biológicos, Mecanismos Imunes, Distúrbios Genéticos, Distúrbios Nutricionais, Envelhecimento. Oxigênio • Hipóxia ( O2 baixo) - anemias, envenenamento( CO, cianetos), insuficiência cardiorrespiratória. • Anóxia ( O2 ausente) - afogamento. • Isquemia ( falta de circulação) - trombos, embolos, aterosclerose, compressões. • Radicais Livres. Agentes Físicos • • • • • Mecânicos - traumatismos, Temperatura - frio, calor, Pressão atmosférica - variações repentinas, Radiações ionizantes, Correntes elétricas • • • • • • Agentes Químicos Venenos - mercuriais, arsênico, cianeto, fenóis, CCL4, agentes alquilantes etc, Drogas medicamentosas, Drogas não terapêuticas - álcool, narcóticos, Poluição do ar - tabagismo, Inseticidas, herbicidas, CO, Agentes inócuos em proporções inadequadas - sódio, glicose, O2. “Todas as substâncias são venenos; não existe nada que não seja veneno. Somente a dose correta diferencia o veneno do remédio. "Paracelsus (1493-1541) Agentes Biológicos • Vírus - citolíticos, citopáticos e • • • • oncogênicos, Rickettsias, Bactérias - endotoxinas / exotoxinas, Metazoários, Fungos. Louis Pasteur (1822-1895) e Robert Koch (1843-1910) foram os primeiros cientistas a descrever o papel das bactérias como vectores de várias doenças. Organismos unicelulares procariontes Reino Monera. BACTÉRIAS FUNGOS VÍRUS Imagem de microscópio do vírus influenza (gripe) Mecanismos Imunes • • • • Imunidade humoral - células B, imunidade celular - células T. Defesa contra agentes biológicos. As reações auto-antígenos endógenos sejam responsáveis por uma série de doenças autoimunes. • Reação Anafilática. Distúrbios Genéticos • Hereditários, • Adquiridos. • Lesão genética - Síndrome de Dawn (malformação congênita). • Lesão genética - Substituição de um único aminoácido da hemoglobina S na anemia falciforme. Trissomia do 21 - Dawn Anorexia Nervosa/ Obesidade/ Bulimia/ Excesso Alimentar Distúrbios Nutricionais Distúrbios Nutricionais • Avitaminoses - escorbuto, • Desnutrição Protéico-Calórica - marasmo, • Problemas Nutricionais Auto-infligidos (anorexia nervosa ou inanição auto-induzida) • Os excessos de lipídios predispõem à aterosclerose. • Subnutrição/Hipernutrição - composição da dieta • Envelhecimento. Lesão Celular - Princípios • A resposta celular a estímulos nocivos depende do tipo de lesão, sua duração e sua intensidade. Lesão reversível - Baixas doses de toxina ou períodos breves de isquemia. • As conseqüências da lesão celular dependem do tipo, estado e adaptabilidade da célula lesada. Perda do suprimento sangüíneo e hipóxia? • Sistemas intracelulares vulneráveis - manutenção da integridade das membranas celulares, respiração aeróbica, síntese de proteínas, preservação da integridade do aparelho genético da célula. Lesão Celular - Princípios(cont) • Os elementos estruturais e bioquímicos da célula estão tão intimamente relacionados que; seja qual for o ponto preciso do ataque inicial, a lesão em um locus produz efeitos secundários generalizados. • As alterações morfológicas da lesão celular tornam-se evidentes somente depois algum sistema bioquímico crucial dentro da célula ter sido atingido. Mecanismos Bioquímicos Gerais - Lesão e Morte Celular. • Depleção de ATP, • Oxigênio e Radicais Livres derivados do Oxigênio, • Cálcio intracelular e perda da Homeostase do cálcio, • Defeitos da Permeabilidade da Membrana, • Lesão Mitocondrial Irreversível. • • • • • • • DEPLEÇÃO de ATP É essencial a muitos processos sintéticos e degradativos dentro da célula - fosfato de alta energia: Transporte na membrana, Síntese de proteínas, Lipogênese, Reações de desacilação-reacilação - turnover de fofolipídios. O ATP é produzido de duas maneiras Fosforilação oxidativa do ADP(mamíferos), Via Glicolítica - gera ATP na ausência de oxigênio usando glicose dos líquidos corporais ou da hidrólise de glicogênio. A depleção de ATP e redução da síntese de ATP são conseqüências comuns da lesão isquêmica e tóxica. Oxigênio e Radicais Livres Derivados do Oxigênio • Célula/energia = redução do oxigênio molecular em água. • Durante esse processo, pequenas quantidades de formas de oxigênio reativas parcialmente reduzidas são produzidas como um subproduto inevitável da respiração mitocondrial. • Algumas dessas formas são radicais livres(espécies de oxigênio reativo) que podem danificar lipídos, proteínas e ácidos nucleicosestresse oxidativo. Cálcio Intracelular - Perda da Homeostase do Cálcio • Cálcio livre no citosol < 0,1micromol (mitocôndrias e retículo endoplasmático) • Cálcio extracelular = 1,3 milimol, • Gradiente modulados por Ca2+, Mg2+ -ATPases dependentes de energia associadas á membrana, • A isquemia e certas toxinas causam aumento da concentração citosólica de Ca. Devido ao influxo líquido de Ca2+ através da membrana plasmática e a liberação de Ca2+ das mitocondrias e ret. Endoplasmático. Ca2+ Permeabilidade membrana Fosfolipases Proteases ATPases Endonucleases Ca2+ Lesa a membrana Degradam as proteínas Depleção de ATP Fragmentação Cromatina Enzimas Defeitos da Permeabilidade da Membrana • A perda inicial da perm. Seletiva da membrana, levando a lesão franca da membrana, é uma característica constante de todas as formas de lesão celular. • Tais defeitos podem advir de uma série de eventos que envolvem depleção de ATP e ativação das fosfolipases modulada pelo cálcio. • Pode afetar a mitocondria, membrana plasmática e outras membranas celulares. Lesão Mitocondrial Irreversível • As células mamíferas são obrigatoriamente dependentes do metabolismo oxidativo para sobrevida, independente da capacidade glicolítica. • São alvos de muitos estímulos nocivos - hipóxia, toxinas. • Podem ser danificadas: pela elevação do Ca2+ citosólico, estresse oxidativo, degradação de fosfolipídios(fosfolipases A2). • Uma lesão irreparável das mitocondrias destruirá as células. Disfunção Mitocondrial Lesão Isquêmica • É uma perda do suprimento sangüíneo por redução do fluxo arterial ou da drenagem venosa em um tecido. • A isquemia compromete a oferta de substrato metabólicos(fornecidos pelo sangue corrente), incluindo a glicose. • Lesa mais rapidamente que a hipóxia( prejudica a respiração oxidativa aeróbica). O primeiro ponto de ataque da Hipóxia é a respiração aeróbica celular, isto é, a Fosforilação Oxidativa pelas mitocondrias. Á medida que a tesão de oxigênio cai, há perda da fosforilação oxidativa e diminuição da geração de ATP. A resultante depleção de ATP exerce efeitos difusos sobre muitos sistemas dentro da célula: Bomba de Sódio • A atividade da bomba de sódio depende de energia na membrana plasmática (Na+, K+ - ATPase) é reduzida. • A falha desse sistema de transporte ativo, devido a uma concentração reduzida de ATP e aumento de atividade de ATPase, leva ao acúmulo de sódio no meio intracelular, com difusão do potássio para fora da célula. • O ganho final do soluto é acompanhado por ganho isosmótico de água, tumefação celular e dilatação do retículo endoplasmático. BOMBA Na/K O Metabolismo Energético Celular é Alterado • Quando os níveis de oxigênio baixa, a fosforilação oxidativa cessa e as células dependem da glicólise para produção de energia. • A glicólise anaeróbica, visa manter as fontes de energia da célula, gerando ATP através do metabolismo de glicose derivado de glicogênio. • Em conseqüência, as reserva de glicogênio são rapidamente exauridas. • A glicólise resulta no acúmulo de ácido lático e fosfatos inorgânicos. Isso diminui o Ph intracelular. O próximo fenômeno a ocorrer é a ruptura estrutural do aparelho de Síntese de Proteínas, manifestada por desprendimento dos ribossomas do RER e dissociação dos polissomas em monossomas, com conseqüênte redução da síntese de proteínas. •Se a hipóxia continuar, a depleção de ATP crescente causa deteriorização morfológica adicional: O citoesqueleto sofre dispersão, resultando na perda de características ultraestruturais como as microvilosidades e a formação de bolhas na superfície celular. “Figuras de mielina”, oriundas da MP e organelas, podem ser vistas dentro do citoplasma ou no meio extracelular. •Nessa fase, as mitocôndrias geralmente estão tumefactas, devido a perda do controle do volume; o RE permanece dilatado; e toda a célula sofre tumefação acentuada, com concentração aumentada de água, sódio e cloreto e uma concentração reduzida de potássio. •Se o oxigênio for restaurado, todas essas perturbações são reversíveis, caso persista sobrevém uma Lesão Irreversível. •A lesão irreversível está associada morfologicamente a tumefação intensa das miticôndrias, lesão extensa da MP e tumefação dos lisossomas. No miocárdio, estas são indicações de lesão irreversível e podem ser encontradas 30 a 40 minutos após isquemia. •Dois fenômenos caracterizam a irreversibilidade de maneira consistente: o primeiro é a incapacidade de reverter a disfunção mitocôndrial que causa depleção acentuada de ATP, e o segundo é o desenvolvimento de perturbações profunda na função da membrana. •Um grande volume de evidências indica que a lesão da membrana é um fator crucial na patogenia da lesão celular irreversível. •A perda da função da membrana mitocondrial, aumento da permeabilidade ás moléculas extracelulares e defeitos ultraestruturais da membrana plasmática ocorrem nos primeiros estágios da lesão irreversível •A hipóxia afeta a fosforilação oxidativa e, por conseguinte, a síntese de suprimentos vitais de ATP. A lesão da membrana é crucial para o desenvolvimento da lesão celular letal, e o cálcio é um mediador importante das alterações bioquímicas e morfológicas que levam á morte celular. Padrões de Lesão Celular Reversível - MO • Tumefação celular e Degeneração gordurosa. • A tumefação celular aparece sempre que as células são incapazes de manter a homeostase iônica e hídrica. • Degeneração Gordurosa ocorre na lesão hipóxiae em várias formas de lesão tóxica ou metabólica. Manifesta-se pelo aparecimento de vacúolos lipídicos pequenos ou grandes no citoplasma. Morfologia • Ao exame microscópio, pode-se ver pequenos vacúolos claros dentro do citoplasma - alteração hidrópica ou degeneração vacuolar. • A tumefação celular é reversível. • Alterações ultra-estruturais: alteração da membrana plasmática ( formação de bolhas,distorçaõ das microvilosidades, criação de figuras mielínicas, afrouxamento das fixações intercelulares ), alterações mitocondriais (tumefação) , dilatação do RE, alterações nucleares. LESÃO DE ISQUEMIA/REPERFUSÃO • A restauração do fluxo sangüíneo para tecidos isquêmicos permite a restauração das células caso elas tenham sofrido lesão reversível, ou não afeta o prognóstico caso já tenha ocorrida lesão celular irreversível. • De acordo, com a intensidade e duração do insulto isquêmico, números variáveis de células podem continuar a morrer após a recuperação do fluxo sangüíneo, por necrose ou por apoptose. •A lesão de isquemia/reperfusão é um processo clinicamente importante em distúrbios como infarto do miocárdio e acidente vascular cerebral, podendo ser acessível a intervenções terapeuticas. Como a lesão de Reperfusão Ocorre? • Várias células isquêmicas estão estruturalmente intactas, isto é, ainda não estão necróticas, mas bioquimicamente comprometidas e perdem a integridade durante a reperfusão. • Novos processos lesivos são desencadeados durante a reperfusão, causando a morte de células que, de outro modo, poderiam ter se recuperado: Mecanismos: • Uma lesão nova pode ser desencadeada durante a reoxigenação por aumento da geração de radicais livres de oxigênio por células parenquimatosas e endoteliais e leucócitos infiltrantes. • As espécies reativas de oxigênio podem promover a transição da permeabilidade mitocondrial. • A lesão isquêmica está associada á produção de citocinas e ao aumento da expressão de moléculas de aderência por células parenquimatosas e endoteliais hipóxicas. Lesão Celular Induzida por Radicais Livres: • São espécies químicas que possuem um único elétron não-pareado em órbita externa. • A energia criada por essa configuração instável é liberada através de reações com moléculas, como substâncias químicas inorgânicas ou orgânicas proteínas, lipídios e carboidratos.-particularmente com moléculas essenciais das membranas e ac. Nucleicos. • RL desencadeiam reações autocatalíticas através das quais as moléculas que reagem com eles são convertidas em radicais livres e propagam a cadeia de lesão. Os RL podem ser desencadeados dentro das células por: • Absorção de energia radiante (p.ex., luz ultravioleta, raios X). • Metabolismo enzimático de substância químicas exógenas ou drogas ( p.ex., tetracloreto de carbono), • Reações de redução-oxidação que ocorrem durante processos metabólicos normais. Efeitos dessas espécies reativas: • Peroxidação lipídica das membranas, • Modificação oxidativa das proteínas, • Lesões do DNA. Inativação dos RL • Antioxidantes ( vit. Lipossolúveis E e A, ac. Ascórbico.) • Enzimas ( catalase, superóxido-dismutases, glutationa-peroxidase). •Substância química - metabólitos tóxicos reativos - atuam sobre células-alvo. Essa modificação costuma ser realizada pelas oxidases de função mista do citocromo P-450 no retículo Endoplasmático liso do fígado. •Embora esses metabólitos possam causar lesão da membrana e lesão celular por ligação covalente direta á proteína e lipídios da membrana, o mecanismo mais importante de lesão da membrana envolve a formação de radicais livres reativos e subseqüente oxidação lipídica. MORTE CELULAR CCL4 Conversão pelo P-450 no Ret. End. CCL3 Liso - metabólito tóxico e reativo. Aumento da permea. MP Influxo de cálcio Auto-oxidação Tumefação progressiva Ac. Graxos poliênicos presentes dentro dos LESÃO MIT. Esteatose Hepática fosfolipídios da membrana - decomposição oxidativa do lipídio é iniciada. Peróxido orgânicos são formados após reagirem c/ oxigênio - peroxidação lipídica (autocatalítico) •A exportação de lipídios dos hepatócitos é reduzida devido á incapacidade de sintetizar apoproteínas para formar complexos com triglicerídios, o que facilita a secreção de Lipoproteínas. •A Necrose refere-se a um espectro de alterações morfológicas que sucedem a morte celular no tecido vivo, em grande parte resultantes da ação degradativa progressiva de enzimas sobre a célula letalmente lesada. É o correlato macroscópico e histológico da morte celular que ocorre no contexto de uma lesão exógena irreversível. •Sua manifestação mais comum é necrose de coagulação, caracterizada por desnaturação das proteínas citoplasmáticas, degradação das organelas celulares e tumefação celular. Morfologia • A aparência morfológica da necrose resulta de dois processos essencialmente concomitantes: 1. Digestão enzimática da célula e 2. Desnaturação de proteínas. • As enzimas catalíticas provêm dos lisossomas das próprias células mortas digestão enzimática - autólise. Quando provêm dos lisossomas de leucócitos imigrantes - heterólise. Morfologia da Necrose • • • • • • Células necróticas mostram eosinofilia aumentada, Célula com aparência homogênea mais vítrea, Citoplasma vacuolizado e parece roído por traças. Calcificação das células mortas. Núcleo: a basofilia pode esmaecer ( cariólise), picnose- retração nuclear e aumento da basofilia, cariorrexe - o núcleo sofre fragmentação. Tipos de Necrose (Padrões Morfológicos) • • • • • • • • Coagulação, Liquefação, Caseosa, Gordurosa, Gomosa, Hemorrágica, Fibrinóide, Gangrenosa. Necrose de Coagulação • Quando a desnaturação é o padrão primário. • Tipo mais comum. • Representam necroses observadas nos infartos, como aqueles que ocorrem no coração, rim e baço e nos tumores de crescimento rápido, queimaduras e nas lesões produzidas por ácidos e bases fortes. • MO ( preservação do contorno básico da célula, acidofilia do citoplasma, picnose, cariorrexe, cariólise. Infarto Renal – Necrose de Coagulação. Infarto do Miocárdio Necrose de Coagulação Necrose de Coagulação Miocárdio Necrose de Liquefação • É típica de infecções bacterianas focais. • A morte hipóxica de células dentro do SNC é por necrose liquefativa. • Digestão( enzimas hidrolíticas) de células mortas e a transformação do tecido em uma massa viscosa líquida. Cérebro – Necrose Liqüefativa Infarto do Miocárdio Necrose Caseosa • É uma forma distintiva de NC, é encontada com maior freqüência em focos de infecção tuberculosa. • O termo caseoso origina-se da aparência macroscópica(branco e semelhante a queijo) da área de necrose. • Ao exame microscópico, o foco necrótico aparece como detrítos granulares amorfos compostos de células fragmentadas e coaguladas dentro de uma borda inflamatória nítida - reação granulomatosa. Necrose Caseosa Tuberculose – Necrose Pulmonar Necrose Caseosa Necrose Gordurosa • Esteatonecrose - ocorre no tecido adiposo. • É o resultado da ação lítica de enzimas pancreáticas(necrose gordurosa enzimática), ou como conseqüência da agressão mecânica traumática no tecido gorduroso(N. gordurosa taumática.) • Macroscópica - pingos de velas ou depósito de giz branco sobre o tecido adiposo. • Microscópico - focos com contornos sombredos de adipócitos necróticos, circundados por uma reação inflamatória. Necrose Gordurosa Necrose Gordurosa no Pâncreas Necrose Gordurosa Necrose Hemorrágica • Predomina no local necrótico uma grande quantidade de sangue. Necróse Gomosa • Rara, tipo de n. coagulação • Encontrado na sífilis tardia ou terciária e na sífilis congênita - goma sifilítica, • A área necrótica apresenta-se compacta, uniforma e elástica, como uma goma, isto é, uma borracha, ou mais raramente fluida viscosa como a goma arábica. Necrose fibrinóide • Pode acontecer nas paredes dos vasos nos casos de hipertensão arterial malígna, na poliartrite nodosa e no lupus eritematoso. • A necrose é representada por alteração granular, eosinofílica da parede vascular. • Histologicamente: demonstra-se fibrina na parede. Necrose fibrinóide Necrose Gangrenosa • Gangrena é um tipo de n. considerada uma evolução de uma n. de coagulação(isquêmica). • São necroses que ocorrem sempre ás custas do somatório de dois fenômenos anatomopatológicos: isquemia e liquefação ás custas de bactérias e leucócitos ( putrefação do tec. Necrótico). GANGRENA É NECROSE QUE SOFREU AÇÃO DO AR OU DE BACTÉRIAS Necrose Gangrenosa APOPTOSE “ Cair fora”. “Cair das Folhas” Apoptose APOPTOSE • Reconhecida em 1972 - morfologia distintiva. (Australiano-John Kerr) • È uma forma de morte celular destinada a elimunar células do hospedeiro indesejáveis através da ativação de uma série coordenada e programada internamente de eventos executados por um conjunto exclusivo de produtos gênicos. • Autodestruição ativa de células, espontâneo, como se as células cometessem suicídio, uma vez, que sua função não é mais necessária. Importância da Morte Celular Programada no desenvolvimento de anfíbios Aumento do hormônio tiroxina dispara a apoptose Exemplos da importância da Morte Celular Programada no desenvolvimento embrionário em mamíferos Ocorrência: • Durante o desenvolvimento. • Como um mecanismo homeostático para manter as populações celulares nos tecidos. • Como um mecanismo de defesa, como nas reações imunes. • Quando as células são lesadas por uma doença, ou agentes nocivos. • No envelhecimento. A apoptose é responsável por numerosos eventos fisiológicos, adaptativos e patológicos: Uma característica marcante é que a apoptose é “silenciosa” . Não há, como na necrose, o “alvoroço” da inflamação. As células apoptóticas – Macrófagos =ingeridas antes da sua desintegração. Isso evita o derrame do conteúdo celular, não havendo inflamação e lesão de tecido, garantindo o seu funcionamento normal. APOPTOSE FISIOLÓGICA • A destruição programada de células durante a embriogênese. • Involução dependente de hormônio no adulto, como a degradação de células endometriais durante o ciclo menstrual, atresia folicular ovariana na menopausa, a regressão da mama lactante após o desmame e a atrofia prostática após a castração. • Deleção celular em populações de células em proliferação, como nos epitélios das criptas intestinais. • Morte celular em tumores, em tumores em regressão, e de crescimento celular ativo. APOPTOSE FISIOLÓGICA • Morte das células do hospedeiro que já cumpriram seu propósito, tais como os neutrófilos, na resposta inflamatória aguda, e os linfócitos ao final da resposta imunológica. • Eliminação de linfócitos auto-reativos potencialmente danosos. • Morte celular induzida pelas células T citotóxicas: elimina células infectadas com vírus ou células neoplásicas e também é responsável pela rejeição celular dos transplantes. Apoptose Patológica • Morte celular produzida por vários estímulos • • • • nocivos: lesão do DNA pela radiação, drogas citotóxicas anticancerosas. Lesão celular em certas doenças viróticas, como a hepatite viral. A atrofia patológica dos órgãos parênquimatosos após obstrução ductal, como ocorre no pâncreas, na parótida e nos rins. A morte celular nos tumores (regressão) e em tumores em crescimento. Estímulos nocivos que causam aumento da permeabilidade mitocondrial. Morfologia - Apoptose • Retração Celular - a célula exibe um tamanho menor, o citoplasma é denso, as organelas mais compactadas. • Condensação da Cromatina - característica mais marcante. A cromatina agrega-se na periferia, sob a membrana nuclear, em massas densas de forma e tamanhos diversos. O núcleo pode romper-se, produzindo dois ou mais fragmentos. Morfologia - Apoptose • Formação de Bolhas Citoplasmáticas e Corpúsculos Apoptóticos. • Fagocitose das células ou corpúsculos apoptóticos. Características Bioquímicas da Apoptose • Degradação de Proteínas • Decomposição do DNA • Reconhecimento Fagocitário. DEGRADAÇÃO DE PROTEÍNAS • É a hidrólise de proteínas envolvendo a ativação de varios membros de uma família de cisteínoproteases chamadas de caspases. • Células normais pré-enzimas inativas – ativadas – apoptose: • As caspases ativas clivam proteínas celulares vitais – as lamininas – destruindo a estrutura nuclear e citoesqueleto; as DNases (degradam o DNA nuclear) DECOMPOSIÇÃO DO DNA • Decomposição característica do DNA em grandes pedaços de 50 a 300 quilobases; • Ocorre clivagem internucleossomal do DNA em oligonucleossomos , em múltiplos de 180 a 200 pares de bases, por endonuleases dependentes de Ca+2 e Mg+2. RECONHECIMENTO FAGOCITÁRIO • As células apoptóticas expressam a FOSFATIDILSERINA na camada mais externas de suas membranas. • TROMBOSPONDINA – glicoproteína adesiva – opsonizam – fagocitadas. • Fagocitose sem liberação de componentes celulares que induzem a inflamação… Apoptose • Certas PROTEASES, chamadas de CASPASES(nome derivado da cisteína-protease que cliva) têm papel central na apoptose. • A família já tem + 14 integrantes. • Ao ser ativada, uma caspase iniciadora(2,8,9e 10) cliva outras, em sequência , até gerar uma caspase executora (3,6 e 7). Esta destroi proteínas essenciais á célula, ativa proteínas tóxicas ou destroi proteínas que protegem a célula da apoptose. • Genes: Bcl-2 protege as células de morte(antiapoptótico) . P53 desencadeia a apoptose. Apoptose Insuficiente • Câncer :câncer de mama, linfomas, carcinomas, câncer de ovário e câncer de próstata. • Doenças auto-imunes: LES, • Infecções viróticas: herpesvírus, adenovírus, poxvírus Apoptose Excessiva • AIDS • Doenças Neurodegenerativas: Parkinson, Alzheimer • Lesões Isquêmicas: infarto do miocárdio, AVC • Doenças do fígado induzidas por toxinas: Álcool. A via extrínseca da apoptose é mediada pelos chamados “receptores de morte” os quais encontram-se nas superfícies celulares, transmitindo um sinal de morte para o interior da célula. Receptores de morte incluem o gene da superfamília de receptores para o fator de necrose tumoral (RTNF), incluindo RTNF-1, Fas (CD95), DR-4 e DR-5 (receptores TRAIL). (Ashkenazi, 2002). Todos os membros da família do RTNF consistem em cisteínas ricas em domínios extracelulares, com substancial especificidade, resultando na trimerização e ativação dos seus respectivos receptores de morte. Subseqüentemente o sinal é transduzido para o interior do citoplasma sendo reconhecido pelo domínio de morte do receptor (DD). Moléculas adaptadores do tipo FADD ou TRADD possuem DDs os quais recrutam e ativam os complexos indutores dos domínios de morte, reconhecidos como DISC. Em adição aos DDs, os adaptadores FADD contém os domínios efetores de morte (DED), os quais interagem formando um complexo DED-DED seqüestrando pró-caspases 8 para o complexo DISC. (Scaffidi, 1998). •A via intrínseca de apoptose envolve a ativação da prócaspase 9 a qual é ativada por eventos de transição da permeabilidade mitocondrial (TPM) , com liberação de citocromo c para o meio intracitoplasmático. • Neste casos de ativação da caspase 9, há interação com o fator de ativação das proteases pró-apoptóticas 1 (Apaf-1). •Uma vez ativada, a caspase 9 ativa uma série de outras prócaspases como por exemplo a caspase 3, 6 e 7 subseqüentemente, clivando estas pró-caspases em substratos menores, resultando numa amplificação do sinal de morte. • Neste momento poderíamos observar alterações bioquímicas e morfológicas nas células, agora, em apoptose. (Earnshaw, 1999). O mecanismo celular da apoptose é marcado por alterações na permeabilidade celular (transição da permeabilidade mitocondrial) – TPM – onde há formação de um canal de alta condutância com perca do potencial para fosforilação oxidativa; há extravasamento de citocromo c para o meio intracitoplasmático; ativação de uma série de substâncias serino-proteases como caspases (realizam clivagem protéica), transglutaminases (entrecruzamento de proteínas), endonucleases (clivagem nuclear) e fosfatidilserina / trombospondina (marcadores da membrana externa dos corpúsculos apoptóticos com indução da fagocitose). O processo implica na fragmentação da cromatina e das organelas com posterior clivagem das mesmas. Corpúsculos apoptóticos são fagocitados por macrófagos, que reconhecem suas sinalizações. O sistema imunológico não desencadeia uma resposta inflamatória, não havendo lesão de células periféricas (Damiani D, 2004).
Baixar