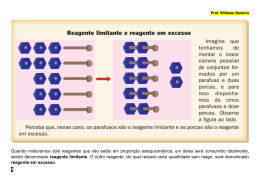
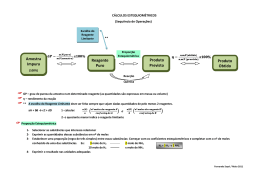
Departamento de Matemática e Ciências Experimentais Curso de Educação e Formação Tipo 6 Nível 3 Actividade Prática de Sala de Aula n.º 09 Assunto: Reagente limitante e reagente em excesso __________________________________________________________________________________________ 1. Classifique cada uma das proposições seguintes de verdadeira (V) ou falsa (F). Numa reacção química o reagente limitante... (A) ... é aquele que existe em menor quantidade química. (B) ... é aquele que existe em menor massa. (C) ... é aquele que existe em menor quantidade em relação à estequiometria. (D) … não existe se os reagentes se encontrarem nas proporções estequiométricas. 2. Durante muitos anos utilizou-se a combustão de magnésio como fonte de luz para fotografia; observava-se uma luz branca muito intensa que "feria" os olhos quando se olhava directamente, e era visível a deposição de um pó branco na lâmpada, como produto da combustão. 2.1. Traduza esta reacção pela respectiva equação química. 2.2. Para cada fotografia era necessário utilizar uma amostra de 2,0 g de magnésio e um volume de 3 O2 de 1000 cm (CNPT). Justifique qual dos reagentes é o limitante. -2 2.3. Determine a quantidade de produto formado. (8,2 x 10 mol MgO) 3. Fizeram-se reagir 3,00 g de alumínio puro com 200 mL de ácido sulfúrico (H2SO4), de concentração -3 0,50 mol dm , para obter sulfato de alumínio e hidrogénio. A equação que traduz a reacção é: 2 Al (s) + 3 H2SO4 (aq) Al2 (SO4)3 (aq) + 3 H2 (g) 3.1. Qual é o reagente limitante? 3 3.2. Que volume de hidrogénio se obteve, em condições PTN? (2,24 dm ) 3.3. Determine a massa de reagente em excesso que ficou por reagir. (1,19 g) 3 -3 4. Numa reacção utilizaram-se 4,90 g de ácido sulfúrico e 150 cm de uma solução 0,50 mol dm em hidróxido de sódio. A equação química que traduz a reacção é: H2SO4 (aq) + 2 NaHO (aq) Na2SO4 (aq) + 2 H2O (l) 4.1. Qual dos reagentes é o limitante? 4.2. Que quantidade de sal se formou nesta reacção? -2 (3,75 x 10 mol Na2SO4) 5. A redução do óxido de crómio pelo alumínio processa-se segundo a equação química: 2 Al (s) + Cr2O3 (s) Al2O3 (s) + 2 Cr (s) Misturaram-se 6,0 g de alumínio com 8,0 g de óxido de crómio. 5.1. Qual é o reagente em excesso? 5.2. Que massa de crómio se obteve? 5.3. Determine a quantidade de reagente que ficou por reagir. (5,47 g) (0,117 mol) Prof. Luís Perna
Baixar