UNIVERSIDADE FEDERAL DE SANTA CATARINA
CENTRO DE CIÊNCIAS FÍSICAS E MATEMATICAS
DEPARTAMENTO DE QUÍMICA
CURSO DE PÓS-GRADUAÇÃO EM QUÍMICA
A
ESTUDO DE COMPLEXOS METÁLICOS UTILIZANDO LIGANTES
MACROCÍCLICOS DERIVADOS DO mes0-5,5,7,1_£§¿p,_1I2,14»-
HEXAIVIETIL-1,4,8,11-TETRAAZACICLOTETRADVECANO
Marco Aurélio Guedes
Dissertação apresentada ao
'
Programa de Pós-Graduação
em Química da
Universidade Federal de Santa Catarina
como
dO
título
de ›Mestre
Florianópolis
2002
requisito parcial para Obtenção
em Química Inorgânica
Marco Aurélio Guedes
EsTUDo DE coM1=LExos METÁL1cos UTILIZANDO L1GANTEs
MACRocÍcLIcos DERIVADOS Do meso-5,5,7,12,12,14-HExAMETIL1,4,8,11-TE'rRAAzAcIcLoTETRADEcANo
Esta dissertação foi julgada e aprovada em sua forma final pelo orientador e
demais membros da banca examinadora para a obtenção do título de Mestre em
Química, especialidade Química Inorgânica.
,
BANCA EXAMINADORA
`)/'U1/v0/ršíaø
/ Prof. Dr. Bruno
/i
Prof. Dr”.
a
/
rof.
~[
Dr. Valdir Soldi
(Coordenador do Curso)
au/\,fc;2.
zpo
icz (Orientador)
Tereza Cristina Rozone de Souza
(Co-orientadora)
p
š
`
Prof”.
.A
×
A
P
Prof. Dr.
*szfõ-Ú
f.
Dr. Valfredo Tadeu e
Vanêãlei
gei
Florianópolis, 22 de fevereiro de 2002.
iii
mw
DÊ. Inês Maria Costa Brighente
VL?
F ávere
Machado (UNISUL)
aos nzeaspaís Franóism
e
à namorada
e
Vanda
.S`z`r/a"na'z`a_,
min/Ja eterna gratz'a'ão...
AGRADECIMENTOS
Ao CNPq pelo apoio financeiro;
À Universidade Federal de Santa Catarina pelo acolhimento;
Aos
A
funcionários da Biblioteca Setorial pelos serviços prestados;
todos os colegas do Departamento de Química, pelo convívio e
conhecimentos compartilhados;
_/los
professores
do Departamento de Quírnica que, dashmai-5
formas, contribuiram para a minha formação;
Ao
orientador Prof. Dr.
Bruno Szpoganicz
V
e ã co-orientadora Prof. Dra
Tereza Cristina Rozone de Souza pela colaboração
acadêmica;
Aos
diversas
com minha formação
~
funcionários da Coordenadoria
do Programa, Graça
e jadir, pela
amizade, eficiência e dúvidas esclarecidas;
Aos
principais colegas dos laboratórios
convivência e
momentos de
descontração;
iv
QMC
313 e
QMC
311 pela
Aos
professores Dr. César_Zucco, Dr. Norberto Sanches Gonçalves e Dr.
Eduardo
Stadler* pela riqueza de seus ensinamentos ao longo da
minha
vida acadêmica;
Aos amigos de
*
laboratórios diversos: Amarildo, Atche, Davi,
.
~
.A
Aqueles que de
uma forma ou
`
.
in
t
de outra contribuíram para a concretizaçao
deste trabalho.
'
e
.
Mellatie pelas discussoes e expenencias compartilhadas;
.
Marcos
_
memoriam
\Í
'Í/1
eiëncíafiefz de nós deuƒeƒ antes
de
memzo
merecemos ser homem
H
jean.Rostand
vi
RESUMO
A
estrutura
do
cristalina
tetraazamacrocíclico
ligante
1,8-bis(2-
cianoetil)-5,5,7,12,12,14,-hexametil-1,4,8,11-tetraazaciclotetradecano
determinada.
plana
em
coordenar
O
uma
ligante possui
aos
relação
seis
geometria aproximadamente quadrada
nitrogênios do esqueleto macrocíclico,
com íons metálicos em posições
podendo
adicionais devido à presença de
(-CHZCHZCN), formando
dois braços pendentes cianoetil
foi
anéis quelatos de
átomos.
Este ligante foi utilizado
novo
o
ligante,
como ponto de
partida para sintetizar
um
5,5,7,12,12,1 4-hexametil-1,4,8,11-
ácido
tetraazaciclotetradecano-1,8-dipropiônico (L3), que teve suas constantes de
protonaçãéíc determinadas:
I-IML
Km =
Os
+ H*
= HnL, onde
_..ll1Ír.Ll__
[HM] lH+l
valores encontrados para os logaritmos
protonação
são
11,6ÍO,1,
8,5ói'0,01,
das constantes de
3,78Í0,01
e
2,11Í0,01,
respectivamente.
O ligante apresenta a constante de formação do complexo com o íon
cobre
(II)
elevada, preclorninando o
espécies protonadas
A
síntese
complexo normal
em
p[H]>6,00, e
em p[H]<6,00.
de
outro
novo
ligante,
o
1,8-bis(3-hidroxipropil)-
5,7,7,12,14,14-hexameúl-1,4,8,11-tetraazaciclotetradecano
é
descrita.
Com este ligante pretende-se aumentar a seletividade a metais “duros”. Este
foi sintetizado
adicionando-se dois braços pendentes' de hidroxipropil ao
ligante mero-5,5,7,12,12,1 4,-hexametil-1,4,8,11-tetraazaciclotetradecano
vii
ABSTRACT
The
crystal structure
of the tetraazamacrocyclic ligand
1,8-bis(2-
cyanoethyl)-5,5,7,12,1 2,14,-hexamethyl-1 ,4,8,1 1 -tetraazacyclotetradecane
(LZ)
was determined. The ligand has
a square-planar geometry in relation to
the nitrogen atoms of the rnacrocyclic skeleton,
making possible coordinate
with ions of metals in additional positions due to the presence of two
of
pending arms cyanoethyl (-CHZCHZCN), forming chelate
atoms.
six
'
_
This ligand was used as starting material to synthesize a
new
ligand,
5,5,7,12,12,14-hexamethyl-1 ,4,8,11-tetraazacyclotetradecane-1,8-
the
dipropionic acid
(L3), that
l-IML
1<`¬1
+ H+
had it is prottmation constants determined:
= HUL, where
=
mn-1][H+]
The
/og
i
A
values found for the protonation constants are 11,6iO,1,
8,5óÍ0,01, 3,78Í0,01 and 2,11Í0,01, respeciively.
The
(II)
ligand
ion, prevailing the
shows
normal cornpound
species in p[H]<6,00._
The
synthesis
a high formation constant With the copper
in p[_H]>6,()O,
_
of another
ligand,
the
1,8-bis(3-hidro›:ypropyl)-
5,7,7,12,1 4,14-hexamethyl-1,4,8,1 1 -tetraazacyclotetradecane
described.
With
and protonated
this ligand it is
"hard" metal ions. This
is
(L4)
intend to increase the seletivity toward
compound was
synthesized by adding
two
hydroxypropyl arms to the ligand mesa-5,5,7,12,12,14,-hexamethyl-1,4,8,11`
tetraazacicotetradecane
,
viii
ÍNDICE GERAL
Resumo
........................................................................................................................... _.
Abstract..... .....................................................................................................................
..
vii
viii
Lista de figuras ..............................................................................................................
Lista de tabelas ........................................................................................................... xiv
..
Lista de reduções ........................................................................................................ xv
..
1
INTRODUÇÃO
2
OBJETIVOS
2.1
4
01
............................................................................................................. ..
os
Objetivos Gerais ..................................................................................................... O3
..
2.2 Objetivos
~
3
...................................................................................................... _.
Específicos ................
..........................................................................
REVISAO DE LITERATURA
PARTE EXPERIMENTAL
4.1
........................................................................
..
..
............................................................................. ..
O3
04
12
Reagentes .................................................................................................................. 12
..
4.2 Instrumentação
4.3 Síntese
4.3.1
.......................................................................................................
._
12
dos ligantes ................................................................................................. 16
_.
do
Síntese
lígante
macfodclico
5,7,7,12,14,14-hexametil-1,4,8,11-
diperclorato
tetraazacíclotetradeca-4,11-díeno
-
(5,7,7,12,14,14-
Me(,[14] -4,1 1 -dieno-1 ,4,8,1 1 -N 4.21-ICIO 4) .................................................. .. 16
4.3.2
Alem
e
m:e”mz`m'~ (5, 5, 7, 12, 12,
tetraazaciclotetradecano)
1,4,s,11-N¬..><H,O)
4.3.3 Separação
hidratado
14
-
-
hexametil
Síntese
11
............................................................................................
dos isômeros mesa
do
1, 4, 8,
ligante
-
(5,5,7,12,12,14-Me6[14]ano._
17
e racëmzko-(5,5,7,12,12,14-hexametík
1,4,8,1 1 -tetraazaciclotetradecano) díhidratado
4.3.4
-
macrocíclico
.......................................... ..
19
1,8-bís(2-cianoetil)-5,7,7,12,14,14-
hexametil-1,4,8,11-tetraazaciclotetxadecano (L) ...................................... .. 20
IX
4.3.5
do
Síntese
ligante
macrocíclico
ácido
5,5,7,12,12,14-hexametil-
1,4,8,1 1 -tetraazaciclotetradecano-1,8-dipropiônico (L3) ................... ..21
4.3.6 Síntese
'
do
ligante macrocíclico 1,8-biS(3-hidroxipropil)-5,7,7,12,14,14-
hexametil-1,4,8,11-tetraazaciclotetradecano (L4) ................................ ..22
4.4 Síntese dos
complexos .......................................................................................... 23
_.
4.4.1 Síntese
do Complexo Ni-Ll ............................................................................. 23
4.4.2 Síntese
do Complexo Cu-L1 ............................................................................. 24
4.4.3 Síntese
do Complexo Ni-L2
4.4.4 Síntese
do Complexo Cu-L2 .................................................................... ..25
4.4.5 Síntese
do Complexo Cd-Lg ............................................................................. 26
5
..
..
........................................................................
LI
-
......................................................................
..........................................................................
-
......................
Espectroscopia vibracional dos ligantes ............................................
5.4 Espectroscopia Vibracional
5.5 Titulação potenciométrica
5.6 Titulação
30
.....
..31
..33
dos complexos .............................................. ..37
do
ligante L3 ................................................... ..41
potenciométrica do sistema Cu(ID-L3 ..................................... ..46
6
coNcLUSÕES E PERSPECTIVAS
7
BIBLIOGRAFIA
ANEXO
..
1,8-BiS(2-cianoetil)-5,7,7,12,14,14-hexametil-1,4,8,11-
tetzraazaciclotettadecano .................................................
8
27
[l\/le6(14-ano)N4].2H2O .................................................................... ..3O
5.2.2
5.3
..
dos ligantes e complexos .............................................................. ..27
5.2 Cristalografia ..................................
5.2.1
24
..
RESULTADOS E D1ScUSSÃo
5.1 Sínteses
..
......................................................
.52
.................................................................................................... ..
.......................................................................................................
X
..-
......
54
..62
LISTA DE FIGURAS
Figura 1 - Estrutura
terciáría
Figura 2 - Fórmula
estrutural
Figura 3 - Fórmula
R
da hemoglobina .............................................. ..O2
do ligante
estrutural
do
1,4,7-tríazaciclononano ............. ..O4
ligante tetrakis(2-cianoetíl)-1,4,8,11-
tetraazaciclotetradecano ................................................................ ..O5
Figura 4 - Representação para a síntese do
a
1,4,8,11-tetraazaciclotetradecano
ligante 1,8-carboximeti1partir
do seu derivado
1,4,8,11-tetraazaciclotetradecano (cyclarn) ................................. ..O6
_
Figura 5
_-
Configurações
trans-I,
tram'-ll
e
tram-Ill
para 0 lígante
1 ,4,8,11 -tetraazacíclotetradecano
tetraazamacrocíclíco
(cyclam) ............................................................................................. ..O7
Figura 6 - Rota
sintética
do
ligante tetraazarnacrocíclico ácido 1,4,7,10-
tetraazaciclododecano-1,7-díacétíco ............................................ ..O9
Figura 7
1-
Fórmula
estrutural da D-penicilamina,
do 2,3-dimercapto-L
propanol (BAL) e trietilenotetrarnina (TRIEN) ........................ ..1O
A
Figura 8 - Representação esquernátíca da
célula termostatizada utilizada
nas titulações potencgnétrícas ...................................................... ..13
Figura 9 - Representação para a
-
síntese
do
lígante
macrocíclico
5,7,7,12,14,14-Me6[14]-4,11-díeno-1,4,8,11-N4.2HClO4 .......... ..17
Figura 10 - Representação para a
síntese
dos ligantes macrocíclicos meso-
5,5,7,12,12,14-Meó[14]ano-1,4,8,11-N4.xH¿O e seu respectivo
racemato ..........................................................................
Figura 11 - Representação para a
síntese
do
............... ..1
8
ligante 1,8-bísâf2icíanoetil)-
5,7,7,12,14,14-hexametíl-1,4,8,1 1-tetraazacíclotetradecano ..... ..21
Xl
Figura 12 - Representação para a
do
síntese
ligante ácido 5,5,7,12,12,14-
hexarnetil-1,4,8,1 1 -tetraazaciclotetradecano-1,-8-dipropiônico
E
(L3) .................................................................................................... ..22
Figura
-
1.3
Representação
para
a
síntese
do
ligante
1,8-bis (3-
hidroxipropil)-5,7,7,1 2,14,14-hexametil-1,4,8,11 -
tetraazaciclotetradecano (L4) ......................................................... ..23
Figura 14 - Exemplo de adição de Michael .................................................. ..28
O,O15mol.L`1.
UV de uma solução de EDTA 2
Espectro de absorção no UV de uma solução
z
......................................
Figura 15 ›-
(a)
Espectro de absorção no
E
de L,
t
0,01 m<›1.L~1 ................
17
..29
..31
ORTEP do ligante [Me6(14-ano)N4].2H2O
- Diagrarna ORTEP do ligante 1,8-bis(2-cianoetil)-
Figura 16 - Diagrama
Figura
.............
...........
5,'/,7,1 2,14,1 4-hexametil-1 ,4,8,1
1-tetraazaciclotetradecano ..... ..32
Figura 18 - Espectro de infravermelho do
em pastilhade
ligante [Me6(14p-ano)N4].2H2O
KB1: ......................................................................... ..33
Figura 19 - Espectro de infravermelho do
ligante 1,8-Bis(2-cianoe_til)-
em
5,7,7,1 2,1 4,1 4-hexametil-1 ,4,8,1 1 -tetraazaciclotetradecano,
pastilha de
KBr
...... ..'. .............................................................. .; ......
Figura 20 - Espectro de infravermelho do
..34
ligante acido 5,5,7,12,12,14-
hexametil-1 ,4,8,1 1 -tetraazaciclotetradecano-1 ,8-dipropiônico,
em pastilha de KBr
................
Figura 21 - Espectro de infraverrnelho .do
ligante 1,8-bis(3-hidroxipropil)-
5,7,7,12,14,14-hexametil-1,4,8,11-tetraazaciclotetradecano
em pastilha de KBr
Figura 22
-(a)
..35
.......................................................
-› L4
..37
.........................................................................
Espectro de infravermelho do complexo (Cu(lI)-L]) e
(Ni(lI)-Li),
em pastilha de KB:
....................................................
Figura 23 - Espectro de infravermelho do complexo
pastilha de
KBr
(Ni(Il)-Lg),
...............................................................................
xii
..38
em
..39
Figura 24
- (a)
Espectro de infravermelho do complexo (Cu(Il)-LZ) e
(Cd(II)-L2),
em pastilha de KBr
Figura 25 - Curva de
titulação
...................................................
..4O
potenciométrica do ligante ácido
5,5,7,1 2,12,14-hexametil-1,4,8,1 1-tetraazaciclotetradecano-1 ,8-
dipropiônico, a
T=
298,15K e ¡.L=O,1M (KNO3); a = mmol de
base adicionada/ mmol de ligante ................................................ ..41
Figura 26 - Curvas de
em
-
distribuição das espécies
em
solução do ligante L3
função da variação de p[H], a T=298,15iO,1K e ¡.L=O,1OO
mol.L`1(KNO3) ...............................................................................
Figura 27
--
em
Etapas de protonação do ligante L3
solução aquosa,
..42
em
função da variação do p[H] ...........................................................
Figura 28 - Fórmulas
estruturais
dos ligantes doda e dota* ...................... ..45
Figura 29 - Ligações' de hidrogênio intrarnoleculares
tetraazamacrocíclico substituído .........
V
Figura 'W230 -- Curvas de
mmol
T
=`
298,15K
e
eligante
....................................... ..46
titulação potenciométrica para os sistemas (a)
L3, a
L¡,e
no
u=O,lOO mol.L`1
de base adicionada/ mmol de
ligante.
Cu”-
(Kl\lO3); a
A
=
proporção
metakligante é 1:1 ........................................................................... ..47
Figura 31 - Curvas de
l
L3
em
distribuição das espécies
formadas no sistema Cu”-
função do p[H] a T=298,2ÍO,1K e u=0,10OmolL`1
(KNO3) ............................................................................................ "48
Figura 32 - Fórmula
estrutural sugerida para
CuH2L formado em
o complexo diprotonado
solução entre o ligante L3 e o íon cobre
(II) ..................................................................................................... ..49
Figura 33
-
Gráfico de variação da estabilidade (Aloglía) de cobre
relativo
dezesseis
aos ligantes macrocíclicos
com
anéis
(II),
de doze a
átomos, contendo quatro átomos de nitrogênio
doadores ...........................................................................................
xiii
..51
LISTA DE TABELAS
Tabela 1 - Rendimento,
solubilidade e análise 'elementar
do ligante L,
Tabela 2 - Rendimento,
solubilidade e análise elementar
do
Tabela 3 -_ Rendimento,
solubilidade e análise elementar dos ligantes L3..22
Tabela 4 - Rendimento,
solubilidade e análise elementar
Tabela
5
- Rendimento,
....
..l9
ligante L2.....21
do .ligante
L4.....23
solubilidade, análise elementar e coloração
do
complexo Ni-LI., ............................................................................ ..24
Tabela 6 - Rendimento,
solubilidade, análise elementar e coloração
do
complexo Cu-LI .............................................................................. ..24
Tabela
7
- Rendimento,
solubilidade, análise elementar e coloração
complexo Ni-Lg ..................................................................
Tabela
8'
- Rendimento,
complexo
sol-šafoilidade,
..........
análise elementar e coloração
do
..25
do
Cu-L3....Â`. ........................................................................ ..25
Tabela 9 - Rendimento,
solubilidade, análise elementar e coloração
do
complexo Cd-L2 .............................................................................. ..26
Tabela 10 - Constantes de protonação
a
298,15K para o
L3,
dota e
doda ..................................................................................................
Tabela
11
-
..45
Constantes de complexação e de protonação a 298K para o
R
cu-L,,
cu-dm
<z
cu-asda ............................................................ ..5o
xiv
LISTA DE REDUÇOES
BAL - 2,3-dimercapto-1-propanol.
Cyclam -
1,4,8,11-tetraazaciclotetradecano.
Cyclen - 1,4,7,10-tetraazaciclododecano.
EDTA - etzilenodiaminotettaacético.
1
HSAB - Teoria dos ácidos e bases duxos e macios.
'
'
LI
- mexo-5,7,7,12,14,14-hexarnetil-1,4,8,11-tetxaazaciclotetradecano.
L¬,_
-
1,8-Bis(2-cianoetil)-5,7,7,12,14,14-hexametil-1,4,8,11-tetraazacic1otetra-
decano.
L3
- acido
5,5,7,12,1 2,14-hexametil-1,4,8,11 -tetraazaciclotetradecano-1 ,8-di-
propiônico.
L4
-
1,8-bis(3-hidroxipropil)-5,7;/,12,14,14-hexametil-1 ,4,8,1 1-tetraazacic1o-
tetradecano.
V
MRI - Imagem de Ressonância Magnética.
TRIEN - trietilenotetramina.
XV
1
1NTRoDUçAo
O
e
entendimento
da
química
dos íons
metálicos
e
ligantes
macrocíclicos possui grande implicação nas áreas de química e bioquímica.
Ligantes macrocíclicos são ligantes polidentados contendo seus átomos
doadores incorporados no
ciclo, e
muitas vezes ligados ao ciclo
como
doadores pendentesl
A
química destes ligantes e de seus complexos metálicos representa
uma
hoje
das maiores subdivisões da química inorgânica, e de contínuo
interesse para o futuro.
f
Um
2
_
_
numero consideravel de macrociclicos
naturais são hoje estudados.
as
propriedades
smteticos
A maioria das pesquisas
eletroquímicas,
espectrais,
bem como
está relacionada
estruturais,
com
cinéticas
e
termodinâmicas da formação dos respectivos compleXos.3
O fato dos
em
complexos de
é reconhecido.
A
como por exemplo, no mecanismo
de
vários sistemas biológicos fundamentais
importância de seus complexos,
fotossíntese,
também
ou no transporte de oxigênio em mamíferos
outros sistemas respiratórios,
para a investigação
como nos
estarem envolvidos
ligantes macrocíclicos
promoveu
da quírnica dos
e ainda
(Figura 1) e
promove uma motivação
íons metálicos nestes sistemas,
sistemas contendo ligantes cíclicos
em geral.
~
bem
Hemez
Heme
Fzgura
7
- Estrutura terciária da hemoglobina,
heme - responsáveis pelo transporte de
destacando-se os grupos
oxigênio
no sangue dos mamíferos
Tal interesse conduziu à síntese .do primeiro composto biomimético
que forma interação
Há
Tc
axial
com o imidazol.4
boas razões para a natureza preferir derivados de ligantes
macrocíclicos
geralmente
para .os
importantes
uma estabilidade
cinética e
ligado ã cavidade
com reações
,
cíclicos.
O
íon metálico é
do macrociclo de maneira a exercer sua
uma ínfima competição
função biológica, existindo
-
termodinâmica adicional é conferida
aos respectivos complexos, pelos ligantes
firmemente
acima mencionados
sistemas
(ou nula), por exemplo,
de desmetalaçãol
A relevância do estudo dos compostos macrocíclicos expandiu-se em
diversas subdivisões,
analíticos,
síntese
como
orgânica,
ambientais e medicinais.
destruição
do
catálise, seletividade
À
HIV
bem como
a íons metálicos,
certas
aplicações
esta última, incluem-se
das
e
2
métodos
industriais,
novas tentativas de
células
cancerosas.5`12
2
oBJETIvos
2.1 Objetivo geral
Sintetizar
caracterizar
e
tetraazamacrocíclicos
com grupos
novos
ligantes
complexos
e
funcionais pendentes.
2.2 Objetivos específicos
Determinar
as
constantes
de
protonação
do
ligante
acido
5,5,7,12,1 2,1 4-hexarnetil-1,4,8,1 1-tetraazaciclotetradecano-1,8-dipropiônico,
caracterizando as espécies formadas
força iônica controlada,
em
em
solução aquosa
com
função da variação do p[H]
temperatura e
com o
auxílio
da
titulação potenciométrica;
Calcular as constantes de formação das espécies complexadas
íon cobre
com o
(II);
Expressar os resultados na forma de curva de distribuição das
espécies
em solução - °/o de espécies versus ~log[H¬`].
3
REVISÃO DE LITERATURA
Por definição,
/-9
cíclico
ligantes macrocíclicos
consistir
compostos por no mínimo nove átomos dos quais
mínimo devem
s
Fzgum 2 - Fórmula
O
em um ligante
três
átomos no
ser doadores de elétrons (Fig-ura 2).2
N N
__,
devem
estrutural
desenvolvimento nas
do
s
ligante 1,4,7'-triazaciclononano
características estruturais e
ligames poliazamacrocíclicos está atualmente relacionado
na
com
síntese
de
a adigào de
grupos doadores pendentes a macrocíclicos nitrogenados.
O
termo macrociclo “doador pendente” é aplicado a
macrocíclico o qual possui
um
ou mais grupos doadores
um
ligados
ligante
em
sua
periferia.
Tal termo provavelmente foi utilizado pela primeira vez na
literatura
química
em
1980.13
O
ligante
o qual
foi aplicado, tetralris(2-
cianoetil)-1,4,8,11-tetraazaciclotetradecano (Figura 3),
não
foi
o primeiro
ligante deste tipo publicado,
o que ocorreu quatro anos mais cedo.”
um
termo formal para o reconhecimento desta
Todavia, o surgimento de
modificação estrutural
também
possui importancia química, influenciou e
influencia o desenvolvimento atual e futuro desta classe de
compostosfs
V
:AÊN
N_
Fágura 3
~
“Q/\_
:N
- Fórmula estrutural do ligante tetrakis(2-cianoetil)-1,4,8,11tetraazaciclotetradecano
Com
o passar dos anos, novos
ligantes macrocíclicos
doadores pendentes foram produzidos para
uma
com
grupos
variedade de diferentes
aplicações químicas. Pode-se citar as simulações de sítios metálicos de
enzirnas
7
li
cão a antico
tv
radionuclídeo a
uma
estabilidade
progressivas
com
3
a
célula alvo, utilização
- MRI
ressonância magnética
com
os
cinética
investigações
(tais
e
como
de
reagente
termodinâmica
mais
n
de
elaboradas
em
sua
relação
ç
tais
compostos para
estas aplicações deve-se ao fato
átomos doadores possivelmente mais
os íons metálicos
iinagem de
bem como
extrema),
que enquanto os átomos doadores que fazem parte do
metal, outros
em
técriicasrequerem complexos de metal
estrutura/atividade.l6`19
A utilização
um
roiosta de trans ortar
sítios
substratos externos, assim
lábeis
de coordenaçao adicionais,
como podem
ciclo
em
imobilizam o
podem perturbar
competiçao
com
ser utilizados para anexarem-se a
determinados pontos de outras moléculaszo
As propriedades de complexação dos
A
poliaza-macrocíclicos,
governadas principalmente pelo tamanho do anel macrocíclico.21
funcionalização destes macrociclos
íons de metálicos
e
a
podem aumentar
estabilidade
A
a sua seletividade a
dos respectivos complexos, que
dependem das propriedades de coordenação dos braços pendentes.22`37
5
são
Uma
conveniente estratégia para sintetizar complexos de metais
altamente estáveis e neutros, os quais são freqüentemente buscados para
aplicação
em
medicina terapêutica e de diagnóstico, tem sido
estabilidade conferida aos
com
compostos poliazamacrocíclicos,
a neutralização da carga
utilizar a alta
em
do íon metálico promovida por
de grupos carboxilatos pendentes
em número
conjunto
um número
suficiente para neutralizar a
carga do íon de`metal. Desta forma, complexos neutros de íons de metais
com o
bivalentes
'ligante
1,4,8,11-tetraazaciclotetradecano (cyclam)
são
formados anexando dois grupos carboximetil (-CHZCOOH) a dois átomos
de nitrogênio (Figura 4).”
ta
Ez/Íízz
cyclam
Fzgura 4
ea
2 BzcH_cooH
,fclšãf
- Representação para a síntese do
1,4,8,11-tetraazaciclotetradecano a partir
ligante 1,8-carboximetil-
do seu derivado
1,4,8,11-
tetraazaciclotetradecano (cyclam).
Normalmente, por
características
de seletividade, estes grupos
carboximetíl são ligados aos átomos de nitrogênio nas posições 1,8 (N',
N”'),
as
quais
possuem vantagem quando o cyclam assume sua
configuração mais estável
trans-III,
onde
6
um carboxilato
é projetado abaixo
do plano do macrocíclico,
e outro carboxilato
~>
21,39
acima do plano (Figura
.-I*
z
H
IMHÍ läflfll
Iflmrl [R$85]
hihi»-lil
5).
"
rf
[Jimi
l
3
W»
v
i
'
J
t
q
l
'z
Vl
Fzgura 5 - Configurações tram*-I, trans-II e tram'-III
(em destaque) para o
ligante tetraazamacrocíclico 1,4,8,11-tetraazaciclotetradecano (cyclam)
Isto permite
induzir
uma
que o complexo assuma
em
tensão de anel excessiva
uma geometria
octaédrica
sem
quaisquer dos anéis quelatos, e
assim maximiza a estabilidade que pode ser provavelmente alcançada para
muitos íons de metais
com
esta
combinação
particular de macrociclo
com
doadores pendentes.
Esta tentativa de gerar complexos neutros possuem a vantagem que
a lipofilicidade
alquilação
do complexo pode
das
aminas
ser
aumentada posteriormente através da
secundárias
carboximetiladasss
7
restantes,
as
quais
não
são
As
menores,
tetraazamacrocíclicos
para
sintéticas
estratégias
seletivamente
bifuncionalizar
como
por
exemplo
o
tetraazaciclododecano (cyclen), foram inexploradas por algum
1,4,7,10-
tempo
e
conseqüentemente a .possibilidade de preparação de complexos neutros
com
íons
de metais bivalentes pela ligação de dois
carboxirnetil a dois
átomos de nitrogênio do macrociclo. Isto
grupamentos
é significante
que complexos originados de
porque freqüentemente demonstra-se
derivados do ligante cyclen tendem a ser mais estáveis que os respectivos
complexos derivados do cyclam, especialmente quando o íon de metal
bivalente possui»
um raio iônico grande.”
_
Porém, recentemente, demonstrou-se que pode ser efetuada a
sulfometilação
seletiva
quantitativo, abrindo
\.'._r.=1
do cyclen nas posições
caminho
viável
átomos de nitrogênio nas posições 4
seja,
em solução aquosa a pH =
grupos sulfonato por grupos
e 10
do
ciclo são
para a obtenção de
Os
impedidos de reagir
eles
são protonados,
Em estudo posterior, substituiu-se os
7.
nítrila
rendimento
na obtenção destes derivados.
porque a síntese é procedida sob condições nas quais
ou
em
1,7
(R-CN), os quais foram hidrolisados
um composto com dois grupos
38,41
carboxílicos (Figura
›
8
6).
NH N
IBN HNH]
QH7
--+›
-
+
2
HocHzso3Nz
Nzso3-/
/
\
l: N
/"_SO3Na
N
Í
`
NI-I
HN
+2 0Hz
/
\
cyclen
gl
ZÍ_\š+-
_
L
O
_
/"\/';iN
INH N]
HQ
oi
L/
[5 +
~N:--/
-
`
OÍO
NaCN
2
Fágura 6 - Rota sintética
do
N HN
\
/
ligante tetraazamacrocíclico ácido 'l,4,7,10-
tetraazaciclododecano-1,7-diacético
No
presente trabalho, demonstra-se outro
com
ligantes
doadores pendentes
adição de Michael, que fornece
o qual
nitrila,
um produto
final
é
método
de síntese de
obtido através de
em
uma
grau de pureza e
alto
excelente rendimento.
O
ligante
obtido,
1,8-bis(2-cianoetil)-5,7,7,12,14,14-hexametil-
l,4,8,11-tetraazaciclotetradecano, teve sua estrutura elucidada na
forma não
complexada, e é material de partida para a síntese do ligante ácido
5,5,7,12,12,14-hexametil-1 ,4,8,1 1-tetraazaciclotetradecano-1,8-dipropiônico,
que teve suas constantes de protonação/desprotonação determinadas por
titulação potenciométrica.
Com
cobre(lI),
este ligante busca-se
como
excesso de cobre
teste inicial para
formar
um
em organismo vivo.
Embora
complexo
estável
possível agente de
com o
remoção do
›
~O excesso de cobre no organismo
\lVilson.
um
está relacionado
com a doença
W/ilson tenha descrito os aspectos clínicos da doença
9
de
em
1911, somente após aproxirnadamente quarenta anos que esta foi associada
ao excesso de cobre no organismoflo
A
doença de W/ilson pode
_
ser
de origem autossômica recessiva,
havendo uma degeneração hepatolenticular associada a anomalias no
metabolismo do cobre com- excreção urinária excessiva e níveis reduzidos
de ceruplasmina no plasma devido à diminuição na “síntese hepática”, além
Com os níveis reduzidos de ceruplasmina,
de aminoacidúria generalizada.
cobre
liga-se
fracamente ã albumina sérica e desta forma é facilmente
transferido para os tecidos,
ode
'
ori
ar cirrose e
nos
havendo deposição anormal, que no fígado
ode levar a uma lesão tubular renal
'rins
moácidos,
ocasionando aumento da excreção urinária de
ocasionalmente
O
BAL,
o
peptídeos e
glicose.42”43
primeiro composto utilizado para tratar a doença era o ligante
o
2,3-dimercapto-1-propanol,
qual
injetado
era
forma
de
intramuscular e era doloroso e desagradável. Este logo foi substituído pela
Embora
D-penicilamina que poderia ser administrada oralmente.
a
D-
penicilamina apresente baixatoxicidade para a maioria das pessoas, alguns
podem
pacientes
desenvolver
uma
alergia depois
tratamento. Outro agente quelante para o qual
indivíduos é a trietilenotetramjna,
de certo tempo de
podem
ser trocados tais
TRIEN, que também
é efetivo para
aumentar a excreção urinária do cobre, mas não tão efetivo quanto a Dpenicilarnina (Figura
CH,
'
H5
40
o
Hz-
H,c.*
7).
O
~
oH
Hs
SH
'
HZN
\ f
\
_'
\
NH,
NI-13-+
›
D-penieflzmúzz
BAL
TRIE-N
Fzgura 7 -› Fórmula estrutural da D-penicilaminá, do 2,3-dimercapto-L
H
`
propanol
e trietilenotetramina
10
(TRIEN)
A
D-penicilamina promove a excreção do cobre na forma de
complexo
estável.
Seu uso provoca hipersensibilidade
em
um
pacientes jque
apresentam reação alérgica à penicilina.
Verifica-se
metal
assim a importância do estudo de quelantes para este
com a finalidade de aprimorar o tratamento de tais intoxicações.44*45
Outro ligante foi obtido com a_ adição de dois grupos funcionais
ao
doadores
tetraazaciclotetradecano.
ligante
V
Os grupos
mesa-5,7,7,12,14,14-hexametil-1,4,8,11¿
adicionados são átomos de oxigênio
neutro na forma de terminais alcoólicos, os quais pretende-se futuramente
avaliar a seletividade e constantes
chumbo
(II),
também
de complexação
com o
íon metálico
responsável por diversos efeitos tóxicos quando
exposto ao organismoihumano.45
11
4
PARTE EXPERIMENTAL
4.1
Reagentes
Nas
sínteses dos ligantes e
complexos foram
utilizados acetona,
etilenodiamina, metanol, hidróxido de sódio e os sais de perclorato dos
metais da marca
EDTA,
Vetec.
Foram
utilizados reagentes
como
a acrilonitrila,
hidróxido de potássio, boroidreto de sódio, óxido de trimetileno,
cloreto de cobre, nitrato de
cádmio
e
o solvente metanol
HPLC/ UV
da
marca Sigma-Aldrich.
Os
solventes etanol, diclorometano e éter
etílico,
o agente dessecante
pentóxido de fósforo, os ácidos clorídrico e perclórico e o
potássio foram adquiridos da Merck.
4.2
sal
brometo de
.
Instrumentação
As
termostatizada e selada (Figura
a temperatura constante
água circulante
atmosfera
foram
titulações potenciométricas
foi
em
em
'sistema
8),
com Volume
25,0-iO,1°C,
um
célula
de 100mL, mantendo
com um banho
termostatizado de
uma
A
fluxo contínuo de argônio, fornecido
com
a passagem
solução de
em›KOH 0,1
pela Vl/hite Martins e purificado
titulação, as soluções
total
em uma
fechado de fabricação da Nlicroquímica.
mantida inerte por
primeiramente através de
realizadas
do
fluxo de gás
mol.L`1.
Durante a
experimentais eram mantidas sob constante agitação
um agitador magnético. O sistema de medidas de pH é
constituído por um eletrodo de referência do tipo Ag/ AgC1 e um eletrodo
indicador de vidro marca lngold, conectados a um potenciômetro digital
com o
auxílio
de
Coming, modelo 350.
O
titulante foi
adicionado
em
alíquotas de
O,10mL
com o
auxílio
de
uma
bureta automática tipo pistão marca
SCHOTT
GERATE.
Entrada de Argôniol
âmmâê
ü¿
Isajda de Argônio
bureta automática
Potenciômetro
Termostatizado
Banho Tennostaii
298K
Fzgum 8 - Representação esquemática da
célula termostatizada
~
utilizada nas titulaçoes potencimétricas
A
atmosfera foi mantida inerte por
fornecido pela White Martins e purificado
primeiramente através de
uma
solução de
titulação, as soluções experimentais
um
fluxo contínuo de argônio,
com a passagem do fluxo de gás
em KOH 0,1 mol.L'1. Durante a
eram mantidas sob constante agitação
um agitador magnético. O sistema de medidas de pH é
constituído por um eletrodo de referência do tipo Ag/AgCl e um eletrodo
indicador de vidro marca Ingold, conectados a um potenciômetro digital
com o
auxílio de
Coming, modelo 350.
com o
auxílio
de
O
uma
titulante foi
adicionado
em
alíquotas de O,10rnL
bureta automática tipo pistão marca
GERATE.
13
SCHOTT
A
do potenciômetro
inclinação da resposta
de soluções-tampão Carlo Erba,
utilização
a resposta
com valores
de
do sistema (pHmetro
e eletrodos),
foi verificada
com a medida do pH
de
solução padrão de ácido clorídrico diluído ([HCl]=0,01018mol.L'1;
mol.L`1/KNO3; pH=1,992),'para obtenção de
intuito de obter
que deveria
A
o Valor de p[H],
um
a diferença entre
Além
com o
o valor observado
com o
aproximadamente
com a adição de KNO3.
mol.L`1,
disso, para
i
-
manter a linearidade na calibração, medida pela
H*
e a
pequena
em
força eletromotriz exercida pelos íons H+, a concentração dos íons
concentração dos íons hidróxido foram limitadas ã
do
relação à concentração
-lo‹r
J'
P ara
ez
faixa de
].L=0,1
`
ser.
em 0,1
uma
fator de correção
força iônica dos experimentos foi mantida
constante
a
pH = 4,00i0,05;
Após o experimento potenciométrico
7,00i:0,05 e 9,00i0,05.
com
foi ajustada
eletrólito.
funçfío
Esta limitação restringiu as medidas de
a faixa de 2,000 a 11,000,
_
PH, a linearidade de
uma
res P osta
sendo
não
(-1
seria
ue acima ou abaixo
'desta
obedecida e os resultados
obtidos seriam duvidosos.
A
solução estoque do nitrato de cobre foi preparada para que
possuisse concentração
do cátion em aproximadamente
concentração foi deterrninada
solução
com
0,01_mol.L'1. Tal
com maior exatidão por titulação
direta desta
solução padrão de ácido etilenodiaminotetraacético
em concentração de 0,01
mol.L`1,
em presença do indicador apropriado.”
A solução padrão de KÔH sem COZ, para uso nos
potenciometria, foi preparada
(EDTA)
com ampolas
de “Diluit
Baker, contendo hidróxido de potássio concentrado
-
experimentos de
It”,
marca
sem CO2,
J.
T.
as quais
em água bidestilada e fervida. Esta solução final foi
padronizada com biftalato acido de potássio e fenolftaleína como indicador,
foram
diluídas
14
foi estocada
KOH
frasco de polietileno e ligada a
um
outro frasco
'(“trap”)
KOH concentrado, para evitar a entrada de CO2 atmosférico.,
contendo
'
em
Os
de
resultados das variações
a adição de alíquotas de
de CO2, obtidos pelas medidas
isento
padrão,
pH com
de titulação
potenciométrica do ligante L3, foram tratados pelo programa BEST7,48
em
baseado
linguagem
FORTRAN,
e
componente em solução, o volume de base
de cada
os milimols
utiliza
e os valores de -log[l-Il] obtidos
para calcular as constantes de protonação.
Os
equilíbrios
envolvendo o
Í
ligante L3 e
o íon cobre
(ll)
também
foram calculados -pelo programa BEST, definindo as espécies determinadas
na etapa
anterior, suas
concentrações e a estimativa
equilíbrio para cada espécie
do complexo em
calculos sucessivos baseados
em um
inicial
solução.
O
da constante de
programautiliza
algoritmo de balanço de massa para
todos os componentes indicados a cada incremento de base adicionada.
As
constantes de equilíbrio são variadas
+
diferenca entre os valores de -lo
_»
assim
uma
relativa
potenciométrico
com
no sentido de minimizar
e os valores ex erimentais 7
aproximação da curva experimental de
a
dando
equilíbrio
a curva teórica calculada a partir da concentração da
espécie individual presente a cada ponto, e a correspondente constante de
equilíbrio para a
A
formação do complexo
e sua protonação.
distribuição das espécies formadas
em
solução,
ç
em
função do
p[H], foi calculada pelo programa SPE,48 que utiliza o resultado do
refinarnento de dados obtidos
resultados
em
no VBEST7
para
tal
cálculo,
expressando os
concentração percentual de cada espécie a cada valor de
P[Hl-
Com estas ferramentas
ç
computacionais, as constantes de equilíbrio, a
em função do valor de pll-I] e o valor de p[H]
corrigido foram determinados, bem como o desvio padrão.
concentração de cada espécie
15
Os
de
pastilhas
KBr
dos ligantes
espectrofotômetro FT-IR
uma
do infravermelho foram obtidos
espectros na região
complexos
e
BOMEM,
Hartmann
resolução de 4cm`1, utilizando
uma
a partir
de
em um
MB-Series, com
sintetizados,
& Braun,
pastilha de
KBr
puro para a
obtenção da linha-base (branco). Medidas de espectroscopia na região do
espectro ultravioleta e visível foram obtidas
compostos solúveis
purissimo
para
em meio
em metanol
compostos, com
aquoso, e
demais
os
espectrofotômetro de feixe duplo marca
V
Os dados de
em um
em
cristalografia
bidestilada para os
(grau espectroscópico)
o
auxílio
de
um
HITACHI, modelo U-3000.
por difração de raios-X foram coletados
difratômetro automático de raios-X para monocristais, Enraf
N onius CAD-4.
As medidas de ponto de
fusão dos ligantes foram obtidas
aparelho de ponto de fusão da Microquímica, modelo
em um
MQAPF-301.
4.3 Síntese dos Ligantes
4.3.1 Síntese
do lígante macrocíclico
5,7,7,12,14,14-hexametil-
1,4,8,11-tetraazaciclotetradeca-4,11-dieno
diperclorato
-
(s,7,7,1z,14,14-Me6[14]-4,11-óàeno-1,4,s,11-N,,.zH(3104).“°
Em um
adicionaram-se,
erlenmeyer de
25mL
gotejou-se lentamente
funil
'
1
litro
contendo
500mL
de acetona,
de etilenodiamina. Sobre esta solução remanescente,
35mL
de ácido
percló1:ic_o,.
com o
auxílio de
um
de adição, sob agitação constante.
Precaução. O uso de uma proteção de segurança é recomendado. Sais de perclorato
ser considerados como perigo em potencial por causarem explosões violentas.
devem
i
16
A reação
(Figura 9) se processou exotermicarnente, sendo que
uma
coloração vermelho-alaranjadase desenvolveu no decorrer do experimento.
Após
a adição completa
do
ácido, a solução foi agitada» rapidamente e
deixada esfriar até que atingisse a temperatura de 25°C.
Reduziu-se o volume da solução a
um
terço
_
do volume
com
rota-evaporador, e o precipitado branco cristalino foi lavado
A
massa obtida
equivalente a 77°/o
z
no
acetona
vácuo na presença de pentóxido de fósforo como agente
gelada, e seco a
dessecante.
original
foi
68,61 g, representando
o rendimento
em relação ao reagente etilenodiamina.
uu”
-___-
.F
+
N,
zF
Figura 9
*Q
Hc1o
2'
-J>
Zz
zm
::
`-
mz
.2
\_J
Hc1o4
1,,
z
Representação para a síntese do ligante macrocíclico
5,7,7,12,14,14-M@ó[14]-4,11-dàzno-1,4,s,11-N4.2Hc1o,,
4.3.2
Mesa e racênlico - (5, 5, 7, 12, 12, 14 - hexametil - 1, 4, 8, 11
-tetraazaciclotetradecano)
hidratado
-
(5,5,7,12,12,14-Me6[14] ano-
1,4,s,11-N4.XH2o).4°'
Em um
erlenmeyer de
~
2L contendo 400rnL de metanol,
foi
adicionado todo o composto obtido na síntese anterior, 5,7,7,12,14,14' Ver
precauções
com compostos de perclorato,
17
item 4.3.1.
A
Me6[14]-4,11-dieno-1,4,8,11-N4.2HClO4.
solução
em
agitada
foi
condições de banho de gelo, quando se adicionou porções alternadas de
boroidreto de sódio (17g)
com
um
hidróxido de sódio (15g), por
período
uma hora.
de
Após
mais
uma
A
a adição estar completa, deixou-se a solução
hora e depois
resfriou-se o
adicionou
meio
em
refluxo durante 15 minutos. Após o refluxo,
reacional até atingir a temperatura ambiente,
800mL de uma
por doze horas, quando
uma
se obteve a precipitação da
esperado. Este foi lavado
com
como
pentóxido de fósforo
o qual
foi
quando
se
solução de hidróxido de sódio 1,25mol.L`1.
Deixou-se então a mistura sendo agitada por mais
material adicional,
sendo agitada por
em repouso
hora, e
maior parte do produto
água e seco a vácuo
em
presença de
agente dessecante. Obteve-se ainda
um
recuperado reduzindo-se o volume do filtrado.
Fora obtido 42g! do ligante macrociclico reduzido, sendo que o
produto da reação de redução representa
uma mistura
de isômeros (Figura
10).
~"'I/
L
N
H
N
H
NZBH
~"|›/
NH N
zHc1o4 -_---1*--›
H
NHI\‹
Z/¬
Fágum 70 - Representação para a
H
I”,
rrrso
síntese
T
.'ñ{"I:/ \\\\\\Z¬`
+
NH N
H
H
NI-IN
T
ll"~'.
NH N
_-~".
racemato
dos ligantes macrocíclicos meso-
5,5,7,12,12,14-Me6[14]ano-1,4,8,11-N4.xH¿O e seu respectivo racemato
18
H
NHN
1-1
4.3.3
mesa
Separação dos isômeros
e racêmíco-(5,5,7,12,12,14-?›
hexametil-1,4,8,11-tetraazaciclotetradecano)x-hidratado.49
da isâmero mesa (Lt)
.S13/>ara_cão
O produto da reação anterior foi solubilizado em 400rnL de metanol
em um
béquer de
filtrado à
um
litro,
aquecido até a temperatura de ebulição, e
quente para remover algumas possíveis impurezas.
O filtrado foi
em um erlenmeyer de um litro e completou-se novamente o
volume de 400mL com a adição de metanol, quando a solução foi aquecida
colocado
até
o seu
A seguir adicionou-se agua fria (300mL) na solução ainda
refluxo.
quente, agitou-se e deixou-se esfriar até que atingisse a temperatura
ambiente.
O sólido precipitado foi considerado sendo o isômero mem puro,
o qual
removido da mistura por
a
foi
vácuo na presença
recristalização
do
filtração,
um
dias
da solução
em
Tabela
1:
um
L
Rendimento, solubilidade
Rendimento Solubilidade
M¢oH
25°/O
1
seco
uma
quantidade
sólido branco cristalino após
rendimento de
25% em
uma
relação
lirnitante inicial, etilenodiamina.
e análise elementar
I
do
Calc,
l
Exp
I
Calc,
--›
l
Exp
1
Í
°/«N
C¿¡1C_
I
EXP
|59,9óÍóo,1o|12,5s|12,ssi17,4s|1s4o
|
Li
ligante L1.
°/«H
°/oc
v
Ligante
em uma
repouso sob resfriamento, obtendo
massa de 14,83g de L1 que representa
ao reagente
um
Efetuou-se
fósforo.
o mesmo
ligante solubilizando
mínirna de metanol, quando se obteve
vinte e
de
de pentóxido
com água gelada e
lavado
C,(,H36N4.2H3O (32O,52g.mol'1)
19
Sóparaƒão do racemato
i
Ao
anterior,
filtrado remanescente após a
remoção do isômero mem na etapa
A
foram adicionados aproximadamente 150rnL de água.
foi agitada
rapidamente por cerca de trinta minutos, peiíodo
precipitado foi formado. Este sólido é
uma
racemato sendo removido por filtração.
em um
quase completamente
foi isolado.
O
que
um
mistura dos isômeros mesa e o
evaporado
filtrado foi então
evaporador rotatório e
um
produto branco
O sólido foi lavado com pequenas quantidades de água gelada, e
seco a vácuo na presença de pentóxido de fósforo.
4.3.4
em
solução
do
Síntese
›››››"
ligante
'
s
macrocíclico
1,8-Bis(2-cianoetil)-
5 7 7 12 14 14 hexametil ' 1,4,8,11-trtraazaciclotetradecano (IQ).5°
iEm um
erlenmeyer de 100mL, adicionou~se sobre 2,00 gramas do
ligante mesa -5,5,7,12,12,14-Me6[14]ano-1,4,8,11-N4.2H¿O obtido
anterior
30mL
de
acrilonitrila,
sendo
em
na etapa
seguida esta solução agitada e
mantida sob refluxo por duas horas. Obtém-se após este período
um sólido
branco, o qual representa o ligante requerido, que foi lavado várias vezes
cometanol
gelado.
A massa obtida foi 2,27g e o produto (Figura 11) possui
um grau elevado de pureza, com rendimento acima de 90%.
Efetuou-se
uma recristalização do ligante,
uma quantidade mínima
em
quantidades iguais
de
uma mistura dos
(1:1),
após 15 dias da solução
quando
se
solubilizando o
solventes acetona e éter etílico
obteve
um
sólido branco cristalino
em repouso sob resfriamento.
20
mesmo em
~|r|¡l
NH
N~|,,¡,
A
-í--í»
[N
zcúionâzfuz,
V
HN
I|¡:|~.
ZE
N
ZE
Il||.~
1
'
> 90%
meso
Fzgura 77
EZ
- Representação
para a síntese do ligante 1,8-bis(2-cianoetil)-
5,7,7,1 2,1 4,14-hexametil-1,4,8,1 1 -tetraazaciclotetradecano
Tabela 2: Rendimento,
Lwante
solubilidade e análise elementar
°/oc
R€ndim€HIO S01UbÍ1idfld€
93%
L:
cl-13cN
Calc.«I
4.3.5
Síntese
Exp.
Í
ó"/,73
ló7,ó5
Lj-› c22H42N6
1
do
ligante L2.
°/«H
Calc.
Exp.
10,84
10,89
|
1
°/ON
|
Calc.
I
21,51
Exp
12133
Í
¡
(2›9o,ó2g.m<›1~
do ligante macrocíclico ácido
5,5,7,12,12,14-
hexametil-1,4,8,11-tetraazaciclotetradecano-1,8-dipropiônico (L3).
Em um
béquer de
125mL
adicionou-se sobre o ligante 1,8-bis(2-
cianoetil)-5,7,7,1 2,14,14-hexametíl-1 ,4,8,1 1 -tetraazaciclotetradecano
1mmol), obtido na etapa
37°/0).
anterior,
25mL de
(O,39g;
ácido clorídrico concentrado (2
Esta mistura foi agitada e aquecida brandamente (45°C) por seis
horas. Obteve-se após este período,
ligante pretendido (Figura 12).
solubilizando o
um
sólido branco o qual representa
Efetuou-se
mesmo em uma
uma
recristalização
do
o
ligante
quantidade mínima de água bidestilada.
Filtrou-se a solução para a remoção' de qualquer fragmento remanescente
referente ao ligante L2
não hidrolisado. Após 21
21
dias
da solução
em
repouso sob resfriamento recuperou-se aproximadamente O,43g do
que
foi filtrado e seco a
vácuo na presença de pentóxido de fósforo.
O
\/\N
ligante,
N
H
O
HC <°°"°>° A
1
.
i
N
CF
NE
\/\EN
Ú
Ela'
'Z.
1+
.2Hc1
\
O
.-
'
Ls
L2
Fzgura 72 - Representação para a síntese
do ligante ácido
Z
5,5,7,12,12,14-
hexametíl-1,4,8,1 1 -tetraazaciclotetradecano-1,8-dipropiônico (L3)
Tabela 3: Rendimento,
solubilidade e análise elementar dos ligantes L3.
%H
°/OC
Ren‹'1im¢nt0
Ligante
Exp.
Calc.
|49,1ó
49,42
9,37
Hzo
80%
L3
S0111bÍ1Íd8d€' Calc.
I
°/‹›N
Exp.
Calc.
1o,421o,oõ
8,59
1
I
L3 -› c22H4_,N4o4.2Hc1.2H2o (5õí',57
4.3.6 Síntese
do ligante macrocíclico
g.m<›1~1)
1,8-bis(3-hidroxipropil)-
5,7,7,12,14,14-hexameti1-1,4,8,11-tetraazaciclotetradecano (L4).
Um volume de 10mL de óxido de trjmetileno foi adicionado sobre o
ligante Lj (O,9óg,
condensador.
_
dias,
quando
remanescente.
ómmol) em
um balão
de fundo redondo adaptado a
um
A mistura remanescente foi mantida sob refluxo durante dois
foi resfriada à
Após
temperatura ambiente, e filtrou-se o sólido
a filtração, lavou-se o precipitado
com
pequenas
porções de água bidestilada, e secou-se o ligante sob vácuo na presença de
cloreto de calcio (Figura 13), obtendo-se 1,14g
22
do ligante
Exp.
alcoólico.
Q
...~|1/1
ÍNH
/\/Á-.~›:¡1/
N
Ho
ä
--í--_->
I N1
A
O
HN
1
III|~
NH HN
Fágum 73 - Representação para a
/II|¡~
ZII1
síntese
do
OH
~
ligante 1,8-bis(3-hidroxipropil)-
5,7,7,1 2,1 4,14-hexametil-1,4,8,l1-tetraazaciclotetradecano
Tabela 4: Rendimento,
solubilidade e análise elementar
°/oc
Rendimento Solubilidade
Ligante
Hzo
95%
L,
Calc.
I
ó5,95
ligante L4.
°/«N
_°/OH
]
Exp.
Calc.
ó4,55
12,03
I
|
L, _› c2,H,,8N,o2 (4oo,ó5 gmol-)
¡
do
I
Exp.
12,15
1
Exp.
Calc.
13,35
13,93
|
I
1
4.4 Síntese dos
Complexos
H
4.4.1 Síntese
49
do Complexo Ni-LI
O ligante L1 (O,96g, Smmol) foi solubilizado em metanol, aquecendo
a solução a 50°C,
níquel
em
com agitação
constante. Adícionou-se então perclorato de
quantidade equimolar à do lígante, obtendo-se o complexo
quinze minutos após a adição.
O
complexo
é filtrado, lavado
com
metanol, obtendo-se 1,13g do complexo.
23
éter etílico e recrístalizado
em
Tabela
5:
Rendimento, solubilidade, análise elementar
complexo Ni-L1.
..
HZO
70%
Amarelo
Ni-L1
°/oc
Rendimento Solubilidade
Cor
Complexo
%H
|
EXp,|Ca1‹;.
35,45 35,60 6,69
Ca1<;_
Ni-L, -› c,6H,,N,c1,o8Nâ (542,1o
do
e coloração
%N
Exp.
Calc.
6,45
10,34
Exp.
10,40
0
g.m<›1~*)
t
H
4.4.2 Síntese
do Complexo Cu-L1
O ligante L1
Bmmol)
a solução a 50°C,
cobre
em
(0,96g,
com agitação
foi solubílizado
em metanol,
constante. Adicionou-se então perclorato de
quantidade equimolar ã do ligante, obtendo-se o complexo
quinze minutos após a adiçao.
O
aquecendo
complexo
-
é filtrado, lavado
com
em
éter etílico e recristalizado
metanol, quando obtém-se 1,14g do complexo de cobre.
Tabela
6:
Rendimento, Solubilidade, análise elementar
complexo Cu-Ll.
cu-L,
70%
violeta
Í
'
|
Calc,
Hzo
I
Í
Cu-LI -› Clól-I3¿N4Cl2OSCu (546,93
lígante
Exp
°/OH
}
l
1
|
I
g.mol'1)
do Complexo Ni-LZ
L2
(0,58g,
aquecendo a solução a 50°C,
1,5mmol)
com
foi
solubílizado
em
metanol,
agitação constante. Adicionou-se então
'
24
%N
Calc Exp
ó,7s |1o,24l1o,29
Cal; EXp_
35,38' ó,ó3
35,14
l
4.4.3 Síntese
O
°/oc
Rendimento Solubilidade
Cor
omplexo
do
e coloração
em
perclorato de níquel
quantidade equímolar
complexo quinze minutos após
O
complexo
a adição.
é filtrado, lavado
51
do
lígante,
obtendo-se o
›
com
em
éter etílico e recristalizado
metanol, obtendo-se 0,77g do complexo de níquel.
Tabela
7:
Rendimento, solubilidade, análise elementar e coloração do
complexo Ni-L2.
°/oc
Rendimento Solubilidade Calc
Cor
Êomplexo
Azul
Ni-L,
M@oH
80°/O
1
Exp_
°/«N
°/«H
|
C;¡1¢_
Exp_
ó,74 112,96
13,05
Calc Exp_
l
4o,7ó 41,o1|
ó,53›
l
1
Ni-L, -› c,,H,,N,c1,o,1×1à (ó4s,2õ gmol-)
1
4.4.4 Síntese
O
1
ligante
do Complexo Cu-L2
L2
(0,58g,
50°C,
aquecendo a solução
'a
cloreto de cobre
em
(ll)
1,5rnmol)
com
foi
em
solubilizado
metanol,
agitação constante. Adicionou-se então
quantidade equimolar
51
do
ligante,
obtendo-se o
complexo quinze minutos após a adição.
O
complexo
é filtrado, lavado
com
V
em
éter etílico e recristalizado
metanol, obtendo-se 0,46g do complexo.
Tabela
8:
Rendimento, solubilidade, análise elementar e coloração do
complexo Cu-Lg.
Rendimento Solubilidade
Cor
omplexo
Cu-L:
Violeta
`MeOH
60°/o
1
1
V
`
Cu-L2
1
-_›
°/OH
°/oc
(j9_1¢_
Exp_
50,33
50,54
1,,
(j9_1¢_
Exp_
1
°/ON
C3_1¢_
|
1
Exp
16,41
16,01
7,72
8,06
1
C¡,_2H42NóCl2Cu (525,07 g.mol'1)
25
|
1
1
4.4.5 Síntese
O
lígante
do Complexo Cd-L2
L2
aquecendo a solução a 50°C,
nitrato de cádrnio
em
l,5mmol)
(O,58g,
com
complexo
em
solubilizado
metanol,
agitação constante. Adicionou-se então
a adição.
é filtrado, lavado
com
*
em
éter etílico e recristalizado
água bidestilada, obtendo-se O,69g do complexo de cádrnio.
Tabela
9:
W
Rendimento, solubilidade, análise elementar e coloração do
complexo Cd-L2.
_
°
omplexo
cd-L2
ç
Cor
Bmw
_
quantidade equimolar à do ligante, obtendo-se o
complexo quinze minutos após
O
foi
Rendimento Solubilidade
70%
+120
Cz1¢_
]5'¿X_p_
59,85
40,03
Cd-L2 -› C¿2H42N8O6Cd.2H2O (663,06
26
OH
°/ON
Calc EXp_l
(j¿1¢_
Exp
ó,99
1ó,9o
1ó,99
g.mol`
)
7,21
1
5
RESULTADOS E DISCUSSAO
dos ligantes e complexos
5.1 Sínteses
O ligante
[Me6(14-ano)N4].2H2O
(L1) foi sintetizado
de acordo
com
um método previamente descrito na literatura química. A reação ocorre sob
de
condições
diluição
usualmente chamada síntese de
condensação
adição
e
onde mecanismo proposto para
elevada,
de
Curtis,51
Nlichael
é
`
dado por
uma
reação de
envolvendo duas moléculas
etilenodiamina e outras' quatro moléculas de acetona,
eliminação de água, para a obtenção do ligante
com duas
com
a
de
subseqüente.
ligações imínicas.
A formação do ciclo requer um grande volume de acetona, mas outra
de molde (templato), onde utiliza-se um
possibilidade é a síntese sob
ef‹1'Í_to
íon metálico para orientar a estrutura final do ligante, possibilitando evitar a
polirnecização da reação de condensação que ocorre
com volumes menores
quando
trabalha-se
i
de solvente.”
Em reação posterior do ligante insaturado, a face da ligação imínica
que sofre redução determina a formação do isômero mesa ou do mcemata.
Os
ligantes
se a eficácia
isolados,
foram isolados por diferença de solubilidade, e verificou-
da separação determinando-se o ponto de fusão dos materiais
em
vista de
temperaturas distintas.
possuírem esta propriedade fisica definida e
em
O isômero mexo funde a 146-148°C, e o racemato na
faixa de 97-101'°C.
Ambos foram purificados por recristalização em metanol,
em
rendimento
final
de 15-20°/o do mcemaío, e 25-30°/o do mero
ao reagente limitante (etilenodiamina).
e
obtém-se
em
relação
O
reservado
racemato, por não fazer parte do objetivo deste estudo, foi
para
trabalhos
posteriores,
para
possivelmente
com adição de doadores
semelhantes de substituição nucleofilica
sínteses
adicionais,
~
com
que deverá fornecer resultados importantes para comparação
as
propriedades dos ligantes aqui sintetizados.
A
obtençãofldo
ligante 1,8-bis(2-cianoetil)-5,7,7,12,14,14-hexametil-
uma
1,4,8,11-tetraazaciclotetradecano (LB), foi efetuada por
adição de Michael, onde o efeito de conjugação da ligação
de
das moléculas
14).52” 53
dá o caráter eletrofilico ao carbono terminal (Figura
acrilonitrila
.
'rc
reação de
H2cQ(_
R-NH
-‹
H
RI/
í›
'
/
R7N+
'
R'
I
R-N
7?
\/\-__N
/
Fágura 74
<---
- Exemplo de
R_
R"
v/l/Hr)
_
.
H
_
adição de Michael
A adição de dois grupos etilciano é efetivada apenas nas posições
do anel macrocíclico em função da presença de
geminais nas posições 5 e 12, que efetuam
substituintes dimetil
um maior impedimento estérico
para adições nos átomos de nitrogênio adjacentes (posições 4 e 11).
ligante final é obtido
de pureza, tendo
compatibilidade
em excelente rendimento
um
na
de síntese e
ponto de fusão definido
relação
em
O
em elevado grau
147-148°C
calculado/ valor
valor
1,8
e
grande
experimental
da
H
microanalise.
Tal reação
como
também pode
ser efetuada
com
outras espécies acrílicas,
a aciilamida, obtendo-se agentes quelantes que
28
formam complexos
com
estáveis
lantanídeos trivalentes, principalmente
quando
se
combina o
grupamento amida com a neutralização de cargas promovida pela adição de
acetatos.54
A partir do ligante L2 puro, sintetizou-se o ligante macrocíclico ácido
5,5,7,1 2,1 2,1 4-hexametil-1 ,4,8,1 1 -tetraazaciclotetradecano-1,8-dipropiônico
(L3),
hidrolisando os grupamentos
que o
mesmo
nitrila
ácido concentrado. Prevê-se
também
tipo de reação poderá
hidrólise básica.”
em
ser obtido
O composto obtido é solúvel em
banda de absorção na região da radiação
por meio de
e apresenta
ultra-violeta
uma
de 204 nanômetros,
referente ã transição fz-nt* dos grupos carboxilatos, utilizando
como
banda apresenta grande semelhança
com a
bidestilada.” Esta
solvente
banda referente ã mesma transição
carboxílico,
o EDTA
eletrônica de outro ácido
amino-
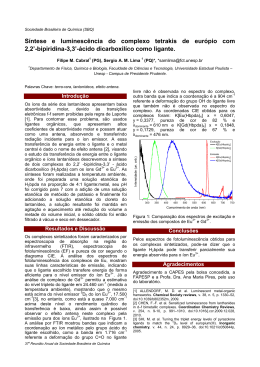
(Figura 15).
1,41,21,00,8
_ (a)
O)
Absorbância
_o
0,4 0,2
(b)
0,0
'I
'
190
I
200
'
'
I
I
comprimento de onda.
Fágura 15 -
(a)
'
220
21 0
'
I
240
nm
UV de uma solução de EDTA Z
Espectro de absorção no UV de uma
Espectro de absorção no
O,015mol.L`1.
I
230
solução de L3
2
29
0,O1mol.L'1
O
ligante
[Me6(14-ano)N4].2H2O
(L1),
também
foi
o precursor do
1,8-bis(3-hidroxipropil)-5,7,7,12,14,14-hexametil-1,4,8,11-
ligante
tetraazaciclotetradecano (L4), que é obtido após a quebra
átomos do óxido de propileno. Esta reação
do
anel de
é relativamente lenta,
4
sendo
com grupos hidroxietil pendurados,
reação efetuada com óxido de etileno. A reação com este éter cíclico é mais
rápida devido à maior tensão no anel de três átomos, refletindo uma maior
mais comuns as reações de substituição
facilidade
Porém,
de abertura do anel, sendo efetivada a baixa temperatura (O°C).
em
condições mais severas é possível obter o ligante
com
grupos
“'50
hidroxipropil pendurados.
Espera-se que a presença de átomos de oxigênio neutro pendurados
a seletividade a metais de caráter mais “duro”, segundo a teoria
aumentem
de ácidos e bases duros e macios (HSAB),4°
Os complexos
níquel, cobre e
como o chumbo
de níquel e cobre do ligantes L1 e os complexos de
cádmio do
ligante L2,
foram obtidos basicamente mediante
adaptações do método de Busch”.
A síntese
íon metálico
dos complexos é efetivada após a reação do ligante
com o
em proporções equimolares.
5.2 Cristalografia
5.2.1
L,
-
meso-(5,5,7,12,12,14-hexametil-1,4,8,11-
tetraazaciclotetradecano) di-hidratado
Os
monocristais do ligante L1 foram obtidos
deste ligante
em metanol.
30
com
a recristalização
O
uma
ligante apresenta
estrutura de fórmula empírica
CBHZONZO,
320,52gmol`1, sistema cristalino tetragonal, grupo espacial I4(7)/ a, e as
dimensões da
12,o11(3)Á,
À3,
Z=
zz
=
célula unitária são a
=
= 9oâ¢g C y =
9odeg, 5
9od‹-zg.
em todos
foram usadas
1,/
Í(IQ» I
N‹2›
É
Í\
,
'\Ê
5.2.2
L2
-
Q)
\f'=;lz»
\
qa)
N(2 O
l
z
a
Fzgura 76 - Diagrama
l
W*
c‹2<z›
\\`
=
=
0,0449) que
=
0,0446.
9
Cm
c‹2›
I,
C1 >
Nil O
\\\ä
l
Ç
gl
,
‹
_
Ç
Oilgliõ
c‹ô›
\
Cll °
,
|IIä\
ll
*
Nm
(tg
lí/à'
c‹5›
`=Í'zfh.
'Í\
“l>/M
c‹3›
~
c
1
Q
CW
¡
He,
(int)
O zz/R(F2) final foi 0,0974, R1
os cálculos.
z
18,646(3),
o vølume foi de 4175,9(14)
3599 reflexões coletadas, 1826 únicas (R
16,
=
18,646(3), b
l
*
c‹7z>
c‹5¢›
“M
Í c
*"
*
:‹3<z›
ORTEP do ligante
[l\/Ie6(14-ano)N4].2H2O
1,8-bis(2-cianoetil)-5,7,7,12,14,14-hexametí1-1,4,8,11-
tetraazaciclotetradecano
A estrutura cristalina do ligante Lg neutro foi determinada após a sua
recristalização
em uma mistura de
em proporção
1:1.
O
ligante apresenta
390,62gmo1`1,
sistema
um
solventes orgânicos, acetona e éter etílico
estrutura de fórmula empírica
cristalino
tnclínico,
31
CUHZIN3,
grupo espacial P-7, e as
dimensões da
=
111,51deg,
=
2,
célula unitária são a
,3
= 115,07deg e y =
=
=
8,300(2), b
em todos os cálculos.
=
9,755(2)Â, a
O volume foi de 580,9(2) Á3, Z
93,61deg.
2675 reflexões coletadas, 2502 únicas [R
usadas
8,814(2), c
=
(int)
0,0121] que foram
O zz1R(F2) final foi 0,1126, R1
=
0,0429.
/ã¡ CIB
019
/
C8
'À
'LM
c14A
C7
.`
âi\\\\\~
ll”//'×
1
N A
C1A
fé.
_
C1
(14
Nf,
Fágum 77 - Diagrama
MA
Nl
va
ty\
C1 IA
C12A
CIOA
M?/á\z-‹'*
013
c13A
Ê.
`
U0
'Ê CH
_
.-ד
1
Q;
C9
NM
CQA
l
-
cn
csà
Cl9A
/
¿
\
lã!
C18A
ORTEP do ligante 1,S-bis(2-cianoetil)-5,7,7,12,14,14-
hexametil-1,4,8,1 1-tetraazaciclotetradecano
Os átomos
de hidrogênio foram omitidos, para melhor visualização
do diagrama.
A
estrutura confirma a presença dos substituintes cianoetil apenas
nas posições
impedimento
(N4
e
1 e
8
(N 1
e
N1A - Figura 17) do anel macrocíclico, devido ao
estérico para substituições
nos átomos de nitrogênio 4 e 11
N4A - Figura 16).
Observa-se que o ângulo das ligações C1-N1-C10 passa a ser de
113,18° para fora do macrociclo, enquanto que
em L1
o ângulo equivalente
(C2-N1-C3) era 113,8° para dentro do macrociclo (Anexo).
32
dos ligantes
5.3 Espectroscopia vibracional'
Ugante L,
A
do infravermelho para 0
ligante
[Me6(14-ano)N4].2H2O (Figura 18) pode-se destacar, entre outros
modos
do espectro na
partir
vibracionais
do
ligante,
região
o estiramento de
a combinação de estiramentos de
1,
estiramento simétrico de
em
em
CH2 em
N-H na região de 3240 a 3270cm`
C-H
alifático
de 2900 a 2965cm`¡, o
2840cm`1, a deformação angular de
17O0cm`1, a deformação angular do grupo metileno ligado â
N-H
uma amina
15O4cm`1, a combinação de deformações angulares dos grupamentos
em
metil e metileno
(umbrella)
em
1466cm'1, a deformação sirnétrica das ligações
H3C-C em 136Ocm`1
1375cm`1, o estiramento de
CH3
e
o
C-N em 1180 cm`1.
estiramento de
W
_....‹..-.__.___._...._...___.,.._..._._....<._._..~.H._._._..__.-.....___._.__,.__..._.r_.._.._._._._..-...._.....
_..__..l..c..._..._._.....-.._.._.......-._...__.....-...‹_.____.¬
›
M
_.
rm..
linea
Transm
§-,1°.._`n-,_ä__,._,`_°`i-_.¬.§.^_,_.
`“""
'
""`
f"""
"
'
"""'
"
3500
""
"f°”"_'
3000
1
"""
2500
"”"
""i"""
2000
'_"__'
›`“"""
1500
"
'
""1"""'
1000
""""`°'
`T""
500
Número de onda. cm-1
Res=4 cm-1
tet-a
Fágura 78 - Espectro de infravermelho
do ligante [Me6(14~ano)N4].2H2O
em pastilha de KBr
Os valores das freqüências cârãcéerístiws foram atribuídos
citados na literatura científiw.
'
em concordância com valores
'
Bim
.
wi farsitária
-
.
_
\
_.
J
W*
33
-f
_
'°
I_1;gante
L2
O espectro na região do infravermelho do ligante 1,8-bis(2-cianoeti1)(Figura
5,7,7,12,14,14-hexametil-1,4,8,11-tetraazaciclotetradecano
demonstra destacadarnente
estiramentos de
de
C-H
um
alifático
N-H em
estiramento de
série
3270cm`1, os
de 3000 a 2900cm`1, o estiramento simétrico
CH2 em 2843cm`1, a intensa, banda de estiramento
uma
19),
de
CEN em 2242cm'1,
de bandas resultantes da deformação angular dos grupos
metilênicos e das metilas entre 1450 e 1480cm`], a deformação simétfica das
CH3 em
ligações
1377cm`1 e o estiramento das ligações carbono-nitrogênio
em 1158cm`1.
_
.
_t_.__
___
_
.-._
_
É
--,..¬
30t
L
,
1
x
a
`I;an9mItânc
._t_.l._s=_l__t..r,..~?_.i_W.šâ,__._
1
z
â
l
_
_-«~¬»_.fi_...-¬-~-_~ uzsoo
¬~-~ MM~_.,-_«__~~-¬-_»_~ __._¬~«_.-~«._¬...1
M
_
asoo
H
i
i
zooo
aobo
1soo
moo
l
ll
f
500
Númemdeonda. em-1
Res=4cm-1
tal-a-nílrila
Figura 19 - Espectro de infravermelho
do ligante
1,8-bis(2-cianoeti.l)-
5,7,7,1 2,14,1 4-hexametil-1 ,4,8,1 1-tetraazaciclotetradecano
em pastilha de KBr
34
Lzggante L,
O
do
espectro de infravermelho
ligante,
ácido 5,5,7,12,12,14-
hexametil-1,4,8,11-tetraazaciclotetradecano-1,8-dipropiônico
(Figura
20)
evidencia a estrutura proposta para o composto. Apresenta bandas de
estiramento de
N-H
C-H alifático na região
de 2930 a 299Ocm`1, estiramento de
de aminas protonadas (R2NH2+)
em
de
bandas
com
2622cm`1, juntamente
a
bandas
Outras
sobreposição
de
características
da estrutura são a deformação angular assimétrica do
outras
agrupamento +NH2
em 1610crn`1,
ressonância.
a deformação angular assimétrica
do íon
carboxilato
em 1580cm`1 e seu respectivo modo simétrico em uma pequena
em
1405cm`l. Estas bandas são tipicamente características de
banda
aminoácidos,
aí'-_'_`*"
_
mesmo na forma de clo1:idrato.55
Í
'*"
"`_"*"_"
"_“"°"`
V
___`
_
“_
'“"__`““" " `“i;'_""1
1
75--
_.ÊL_
Transmltânola
3
_¬,L.`.____..›.___-
3
1
4
à
í
Fi,».._3.L_
*
'”"“"'_""¬"“"°"""""""°""í" '
3500
3000
'
'
"`1"_`"""
2500
'
_"“°T'““
'
'
2000
'
'
"“`“"""F_`_"""'í"""`_I"“"""""°-_""“"`T"'°J
1500
1000
500
Número de onda. cm-1
Res=4 cm-1
tet-a-propiõnioo
Fzigura
20 - Espectro de infravermelho do ligante ácido
5,5,7,12,12,14-
hexametil-1 ,4,8,1 1 -tetraazaciclotetradecano-1,8-dipropiônico
em pastilha de KBr
35
Vale salientar as bandas
em
1440
1470cm`]
e
referentes
às
deformações angulares das metilas e metilenas, e o estiramento simétrico
do grupo CH3
em 1386cm'1.
Outro
dado
extrema
de
relevância
que
fornecido
é
é
desaparecimento completo da banda representativa do estiramento de
o
CEN
em 2242cm'1.
Lzgante
L
4
Observando-se o espectro na região do infravermelho para o
5,7,7,12,14,14
-
1,8-bis(3-hidroxipropil)
-
hexametil
tetraazaciclotetradecano (Figura 21), verifica-se a relação
proposta.
em
em
-
com
ligante
1,4,8,11
-
a estrutura
O espectro apresenta uma banda de estiramento de O-H, quando
ligação de hidrogênio, entre
3250cm'1 e
uma banda
3400
e 3300cm`1,
um
O-H quando em
intramoleculares na forma de anel,62 a qual encobre os
A deformação
em
1375cm'1.
claramente a presença de
um
modos
ligações
vibracionais
angular dos grupos metilênicos e
metilas ocorre entre 1450 e 1480cm`1, e o
do grupo CH3
N-H
intensa e muito larga entre 3000 e 2800cm`1,
provavelmente referente ao estiramento de
dos estiramentos de C-H.
estiramento de
modo
de deformação simétrica
Outra banda intensa que caracteriza
grupo funcional alcoólico
é
do estiramento de C-O para álcoois primários em 1050cm`1.
36
o aparecimento
[_.__..n..__..._.______...___________.____ _______ ..____ _______ ..._ ___________ _.__.._._
....
..__...--__...._...._.-........__.__.-.-_...__..«-‹...-..._....._.......__.._..-._...._.-....-,._..\.___
._
l
if
sol
11
l
ê
Y
1.
WW
U,
Transmltàëcla
l
,
E
z
_,,_._
š
zzl
fl
il
li
E
oi
É
l"""""_""°""""""""T"""""""""'_°"""*{"""“'_"""""`~"'
4000
3500
25%
2000
Númem de onda. cm-1
3000
M-8-Pf0P8fl°|
Fggura 21
°°"""""""""` "_"""
""_'""""` """""""""""_""T""""""`_""""""""
- Espectro de infravermelho do ligante
1300
SÉ
1000
"'i
Res=4 om-1
1,8-bis(3-hidroxipropil)-
5,7,7,12,14,14-hexametil-1,4,8,11-tetraazaciclotetradecano (L4)
em pastilha de KBr
5.4 Espectroscopia vibracional dos
complexos
{NilM€ó(14'afi°)N4l}2+(ClO4')2
3-n°)N4l l
2+
(Ni(H)'L1)
C
{Cl1lMeó(14'
(ClO4_)2 (Cu(H)°L1)¡
Estes dois complexos apresentam duas bandas intensas referentes a
modos
vibracionais
do íon
perclorato,
em 626cm`1
e 11O0cm`1. Esta última
encobre toda a região espectral de 975 a 1230cm'1, e apresenta sua
ressonância de Fermi entre 2000 e 2060cm'1 (Figura 22).
37
_._i-_.______._.-_._.._
___---
_.-
.--.___-_o.__---.__-...__._._..___.o_....._.--1
i2°`l'_'
'I
K8)
1(D
_;L_.š._
1
Tranamitâncla
š
1
-ii
Ê
§__
1
\
|
›
o-'š
if'
"
""
4ooo
f'_""
7
asoo
'V
“_
"`”"_T
_"\
_"""_'l
7
:ooo
zsoo
sooo
"""""
"""'_T_."""`_"`”__""""`7"_""~'_"`.""_-'l'_`
1soo
1ooo
il
sao
Número de onda. cm-1
{cu[Me6(14-ano)N41}2(CI04)2
Figura 22 -
(a)
(a)
{Ni[Me6(14-ano)N41)2(CIO4)2
Res=4 em-1
(b)
Espectro de infravermelho do complexo (Cu(II)-L,) e
(Ni(Il)~L1)
Uma banda
em pastilha de KBr
que pode representar o indicativo de complexação é o
deslocamento da deformação angular da ligação N-H, que passa de
17OOcm`1
no
ligante livre, para 1633cm`1
no complexo com
níquel e
1647cm`1 no complexo de cobre.
As demais bandas representam
ligante, já descritos
na seção
os outros
modos
vibracionais
do
5.3.
Estes valores auxiliam na interpretação do espectro vibracional dos
complexos
com o ligante L¿.
Complexo Ni2+ -L2:
Assim como os
o espectro
perclorato
anteriores, sintetizado
vibracional deste
na forma de
complexo demonstra
sal
as bandas intensas
em 1120 e 624cm`1, respectivamente (Figura 23).
38
de perclorato,
do
Uma banda em
1633cm`1 é atribuída a deformação angular
N-H
da
amina secundária coordenada, novamente apresentando deslocamento e
um perfil de banda mais definido.
As demais bandas do
virtude da intensidade dos
ligante
modos
aparecem
vibracionais
em menor
do íon
intensidade
em
perclorato estarem
em destaque, mas salienta-se a considerável diminuição relativa a frequência
do estiramento de
CEN em
2242cm'1, possivelmente caracterizando a
coordenação deste grupo doador
com o metal.
›
'|
,,
l
5°'
G
..__r.__.r_
š
A
«
t
¡
Transmltãncla
›
V
i
,._°:.r..___§'L.~,..r;*zí_M__,'â_
N
4000
-
----›
1-~~›~
3500
~-.
-¡~~-
3000
--4--z----¬-»--»--~«---~¬›«-----~--_-----›--,‹--_.--~-H_-----.-¡‹_-..-----_----¬-_-4
te!-a-nilrila-N¡2+
Figura 23
2000
2500
Número de onda, om-1
1500
1000
500
Res=4 cm.1
- Espectro de infravermelho do complexo (Ni(II)-LY) em pastilha
de
KBr
Complexos Cuz*-L2 e Cd2+-L2:
O complexo de cobre foi sintetizado na forma de cloreto, e mostra
todas as freqüências características do ligante L¿, incluindo a deformação
angular de
N~H
deslocada para 1614cm`1, e a banda
39
de estiramento de
CEN em
2243cm`1 (Figura 24a).
vibracional
caracteriza
A
intensidade relativa deste
a independência
deste
indicando a preferência do cobre(II) a formar
um
modo
grupo no complexo,
complexo de geometria
quadrada plana.
W
A
(a)
S
!
Í
/~
.._,,-§¿,r__.
l
a
Transmitánc
É
l
'M
É
l
fair.--
É
4000
-.___r.«-___ r;
.-.-...__¬.__._,_r-_¬,--r-__._.r-..,..-.._.-_×-.-._T..-.--...-_._._.._.¬r.l.__._...
3500
Figura 24
2000
Número de onda, em-1
cadmio.
Res=4 cm-1
(Cu(II)-IQ) e
em pastilha de KBr
figura 24b mostra o espectro infravermelho do complexo de
A banda intensa e larga de 1340 a 1410cm`1 refere-se à vibração do
íon nitrato, que foi o respectivo
do metal
sal
complexo. Aparece a deformação angular de
complexo de cobre, e
intensidade
em
um
utilizado
N-H em
na
síntese deste
1614cm`1
desdobramento desta banda
que
como no
com maior
1662cm`1. Salienta-se a larga banda de estiramento de
entre 3300 e 3560cm`1, e a diminuição da intensidade relativa
nitrila,
53)
1761)
- (a) Espectro de infravermelho do complexo
(Cd(II)-L2)
A
150)
2500
3000
se desloca para 2255cm'1 e
pode
o câdmio
40
caracterizar a
O-H
do grupo
coordenação
com
5.5 Titulação
potenciométrica do ligante
I.¿
A curva de titulação do ligante L3 apresenta a primeira inflexão em
a=2, significando que dois mols de
para cada
mol de
segunda inflexão
ligante,
em
em
KOH neutralizam dois mols de prótons
valores de pl-I abaixo de 4,00.
a=3, indicando a neutralização de mais
próton para cada mol de
ligante,
que ocorre na
faixa
de
Ocorre
uma
um mol
de
pH = 7,0 - 9,0. Um
em valores de pH acima deste valor, que extrapola o
valor de pH=11,00, mas é estimado com o refinamento dos dados obtidos
terceiro
tampão ocorre
(Figura 25).
12~
Z/
10-
3-
Etm
_
5..
4_
2 “I
_ø'ø_'___/z
|
O
I
,Í/'/'.z-/
|
1
I
I
I
2
|
I
3
|
4
I
|
5
il
Fzgura 25 - Curva de titulação potenciométfica
do ligante ácido
5,5,7,12,12,14~hexametil-1 ,4,8,1 1 -tetraazaciclotetradecano-1 ,8-dipropiônico,
aT
= 298,15K e ¡.L=0,1molL`1 (KNO3); a = mmol de base
adicionada/ mmol de ligante
41
Os
valores das constantes de protonação, K” (n
=
1
a
4),
estão
relacionados aos equilíbrios demonstrados pela Equação 1
Hz.1L
+ H*
= HnL›
= ___UiaLl__-
K..
valores dos logaritmos dos valores das constantes de protonação
encontrados
lê, Za,
3a e 4a
3,78Í0,01
8,56Í0,01,
11,6ÍO,1,
são:
correspondendo a
A
(1)
lH.z-zL][H+l
'
Os
'
e
2,11Í0,01,
protonação, respectivamente.
figura 26 mostra as curvas de distribuição das espécies formadas
em solução em funçao da variaçao do
100
_
.21:
-
L
ç
eo
i
8070
¿
H L
Í-
õcq
l
Q¬›
so.
.
-
4L
vç
1'\\
-as
i
30r29;
10
O
1-*
*
2
4
3
4
'se
i
5
6
zu/
/
i
1
1
8
'F
«LOG[E*]
9
.
10
11
12
ç
Fzgura 26 - Curvas de distribuição das espécies
função da variação de p[H], a T=298,2ÍO,1K
é a espécie
completamente desprotonada
espécies
mono,
di, tri e
42
e
em solução do ligante L3 em
e
u=O,1OOmolL'1 (KNO3).
HL, H2L, H3L e H4L são
tetraprotonada.
as
L
Em
elevado
p[H]
desprotonada
(L),
predomina
(12,0),
com 70,7ç°/o de formação em solução.
um nitrogênio
a espécie HL que é máxirna em
menores, ocorre a protonação de
11,6),
p[I-I]
formando
'-=
10,1.
A
a
segunda protonação (pK2
=
espécie
totalmente
Em valores de p[H]
amínico secundário(pK,
=
solução (94,3°/0) quando o
8,56) ocorre
no outro
nitrogênio amínico secundário, formando a espécie HZL, que é a espécie
predominante para valores de p[H]>3,8
99,1% formada quando o p[H]=6,0.
As duas
terminais (pK,
'
*
últimas protonações
=
3,78 e pK,,
=
e p[H]<8,6. Esta espécie está
ocorrem nos ácidos propiônicos
2,11), e
correspondem
a
formação das
H3L (7 7,2% em p[H]-13,0) e H4L (56,3% em p[H]=2,0).
A ordem das protonações é baseada em comparações com
espécies
que apresentam os mesmos grupos doadores descritos na
científica, possibilitando 'a previsão das espécies
43
ligantes
literatura
em solução (Figura 27).
HN
N
O
+H+
_
E
,,)V\_)=
m
.
fl<¡)
O
+
HN
048
Íë/Íz
_
\¿z
E
H+
-
.
+H"'
(K2)
'
onde:
P K, =
O
11,6
P Kz = 8,56
É
_
O~ É
-
p Kz = 5,78
p K4 =
›
2,11
_
H+
E+
N
O
ça
O
HZL
+ H+
(K)
"
O
ml
Olñ
CEI
mzüz
3
N
O
:_
Q/_/ä
:E+
OI
@@HH
Qi]
%O
Ljä¿
N
+
};L/K
U1
O
~"
HSL
Fzgum 27 - Etapas de protonação do
ligante L3
em solução aquosa, em
função da variação do p[H]
Os
Valores obtidos encontram-se
na tabela
10,
juntamente
com
os
valores das constantes de protonação de outros ligantes semelhantes, doda
e dota (Figura 28),
~
nao coordenante.
em
condições de
mesma
'
44
força iônica
com um
eletrólíto
Tabela
10:
Constantes de protonação a 298,15K para o L3, dota e doda
Ligante
log E211
'log K'a2
log K2,
log Kay,
L3
11,óÍO,1
8,56i0,01
3,78Í0,01
2,11Í0,01
Dota
11,73
9,40
4,50
4,19
Dodz
111,45
9,54
4,00
2,só
T
o
O
O
próton
1,71
<2,3
<2,1
O
Q
Ê] +\__,l\ O
É/¬Z/-<š
Í;
O
,I
I, WML
o
O
-O
doda
Pzgura
1,88
i
|
Z/¬Z+
dota
28 - Fórmulas
estruturais
O
4-
dos ligantes doda e dota*
pKa do prinleiro grupamento amônio
é estabilizado
Ka
log KÃa5 log
é elevado
porque este
por ligações de hidrogênio intramoleculares
demais grupos amino do ligante (Figura
29).
A iprotonação
com
do segundo
grupo arnino ocorre no outro nitrogênio básico que está na posição
primeira protonação, portanto na outra amina secundária
Estima-se que a protonação das aminas
terciarias
soluções extremamente ácidas, por serem muito
menos
os
trans à
do macrociclo.
deva ocorrer
básicas
de
em
estarem
compartilhando os prótons das demais aminas protonadas no anel
macrocíclico.
`
-
45
R\
r
+
N~~~H-N
H
H
N-H»-‹--N
/¡,,".
\
z
R
,Í
'/
Fzgura
29 - Ligações de hidrogênio intramoleculares no
ligante
tetraazamacrocíclico substituído.
5.6 Titulação potenciométrica
A curva de titulação
quando comparada com
(Figura ʛ0b), apresenta
que dois mols de
do
sistemf;_:ÍCu(II)-Lê
do sistema
metal-ligante' Cu(II)-L3 (Figura 30a),
a curva potenciométrica
novamente
do
a primeira inflexão
ligante
independente
em a=2,
significando
KOH neutralizam dois mols de prótons para cada mol de
em solução, em valores de pl-l abaixo de 4,00. Ocorre uma
segunda inflexão em a=4, indicando a neutralização de mais dois mols de
próton para cada mol do sistema metal-ligante, que ocorre na faixa de pH =
ligante e metal
5,00
- 7,00.
'
-
46V
12
10-
b
a
3..
IQ.
_
(,_
4..
2¬
|
|
0
|
|
|
|
|
2
1
3
|
|
|
4
|
|
5
|
6
3
Fágura
L3e
30 - Curvas de
L3, a
titulação potenciométrica para os sistemas (a)
Cu2+-
T = 298,15K e u=O,1001no]L`1 (KNO¡,); a = mmol de base
adicionada/ mmol de ligante.
A proporção rnetalzligante é 1:1.
Esta situação é crucial para a confirrnação da presença da espécie L2`
em
valores de p[H] elevados e indica que, devido ã elevada constante de
formação do complexo neutro, a primeira protonação do
reduzida consideravelmente
ligante L3 é
em cinco unidades logarítmicas.
A figura 31 mostra o diagrama de distribuição das espécies formadas
do sistema
metal-ligante
em
função da variação de p[H] e
visualização das constantes de formação e protonação
L,
47
auxilia
na
do complexo Cu”-
10°
Yšunzi.
90
"-
'
cut.
^
aovo°/:
âo
1-
50‹-éoff-
30%zo
-
10
«-
U
it
I
2
4
3
5
L
7
6
P
9
8
4
10
~
1
11
12
.
-1°â[f¬I1
Fzgura 3 7
L5
- Curvas
de distribuição das espécies formadas nctsistema Cu2+-
em função do p[l-I] a T=298,2ÍO,1K e u=O,1OOmolL`1 (KNO3). CuL é o
complexo normal e CuHL e CuH2L são espécies mono e diprotonadas.
Nota-se que
do complexo neutro
deste a presença
torna-se
em p[H] acima de aproximadamente 6,0, a formação
CuL é predominante, assim como em valores abaixo
do complexo duplamente protonado (CUHZL) também
majoritária.
Em
suas
respectivas
representam cerca de 99,5% das espécies
escalas
em
solução,
elevada constante' de formação deste complexo de cobre.
Apenas uma
p[H], a espécie
formada
em
fração de outra espécie aparece
monoprotonada
solução.
A
CuHL.
Em
espécie diprotonada
diminuição do p[H]. Isto deve-se à preferência
48
de
p[H],
ambas
demonstrando a
l
em uma estreita
faixa
de
35%
logo se forma com a
do íon Cu* em formar
p[H]=5,90, ela está
provavelmente
uma
espécie apresentando geometria quadrada,
complexo proposto CuH2L (Figura
como o
32).
|l'I,II
/'CN
~
\z
Ó E?ÍO
H1\§HN
o~
I-1i\IH
~
f
O
1/I/
Fágum 52 - Fórmula
estrutural sugerida para
CuH2L formado em solução
O
complexo CuL predomina
provavelmente
é
formado na
átomos nitrogênio amínicos
axiais.
ligação
o
ligante L3 e
em
valores
do íon cobre
e os carboxilatos
o íon cobre
de p[H]
(II)
com
'
(II).
>
6,0
e
os quatro
coordenados nas posições
-
me
Os
cobre
entre
o complexo diprotonado
valores obtidos para a constante de formação
em
juntamente
solução
com
em
encontram-se na Tabela ll,
os valores das constantes de protonação defloutros
complexos de cobre (H)
condições de
função do
do complexo de
com
ligarites
semelhantes para comparação
mesma força iônica com um eletrólito não coordenante.
49
em
Tabela
11:
L3,
Cu-dota e Cu-doda
K
Log K
Dota
Doda
21,ó1:o,o3
29,80
21,1
5,sõio,oõ
3,77
3,0
5,88Í0,03
3,78
*
L3
|CuHL+|
[Cum [H+¡
[cuH_2L2*
[CuHL¬f] [Ef]
_
'
”"./*rparentemente
não é observada a formação do compleso
Estes resultados indicam que L3 coordena para a formação
um
como um
ligante
complexo
tetra,
»
s
mil[CW] [Ú]
':
298K para o Cu-
Constantes de complexação e de protonação a
com
estabilidade significativa,
podendo
atuar
penta ou hexadentado, provavelmente complexando
átomos de nitrogênio
menor que
terciário e os dois terminais
6,00.
com
propiônicos
os dois
em
p[H]
_
Em comparação com os demais ligantes, L3 apresenta a constante de
formação do complexo
ligante di-acetato e
CuL
intermediária, levando
um pouco menor que
deve estar relacionado
com
a carga global
número de centros de coordenação do
As duas demais
com
espécies
vantagem sobre o
do
ligante tetra-acetato. Este fato
do
ligante
em
solução, e o maior
ligante dota.
~~
z
possuem constante mais elevada do que
os outros ligantes, porque passa a predominar a estabilização pelo
efeito macrocíclico.
Os
íons de cobre
ligarem-se a ciclos e quatorze
átomos
33), ajustando-se perfeitamente
(ll)
com
possuem maior
preferência
nitrogênios coplanares (Figura
na cavidade deste macrocíclico,
50
em
e desta
forma torna-se mais
anel macrocíclico.
fácil
para o íon Cuz* deslocar os prótons contidos
`
-
/\_
logwlí
A
u
O
no
L._..v_.J
*-*
_2 _.
l
-3_¡
:1
12
1
A
|
Í
14
15
|
_1ó
Tai nanlao do anel macrocíclico
V
Fzgufzz
I
›
|
'13
CU2-W
33 - Gráfico de variação da estabilidade (Aloglí) de cobre
relativo aos ligantes macrocíclicos
com anéis
(Il),
de doze a dezesseis átomos
contendo quatro átomos de nitrogênio doadores.”
O
preserva
ligante
sua
que combina anéis quelantes de cinco
conformação
tram-III
membros
quando complexado com cobre,
variando pouco a enttopia total do sistema.
51
e seis
l
-
6
O
~
CONCLUSOES E PERSPECTIVAS
em
ligante LI é obtido
formação de vários subprodutos.
com
baixo rendimento de síntese, devido à
Em contrapartida a sua síntese é efetuada
reagentes de relativamente baixo custo, o que foi primordial para
síntese dos outros três ligantes, L2, L3 e L4.
foram obtidos
em excelente rendimento
Todos os ensaios
até
aqui
Dentre
de síntese
efetuados
eles,
L3 e L4 são novos e
em relação ao ligante LI.
indicam
a
eficácia
da
metodologia utilizada na síntese destes novos ligantes contendo .grupos
doadores pendurados, sendo que tentativas de obtenção de monocristais de
L3 e L4 para determinação estrutural por raios-x foram realizadas até o
momento sem
sucesso.
Novas
recristalizaçöes variando os solventes estão
sendo desempenhadas, no intento de obter monocristais.
A
eficiente,
novos
metodologia de síntese dos complexos também demonstram
servindo
como
base para a síntese de futuros complexos
com
ser
os
H
ligantes.
O
complexo Cd2+-Lg
é
formado rapidamente na sua
solução, o que se torna interessante
A
síntese -em
do ponto de vista ambiental.
elevada constante de formação do complexo Cuz*-L3 reflete na
prática a influência
do
efeito macrociclico
aliada ã adição de grupos
funcionais doadores pendurados, sendo o complexo
formado
solúvel
em
toda a escala de
Será interessante efetuar
um
organismo vivo para
um estudo
do metabolismo deste
avaliar a possibilidade
ligante
de utilização deste
tratamento quelatoterápico, verificando se o complexo de
um
metal
em
em
em
questão é expelido pelo organismo sem efeitos colaterais ao paciente. Este
estudo pode ser justificado pelo fato que o agente quelante possui algumas
características necessárias,
complexação na
estável
faixa
a solubilidade
água, capacidade de
um
complexo
está relacionado a diversas patologias.
pretende-se posteriormente avaliar a seletividade a outros
metais de importância medicinal,
Com a adição
como o Fe(lII)
por
e Zn(lI).
de átomos de oxigênio neutro ao ligante L4, pode-se
buscarvestudos de seletividade deste ligante ao
é responsável
em
de p[H] fisiológico e formação de
com o cobre, que
Também
como
efeitos tóxicos
chumbo
nos organismos vivos
53
(ll),
o qual também
7
01.
LINDOY, L. F.,
BIBLIOGRAFIA
ofMaorog1olz`t Lzègand Comíblexes,
T/:fe C/yefnzlvtzy
Cambridge
University Press, 1989.
02.
MELSON,
40,
03.
G. A., Coordination
Plenum
IZATT,
C/Jefnlstgø
of Maorog/clio Cornponndi, p. O2-
London, 1979.
Press,
R. M., Christensen,
J., Synt/oesz`i^
of Àlamgoles
& Sons, New York, 1987.
KIMURA, E., Shionoya, M., Mim, T. Yoichí,
john Wfley
Appended Inzidazole.
Interaction wit/J
HAINES,
R.
I.,
A I\7ew Q/olafn
an
Wit/9
T/oe First Bz`ofnz`metz`o Lzgation of Inzidazole for Axial
Chem.
Metal Ions,
1714, 1987.
05.
Deózgn of
T/Je
Conzplexzng Agents, Progres in Macrocyclic Chemistry, V. 3,
.Íeletioe
04.
-`
Soc.,
Chem, Commun.,
p.
rr-
1712A
'
Hutchings, D. R., McCormack, T. M., Platinum
I.,
Carboâgflatoyfiendant-arm Maorogclex: Stmoture,
Redox
Journal of Inorganic Biochemistry,
oanoor Potentíal,
and Anti-
Pnr¿~pen*z`e.v
V. 85, p.
01-07,
L
2001.
06.
KONG,
D.,
Meng,
L.,
Ding,
L{gand
Tetraazamaorooz'olz`o
J.,
Xie,
Y., .I~Iuang,
Gmtçxf
Neutral Pendent
wzt/9
and
tetra,êz`s{2-9/anoet/9/l}7,4,7,70-tetraazag/clododeoane
and
Niozêel
C/Jaraoterífzation
2000.
07.
(II)
Cornplexes:
ítƒ
7,4, 7,70-
Cobalt
Ájfnt/Jeóis,
and Antltumor Attíoig, Polyhedron,
I\Teu/
v. 19, p.
(II),
Structural
217-223,
.
Kong, D., Qin,
Cl2araotm`zatz'on
u/it/J
Copper
X.,
C.,
Men,
and Xie, Y.,
L.
and Antztumor Actíoígt
Tetraazafnaoroglclio I_1;gand,
Ez/alnations of Cooper
Bioorganic
Letters, V. 9, p. 1087-1092, 1999.
5)/nthexzbj.
&
Structural
Complex
Medicinal Chemistry
08.
Kong, D. and Xie, Y.,
.$`tudz`e.‹
.Q/nt/Jeszk,
Straetura/ Characterization
and Potentz`ornetrz'ø
of Diva/ent Meta/ Complexey with na Octadentate Tetraarza/naorog/o/ie
Ligand and
t/yeír
DNA
Polyhedron,
C/eaoageabí/z`§/,
V. 19, p.
1527-
~
1537,2ooo.
09.
LITERATURE HIGHLIGHTS,
Tranƒztzon Ãletalf in
and Terzpy,
Dz`agnoó*z`.r
H
Transition Metal Chemistry, v. 18, p. 439448, 1993.
10.
LEWIS,
S.,
and In
`
_
Srinivasan, A., Schmidt,
Vino
wit/2
Medicine and Biology,
11.
KOTHARI,
A.,
Anderson, C.
J.,iIn Vitro
of 64Cn-TETA-Íjflrg-Oetreotate.
Eva/nation
Ana/og
.Yornatostatín
M.
Innbrooed
V. 26,» p.
Taget
Tísxne
Uptazêe,
267-273, 1999.
K., Samuel, G., Banerjee,
S.,
A
New
Nuclear
J
_
Unni, P. R., Sarma, H. D.,
cmmmm¢IxR,Ummúmmm¶iP,Hm¿mlRna/“nwnfinr
tetraazagyelotetradegll- 7,4, 8, 7 7-tetrarnet/_oy/eng)/Joip/oonie _/Í cid:
for
Po.v.rz'1e[e
use in Metaƒtatie
Bone
Pallíatíon,
Biology, V. 28, p. 709-717, 2001.
12.
A
1\7ooe/ Agent
Nuclear Medicine and
_
DADACHOVA, E., Chappell, L. L., Brechbiel, M. W., .Yjbeotrop/Jotornetrie
Met/Jod for Determz'natz`on of Bdnnotional Maerog/e/io
I_z;gand-Protein Cafyngates,
I_.zgand.f in
Nuclear Medicine and Biology,
Maoroglelíe
V. 26, p.
977-
982, 1999.
13.
WAINWRIGHT,
K.
P.,
of Chemical Society, Dalton
Journal
Transactions, p. 2117, 1980.
14. Stetter, H., Frank,
15.
WAINWRIGHT,
W., Angew. Chem.
K.
P., Ájlnt/Jetie
Int.
Ed. Engl.,
and Structural
p.686, 1976.
V. 15,
aipeets
of t/Je C/Jemzktg' of
.Yaturated Poá/aza Maeroglo/ie L1;gand.f bearing Pendant Coora'z'natz'ng Grozqbs
attaebed to Nztmgen,
Coordination Chemistry Reviews,
V.
166, p. 35-90,
1997.
16.
COSTANIAGNA, J., Ferraudi,
Canales,
J.,
G., Matsuhiro, B., Campos-Vallette, M.,
Villagrán, M., Vargas,
55
J.,
Aguirre,
M.
J.,
Cofnp/exe: of
Maerogieles
11/it/9
Army
Pendant
_
'
17.
Coordination Chemistry Reviews,
ANDRÉ, J.
Model; for Biological Moleoules,
v. 196,
p.125-164, 2000.
P.,Mz@¢1<¢, H. R., zehnâez, M., Mzzko, L.,A1<yz1, K. G.,
Aeid
7,4,7-Triafzaglelononane-7-sueoinic
New Bzfunetiona/ C/Jelatorfor Radio
Commun., p. 1301-1302,
18.
ax
DISCHINO, D.
Prasad,
4, 7 -diaeetio
Galliufn-labellin,g
D., Delaney, E.
A
Chem.
of Biornoleoi/lex,
1998.
V
J.,
Emswiler,
M.
Srivastava, S. K., Tweedle,
S.,
Aoid fl\TÓDA.ÍA):
F.,
Gaughan, G.
T.,
F., S)/nt/Jeszk of Nonz`onz`c
Gadoliniurn C/Jelaíes Usgfnl as Contrast Agents for Ma¿gnetie Reƒonanee
Iinaging.
7,4, 7-T1^zÇr(ear11o>g/nzet/9/0 7 O-.fii/9§íz'z*ated- 7,4, 7_,
teíraafzagfelododeeaney
Chem.,
19.
V. 30, p.
KODAMA,
and
1\»Í._,
and Their
Correó]bondz'ng Gadolininfn C/yelates,
of
.S`tndie.v
Lant/fianide
B.,
Kimura, E.,
Coniplexes
T/Jerrnoaj/nafnie
7,4,7,70,73-
of
7
Peníaazag/elopentadeeane-I\Í.1\7,N ”,1\7 "Í.N ””¡beníaaeetio
7,-4,7,
Inorg.
1265, 1991.
Koíke, T., Mahatma, A.
Kz`netiø
70-
Aeid
and
70, 73, 76-Hexaazaglolooetadeeane-1\7Í.1\7'Ç1\7”Í.I\7””fl1\7”'”-/Jexaeetie
Acid, Inorg. Chem., v. 30, p. 1270-1273, 1991.
20.
CHARTRES
transition
D., Líndoy L.
Metal
.SJ/:tenis
.Ytmetnral Elernents,
F.,
Meehan G.
Ineonvorating
linked
V.,
Tran.riz*ion
J)/ntbetie
Coordination Chemistry Reviews,
and Post-
Maorogle/es
V.
ay
216-217, p.
249-286, 2001.
21.
HANCOCK,
Recognition,
22.
R. D., Molecular Meo/oanióiv Calenlations and Metal Ion
Acc.
Chem.
Res., V. 23,
253-257, 1990.
MARTELL, A. E., Clarke, E. T., .ffabilzfies of í/Je Fe(UI),
ay'
l\7,1\.TÍ.1\T”-mazag/e/ononanemaeetie Aóid,
181, P. 275-280, 1991.
Ga(IH)_and In([II)
Inorganica Chírnica Acta, V.
3
só
MARTELL,
23.
A. E., Clarke, E.
T., ftahi/ities
Meta/ Comp/exe: of
Diz/a/ent Tramition
the
A/ka/ine Earth and
the Tetraafzamaeroglo/ie Tetmaeetio
Aoid I_1;gand.r, Inorganica Chimíca Acta,
24.
cy"
190, p. 27-36, 1991.
V.
MARTELL, A. E., Clarke, E. T., .Ytahi/ities of Trina/ent Meta/ Ion Comp/exex
of the Tetraaeetate
Dera?/ate.f
of 72-, 73- and 74-menzhered Tetraazanzaerogfe/es,
Inorganica. Chíxnica Acta, v. 190, p. 37-46, 1991.
STUDER,
25.
M., Kaden, T. A., One-step
Afzafnaerg/o/es with
C/+
with
and
a
Carhoâgflie
Growo
in the Side-chain
Helvetica Chjrnica Acta,
l\7i2+,
zy'
5)/nthe.ris
_
Mono-1\7-snhstitzited
and
v. 69, p.
1986.
D., Basak, A., Kaden, T. A.,
R., Siegfried, L. C.,
Congo/exation Properties
zy'
Earth-a/ka/i Ione, Helvetica
OBERHOLZER,
M.
R.,
Kaden, T. A.,
Chímica Acta,
Neuburger,
Efiíeots in the Copj>er(II)
INT.,
with
shzúlqee,
M.
Mixed I\7itrogen- and
KOVACS,
Z., Sherry,
with
Zehnder, M., Kaden, T. A.,
Tetra-1\T-a/zé)//ated
R
v. 78, p.
505-
D., szfza//Aozzmfyz/zz Lzgzzzdf
Oâgzgen-donor Atorns, Inorganic Chemistry, V.
A. D.,
7,4,7,70-tetraazag/o/ododeeanes,J.
186, 1995.
and
140-153, 1990.
Helvetica Chimica Acta,
S., Hzzzzmzzê,
25, p. 2992-3000, 1986.
30.
V. 73, p.
and Nz`e,êe/ Comp/exe; with
513, 1995.
THÓM, V. J.,
Protonation .ftudies
Tetraazanzaorg/e/io Met/:]))/eneybhoóphonates
7,4,8_,77-tetraazag/elotetradeoanes,
29.
71, p. 100-106,
V.
'
DELGADO,
.Yterie
and _S`peotra/P1^ope1tz'es
7,4,8-trifneth)1/-7,4,8_,77-
Helvetica Chímíca Acta,
1988.
28.
S)/ntheszb'
of Cid* Congo/exe: with Mono-1\7fanotiona/ized
tetraazagfe/otetradeeanes,
27.
2081-2086,
_
26.TSCHUDIN,
V
their Congo/exe;
A
General
Chem.
'
.
57
Soc.,
Syntheszflv
of 7,7-dixuhstinzted
Chem. Cornmun.,
p.
185-
BU,
31.
Fu1zetz'onalz'zed
~
Zhang, W. Zhang,
X., Cao, X.,
a
u/it/9
Peadam* Pjriefifl Groøeps:
Coazfp/ex
Copper(II)
R.,
A
New
5]/nt/oeƒzb'
Tetraazamaerog/e/e
and Czyfta/ .Yímeture of
7,4,7,7O-tetrakzk(2¡Dy1ieÚ/metly/A7,4,7,70-
zy'
Chem.,
tetraazagw/ododeeane(L), [CuL].(C/O4)2, Transition Met.
513-515, 1997.
32.
'
'
_
V
ALCOCK, N. W., Balakríshnan, K. P., Moore, P., Preíbaratíofl of 7,4,8,777-tetraazagw/otetradeeane (LI)
tetra,èzlr(2-p)1rz`aj//mef/y1/)-7,-4,8, 7
Comp/ex
CHE,
12/it/2
u/it/9
Cop_,Óer(II
Dalton Trans.,
Soc.,
33.
v. 22, P.
C.,
p.
X-Rg Síraeture of [Cu_,L7Br2][C/O,¿]2,
Amíne
1\T6--eo-ordz`rzaz*ed
Chem.
1743-1745, 1986.
Tang, W., Mak, T. C.
C/ye¿'atz`n<g
and a Bínaelear
\X'.,
Co-ordzhatzon C/yemzkízy of Rat/oeniam
Lz;gand.f.' .Sjlnt/vem"
Rat/¶erzz'am(II)
and X-ray Símetara/ Staefl of t/oe
g'
Comp/ex
Chem.
7,4,8,77-tetraazagfe/oíetradeeane,
7,4,8-,77-íetra×êzlv(2¿b_yn'e@'/met/9/Q
Soc.,
Daltfm Trans.,
p.
2879-
2883, 1988.
34.
ASATO,
E. Hashimoto,
Structure,
Matsumoto, N., Kída,
S.,
and Quasz'-reoerszb/e Dioàggea
Bz'1zdz'ng
S., Synt/JeĒs,
of [Cu({z9me)X¿] [game
7_.4,8,77-tetrazëzLf(2”¡1>]n"a§›/met/ylfl-7,4,8,77-tetraazage/otetradeeafie;
Chem.
C/O4, P135, of CF,SO,],
Czysta/
X
=
=
Soc. Dalton Trans., p. 1741-1746,
1990.
35.
MEUNIER,
Synt/aesis
and
.fulaftzíated
36.
I.,
Míshra, A. K., Hanquet, B., Cocolios,
A.
S.,
Guílard, R.,
of Varioux Unsubxtítuted and Mono-1\Í
C/2aracten`zatz'on
Tetraazamaemgw/ef, Can.
BATSANOV,
P.,
Chem.,
v. 73, p.
Goeta, A. E., Howard,
685-695, 1995.
A. K., Maffeo, D.,
A
Puschmann, H., Williams,
Tefraazamaemg/e/ie .Ugaads
A. G.,
7, 7 7-
I\7z`ezèeZ(II)
Coaplexes of the Iƒomeríe
and 7,8 -bzk(2¡Dyrz'a§'/metizy/)-91:/am aad of a
Stmetara/_ly Constrazaed N4, 1\7€~mef/9//eae Bnidged Ana/qgue,
20, P. 981-986, 2001.
58
Polyhedron,
V.
37 BU, X., Zhang, Z., An, D., Chen, Y., Shionoya, M., Kimura, E.,
Cpuía/ Strnotare of a
5)/nt/Jesis,
Met/;)//qnino/ines ay Additional
V.
Now
Dioxog/o/am Appendea'
FVit/J
Tu/o 8-
Donor Pendants, Inorganica Chimica Acta,
249, p. 125-130, 1996.
38 VUEEKS,
M., Max, R., Wainwright, T., \X/ainwright, K. P., Formation
Conrtafztsfor Comp/exe; of 7,4,7, 70-tetraazag›o/oa'oa'eoane-7,7-dzaoefio acid ana'
í/ae
Cgfslal .ftmotnre of
its l\7io,êe/(II)
Chem.
Congo/ex,
Trans., p. 317-322,`199»7.
39 ELIAS, H.,
Kineíio:
7
and Meo/Janzlvm of Meta/ Cony)/ex Forznation
Donor Ãlaorog/o/es of í/ao Q/o/am
v. 187, p. 37-73,
40
MARTELL, A.
Modern
41
E.,
1992.
42.
11/it/2
N
4-
Coordination Chemistry Reviews,
1999.
~
Hancock, R. D., Meta/ Comp/exeƒ
in
van, Sherry, A. D.,
Aaneons
Solutions,
New York, 1996.
Biooo1y`i¿gate Cbemzktgf, V. 3, p.
524,
_
HARPER,
H.
Fisio/ozgioa,
43
Íjpe,
Inorganic Chemistry Series, Plenurn Press,
\7§ÍESTRENEN,
Dalton
Soc.,
A., Rodwell, V.
5ed.,
GAULTIER,
W., Mayes, P.
A.,
Manual
de ,Qnnnioa
São Paulo, Ed. Ateneu, 1982.
-
M., Toxicologia
Radzobato/ogia,
Ed. Expaxs, Barcelona,
1973.
44
.
APOSTOLI,
Poi.roni'ngs,
45
P.,
Della Rosa, H; V., Alesio, L.,
C/ae/ation
Therapy of [Metal
Revista Brasileira de Toxicologia, v. O5 n.1 / 2, 1992.
SCHVARSTSNIAN,
S. Iníoxioa§õe.rA¿¿iidaƒ, 3ed.,
Ed. Savier, São Paulo,
A
1995.
46 LARINI,
To'xioo.r,
L.,
Carvalho, D., Salgado, P. E. T., C/onrnbo: Eêgbosioão
e
Efezíos
Revista Brasileira de Saúde Ocupacional, v. 37, p. 13-18,
1982.
_
V
47 Schwartzenbach, G., Flaschka, H., Conip/exomemk
CO LTD, London, 1969.
59
Titraíions,
Methuen
8:
48
MARTELL,
Constants,
49
A. E., Motekaítis, R.
and Use
Deterrnination
J.,
V CH Publishers, Inc., New York, 1988.
BUSCH, D.
H., Maorog/o/io Ligands and
t/Jeir
,
Meta/ Congo/exes, Inorganíc
Synthesis, v. 18, p. 1-52, 1978.
50
BUSCHNELL,
Chemistry,
G. W.,
'
Fortier,
D.
G.,
52
SMITH, M., Oganio S)/nt/aesis, MacGraw-Hill,
STREITVVIESER,
p.
McAuley, A., Inorganic
.
cURT1s, NF., J. Chem.
C/:1efnistg.',
~
27, p. 2626-2634, 1988.
v.
51
53
ty" Síabi/z`Zz`es
soz., P. 4409, 1960.
A-. Jr.,
1994.
Heathcock, C. H.,
'
Introduction to Organic
755-758, Macmillian Publishing Co., Inc.,
New
York,
1976.
54
MoRRow, 1.
ftmotiøre,
R., Aniân, s.,
and
IÍQfnamz"o
Lake, c. H., chuzzhíu,
Propenies of
t/Je
R., syzzz/zm,
Cony)/ex of
Lant/9annfn(III)
Inorganíc
7,4, 7, 70-z*eíra,êz`s(_°- oarbanio)//et/91/)-7,4 , 7, 70-teíraazagw/ododeoane,
chemiszzy,
55
V. 32, P.
SILVERSTEIN,
56
R. M., Bassler, G. C., Morríl, T. C.,
of Oøganio Coniponnds, 4ed., p. 312,
Identification
Inc.,
'45óó-4572, 1993.
New York, 1981.
DAVIES,
P.
and
Tez*raazainaorog'sZes
Con¢/exes, Inorganíca
57
TURONEK,
M.
\X/'aínw1:ight,
K.
its
Chjmíca Acta,
tetraafzagfo/ododeoane
/9/droâglet/5//)-7,4_.8,
NÍ
t/ae
P.,
&
Sons,
3-Eb/dmâgpmpy/atz'on
Stabilig/
V. 294, p.
and
1\T”_.
ÚÍHEC-72)
G.
S.,
Lincoln,
.N"'-tetra,êis(2-(1)/dmàgfet/zyi)-7,4,
72-tetraazag/o/qbeníadeoane
Chirnica Acta, V. 230, p. 55-57, 1995.
60
of Diva/em* Meta/
S. F.,
Kinetic Studies of Cony)/exes of
and
l\7,
of
103-108, 1999.
P. A., Laurence,
P., Boni'/z'briuin
Pendaf Donor Masrog/des l\T_,
-
Ejëot on
Duckworth,
L.,
john Wfley
`
\X/AIN\X/RIGHT, K.
J.,
.Ypeotroinetiio
t/ae
7 70,
1\7Í.l\7”Í.,Z\T"'-tetrazêz`s(2-
(IÍHEG 75),
Inorgzmjca
58.
MADEYSKY,
C. M., Michael,
Hancock, R. D.,
an I\T-Donor Macrog/ele
tetra/êz`.v(2-/9/droâgfet/9'/)gw/afn,
BUQEN,
Dale,
S.,
J.,
Groth,
Krane,
P.,
60.
Soc.,
LUCKAY,
Rapid
R.,
Chem., Commun.,
p.
J.,
M
»
_
7,4,,7_,70-tetrazêz'.r(2-
1172-1174, 1982.
Hancock, R. D., Cukrowskí,
I.,
Reíbenspies,
H., Stnaj/
q' Pmtonatian
of 7,4,7-m's(2-/y/dm>gfet/y/)-7,4,7-hiazag/c/ononane,
Conga/exe;
u/it/2
Meta/
159-169, 1996.
BELLAMY,
108,
62.
L.
Infrared
L.
its
v.
246, p.
.
J., T/ae I1¶?^ared
Spectra of Congúlex-Ãloleôn/es, v. 01, 3ed., p.
Chapman and Hall, London,
BELLAMY,
and
Ions, @1 Cg)/sta//ograp/9)/, P0/arograply/, Potentio/netgf,
M0/em/ar Mec/aanzks and 1\T_MR, Inorganica Chimíca Acta,
61.
eíalatíon
a .fímng Catíon Conzplexer,
/9)ÊzL^›g'et/9'/)-7,4,7,70-tetraazag/clododecane:
Chem.
n/it/2
l\7,I\TÍ,1\T”,I\T”'-
Inorganic Chemistry, V. 23, p. 1487-1489, 1984.
Reactions,
59.
P.,
J., T/ve I1g9"ared
Grant Frequencia,
1975.
Spectra of
Comp/ex Mo/eva/es
Chapman and
- Advances
in
Hall,
London,
de Eópectmƒcopia Vz`1n^a:z`0na/, p.
210-259,
V. 02, 5ed.,
1
1980.
63.
BUENO,
.
\X/illíe
A.,
Manual
McGraW-I~Hll, São Paulo, 1990.
61
8
ANEXO
^O
mwõ
_
AOE
É
_”
Avg
í
ão
//á
_
`
/N." p\ã
:N55
~
_”
¬\
Ê?_
/_
~
~
šõ
ÉZ
__
,
/%%V`/Q
52
,
Q
$,
V
K
^mõ(`
Añöõ
âvš
~
~
W
ä
š
4
E5
\'
É
Emi
/,¡/L
si
AO
mW
O
"¶,
Q
šz
532%/4% _§
õõ
à
6%
Q/
\â
_`
~
\w
w
SU
~
_›_/H_______""
,Í
E5
xble 1.
Crystal data and structure refinement for
ientification code
picol
mirical formula
C8 H20 N2 O
›rmu1a weight
160.26
:mperature
293(2) K
âvelength
0.71073 A
rystal system, space group
xit
Tetragonal,
I4(1)/a [no. 88]
a = 18.646(3)
cell dimensions
b
=
c =
Calculated density
A
18.646(3) A
12.0l1(3) A
4175.9
zlume
16,
(14)
?.
alpha
beta
gamma
deg
deg
= 90 deg
= 90
= 90
A^3
1.020 Mg/m^3
›
>sorption coefficient
0.068 mm*-1
(000)
1440
:ystal size
0.40 x 0.45 x 0.50 mm
:eta range for data collection
2.97 to 25.00 deg.
xdex ranges
-15<=h<=22, -22<=k<=15, 0<=1<=14
eflections collected
ampleteness to Ztheta
unique
/
=
25.00
restraints
/
parameters
>odness-of-fit on F^2
Lnal R indices
_
/
1826 [R(int) = 0.0449]
47.1%
Full-matrix least-squares on F^2
:finement method
ata /
3599
[I>2sigma(I)]
indices (all data)
1826
/ 0 /
115
1.145
R1 = 0.0446, wR2 = 0.0974
R1 = 0.1311, wR2 = 0.1533
<tinction coefficient
0.0042(6)
argest diff. peak and hole
0.147 and -0.142 e.A^-3
64
Table
3.
Bond lengths
N(1)-C(3)
N(1)-C(2›
N‹2›-c‹4›
N(2)-c‹5›
c(1)-c(2›
C(2)-C(7)#1
C(3)-C(4)
C(5)-C(8)
C(5)-C(7)
C(5)-C(6>
C(7)-C(2)#1
c(3›-N(1›-c‹2)
c‹4)-N(2)-C(5)
N(1)-C(2)-C(7)#1
N(1)-C(2)-C(1)
C(7)#1-C(2)-C(1)
N(1)-c‹3)-c(4)
N(2)-C(4)-C(3)
N(2)-C(5)-C(8)
N(2›-c(5)-C(7›
C(8)-C(S)-C(7)
N(2)-C(S)-C(6)
C‹8›-c‹5)-C(6)
c(7)-c(5)-C(6)
C(2)#1-C(7)-C(5)
[A]
and angles [deg] for
1
4s9(3)
1
471(3)
1
453(4)
1
4a0(3)
?.
1 s26‹4›
1
519‹4›
1 s11(4)
1 s33(4)
1 535(4)
1 536(4)
1 519(4)
113 8(2)
116 s‹z›
110
109
110
111
110
111
107
108
108
109
110
118
9(2)
3‹a›
am
o‹'2›
5(2)
6(3)
8(2)
1‹z›
7(2)
em
vm
$(2)
Symmetry transformations used to generate equivalent atoms
#1 -×+1,-Y41.-2
Table
6.
Torsion angles [deg] for
?.
- 163
C(3)-N(1)-C(2)-C(7)#1
C(3)-N(1)-C(2)-C(1)
C(2)-N(l)-C(3)-C(4)
C(5)-N(2)-C(4)-C(3)
N(1)-C(3)-C(4)~N(2)
C(4)-N(2)-C(5)-C(8)
C(4)-N(2)-C(5)-C(7)
C(4)-N(2)-C(5)~C(6)
N(2)-C(5)-C(7)-C(2)#1
C(8)-C(5)-C(7)-C(2)#1
C(6)-C(5)-C(7)-C(2)#1
7(2)
74 .4(3)
176 3(2)
170. 8(2)
-64 8(3)
57 7(3)
176 3(2)
-63 6(3)
71 .2(3)
- 168
0(3)
-47 7(4)
Symmetry cransformations used to generate equivalent atoms:
#1 -x+1,-y+1,-z
Í
'
66
C18
'CMA
c-|9
Ê?
NsÁ
ft
\Y-'-.=,
cg
~
N_1A
\__\
À
._*z\
A
N4
/
EW
c11A
c1zA
fl/
1'
_
c13A
.
1/
-
¡,
z.-
"\
..
c1o
c1oA
,/
×\
C12@
/
C 11
\
Í
~1
/\
.
J
\
“fl/A
cum
c1sA
Ã.
A
nccn
C11 H21 N3
mpirical formula
195.31
armula weight
emperature
favelength
rystal system, space
group
dimensions
Calculated density
bsorption coefficient
,
[000)
rystal size
heta range for data collection
ldex ranges
eflections collected/ unique
efinement method
K
A
293(2)
0.71073
olume
ata/ restraints / parameters
oodness-of-fit on F^2
indices [I>2sigma(I)]
inal
indices (all data)
xtinction coefficient
argest diff. peak and hole
R
z×
-
Crystal data and structure refinement for NCCN.
lentification code
nit cell
~?
X
1.
ã
Ns
1.
~
c14
CSA
°7~%°5^
4 /""'_
C1
c13
able
*Ê
Triclinic, P-1 [no. 2]
= 8.300(2) A alpha = 111.51(3) deg.
b = 8.814(2) A beta = 115.07(3) deg.
c = 9.755(2) A gamma = 93.61(3) deg.
580.9(2) A^3
2, 1.117 Mg/m^3
0.068 mm^-1
a
216
0.56 x 0.46 x 0.36
2.56 to 26.97 deg.
mm
0<=h<=10, -11<=k<=11, -12<=1<=11
2675/2502
[R(int)
= 0.0121]
Full-matrix least-squares on
2502 / O / 131
1.068
R1 = 0.0429, WR2 = 0.1126
R1 = 0.0557, wR2 = 0.1294
O.232(14)
0.229 and -0.16577 ¢.A^-3
F^2
able 3.
Bond lengths
[A] and angles [deg] for
N(1)-c(11)
N(1)-c(1o)
N(1)-c(1)
N(4)-c(9)
N(4)-C(3)
N(ó)-c(13)
c(x)-c(19)
c(s)-c(1s)
C(3)-C(7)
c(1)-c(7)#1
c(1)-c(14)
c(1o)-c(9)
c(7)-c(1)#1
c(1 1)-c(12)
c(12)-c(13)
1.4ó17(17)
1.47o2(1s)
1.4s24(1s)
1.455s(19)
1.47s1(19)
1.133(2)
1.533(2)
1.53s(2)
1.53s(2)
1.529(2)
1.54o(2)
c<11)-N(1)-c(1o)
c(11)-N(1)-c(1)
c(1o)-N(1)-c(1)
c(9)-N(4)-c(s)
N(4)-c(s)-c(19)
N(4)-c(s)-c(1s)
c(19)-c(s)-c(1s)
N(4)-C(3)-C(7)
c(19)-c(s)-c(7)
c(1s)-c(s)-c(7)
N(1)-c(1)-c(7)#1
N(1)-c(1)-c(14)
c(7)#1-c(1)-c(14)
N(1)-c(1o)-c(9)
N(4)-c(9)-c(1o)
c(1)#1-c(7)-c(s)
112.94(12)
111.37(11)
113.1s(11)
11ó.7ó(11)
1o9.12(12)
N'(1)-c(-11)-c(12)
c(13)-c(12)-c(11)
N(ó)-c(13)-c(12)
Symmeny transformations
#1 -x+1,-y+2,-z+1
NCCN
_1.522(2)
1.529(2)'
1.531(2)
1.453(2)
1
:z3.23(12)
1:.›s.5ó(13)
1o7.4s(11)
1o7.42(13)
11o.só(13)
113.53(12)
113.x2(12)
1o9.7ó(12)
115.s4(12)
112.11(12)
11s.5ó(12)
112.24(12)
112.23(14)
179.o2(19)
used to generate equ1 valen* atoms
Baixar