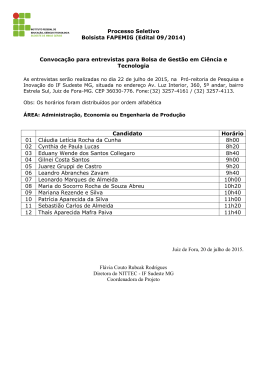
CONCURSO PÚBLICO PARA PROVIMENTO DE CARGOS TÉCNICO-ADMINISTRATIVOS EM EDUCAÇÃO 2012 CATEGORIA: CATEGORIA: TÉCNICO DE LABORATÓRIO/ ÀREA QUÍMICA Atividade 2: (máximo 20 pontos) Com base no slide projetado, responda as questões. a) As vidrarias e equipamentos utilizados na padronização do HCl padrão de bórax (Na2B4O7.10H20), representada na figura, são: (aq) com solução a)suporte universal b) garra metálica c)bureta d) erlenmeyer b) A solução a ser padronizada deve ser colocada: ( X ) bureta ( ) erlenmeyer ( ) suporte universal c) Na padronização, o ponto final da titulação é indicado por qual tipo de ocorrência? Mudança de cor da solução devido à presença do indicador. d) Com as informações mostradas no slide, calcule o volume de HCl(aq) esperado para atingir o ponto de equivalência. Na2B4O7.10H20 + 2HCl → 2 NaCl + 4H3BO3 + 5H20 Relação estequiométrica: 2 mols de HCl/1 mol de Na2B4O7 . 10H20 Como no ponto de equivalência o número de mols do titulante deve ser igual ao número de mols do titulado e seguindo a relação estequiométrica temos que; nHCl = 2x nNa2B4O7 . 10H20 Sabendo que n(número de mols) = C x V, CHCl x VHCl = 2x C Na2B4O7 . 10H20 x V Na2B4O7 . 10H20 VHCl = 2x C Na2B4O7 . 10H20 x V Na2B4O7 . 10H20 CHCl VHCl = 2x 0,1000 mol L-1 x 0,010 L 0,1 mol L-1 VHCl = 0,020 L ou 20 mL e) Supondo que o volume de HCl(aq) gasto na padronização foi de 19,7 mL, calcule a concentração exata de HCl(aq) em mol. L-1. Seguindo o mesmo raciocínio da questão anterior e usando o volume de HCL fornecido na questão, temos que: CHCl x VHCl = 2x C Na2B4O7 . 10H20 x V Na2B4O7 . 10H20 CHCl = 2x C Na2B4O7 . 10H20 x V Na2B4O7 . 10H20 VHCl CHCl = 2x 0,1000 mol L-1 x 0,010 L 0,0197 L CHCl = 0,1015 mol L-1
Baixar