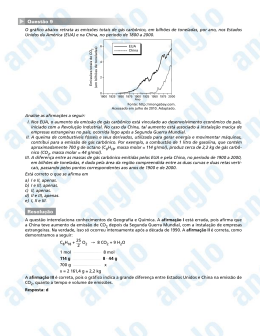
PROCESSO SELETIVO 2009/1 Domingo, 11 de janeiro de 2009 CADERNO DE RESPOSTA DISCURSIVA ESPECÍFICA RESPOSTAS ESPERADAS PELAS BANCAS ELABORADORAS CURSOS • • • • • • • Agronomia Curso Superior de Tecnologia em Agropecuária Curso Superior de Tecnologia em Gastronomia Curso Superior de Tecnologia em Produção Sucroalcooleira Engenharia Florestal Farmácia Zootecnia Identificação do candidato • • • • • • Ciências Biológicas Curso Superior de Tecnologia em Alimentos Curso Superior de Tecnologia em Laticínios Educação Física Enfermagem Fisioterapia NÚMERO ATÔMICO 1 1A 1 H HIDROGÊNIO 3 6,939 4 Li LÍTIO 11 SÓDIO 19 55 40,08 21 Ca CÁLCIO 85,47 38 Cs 87,62 39 Ba BÁRIO Ra [119] [120] RÁDIO Ubn Ti TITÂNIO Lu LUTÉCIO Zr Hf HÁFNIO Lr Nb NIÓBIO B Rf Mo MOLIBDÊNIO Ta TÂNTALO Db Tc W Sg SEABÓRGIO Fe FERRO 10 Ru Re 11 1B Bh Rh RÓDIO Os IRÍDIO (265) 109 Hs HÁSSIO Ni Mt MEITNÉRIO 63,54 30 Pd PRATA 195,09 79 Pt Au PLATINA OURO (269) 111 Cd UN-UN-UNIUM In Hg TÁLIO [113] (277) UN-UN-BIUM Ge GERMÂNIO Uut UN-UN-TRIUM P FÓSFORO As Sn ESTANHO Sb ANTIMÔNIO Pb 114 Bi [115] (285) Uuq S Te Po 116 (289) Uup Uuh Metais Lantanídios 138,91 58 La LANTÂNIO 89 Actinídios (227) 90 Ac ACTÍNIO Superactinídios (121-152) [121] Ubu UN-BI-UNIUM 140,12 59 Ce CÉRIO Pr PRASEODÍMIO 232,038 91 Th TÓRIO 140,907 60 Nd NEODÍMIO (231) 92 Pa PROTACTÍNIO 144,24 61 Pm PROMÉCIO 238,03 93 U URÂNIO (147) 62 Sm SAMÁRIO (237) 94 Np NETÚNIO 150,35 63 Eu EURÓPIO (239) 95 Pu PLUTÔNIO 151,96 64 Gd Am TÉRBIO (247) 97 Cm CÚRIO 158,924 66 Tb GADOLÍNIO (243) 96 AMERÍCIO 157,25 65 Dy DISPRÓSIO (247) 98 Bk BERQUÉLIO 162,50 67 Ho HÓLMIO (251) 99 Cf CALIFÓRNIO 164,930 68 167,26 69 Er ÉRBIO (254) 100 Es EINSTÊNIO 168,934 70 Tm TÚLIO (257) 101 Fm FÉRMIO 173,04 Yb ITÉRBIO (256) 102 Md MENDELÉVIO (259) No NOBÉLIO HÉLIO 20,183 Ne NEÔNIO 39,948 Ar ARGÔNIO 83,80 Kr CRIPTÔNIO 126,904 54 I IODO (210) 85 UN-BI-NILIUM 57 Br TELÚRIO POLÔNIO He 79,909 36 BROMO 127,60 53 UN-UN-QUADIUM UN-UN-PENTIUM UN-UN-HEXIUM [153] CLORO 78,96 35 Se 4,0026 35,453 18 Cl ENXOFRE 208,98 84 BISMUTO F FLÚOR 32,064 17 121,75 52 207,19 83 CHUMBO O SELÊNIO 2 18,9984 10 OXIGÊNIO 74,922 34 ARSÊNIO 17 7A 15,9994 9 30,9738 16 118,69 51 204,37 82 Tl MERCÚRIO N NITROGÊNIO 72,59 33 114,82 50 ÍNDIO 200,59 81 Uun Uuu Uub UN-UN-NILIUM Si SILÍCIO 16 6A 14,0067 8 28,086 15 69,72 32 GÁLIO CÁDMIO (272) 112 26,9815 14 Ga 112,40 49 196,967 80 C CARBONO Al ZINCO 15 5A 12,01115 7 ALUMÍNIO 65,37 31 107,870 48 Ag PALÁDIO 13 Zn COBRE 106,4 47 (266) 110 12 2B Cu NÍQUEL 192,2 78 Ir ÓSMIO 58,71 29 102,905 46 190,2 77 (262) 108 BÓHRIO Co COBALTO RUTÊNIO RÊNIO 58,9332 28 101,07 45 186,2 76 (263) 107 9 55,847 27 (97) 44 TECNÉCIO TUNGSTÊNIO (262) 106 DÚBNIO Mn MANGANÊS 183,85 75 BORO 8B 54,938 26 95,94 43 180,948 74 (261) 105 RUTHERFÓRDIO Cr CRÔMIO 8 7 7B 51,996 25 92,906 42 178,49 73 (260) 104 LAURÊNCIO V VANÁDIO ZIRCÔNIO 6 6B 50,942 24 91,22 41 174,97 72 (226) 103 Fr Uue Y ÍTRIO 5 5B 47,90 23 88,905 40 137,34 71 (223) 88 UN-UN-ENNIUM Sc Sr 4 4B 44,956 22 ESCÂNDIO ESTRÔNCIO 132,905 56 FRÂNCIO 3 3B Mg CÉSIO 87 24,312 14 4A 10,811 6 Elementos de Transição MAGNÉSIO K Rb 5 Be 39,102 20 RUBÍDIO 13 3A NOME BERÍLIO POTÁSSIO 37 (Tabela para uso em atividades e provas) SÍMBOLO 18 0 Ametais 9,0122 22,9898 12 Na (Número de massa do isótopo mais estável) 2 2A 1,00797 Elementos Químicos: Classificação e projeção MASSA ATÔMICA 131,30 Xe XENÔNIO (210) 86 At ASTATO [117] Uus (222) Rn RADÔNIO 118 (293) Uuo UN-UN-SEPTIUM UN-UN-OCTIUM 3 LÍNGUA PORTUGUESA QUESTÃO 1 CIÇA. Pagando o pato. São Paulo: L & PM, 2006. p. 28. Nos quadrinhos acima explora-se a polissemia na língua. Tendo isso em mente, responda: a) Qual palavra contida no primeiro quadrinho é tomada em mais de um sentido pelas personagens? (4,0 pontos) RESPOSTA ESPERADA É a palavra “vivem”. b) Quais interpretações dessa palavra ocorrem nos quadrinhos? (6,0 pontos) RESPOSTA ESPERADA A palavra “vivem” pode ser interpretada como sinônimo de “residem” (é o caso da pergunta inicial dos quadrinhos), mas também pode ser interpretada, em comparação à oposição estabelecida entre “vivente” e “sobrevivente”, como referindo-se a quem tem as necessidades básicas supridas. QUESTÃO 2 “Às vezes, me perguntam se gosto de andar de avião. Não sei responder isso, porque sempre que estou lá o avião só anda um pouquinho. O resto do trajeto ele vai voando”. ÉPOCA, São Paulo, 14 maio 2007. p. 116. Analisando a citação acima, responda: a) Que expressão contida na primeira frase desencadeia o efeito cômico no texto? (3,0 pontos) RESPOSTA ESPERADA É a expressão “andar de avião”. b) Em que consiste esse efeito cômico? (7,0 pontos) RESPOSTA ESPERADA O efeito cômico surge da interpretação literal de “andar” como oposto de “voar”, considerando-se “andar” apenas enquanto se está em contato com o chão. QUÍMICA QUESTÃO 3 Abaixo, são mostradas as estruturas do fenol e do ácido benzóico. OH Fenol O C OH Ácido Benzóico 4 Após a análise dessas moléculas, a) coloque-as em ordem crescente de acidez, justificando o motivo da escolha. (5,0 pontos) RESPOSTA ESPERADA Fenol < ácido benzóico. Isso se justifica, pois o grupo carbonila no ácido benzóico, por efeito indutivo, promove uma polarização adicional da ligação química entre os átomos de oxigênio e hidrogênio, enfraquecendo essa ligação. b) coloque-as em ordem crescente de reatividade diante das reações de substituição eletrofílica aromática, justificando o motivo de sua escolha. (5,0 pontos) RESPOSTA ESPERADA Ácido benzóico < fenol. Os substituintes ligados ao anel aromático do ácido benzóico e do fenol são respectivamente desativadores e ativadores do anel aromático em reações de substituição eletrofílica aromática, o que explica a ordem de reatividade. QUESTÃO 4 A glicose (C6H12O6) sofre combustão completa na presença de oxigênio, produzindo CO2 e H2O. Sabendo-se que nessa reação o sistema era formado por 216 g de cada um dos reagentes, determine a) o reagente limitante na reação. (3,0 pontos) RESPOSTA ESPERADA C6H12O6 + 6 O2 → 6 CO2 + 6 H2O 1mol 6 mol 6 mol 6 mol 1(180g) de C6H12O6 -----------6(44g) de CO2 216 g de C6H12O6 -------------- X de CO2 X = 316,8 g CO2 C6H12O6 + 6 O2 → 6 CO2 + 6 H2O 1mol 6 mol 6 mol 6 mol 6(32g) de O2 --------6(44g) de CO2 216 g de O2 ------------ Y de CO2 Y = 297 g de CO2 Pode-se observar que a menor quantidade de CO2 (297 g) será produzida quando há consumo total de O2. Logo, o O2 é o reagente limitante. b) a massa residual, em gramas, do reagente em excesso. (3,0 pontos) RESPOSTA ESPERADA C6H12O6 + 6 O2 → 6 CO2 + 6 H2O 1mol 6 mol 6 mol 6 mol 1(180g) de C6H12O6 ----6(32g) de O2 W de C6H12O6 -----------216 g de O2 W = 202,5 g de C6H12O6 Reagente em excesso: C6H12O6 Massa residual = 216 g – 202,5 g = 13,5 g de C6H12O6 em excesso 5 c) a pressão, em atm, exercida pelo gás carbônico, caso seja coletado em um recipiente de 200 mL, a 27º C. (4,0 pontos) RESPOSTA ESPERADA C6H12O6 + 6 O2 → 6 CO2 + 6 H2O Dado: R = 0,082 atm.L.mol-1.K-1 180 g de C6H12O6 --------------6(44 g) de CO2 216 g de C6H12O6 --------------Z de CO2 Z = 316,8 g de CO2 PV = nRT → P = 7,2 x 0,082 x 300 → P = 885,6 atm. 0,2 QUESTÃO 5 Em 1911, Rutherford e colaboradores realizaram o experimento mostrado na figura abaixo: CARVALHO, Geraldo Camargo de. Química moderna. São Paulo: Scipione, 1997 p. 15. (Adaptado). Sabendo que as partículas α são carregadas positivamente e de acordo com o contexto e as informações apresentadas na figura, a) comente como as observações colhidas no experimento contribuíram para Rutherford propor o seu modelo atômico. (5,0 pontos) RESPOSTA ESPERADA i. a massa dos átomos constituintes da lâmina de ouro deveria estar concentrada em pequenos núcleos. ii. os núcleos teriam carga positiva, pois sabendo-se que as partículas α são carregadas positivamente, isso explicaria o fato das mesmas, sofrerem desvio de sua trajetória ao passarem muito próximo dos núcleos dos átomos da lâmina. iii. o tamanho do núcleo seria muito pequeno em relação ao tamanho do átomo, o que explicaria a baixa probabilidade de uma partícula α passar próxima ao núcleo ou colidir frontalmente com ele. 6 b) comente a falha do modelo de Rutherford, segundo a física clássica, e como Bohr aprimorou esse modelo. (5,0 pontos) RESPOSTA ESPERADA Segundo a física clássica, uma carga elétrica em movimento irradia continuamente energia. Dessa maneira, o elétron acabar-se-ia colidindo com o núcleo. Bohr, baseado na teoria da quantização de energia de Planck, aprimorou o modelo de Rutherford postulando que: i.os elétrons se movem ao redor do núcleo em órbitas bem definidas, que são denominadas órbitas estacionárias. ii. movendo-se em um órbita estacionária, os elétrons não emitem nem absorvem energia. iii. ao sofrer transição de uma órbita estacionária para a outra, o elétron absorve uma quantidade bem definida de energia, chamada quantum de energia. BIOLOGIA QUESTÃO 6 A diversidade biológica é resultado do processo evolutivo. Fatores como destruição, degradação ambiental, fragmentação de hábitats, aumento do número de doenças ameaçam essa diversidade. O Brasil é um dos países com uma das maiores biodiversidade do planeta, fato que resulta na presença de várias espécies endêmicas. Tendo em vista o assunto apresentado, responda ao que se pede: a) Cite duas possibilidades que fazem com que o Brasil seja considerado um dos maiores centros de biodiversidade do planeta. (6,0 pontos) RESPOSTA ESPERADA O Brasil é considerado um dos centros de diversidade biológica por possuir uma grande quantidade de espécies endêmicas, por estar localizado em região tropical e por ter uma extensão territorial expressiva. b) Por que as espécies são consideradas endêmicas? (4,0 pontos) RESPOSTA ESPERADA As espécies são consideradas endêmicas por que são restritas a determinadas áreas geográficas. QUESTÃO 7 No curso da evolução das plantas, a independência da água para a reprodução, a presença de sementes e o surgimento das flores e dos frutos garantiu às angiospermas um modo bastante eficiente de reprodução sexuada. A respeito das angiospermas, responda ao que se pede: a) A presença de flores coloridas e vistosas é interpretada como uma aquisição evolutiva. De que modo esta aquisição aumenta a eficiência da reprodução sexuada? (5,0 pontos) RESPOSTA ESPERADA A presença de flores coloridas e vistosas possibilitam que as angiospermas atraiam os insetos e outros animais, direcionando o comportamento deles para que polinizações cruzadas ocorram em alta freqüência. b) Em flores que não são coloridas, que fator ambiental contribui para a reprodução sexuada? (5,0 pontos) RESPOSTA ESPERADA Em flores que não são coloridas, a polinização é feita pelo vento. Geralmente, estas flores não produzem néctar e apresentam ovários com um único óvulo por que cada polinização consiste na interpretação de grãos individuais por cada estigma. 7 QUESTÃO 8 Considere o experimento de Mendel, reproduzido no quadro abaixo, em que ervilhas puras para semente amarela e para superfície lisa foram cruzadas com ervilhas de semente verde e superfície rugosa. Quadro 1 – Demonstração do Experimento de Mendel LINHARES, Sérgio; GEWANDSZNAJDER, Fernando. Biologia, Série Brasil. São Paulo: Ática, 2005. p. 388. Ao promover a autofecundação de um indivíduo F1, qual foi a conclusão a que Mendel chegou, quando em F2 apareceram sementes amarelas e rugosas e verdes e lisas? (10,0 pontos) RESPOSTA ESPERADA O aparecimento destes fenótipos de recombinação de caracteres paternos e maternos em F2 permitiu a Mendel concluir que a herança da cor era independente da herança da superfície da semente, isto é, o par de fatores para cor se distribuía entre os filhos sem influir na distribuição do par de fatores para superfície. QUESTÃO 9 Freqüência Em 1978, um pesquisador realizou um levantamento das espécies de algas que ocorriam em um área costeira pouco habitada e desconhecida do Brasil. Passados 30 anos, o pesquisador retornou ao local e encontrou uma situação diferente: grande número de hotéis e incremento do turismo. Encontrou também diferenças significativas na composição (riqueza) e no número de indivíduos das espécies de algas, como apresentado na figura a seguir. 100 90 80 70 60 50 40 30 20 10 0 Nº de Indivíduos Nº de Espécies 1978 2008 Ano a) Elabore uma hipótese para explicar a variação observada no número de indivíduos e de espécies de algas encontradas pelo pesquisador entre os anos de 1978 e 2008. (5,0 pontos) RESPOSTA ESPERADA A variação observada no número de indivíduos e de espécies pode ser explicada pela crescente urbanização e ocupação das margens desta área costeira, ocasionando uma contínua degradação, levando a grandes modificações em seu entorno e a inúmeros danos ambientais, como enriquecimento da água com nutrientes, afetando os organismos de forma diferenciada e provocando distúrbios que alteram a comunidade de algas. 8 b) Considerando o aumento exponencial observado no número de indivíduos até o ano de 2008, o que se espera que aconteça com esse número nos anos subseqüentes? Justifique sua resposta. (5,0 pontos) RESPOSTA ESPERADA Uma diminuição no número de indivíduos, visto que uma hipótese é que com o incremento da eutrofização ao longo dos anos subseqüentes perturbará a dinâmica populacional desta comunidade de algas ocasionando um decréscimo e alternado a composição específica. Outros fatores que podem fazer com que ocorra essa diminuição no número de indivíduos seria a toxicidade de compostos orgânicos antropogênicos presentes nos esgotos domésticos e industriais não tratados, já que a área está urbanizada. QUESTÃO 10 Leia o fragmento a seguir adaptado do texto “O Ovo foi o grande salto da vida”, de Isaac Asimov, escritor russo que, além de obras de ficção científica, escreveu vários textos de divulgação científica. [...] Foi o desenvolvimento do ovo amniótico que possibilitou tudo o que existe atualmente, inclusive o ser humano. ASIMOV, V. I. Ovo foi o grande salto de vida. In: LOPES, S. Bio, volume 1, São Paulo: Saraiva, 2006. a) Em que grupos de vertebrados ocorre o âmnio? (4,0 pontos) RESPOSTA ESPERADA Répteis aves e mamíferos. b) Aponte uma justificativa para a afirmação do autor sobre o ovo amniótico. (6,0 pontos) RESPOSTA ESPERADA O ovo amniótico revolucionou a história de vida dos seres vivos por que permitiu a alguns grupos de vertebrados ocupar a terra firme. Eles não precisavam mais de água para depositar seus ovos. O ovo com casca é responsável pelo suprimento alimentar do embrião em desenvolvimento e por sua proteção contra danos e dessecação. Ao mesmo tempo, possibilita obter oxigênio e desfazer-se dos produtos de desassimilação. 9 VALORES DE CONSTANTES E GRANDEZAS FÍSICAS – aceleração da gravidade g = 10 m/s2 – calor específico da água c = 1,0 cal/(g°C) = 4,2 x 103 J/(kg°C) – carga do elétron (em módulo) e = 1,6 x 10–19 C – constante da lei de Coulomb k = 9,0 x 109 Nm2/C2 – constante de Avogrado NA = 6,0 x 1023 mol –1 – constante de gravitação universal G = 6,7 x 10–11 Nm2/kg2 – constante de Planck h = 6,6 x 10–34 J s – constante universal dos gases R = 8,3 J/(mol K) – densidade da água d = 1,0 x 103 kg/m3 – massa do elétron melétron = 9,1 x 10–31 kg – massa do próton mpróton = 1,7 x 10–27 kg – velocidade da luz no vácuo c = 3,0 x 108 m/s – velocidade do som no ar vsom = 340 m/s – constante dielétrica do tolueno εt = 2,3 εv = 1,0 – constante dielétrica do vácuo TABELA TRIGONOMÉTRICA ângulo θ 0° 5° 10° 15° 20° 25° 30° 35° 40° 45° sen (θ) 0,000 0,087 0,174 0,259 0,342 0,423 0,500 0,574 0,643 0,707 cos (θ) 1,000 0,996 0,985 0,966 0,940 0,906 0,866 0,819 0,766 0,707 ângulo θ 50° 55° 60° 65° 70° 75° 80° 85° 90° sen (θ) 0,766 0,819 0,866 0,906 0,940 0,966 0,985 0,996 1,00 cos (θ) 0,643 0,574 0,500 0,423 0,342 0,259 0,174 0,087 0,000 DIAGRAMA DO ESPECTRO ELETROMAGNÉTICO
Baixar