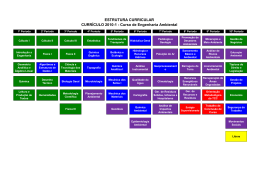
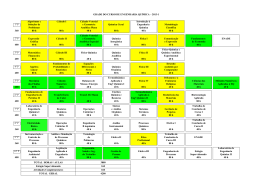
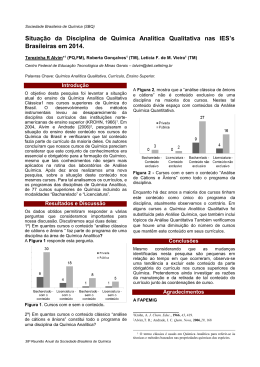
TLC - Cromatografia de camada fina Química Analítica / JCM Cromatografia de camada fina TLC - Thin Layer Chromatography planar / adsorção / zonal / analítica possibilidade de desenvolvimento bidimensional e de quantificação Fases estacionárias Adsorventes / diferentes de absorventes actividade de um adsorvente é determinada pela sua área superficial, a sua natureza química e o arranjo geométrico dos átomos superficiais propriedades de um adsorvente: ☺ ☺ ☺ ☺ ☺ ☺ não deve dissolver na fase eluente não deve reagir com a fase móvel não deve reagir com os solutos deve dar resultados reproductíveis o processo de adsorção deve ser reversível o adsorvente não deve ser muito caro distância percorrida pelo soluto Rf = ----------------------------------------------------------distância percorrida pela frente do solvente Camada Camadade defase faseestacionária estacionária: :250 250µµmm TLC - adsorventes Química Analítica / JCM Polares vários óxidos inorgânicos ( sílica, alumina, magnésia) ☺ ordem de eluição dos solutos segue a polaridade destes - solutos polares são fortemente retidos hidrocarbonetos saturados < hidrocarbonetos aromáticos < éteres < ésteres ≈ aldeídos ≈ cetonas < álcoois ≈ aminas < amidas < ácidos carboxílicos Não-polares carvão activado ☺ ordem de eluição segue a polarizabilidade das moléculas MAIS RETIDOS - compostos aromáticos, homólogos de maior peso molecular, moléculas com átomos de halogénio ou enxofre F o rte s M é d io s F ra c o s s ilic a g e l a lu m in a c a rv ã o a c tiv a d o h id ró x id o d e c á lc io c a rb o n a to d e c a lc io m a g n é s ia ta lc o a m id o s u c ro s e Ácidos Ácidos: : sílica sílica(separa (separaácidos) ácidos) Básicos: Básicos:Alumina Alumina/ /magnésia magnésia(separa (separabases bases TLC - adsorventes Química Analítica / JCM Sílica gel suporte mais popular (5-10 µm) O preparada por hidrólise do silicato de sódio seguida de condensação e polimerização actividade resulta da presença dos grupos Si -- OH (silanol) à superfície controlo da actividade por aquecimento durante a preparação OH Si OH Si O O O O ☺ activação recomendada (110º / 30 - 60 min) Sílica gel é ligeiramente ácida ☺ esteróides, amino-ácidos, álcoois, hidrocarbonetos, lípidos e vitaminas Preparação 50g / 60 ml água destilada - espalhar rapidamente / secar / activar ☺ H - sem impregnante ☺ G - com 13% de sulfato de cálcio ☺ F254 - com indicador fluorescente impregnação com nitrato de prata (20%) - separação de compostos com duplas ligações (menos duplas > Rf) TLC - adsorventes Química Analítica / JCM Alumina O O O Ainda muito comum Al Preparada por condensação do hidróxido de O alumínio hidratado A actividade depende quer dos átomos de oxigénio quer dos de alumínio ☺ mais difícil de preparar dado que geralmente contem mais impurezas o conteúdo de água é muito importante para obter resultados reproductíveis ☺ activação a 75 - 110 º / 30 - 60 min Pode ser obtida com superfície ácida, neutra ou básica (a mais comum) ☺ separação de corantes, vitaminas e alcalóides Preparação 30g / 40 ml de água destilada - espalhar rapidamente / secar e activar ☺ pode conter impregnantes e indicadores de fluorescência O O Al O Al O TLC - adsorventes Química Analítica / JCM Celulose material orgânico diferente da cromatografia de papel ☺ papel - apresenta espaços vazios onde se acumula o solvente - a difusão leva ao alargamento das manchas ☺ celulose - são usadas partículas pequenas / distribuição mais regular - menor difusão Celulose é usada para separar compostos hidrofílicos tal como açúcares, aminoácidos, iões inorgânicos solúveis e ácidos nucléicos - soluções aquosas ☺ geralmente aderem muito fortemente à sílica e alumina Tal como em papel o mecanismo é predominantemente de partilha Preparação 400 mg amido / 10 ml água destilada + 90 ml de água a ferver + 20 g de celulose ☺ o grau de hidratação depende do tempo de agitação ☺ agitação durante muito tempo leva à formação de gel espalhar rapidamente / secar a 110º pode conter indicadores de UV Placas comerciais Química Analítica / JCM Adsorventes Sílica; alumina Suportes Vidro, alumínio ou plástico (tereftalato de polietileno) Espessura 0,25 mm / 0,5 mm / 1,0 mm / 2,0 mm Maior amostra exige maior espessura (TLC preparativa) Activação 15 minutos ao ar + 30 minutos a 110 ºC Nalguns casos pode elevar-se a temperatura a 200 ºC (4 horas) para maior activação Conservação Após secagem / activação as placas devem ser guardadas num excicador As placas de sílica desactivam-se muito rapidamente ☺ 50% de actividade perde-se em 3 minutos numa atmosfera com 50% de humidade TLC – outros adsorventes Química Analítica / JCM Kieselguhr Diatomite - terra de diatomáceas ☺ sílica com plâncton marinho (diatoms) elevada porosidade e área superficial - muito usada como ajudante de filtração muito usada como suporte de fase estacionária líquida - partilha Sephadex gel dextran - hidrofílico e neutro habitualmente usado na filtração em gel - de acordo com os pesos moleculares Fase reversa / inversa a separação de soluto de polaridade semelhante é difícil com sílica gel mesmo para moléculas de pesos moleculares diferentes é possível alterar a superfície da sílica (OH reagem com silanos orgânicos) RP-2, RP-8 , RP-18 ☺ a fase estacionária orgânica apresenta uma retenção preferencial dos compostos nãopolares (fase reversa) e a separação depende dos pesos moleculares a fase móvel é polar (acetonitrilo) cromatografia de partilha TLC - fase eluente Química Analítica / JCM Características - a fase móvel é o componente de mais fácil substituição boa qualidade - a composição não deve variar de lote para lote não reactiva - de outro modo os resultados seriam difíceis de interpretar baixo ponto de ebulição - preferível para a secagem da placa Alta pureza (Analar) e preço razoável !! Escolha a fase eluente deve ser activa ( retirar o soluto da fase estacionária) e selectiva (separar dois solutos diferentes) actividade (capacidade de eluição) em relacção a sílica-gel ☺ água > metanol > etanol > propanol > propanona > triclorometano > ☺ diclorometano > benzeno > metilbenzeno > tricloroetileno > tetraclorometano > ☺ ciclohexano > hexano Misturas de solventes ☺ o mais usual - capacidade de eluição não é proporcional à composição amostra desconhecida ☺ usar sílica gel e um solvente pouco polar (pentano) ☺ acrescentar solvente polar (2, 4, 8, 16, 32%) Separação de pigmentos Química Analítica / JCM Série eluotrópica para adsorventes polares Química Analítica / JCM Tabela definida para placa de alumina A escala vai até cerca de 0,75 para uma placa de sílica Uso de misturas de misturas de solventes (sílica) Química Analítica / JCM J.C. Touchstone (Practice of TLC) Uso de misturas de misturas de solventes (sílica) Química Analítica / JCM J.C. Touchstone (Practice of TLC) Uso de misturas de misturas de solventes (sílica) Química Analítica / JCM J.C. Touchstone (Practice of TLC) Exemplo de fases móveis Química Analítica / JCM TLC - aspectos experimentais Química Analítica / JCM Preparação preparar a mistura eluente nas proporções adequadas ao ensaio saturar a câmara - manter fechada e à temperatura do ensaio evitar evaporação da mistura eluente - alteração da composição controlar o grau de humidade da placa Aplicação da amostra usar micropipeta (1 -2 µl) - não danificar o suporte colocar a amostra a cerca de 1,5 cm da base - todas a amostras na mesma linha a mancha deve ser de reduzidas dimensões (1,5 mm) ☺ no caso de amostras diluídas colocar por diversas vezas, secando após cada aplicação evitar que a mancha toque a superfície do solvente (5 - 8 mm) Desenvolvimento manter a temperatura deixar desenvolver o cromatograma até cerca de 3 cm do topo da placa Revelação usar luz UV (254 / 366 nm) ou revelador adequado (H2SO4) determinar Rf, definir tamanho das manchas - quantificar se desejável Placa de TLC Química Analítica / JCM Saturar a câmara / equilibrar a placa Efeito da insaturação da placa Química Analítica / JCM TLC - maus exemplos Química Analítica / JCM Polaridade soluto muito polar é retido na origem Amostra em demasia / amostra mal seca demasiada amostra cria tailing / amostra mal seca cria anéis Câmara mal saturada saturação insuficiente leva a demasiada evaporação da fase eluente Colocação muito baixa / demasiada humidade amostra baixa difunde-se na fase eluente / muita humidade leva a maior difusão das manchas e também a uma separação deficiente TLC - reveladores Química Analítica / JCM Métodos químicos / métodos físicos Métodos não-destructivos radiação visível e UV (254 nm e 366 nm) Vapor de iodo ☺ evaporação / placa sem alteração água indicadores de pH (bromocresol / bromofenol) Métodos destructivos 50% H2SO4 / 110 C 5% dicromato de potássio ou 5% ácido nítrico em 40% H2SO4 seguido de aquecimento a 110 C UV (vitaminas) / água (hidrólise - ésteres) / iodo (ácidos gordos poliinsaturados) Reagentes específicos são conhecidos para quase todas as classes de compostos NOTA: o uso de métodos destructivos é desaconselhado sempre que a quantificação seja o objectivo da separação cromatográfica TLC - amostras Química Analítica / JCM Classificação (energias de adsorção) Grupo 1: moléculas neutras - hidrocarbonetos ☺ forças de Van der Waal - físicas (não há formação de ligações químicas ☺ grupos metileno - não há separação por peso molecular ☺ separações boas e manchas redondas Energias de adsorção (sílica gel) Grupo 2: ligações polares (C - Cl / C - NO2) ☺ dipolo induzido - físicas / manchas redondas Grupo 3: moléculas polares ( ácidos, álcoois) ☺ Grupos de superfície polar - nucleofílica ☺ interação com adsorvente via lig. H-H ☺ forte - possibilidade de “caudas” nas manchas Grupo 4: ligações químicas (covalentes) ☺ ligações fortes - má separação A forma das manchas depende do equilíbrio de concentrações estabelecido entre as fases móvel e estacionária Cs Cs Cm Grupo Qi interação R-CH3 +0.07 VdW R-CH2- -0.05 VdW R-Cl +1.32 dip. ind. R-O-R +3.61 receptor H R-CHO +4.97 receptor H R-NO2 +5.71 dip.ind R-CO2R +5.27 rec.H /dip.ind. R-COR +5.27 rec.H/dip.ind. R-OH +5.60 H-H R-NH2 +8.00 H-H R-CO2H +7.60 H-H Cs Cm Cm Casos especiais Química Analítica / JCM TLC preparativo Colocar bandas largas de amostra e desenvolver a placa Retirar a sílica de cada mancha e dissolver usando um solvente adequado Analisar noutro equipamento (HPLC, LCMS, FTIR) TLC bidimensional Colocar a amostra no lado esquerdo da placa e desenvolver Secar a placa e desenvolver de novo noutro eluente (colocar o lado esquerdo da placa para baixo) Revelar Separação de aminoácidos F. estacionária: sílica gel F. Móvel 1: tolueno:2-cloroetanol:piridina F. Móvel 2: clorofôrmio:álcool benzílico:ac. Acértico 1: ac. Aspártico, 2: ac. Glutámico, 3: serina 4: alanina, 5: glicina, 6: alanina, 7: metionina, 8: valina, 9: isoleucina, 10: cisteina TLC - vantagens e desvantagens Química Analítica / JCM Vantagens Técnica simples e versátil - aplica-se a quase todas as classes de compostos Pequenas quantidades de amostra – sem grande preparação A separação pode ser obtida com custos razoáveis - bom adsorvente e solventes puros As separações podem ser obtidas em tempos relativamente curtos ☺ começa a não ser vantagem em relação às pequenas colunas de HPLC O processo de separação é “visível” e pode ser melhorado alterando suportes ou a fase eluente ☺ ao contrário do GC ou HPLC e que os solutos muito retidos podem passar despercebidos Desvantagens A preparação das placas é complicada ☺ está a cair em desuso (aquisição de placas preparadas) A quantificação é possível mas implica um enorme custo financeiro ☺ por isso o TLC é a técnica de separação cromatográfica tipicamente qualitativa / semiquantitativa Colocação de amostras em quantidades conhecidas e quantificação por comparação Química Analítica / JCM Linha de frente do solvente Distância percorrida pelo solvente Distância percorrida pelo soluto B Distância percorrida pelo soluto A Linha de colocação das amostras Resolução = X / 0,5 (d1 + d2); x - distância entre as manchas; d1 e d2 – diâmetros das manchas R mínimo = 1 Rf = distância percorrida pelo soluto / distância percorrida pela frente do solvente
Download