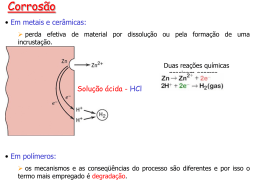
CORROSÃO • Corrosão Processo de desgaste dos metais com perda de material. Como ocorre ? • Formam-se primeiro óxidos à superfície do metal, formando uma película, uma vez que esta é a zona mais exposta ao oxigénio do ar. • • Esta película acaba por se desfazer. O processo de formação dos óxidos continua para camadas mais profundas. Corrosão Dar-se-á de igual forma para todos os metais? Não !!! • Há metais que oxidam lentamente. São pouco reactivos. Por exemplo o Ouro. • Há metais que oxidam rapidamente. São muito reactivos. Por exemplo o Potássio. Corrosão • Ferro Oxida facilmente em contacto com o ar húmido; • Forma-se o óxido de ferro (III) vulgarmente chamado ferrugem. ferro (s) + oxigénio (g) + água (l) óxido de ferro (III) hidratado Corrosão Como prevenir ? • • • • Evitar expor o material ao ar e à água. Evitar o contacto entre metais diferentes. Em certas condições, usar um metal protector. Pintura ou envernizamento dos metais. Protecção catódica - faz-se uso de um metal que seja um redutor mais forte que o metal a proteger Galvanoplastia - é um processo através do qual se aplica uma protecção superficial que consiste na cobertura do metal por outro metal que o proteja dos elementos ambientais que são responsáveis pela sua corrosão. Anodização - baseia-se na utilização de correntes externas que provoquem a deposição regular de uma camada protectora do próprio metal. Protecção catódica O princípio básico é tornar o elemento metálico a ser protegido - um aqueduto, por exemplo - num cátodo de uma célula de corrosão, o que pressupõe a presença de um ânodo. Assim, o processo natural de perda de electrões da estrutura para o meio - fenómeno que causa a corrosão - é compensado pela ligação da estrutura metálica a um ânodo de sacrifício. O direcionamento da corrente eléctrica preserva a estrutura metálica, ocorrendo corrosão controlada no ânodo. Protecção catódica Ânodo de sacrifício – o metal mais redutor vai fornecer electrões ao ânodo que se quer proteger passando este último a funcionar como cátodo, não sofrendo corrosão. Corrente protectora – aplica-se uma corrente eléctrica no ânodo Este método é apropriado para grandes estruturas metálicas como por exemplo pipelines (usados em oleodutos ou gasodutos), tanques de armazenamento de combustível subterrâneos ou pontes. Esta forma de assegurar a protecção de um metal contra a corrosão consiste em ligá-la ao pólo negativo de uma fonte de tensão (p.e. uma pilha de 1.5V). A fonte de tensão injecta os electrões necessários para manter a peça reduzida. Note-se que é necessário ligar o pólo positivo da pilha a outro eléctrodo, o qual poderá ser consumível (sucata de ferro) ou inerte (grafite). Este efeito é usado para proteger os cascos de navio em água salgada. Na protecção dos pipelines faz-se uso de um metal como, por exemplo, o zinco ou o magnésio, que é enterrado em terreno húmido e ligado electricamente ao pipeline (Fe) subterrâneo. O bloco de zinco ou de magnésio vai ser preferencialmente oxidado, fornecendo electrões ao ferro de modo a impedir a oxidação deste pelo oxigénio. O bloco de metal que é chamado eléctrodo de sacrifício, protege o pipeline de ferro e é mais fácil e mais barato de substituir do que se fosse necessária a substituição do pipeline. Pelo mesmo motivo, os automóveis normalmente têm a carroçaria do carro ligada ao ânodo da bateria. O descarregar da bateria é o sacrifício que ajuda a preservar o próprio veículo Anodização O alumínio, por exemplo, reage com o oxigénio do ar através da reacção espontânea: 4Al (s) + 302 (g) → 2Al203 (s) Contrariamente à ferrugem, o óxido de alumínio adere fortemente à superfície metálica e, como não é solúvel, constrói uma barreira protectora que impede a corrosão do metal que fica debaixo desta camada – passivação. Latas de alumínio nunca adquirem um aspecto muito oxidado, mesmo quando em contacto prolongado com soluções aquosas. Galvanoplastia Galvanização da estrutura de um automóvel A galvanoplastia é normalmente feita por imersão do metal a ser tratado numa tina contendo sais do metal que o vai recobrir e que, através do fornecimento de uma corrente catódica externa, que fornece electrões que levam à sua redução, são depositados sobre a superfície a ser recoberta. Choques eléctricos nos dentes chumbados Até recentemente o material mais usado para chumbar os dentes era a amálgama dentária constituída por compostos de mercúrio, prata e estanho Ag2Hg, Ag2Sn e Sn3Hg que têm potenciais normais de redução de +0,85v, -0,05V e -0,13V, respectivamente. Radiografia da face em que são visíveis dois dentes chumbados. Quando alguém com um dente chumbado introduz um utensílio metálico na boca que lhe toque (por exemplo, um garfo cromado (E°cr 3+/cr) = - 0,74V ), vai sentir um desconforto momentâneo devido à descarga eléctrica que se faz sentir no nervo dentário devido à formação da pilha galvânica. É por este motivo, associado a razões estéticas, que gradualmente a amálgama dentária tem vindo a ser substituída por compósitos poliméricos. EXERCÍCIOS 1. Entre o cobre, o níquel, o alumínio e o manganês, qual será o mais adequado para fazer a protecção catódica do ferro? 2. Um guiador de bicicleta cromado sofreu um risco. Será a corrosão do ferro favorecida ou retardada pelo crómio? 3. Sugira dois metais que possam ser usados para fazer a protecção catódica do zinco. 4. Dos seguintes metais indique aqueles que não podem ser usados como eléctrodo de sacrifício para protecção catódica do ferro. a) Zinco b) prata c) cobre d) magnésio 5. Explique por que é que, apesar de estarem permanentemente em contacto com bebidas aquosas as latas de refrigerantes não sofrem processos fortes de corrosão. EXERCÍCIOS - resolução 1. O que tem mais tendência para se oxidar, ou seja é melhor redutor, é o que tem menor potencial de redução. O alumínio é, de entre as opções apresentadas o melhor ânodo de sacrifício. 2. Como o potencial normal de redução do ferro = - 0,41 V) é maior do que o do crómio = - 0,74 V) , então numa solução contendo electrólitos, espontaneamente o crómio oxida-se, reduzindo o ferro, pelo que contribui para a protecção do ferro, mesmo na presença de um risco perfurante da cromagem. EXERCÍCIOS 3. Para que um metal possa efectuar a protecção catódica de outro, terá de ser um redutor mais forte, ou seja, possuir um potencial normal de redução mais baixo. Como o manganês e o magnésio por exemplo têm potenciais normais de redução mais baixos do que o do zinco, então, serviriam para fazer a sua protecção catódica. 4. b)e c) ferro= - 0,44 V a) Zinco = - 0,76 V b) prata = +0,80 V c) cobre = + 0,34 V d) magnésio = - 2,36 V EXERCÍCIOS 5. As latas de refrigerantes são normalmente de alumínio. 0 alumínio, por exemplo, reage com o oxigénio do ar através da reacção espontânea, 4Al (s) + 302 (g) → 2Al203 (s) No entanto, contrariamente à ferrugem, o óxido de alumínio adere fortemente à superfície metálica e, como não é solúvel, constrói uma barreira protectora, que impede a corrosão do metal que fica debaixo desta camada.
Baixar