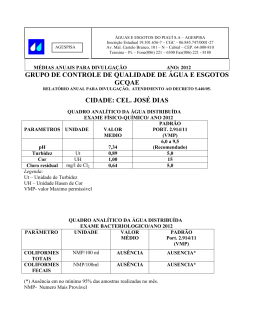
3 Caracterização das formas de residual de cloro e avaliação da eficiência da desinfecção na piscina do Instituto Federal de Educação Tecnológica do Ceará (IFCE) 4 5 Characterization of the forms chlorine residual and disinfection efficiency of assessment used in the pool at Federal Institute of Technology Education Ceará (IFCE) 1 2 6 7 Maria Cândida Barreto Cunha 8 9 Tecnóloga Ambiental pelo Instituto Federal de Educação Tecnológica do Ceará (IFCE) Técnica de Controle Ambiental da CAERN 10 11 Marlon Vieira de Lima 12 Químico pela Universidade Federal do Ceará (UFC) 13 14 Professor Titular do Departamento de Química e Meio Ambiente do IFCE 15 16 17 Endereço para correspondência: Avenida Miguel Castro, 1284 – Lagoa Nova, Natal – Rio Grande do Norte. CEP: 59162-000. Telefones: (84) 3232-4444, (84) 9612-9224. E-mail: [email protected] 18 19 Resumo 20 21 22 23 24 25 26 27 28 29 30 O uso de desinfetantes no tratamento de águas para o abastecimento humano, piscinas e águas residuárias é uma das formas mais utilizadas para eliminação de microorganismos patógenos. O cloro vem se destacando por apresentar grande eficiência nessa remoção, quando observadas as concentrações certas, o tempo de contato ideal e as características da água como pH e temperatura. O cloro pode está presente na água nas formas de ácido hipocloroso e íon hipoclorito, sendo que o primeiro é mais eficiente na desinfecção. A determinação dos residuais de cloro para elaboração desse trabalho foi realizada pelo método titrimétrico com sulfato ferroso amoniacal, juntamente com o indicador DPD. As determinações foram realizadas em amostras de água coletadas na piscina do IFCE, verificando-se o residual de cloro livre e combinado e o pH. Os resultados demonstraram a variação que ocorre no decorrer do dia nesses parâmetros. 31 32 Palavras chave: Desinfecção de água. Cloração. Residual de cloro livre. Residual de cloro combinado. Cloraminas. Tratamento de piscinas. 33 34 Abstract 35 36 37 38 39 40 The use of disinfectants in water treatment for human supply, swimming pools and wastewater is one of the most used for elimination of pathogenic microorganisms. Chlorine has been known for high efficiency make this removal, observed when certain concentrations, contact time and the ideal characteristics of water such as pH and temperature. Chlorine is present in water can in the form of hypochlorous acid and hypochlorite ion, and the first is more effective at disinfection. The determination of residual chlorine in developing this work 1 41 42 43 44 was carried out by the titrimetric method with ammonium ferrous sulfate, together with the DPD indicator. Measurements were performed on water samples collected in the pool of IFCE, verifying the residual and combined chlorine and pH. The results showed the variation that occurs throughout the day in these parameters. 45 46 Keywords: Disinfection of water. Chlorination. Residual free chlorine. Combined chlorine residual. Chloramine. Treatment of pools. 47 48 Introdução 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 A água é o meio pelo qual a vida surgiu; em qualquer época, ecossistema ou mesmo em uma simples atividade cotidiana, tem sido essencial à sobrevivência do ser humano. Segundo a OMS “Toda pessoa, qualquer que seja sua etapa de desenvolvimento e suas condições sociais e econômicas, tem direito a um abastecimento adequado de água potável e saudável”. Todavia, ao longo dos últimos anos, o desenvolvimento tecnológico praticado de forma não sustentável, fruto da imposição de uma sociedade cada vez mais consumista, tem causado sérios problemas aos recursos hídricos, gerando um ciclo hidrológico artificial, caracterizado pelo aumento da carga orgânica, esta oriunda de diversas fontes poluidoras, dentre as quais se destacam os efluentes domésticos e industriais, que contribuem enormemente para a degradação dos mananciais. Nesse contexto, é oportuno questionar qual é o papel dos diversos profissionais preocupados com a conservação do meio ambiente (e, por conseguinte, com a melhoria das condições de vida em nosso planeta), de um modo especial engenheiros e tecnólogos ambientais buscam meios para mitigar e até mesmo remediar esses impactos, através da pesquisa científica e tecnológica, tentando propiciar um desenvolvimento sustentável como consequência de uma atuação ética, pautada na responsabilidade social e ambiental. Dentre os inúmeros processos empregados para devolver à água as condições adequadas à sua utilização em atividades industriais, de recreação e a potabilização para o abastecimento público, escolhemos a desinfecção como tema deste trabalho, em sua variante mais difundida que é a cloração; dando ênfase à tipificação das formas de residuais de cloro, tendo em vista que a otimização dessa operação muitas vezes constitui a etapa crítica do tratamento de água. A cloração utiliza como agente desinfetante o cloro e seus diversos derivados para eliminar os microorganismos presentes na água. Sua aplicação cresceu enormemente a partir do final do século XIX. Anteriormente, quando as populações viviam em situações mais precárias era muito frequente a ocorrência de epidemias e surtos que dizimavam milhares de pessoas, sendo que o principal meio de veiculação dessas doenças era a água contaminada. Era preciso uma maneira eficaz de tratar a água e melhorar as condições sanitárias das cidades. Foi então que a cloração ganhou espaço e valor econômico. O cloro e seus derivados foram sendo desenvolvidos e aprimorados, a fim de não causarem riscos à saúde das pessoas que consumiam a água tratada. Outra aplicação importante da cloração está relacionada com o uso da água em atividades onde se verifica o contato direto. São o caso das piscinas, amplamente empregadas para a prática de esportes aquáticos (natação, saltos ornamentais), atividades terapêuticas (hidroginástica) e recreativas (banho livre). Uma vez que este tipo de contato normalmente está associado à fadiga e esforços mecânicos em áreas do corpo bastante sensíveis como as mucosas, facilita sobremaneira a ação de microrganismos oportunistas, desencadeando diversos tipos de infecções como conjuntivites, otites, doenças de pele e distúrbios gastrointestinais. Desta forma, é imprescindível que as piscinas sejam submetidas a uma manutenção contínua que inclua um 2 89 90 91 92 93 94 95 96 97 98 99 100 101 tratamento adequado da água e um constante controle sanitário. Face à suas potencialidades e baixo custo, o cloro também ganhou espaço no âmbito das piscinas, onde tem sido largamente empregado com comprovada eficiência na eliminação dos microrganismos típicos desses sistemas aquáticos. Nesse contexto, o tratamento de água em piscinas adquire enorme importância sanitária, uma vez que é grande número de pessoas que as frequentam, quer seja para banho, prática de esportes ou até mesmo como local de trabalho, no caso de atletas profissionais, o que, não raro, pode representar risco à saúde de seus usuários, dada à possibilidade de ocorrência de diversos tipos de doenças transmissíveis pela água. Atenção especial foi dada nesse trabalho, ao processo desinfecção atualmente praticado na piscina do IFCE, enfatizando os tipos de cloro residuais presentes e suas relações com o pH. 102 Metodologia 103 104 105 106 107 108 109 110 111 112 113 114 115 116 117 118 119 120 121 122 123 124 125 126 127 128 129 130 131 132 133 134 135 136 137 O trabalho pretende evidenciar a dinâmica da cloração com base na identificação e quantificação dos tipos de residual de cloro presentes. Para tanto, tomou-se como objeto de estudo a piscina do IFCE, cujas características sanitárias são influenciadas por fatores como vazão, quantidade e frequência de seus usuários, tratamento químico, condições ambientais (chuva, vento, sol), dentre outras, o que a torna também um sistema bastante apropriado ao estudo do comportamento do cloro, permitindo uma avaliação razoável da eficiência da cloração. Determinação do residual de cloro As amostras foram coletadas, conservadas e analisadas de acordo com os procedimentos descritos no Standards Methods for the Examination of Water and Wasterwater, 20th ed (APHA et al. 1998). As análises foram realizadas no Laboratório de Química Analítica (LQA) do Instituto Federal de Educação Tecnológica do Ceará (IFCE). Seleção do método O método selecionado foi o DPD por ser operacionalmente mais simples. Os procedimentos foram elaborados para estimar a presença de monocloramina, dicloramina e tricloramina separadas ou em frações combinadas. No entanto, em concentrações elevadas as monocloraminas interferem na determinação de cloro residual livre, para tanto a reação deve ser interrompida com arsenito de sódio ou tioacetamida. Esse método também está sujeito a interferências por formas oxidadas de manganês, que devem ser compensadas por um branco e é inalterado em concentrações de dicloramina na faixa de 0,0 a 9,0mg.L-1 como Cl2/L na determinação de cloro residual livre. Tricloramina, se presente, pode reagir parcialmente como cloro livre no método de DPD. A extensão desta interferência não é significante. Cor e turbidez na amostra também podem interferir como em todos os procedimentos colorimétricos e devem ser eliminadas por filtração ou compensadas com um branco. Contaminantes orgânicos podem produzir uma falsa leitura do cloro livre, tais interferências incluem bromo, dióxido de cloro, iodo, permanganato, peróxido de hidrogênio e ozônio. Porém, as formas reduzidas destes compostos: brometo, cloreto, iodeto, íon manganoso, e oxigênio, na ausência de outro oxidante, não interferem. 3 138 139 140 141 142 143 144 145 146 147 148 149 150 151 152 153 154 155 156 157 158 159 160 161 162 163 164 165 166 167 168 169 170 171 172 173 174 175 176 177 178 179 180 181 182 183 184 185 186 187 Amostragem e armazenamento O cloro em solução aquosa não é estável, a quantidade de cloro diminuirá rapidamente. Exposição à luz solar ou outra luz forte ou agitação acelerará a redução de cloro. Portanto as determinações de cloro foram realizadas imediatamente após a coleta, evitando luz e agitação excessivas. Determinação pelo método DPD ferroso N,N-dietil-p-fenilenodiamina (DPD) é utilizado como indicador no procedimento titrimétrico com sulfato ferroso amoniacal (SFA) 0,00282meq.L-1. Na ausência do íon cloreto, o cloro residual livre reage instantaneamente com o indicador DPD produzindo coloração vermelha. A adição subsequente de pequena quantidade de íon iodeto atua cataliticamente fazendo com que a monocloramina (NH2Cl) produza cor. A adição de íons iodeto em excesso provoca uma rápida resposta da dicloramina (NHCl2). A tricloramina (NCl3) fica incluída com a dicloramina, entretanto, se o íon iodeto for adicionado antes do DPD, uma proporção do NCl3 aparece com o cloro residual livre. Um procedimento suplementar baseado nesta alteração da ordem de adição dos reagentes permite estimar o teor de tricloramina. Onde a completa diferenciação entre as espécies de cloro residual não for necessária, o procedimento poderá ser simplificado para fornecer somente o cloro residual livre e o cloro residual combinado ou o cloro residual total. Controle de pH Para resultados exatos o controle do pH é essencial. O pH deve está entre 6,2 e 6,5. As colorações vermelhas produzidas podem ser tituladas para pontos finais incolores nítidos. Um pH demasiadamente baixo na primeira etapa fará com que a monocloramina apareça na etapa do cloro livre, e a dicloramina na etapa da monocloramina. Um pH demasiadamente alto fará com que o oxigênio dissolvido desenvolva cor. Controle de temperatura Em todos os métodos para diferenciação entre o cloro livre e as cloraminas, quanto maiores às temperaturas, maiores serão as tendências das cloraminas reagirem e levarem a um aumento aparente dos resultados de cloro residual livre. Altas temperaturas também aumentam a descoloração, por tanto deve-se realizar as análises rapidamente, especialmente a temperaturas maiores. Limite de detecção do método = 18μg.L-1 Reagentes utilizados: Solução tampão de fosfato Solução indicadora de N,N - dietil-p-fenolenodiamina (DPD) Solução titulante padrão de sulfato ferroso amoniacal (SFA) 0,00282meq.L-1 Solução de iodeto de potássio Solução de arsenito de sódio Solução de tioacetamida Procedimento operacional 4 188 189 190 191 192 193 194 195 196 197 198 199 200 201 202 203 204 205 206 207 208 209 210 211 212 213 214 215 216 217 218 219 220 221 222 223 224 225 226 As quantidades dadas abaixo são adequadas para concentrações de cloro residual total de até 5,0mg.L-1. Caso o valor exceda, deve-se utilizar uma amostra diluída num volume total de 100,0mL. Em seguida adicionar os volumes da solução tampão de fosfato e da solução indicadora de DPD. Cloro livre ou cloramina: Colocar 5,0mL da solução tampão de fosfato e da solução indicadora de DPD no frasco de titulação e misturar. Adicionar 100,0mL da amostra ou uma fração diluída, e misturar bem. Cloro disponível livre: Titular rapidamente com solução titulante padrão de SFA 0,00282meq.L-1, até que a cor vermelha desapareça (Leitura A). Monocloramina: Adicionar 0,1mL (2 gotas) da solução KI e misturar. Continuar a titulação, até que a cor desapareça novamente (Leitura B). Dicloramina: Adicionar 0,2mL (4 gotas) e misturar. Deixar em repouso por 2 minutos e realizar a titulação, até que a cor vermelha desapareça (Leitura C). Para concentrações maiores que 1,0mg.L-1, deixar em repouso por mais 2 minutos, se a cor voltar indica que a reação está ligeiramente incompleta. Para obter o cloro total em uma leitura, adicionar a quantidade total de da solução de KI, ou seja, 0,2mL (4 gotas) no início da análise, só então adicionar as quantidades especificadas da solução tampão de fosfato e das solução indicadora de DPD. Titular após de 2 minutos de repouso. Tricloramina: Adicionar 0,1mL (2 gotas) da solução de KI em um frasco de titulação. Adicionar 100,0mL da amostra e misturar. Adicionar o conteúdo para um segundo frasco, contendo 5,0mL da solução tampão de fosfato e da solução indicadora de DPD. Titular rapidamente com padrão de SFA 0,00282meq.L-1, até que a cor vermelha desapareça (Leitura D). Cálculos Para uma amostra contendo 100,0mL: 1,0mL da solução titulante padrão de SFA = 1,0mg.L de cloro residual disponível. A Tabela I abaixo é utilizada para calcular os valores de cloro residual livre, monocloramina, dicloroamina e tricloramina, caso esteja presente. -1 TABELA I - Formas de cloro encontradas através da análise titrimétrica com DPD ferroso (APHA e tal, 1998). Leitura Ausência de NCl3 Presença de NCl3 A Cl livre Cl livre B-A NH2Cl NH2Cl C-B NHCl2 NHCl2 + ½ NCL3 D - Cl livre + ½ NCl3 2 (N - A) - NCl3 C-D - NHCl2 A: cloro residual livre; B: monocloramina; C: dicloramina; D: tricloramina. Se a monocloramina estiver presente com NCl3, ela será incluída na Leitura D e NCl3 obtido por 2(D -B). No procedimento simplificado para o cloro disponível combinado e livre, somente a 5 227 228 229 230 231 leitura A (cloro livre) e a leitura C (cloro total) são necessárias. O cloro disponível combinado é obtido de C – A. O resultado obtido no procedimento simplificado para cloro disponível total corresponde à leitura C. 232 233 234 235 236 237 238 239 240 241 Resultados e discussão 242 243 244 245 246 247 248 249 250 251 252 253 254 255 256 257 As amostras foram coletadas em frascos de polietileno opaco, em um ponto próximo ao ralo de fundo da piscina, nos turnos da manhã e da noite, às 08:30h e 18:00h, respectivamente, no período de 01 a 17 de outubro de 2007. Sendo que no dia 17/10/2007 o residual de cloro foi determinado durante a manhã a cada hora. A Tabela II apresenta os dias que foram realizadas coletas e os respectivos períodos de cada coleta. TABELA II – Data das coletas de água para determinação do residual de cloro Data da coleta Manhã – 08:30h Noite – 18:30h 01/10/2007 X 02/10/2007 X 04/10/2007 X 05/10/2007 X 09/10/2007 X X 10/10/2007 X X 11/10/2007 X X 17/11/2007 X Local da coleta: piscina do IFCE Nos dias 03, 06, 07, 08/10/2007 não foi possível realizar a coleta. As amostras foram encaminhadas ao Laboratório de Química Analítica (LQA) para a determinação do cloro residual livre e cloro combinado na forma de monocloramina, dicloramina e tricloramina. Todas as análises foram realizadas em duplicatas. Também foi determinado o pH a 25ºC em todas as amostras. Residual de cloro As análises de residual de cloro foram realizadas com as soluções descritas na Metodologia. Todas as soluções foram preparadas e padronizadas conforme procedimentos descritos em APHA et al. 1998. Na Tabela III estão relacionados os resultados obtidos nas análises de acordo com o dia da coleta e o turno (manhã e noite). 6 258 TABELA III – Resultados obtidos dos residuais de cloro durante os turnos manhã e noite. Data da coleta Cloro livre Monocloramina Cloro livre Monocloramina (mg.L-1) (mg.L-1) (mg.L-1) (mg.L-1) Turno 259 260 261 262 263 264 265 266 267 268 269 270 271 Manhã noite 01/10/2007 - - 0,0 0,2 02/10/2007 - - 0,0 0,2 04/10/2007 - - 0,0 0,1 05/10/2007 - - 0,0 0,1 09/10/2007 1,4 0,1 0,0 0,1 10/10/2007 1,6 0,2 0,0 0,1 11/10/2007 2,7 0,1 0,0 0,1 17/10/2007 3,0 0,1 - - Local da coleta: piscina do IFCE Nos dias 03, 06, 07, 08/10/2007 não foi possível realizar a coleta. Segundo a Tabela III, o cloro residual livre variou entre 1,4 a 3,0 mg.L-1 nos dias 09, 10, 11 e 17/10/2007 no turno da manhã. E durante o período de 01, 02, 04, 05, 09, 10, 11 e 17/10/2007, no turno da noite o cloro residual livre encontrou-se virtualmente ausente. O cloro residual combinado variou entre 0,1 a 0,2 mg.L-1 nos dias 01, 02, 04, 05, 09, 10, 11 e 17/10/2007, nos turnos da manhã e noite, estando presente durante todo o período como monocloramina. A Figura I representa os resultados obtidos do cloro residual, as análises foram realizadas nos dias 09, 10 e 11 de outubro de 2007, às 08:30h e às 18:00h, onde se pode notar a variação que ocorre no decorrer do dia. 7 3 2,5 2 08:30h 1,5 18:30h 1 0,5 0 9/10/2007 272 273 274 275 276 277 278 279 280 281 282 10/10/2007 FIGURA I - Variação do cloro residual livre (mg.L-1 ) no decorrer dos dias 09, 10 e 11 de outubro de 2007, às 08:30h e as 18:30h. Durante os dias 01, 02, 04, 05, 09, 10 e 11/10 de 2007, foram realizadas análises de cloro residual livre, monocloramina, dicloramina e tricloramina, no turno da noite, sempre às 18:30h. A Figura II a seguir ilustra os resultados obtidos nesse período, demonstrando que apenas a monocloramina aparece de forma significativa, mesmo que em pequenas proporções, os resultados de cloro residual livre, dicloramina e tricloramina são virtualmente ausentes. cloro residaula livre (mg.L-1) 0,2 0 0 1 monocloramina (mg.L-1) 0,2 0,1 283 284 285 286 287 288 289 290 291 292 11/10/2007 2 0 3 0,1 0 4 0,1 0 5 0,1 0 6 0,1 0 7 FIGURA II - Variação de residuais de cloro livre e combinado No dia 17 de outubro de 2007 foi realizado o acompanhamento do cloro residual livre da água da piscina numa frequência horária, no turno da manhã, como segue na Tabela IV: 8 293 294 295 296 297 298 299 TABELA IV – Hora e residual de cloro livre encontrado na piscina no dia 17/10/2007 Hora Cloro residual livre 09:00 3,0 mg.L-1 10:00 1,7 mg.L-1 11:00 1,2 mg.L-1 12:00 0,4 mg.L-1 13:00 0,0 mg.L-1 Os referidos valores estão representados na Figura III, que ilustra a curva de decaimento do cloro livre em função do tempo (hora) no decorrer da manhã, denotando claramente o rápido consumo de cloro, que após 5 (cinco) horas encontra-se virtualmente ausente. 3,5 cloro residual livre mg.L-1 3,0 2,5 2,0 1,5 1,0 0,5 0,0 09:00 10:00 11:00 12:00 13:00 hora da coleta realizada no dia 17/10/07. 300 301 302 303 304 305 306 307 308 309 310 311 312 313 314 315 FIGURA III - Comportamento do residual de cloro livre durante o período da manhã Determinação do pH O pH ideal para que o cloro residual livre esteja em maior quantidade sob a forma de ácido hipocloroso, que é o agente de maior eficiência na desinfecção e oxidação de compostos orgânicos e inorgânicos presentes na água, sem causar irritação aos banhistas, deve estar compreendido entre 7,2 e 7,4. A Tabela V apresenta os valores determinados em laboratório conforme o dia e o turno da coleta de água. 9 316 317 318 319 320 321 322 323 324 325 TABELA 05 – Valores de pH encontrados na água da piscina do IFCE Data da coleta pH pH Turno manhã noite 01/10/2007 - 8,00 02/10/2007 - 8,02 04/10/2007 - 7,60 05/10/2007 - 7,67 09/10/2007 7,87 7,88 10/10/2007 7,95 7,97 11/10/2007 7,53 - 17/10/2007 7,54 - Local da coleta: piscina do IFCE Nos dias 03, 06, 07, 08/10/2007 não foi possível realizar a coleta. A variação de pH das amostras oscilou entre 7,53 a 8,02, no decorrer do dia, entre os turnos manhã e noite A Figura IV representa a variação de pH durante o período da manhã do dia 17/10/2007, o pH nesse dia foi determinado com frequência horária, os valores variaram de 7,51 a 7,55. 7,56 7,55 7,54 7,53 7,52 7,51 7,5 7,49 09:00 10:00 11:00 12:00 13:00 pH da piscina 326 327 328 329 330 FIGURA IV – Comportamento do pH durante o período da manhã do dia 17/10/2007. 10 331 332 333 334 335 336 337 338 339 340 341 342 343 344 345 346 347 348 349 350 351 352 353 354 355 356 357 358 359 360 361 362 363 364 365 366 367 368 369 370 371 372 373 374 375 376 377 378 379 380 Conclusões Residual de cloro A partir da análise dos resultados e de acordo com os valores de desinfecção normalmente adotados para controle microbiológico de águas de piscinas, os valores obtidos de cloro residual livre encontrados no turno da manhã, na piscina do IFCE e que variaram de 1,4 a 3,0mg.L-1 são considerados seguros. O que se pode concluir que, como a cloração foi realizada à noite e até o horário da coleta a piscina não apresentava movimentação intensa por parte dos usuários, o cloro que foi adicionado à noite, satisfez a demanda e proporcionou um residual consideravelmente alto, e presente como cloro residual livre, a forma mais eficiente para a eliminação de microorganismos, contudo essa garantia não pode ser comprovada sem a análise microbiológica da água. No entanto o consumo de cloro é bastante intenso e depois de iniciadas as atividades na piscina ocorre uma queda constante no residual de cloro livre chegando a virtualmente ausente em poucas horas, em torno das 12:00h e assim permanece até o final do dia, quando haverá uma nova cloração às 21:30h. O cloro residual livre não é estável durante muito tempo, permanecendo ativo apenas pela manhã, sendo que a partir de 13:00h já foi totalmente eliminado. A piscina do IFCE apresenta grande movimentação, tendo atividades esportivas durante manhã, tarde e noite, ou seja, a demanda de cloro é alta e, como o cloro livre só foi detectado no turno manhã, a água da piscina torna-se vulnerável a uma recontaminação microbiológica. O cloro combinado que está presente durante todo o turno da manhã e da noite em pequenas proporções variando entre 0,1 a 0,2mg.L-1, sendo que no turno da noite é a única forma de cloro existente, o que demonstra a ineficiência do processo de cloração, já que este não tem garantia de eliminar os microorganismos e de oxidar compostos orgânicos e inorgânicos presentes na água. pH Os valores de pH evidenciam que a água da piscina do IFCE favorece a formação de cloro residual combinado, principalmente monocloramina, que prevalecem em pH maior que 8,5. O pH da água influencia na forma como o cloro estará presente, ou seja, o pH da água da piscina do IFCE em nenhum momento favorece a formação do ácido hipocloroso, a forma mais ativa na eliminação de microorganismos, apresentando-se acima dos valores ideais, e favorecendo a formação do cloro residual combinado, sobretudo de monocloramina. Sugestões De acordo com os resultados obtidos nesse trabalho, podemos concluir que: § Apesar de não ter sido possível quantificar a demanda de cloro, é possível inferir, com base na identificação dos tipos de residual de cloro, que a piscina do IFCE apresenta elevada demanda de cloro, sendo que a quantidade deste produto que é adicionada diariamente, não está sendo suficiente para atender tal demanda. 11 381 382 383 384 385 386 387 388 389 390 391 392 393 394 395 396 397 398 399 400 401 402 403 404 405 406 407 408 409 410 411 412 413 414 415 416 417 418 419 420 421 422 423 424 425 426 427 428 429 430 § A cloração que é realizada apenas uma vez por dia, durante o turno da noite, não é suficiente para garantir a segurança microbiológica para os usuários da piscina, uma vez que não favorece o estabelecimento da forma mais eficaz de residual. Diante dessas conclusões, e, à guisa de contribuição para melhoria das condições de funcionamento da piscina do IFCE, apresentamos as seguintes considerações e sugestões: § Realização de ensaios laboratoriais (demanda de cloro, Potencial de OxidaçãoRedução, cor, turbidez, etc), que possibilitem a orientação do tratamento e o estabelecimento das dosagens adequadas. § Eliminação da cloração intermitente pela instalação de uma bomba dosadora, que possibilite a manutenção de um residual de cloro livre durante todo o dia. § Realização de análises microbiológicas periódicas. § Implantação de um Programa de manutenção e Tratamento com base nas boas práticas de tratamento e na norma NBR 10.818 (Qualidade de água de piscinas). Referências A.W.W.A., Água Tratamento e Qualidade, Rio de Janeiro, 1964. APHA – AWWA – WEF. Standards Methods for Examination of Water and Wasterwater. 20th Ed. Washington DC., USA: American Public Health Association, 1998. BRASIL, Portaria n 518/GM, de 25 de março de 2004. Estabelece os procedimentos e responsabilidades relativas ao controle e vigilância da qualidade da água para consumo humano e seu padrão de potabilidade e dá outras providências. Diário oficial [da república federativa do Brasil], Brasília, 26 março de 2004. CETESB, Técnica de Abastecimento e Tratamento de Água, São Paulo, 1977. CETESB. Água, saúde e desinfecção – Série Manuais 13. São Paulo: CETESB - Companhia de Tecnologia de Saneamento Ambiental. 1994. DI BERNARDO, L., Ensaios de Tratabilidade da Água e dos Resíduos Gerados em Estações de Tratamento de Água, São Carlos, 2002. FUNASA, Manual de Saneamento – Orientações Técnicas, Brasília, 2004. GOMES, H. P., Sistemas de Abastecimento de Água, Dimensionamento Econômico e Operação de Redes e Elevatórias, UFPB Editora Universitária, 2004. HAMMER, M., J., Sistemas de Abastecimento de Água e Esgotos, Livros Técnicos e Científicos Editora, 1979. LÍBANIO, M., Fundamentos de Qualidade e Tratamento de Água, Editora Átomo, 2005. 12 431 432 433 434 435 436 437 438 439 440 441 442 443 444 445 446 447 448 449 450 451 452 453 454 455 456 457 458 459 460 461 462 463 464 465 466 467 468 469 470 471 MACÊDO, J. A. B. O processo de desinfecção pelo uso de derivados clorados em função do pH e a Portaria 518/2004 do Ministério da Saúde. Congresso Brasileiro de Química, 2004. Fortaleza. Disponível em: www.aguaseaguas.ufjf.br. MACEDO, J. A. B., BARRA, M. M., Derivados clorados de origem orgânica uma solução para o processo desinfecção de água potável e para desinfecção de indústrias. VI Simpósio Ítalo Brasileiro de Engenharia Sanitária e Ambiental (SIBESA), 2002. Disponível em: www.aguaseaguas.ufjf.br. MACÊDO, J. A. B. Importância do processo de desinfecção em águas de piscinas. Disponível em: www.aguaseaguas.ufjf.br. MOTA, S., Introdução à Engenharia Sanitária e Ambiental. Rio de Janeiro: ABES, 1997. NETO, J. G. V., KOIDE, S., BRANDÃO, C. C. S., Metodologia para seleção de pontos de amostragem de água em redes de distribuição. XXVII Congresso Interamericano de Engenharia Sanitária e Ambiental - ABES. NBR 10.819 (Projeto e execução de piscinas – casa de máquinas, vestiários e banheiros), Rio de Janeiro, Associação Brasileira de Normas Técnicas, 1998. NBR 10.339 (Projeto e execução de piscinas – sistema de recirculação e tratamento), Rio de Janeiro, Associação Brasileira de Normas Técnicas, 1987 OHLWEILER, O. A., Química Analítica Quantitativa - Livros Técnicos e Científicos Editora Ltda, 1981. OPAS – OMS – ILSI Argentina, La Calidad Del Água Potable em América Latina, Ponderación de los riesgos Microbiológicos contra los riesgos de los subproductos de la desinfección química, ILSI Press, Washington, DC, 1996. PAES L.F., Teoria e Técnica de Tratamento de Água – ABES, 1990. RICHTER, C. A.; AZEVEDO N. J. M., Tratamento de Água – Tecnologia Atualizada, Editora Edgard Blücher Ltda, 1991. SOARES, J. B., M., FREIRE, A. C., Água: Microbiologia e Tratamento, 1999. VIEIRA, M., Tratamento de Água e Manutenção de Piscinas. Semana Nacional de Ciência e Tecnologia do CEFETCe, 2004. 13
Download