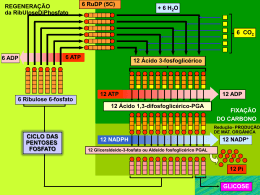
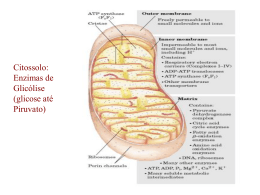
Introdução ao Metabolismo 1. Considerar o mapa metabólico simplificado apresentado em classe e responder: (a) Quais são os passos irreversíveis que aparecem no mapa? Os passos irreversíveis são: PIRUVATO ACETIL-CoA + CO2 AMINOÁCIDOS CETOGÊNICOS ACETIL-CoA OXALOACETATO + ACETIL-CoA CITRATO -CETOGLUTARATO SUCCINATO + CO2 (b) Qual é o primeiro composto comum que aparece na de-gradação de proteínas, lipídeos e carboidratos? ACETIL-CoA (c) Animais de laboratório foram submetidos a dietas compostas exclusivamente de carboidratos, ou lipídeos, ou proteínas. Analisar em que caso haveria sobrevivência, verificando se é possível sintetizar: ácido graxo a partir de glicose Sim, utilizando as vias: glicosepiruvatoacetil-CoAácido graxo proteína a partir de glicose Seria possível sintetizar alguns aminoácidos glicogênicos glicose a partir de ácido graxo Não, pois, a conversão piruvato acetil-CoA é irreversível. proteína a partir de ácido graxo Não glicose a partir de proteína Não, a partir de glicose são produzidos apenas aminoácidos não essenciais. Como uma proteína contem, em geral, aminoácidos essenciais e não essenciais, a resposta é negativa. ácido graxo a partir de proteína Sim, pelas vias: proteínasacetil-CoAácido graxo Em cada caso afirmativo, indicar a via utilizada 2. Que compostos um indivíduo deve obrigatoriamente receber na dieta? Utilizar apenas as informações do mapa metabólico simplificado. Proteínas contendo aminoácidos glicogênicos e micronutrientes (metais, vitaminas). 3. Glicose é utilizada como fonte de energia para a célula, ou organismo com a finalidade de produzir ATP. O excesso de glicose pode ser convertido em gordura. O esquema simplificado abaixo mostra estas duas possibilidades: ATP GlicoseBcitratoC DECO2 + ATP + H2O (citrato) F G ácidos graxos Discuta: (a) Neste esquema, quais são as possíveis reações catalisadas por enzimas alostéricas? BF CD São as reações onde aparecem no esquema, os efetores indicados. Sendo citrato o efetor positivo da enzima que catalisa a conversão BF e ATP o efetor negativo da enzima que catalisa a conversão CD. (b) Como funciona o esquema acima quando há disponibilidade de muita glicose? Neste caso, o "excesso" de ATP formado vai funcionar como efetor negativo da enzima que catalisa a conversão CD, levando à um acúmulo de citrato. O citrato por sua vez, irá funcionar como efetor positivo da enzima que catalisa a reação BF, acelerando a produção de ácidos graxos. Portanto, glicose em "excesso" leva à produção de gorduras. (c) O substrato B pode dar origem a dois produtos diferentes. Faça os gráficos de velocidade em função da concentração de B para cada uma das enzimas. (d) Quando houver pouca disponibilidade de B qual seu caminho preferencial? Por quê? Quando houver pouca disponibilidade de B, o caminho preferencial é a formação de ATP, pois, neste caso, o nível ATP estaria baixo, a enzima que catalisa a conversão CD não estaria inibida, não ocorreria, portanto, acúmulo de citrato. Neste caso, a via de formação de ácidos graxos nào estaria ativada. 4. Lehninger, Principles of Biochemistry, Capítulo 13, Problema 5. Comparação entre via catabólica e via anabólica. A interconversão de glicose a frutose-1,6-difosfato, uma série muito importante de etapas no metabolismo de carboidratos, é mostrada em classe. A quebra da glicose constitui a via catabólica, enquanto a biossíntese de glicose a partir de frutose-1,6-difosfato corresponde a via anabólica. Ambas as vias usam as mesmas hexoses monofosfato intermediárias. Embora estas vias tenham semelhanças, elas apresentam diferenças básicas. A finalidade deste exercício é reconhecê-las. Glicose ATP Pi hexoquinase glicose-6-fosfatase ADP H2O Glicose-6-fosfato isomerase ATP fosfofrutoquinase ADP isomerase Frutose-6-fosfato Pi frutose difosfatase H2O Frutose-1,6-difosfato (a) Esquematize a reação balanceada para cada passo na via catabólica. Escreva a equação líquida que resulta quando soma-se os passos individuais. Glicose + ATPGlicose 6-fosfato + ADP Glicose 6-fosfatoFrutose 6-fosfato Frutose 6-fosfato + ATP Frutose 1,6-difosfato + ADP _______________________________________________ Glicose + 2 ATP Frutose 1,6-difosfato + 2 ADP (b) Repita o item (a) para a via anabólica. Frutose 1,6-difosfato + H2OFrutose 6-fosfato + Pi Frutose 6-fosfatoGlicose 6-fosfato Glicose 6-fosfato + H2OGlicose + Pi _____________________________________________ Frutose 1,6-difosfato + 2 H2O glicose + 2 Pi (c) Baseado nas equações líquidas, quais são as diferenças que podem ser notadas entre as vias catabólica e anabólica? As duas vias são simplesmente o reverso uma da outra? Apesar de envolverem os mesmos intermediários, elas não são simplesmente a reversão da mesma via. O catabolismo consome 2 ATP e gera 2 ADP. O anabolismo consome 2 H2O e gera 2 Pi. As enzimas envovidas são diferentes (com exceção da isomerase). Isto permite que as vias tenham regulação independente. (d) O que assegura o sentido das reações individuais no catabolismo da glicose? Ou seja, o que impede que no catabolismo da glicose passe a ocorrer por vias reversas? O sentido é garantido pelo favarecimento termodinâmico de transferência de ATP para a glicose. (e) Nas vias catabólica e anabólica, a interconversão de glicose e glicose-6-fosfato poderia ser catalisada pela mesma enzima? Explique. A interconversão de glicose-6fosfato e frutose-6-fosfato nas vias catabólica e anabólica poderia ser catalisada pela mesma enzima? Explique ,Nas reações citadas, no catabolismo, a enzima transfere um fosforil grupo do ATP para um aceptor, é portanto uma quinase. No anabolismo, ocorre a hidrólise dos substratos fosforilados, a enzima é portanto uma fosfatase. Glicólise 1. Stryer, Biochemistry 3a edição, Capítulo 15, Problema 3. Escreva a equação balanceada para a conversão da Glicose a Lactato. Glicose + 2 Pi + 2 ADP2 Lactato + 2 ATP (a) Calcule a variação de energia livre padrão desta reação usando os dados apresentados na tabela 15-2 do capítulo 15 de Stryer (3a edição) e levando em conta que o Go' para a reação Piruvato + NADH + H+ Lactato + NAD+, é igual a -6 Kcal/mol Para resolução, basta somar o Go' de cada uma das reações individuais. Não esquecer, que à partir do gliceraldeído temos 2x cada reação, devendo o Go'ser então multiplicado por 2. Resp: Go' =-29,5 Kcal/mol (b) Qual é a variação de energia livre ( G' e não Go') para esta reação quando as concentrações de reagentes e produtos são: Glicose 5 mM ADP 0,2 mM Lactato 0,05 mM Pi 1 mM ATP 2 mM G'= Go' + 2,303 RT log keq G'=-27,2 Kcal/mol 2. Stryer, Biochemistry, 3a edição, Capítulo 15, Problema 2. Glicose marcada com 14C em C-1 é incubada com as enzimas da glicólise e os cofatores necessários. Qual é a distribuiçåo de 14C no Piruvato que é formado? (Considerar que a interconversão entre Gliceraldeído 3-fosfato e Dihidroxiacetona fosfato é muito rápida comparada com o passo subsequente). O metil grupo do piruvato aparece com a marcação CH3 C=O COO3. Discutir a regulação da via glicolítica em função da relação ATP/ADP. Existem dois pontos principais de regulação da via glicolítica em função da relação ATP/ADP: São os pontos regulados pelas enzimas alostéricas : Fosfofrutoquinase e Piruvatoquinase. Fosfofrutoquinase -----------------------------------------------------------------------------------------------------efetores positivos efetores negativos __________________________________________________________________ AMP ATP Frutose 1,6-bifosfato citrato ADP Mg2+ Fosfato Ca2+ K+ Frutose 6-fosfato Frutose 2,6-bifosfato ________________________________________________________________________ Piruvatoquinase -----------------------------------------------------------------------------------------------------efetores positivos efetores negativos _________________________________________________________________ ATP Acetil-CoA Ácidos graxox ______________________________________________________________________ Portanto, um nível alto de ATP irá inibir as duas enzimas alostéricas da via glicolítica. Por outro lado, AMP alto estimula a fosfofrutoquinase. 4. Em relaço a via glicolítica: (a) Verificar os compostos que apresentam ligaçõeses tipo: fosfoenol, anidrido fosfórico e éster fosfórico e identificar aqueles que são compostos ricos em energia Tipo Composto Rico em energia? Fosfoenol Fosfoenolpiruvato Sim Anidrido 1,3-difosfoglicerato* Sim ATP** Sim Éster fosfórico todos os outros intermediários que não estão na forma de anidrido Não *anidrido misto de ácido fosfórico e de ácido carboxilíco ** o ATP tem ligação ester e sua unidade trifosfato contem duas ligações de anidrido fosfórico (b) Indicar as reações de óxidoredução As reações de óxidoredução são aquelas em que participam os carreadores de elétrons (NAD/NADH). (c) Dizer como é regulada a via glicolítica e citar as enzimas e seus moduladores Igual à questão 3.só que devemos também acrescentar a regulação via hexoquinase. Na maioria dos tecidos a reação Glicose + ATPGlicose 6-fosfato + ADP é catalisada pela hexoquinase. O produto de reação, glicose 6-fosfato é um potente inibidor alostérico da enzima. Quando a utilização de glicose 6-fosfato pela via glicolítica diminui, sua concentração aumenta e a hexoquinase fica inibida, restringindo a fosforilação da glicose e , portanto ajustando a captação do açúcar pelo tecido à sua utilização. No fígado a situação é diferente, pela presença de outra enzima responsável pela fosforilação da glicose, a glicoquinase. A glicoquinase não sofre inibição por glicose-6-fosfato, permitindo o armazenamento da glicose como glicogênio. (d) Mostrar os passos irreversíveis que fazem parte do mapa Os pontos irreversíveis são os catalisados pelas enzimas reguladoras: Glicoseglicose 6-fosfato Frutose 6-fosfatofrutose 1,6-bifosfato Fosfoenolpiruvatopiruvato (e) Determinar quantas moléculas de Ácido Pirúvico se formam a partir de uma molécula de hexose. Formam-se duas moléculas de ácido pirúvico. Na reação catalisada pela aldolase ocorre a quebra da molécula de seis carbonos em duas unidades de 3 carbonos (diidroxiacetona fosfato e gliceraldeído 3-fosfato). 5. Rawn, Biochemistry, Capítulo, 12, Problema 14. Uma pessoa incapaz de executar exercícios intensos e prolongados teve suas enzimas analisadas. Todas as enzimas da via glicolítica estavam em concentraçåo normal, com excessão da fosfoglicerato mutase muscular. (a) Como será afetada a produção de energia metabólica em uma célula que apresenta baixos níveis desta enzima? A produção de energia fica reduzida, pois, a pessoa não consegue obter energia suficiente pela via glicolítica. Quando vai executar exercícios intensos, a necessidade de ATP no músculo excede a capacitade do organismo em aerar o tecido, portanto, a obtenção de energia via glicólise anaeróbica fica bastate importante. por este motivo, o indivíduo não consegue executar exercícios prolongados. (b) Como será afetada a produção de Lactato na ausência desta enzima? [Referência: Di Mauro, S.; Miranda, A.F.; Kahn, S.; Gitlin, K. - Human muscle phosphoglycerate mutase deficiency Science 212: 1277-1279, 1981]. Na ausência desta enzima não é possível a produção de lactato. -Oxidação 1. Carnitina é amplamente distribuída nos tecidos, mas atinge concentração elevada no músculo. O que sugere este dado? A oxidação de ácidos graxos é intensa no músculo, portanto a carnitina, que transporta o acil-CoA para o interior da mitocôndria, tem que ter concentração elevada 2. Cite os compostos que devem ser fornecidos para a manutenção da espiral de Lynen. acil-CoA FAD NAD CoA-SH 3. Compare a oxidação de 3 Glicose _____> Acetil-CoA, com a oxidação de Ácido Láurico (12C) a Acetil-CoA, quanto 3Glicose Oxidação (12C) (a) Número de moléculas de Acetil-CoA formadas 6 6 (b) Liberação de CO2 6 0 (c) Gasto em ATP 6 1ATP+1PPi (d) Saldo de ATP 6 -2ATP (e) Número de moléculas de NADH 12 5 FADH2 formadas 0 5 (f) Coenzimas e vitaminas NAD+ NAD+ FAD FAD CoA CoA ác. lipóico tiamina pirofosfato nicotinamida nicotinamida riboflavina riboflavina ác. pantotênico ác. pantotênico tiamina (g) Localização celular citossol até piruvato citossol ativação mit. piruvato acetil-CoA mit. espiral Lynen 4. Indique o caminho percorrido pelos carbonos do Glicerol na sua transformação a Acetil CoA. glicerol 3-fosfato desidrogenase Glicerol + ATP + NAD+ diidroxiacetona fosfato + ADP + NADH + H+ diidroxiacetona fosfato via glicolítica piruvato acetil CoA Cadeia Respiratória 1. A relação entre energia livre de uma reação e o potencial redox é: Go' = -nFEo' onde n é o número de elétrons transferidos F é a constante de Faraday (F = 23.060 cal V-1) Eo' é o potencial padrão da dupla redox. Utilizar esta relação para calcular os pontos da cadeia respiratória onde a energia "liberada" na reação de transferência de elétrons poderia ser usada para a síntese de um composto rico em energia, aproximadamente +7300 cal/mol. A relação entre energia livre e potencial redox é: Go'=-nFEo' portanto, devemos aplicar a equação para cada etapa do transporte de elétrons. Lembrar que n= número de elétrons transferidos e para cada molécula de H2O formada temos a transferência de 2 elétrons uma vez que: 1/2 O2 + 2 H+ + 2 e-H2O Os dados de Eo' encontram-se tabelados nos livros. por exemplo: para a primeira reação: NADH + H+ + E-FMNNAD+ + E-FMNH2 Eo'=+0,02 V Go'= -2 (23,062) (0.02) Go'= -0.9 Kcal/mol, e assim por diante. A tabela abaixo dá os valores calculados para cada etapa. ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------Eo ' Go' (volts) Kcal/mol ---------------------------------------------------------------------------------------------------------------------------------------------------------------------------------NADH + H+ + E-FMNNAD+ + E-FMNH2 +0.02 -0.92 E-FMNH2 + CoQ + 2H+E-FMN + CoQH2 +0.34 -15.7 CoQH2 + 2cit b (FeII)2CoQ + 2H+ + 2 cit b (FeII) -0.03 +0.03 2cit b(FeII) + 2 cit c1 (Fe II)2 cit b (FeIII)+ 2 cit c1(Fe II) 0.16 -7.3 2 cit c1(FeII) + 2 cit c (FeIII)2 cit c1 (FeIII) + 2 cit c (FeII) +0.02 -0.92 2 cit c (FeII) + 2 cit a/a3 (Fe III)2 cit c (Fe III) + 2 cit a/a3 (FeII) +0.04 -1.8 2 cit a/a3 (FeII) + 1/2 O2 + 2 H+2 cit a/a3 (FeIII) + H2O +0.30 -13.8 ------------------------------------------------------------------------------------------------------------------------------------------------------------------ Na pergunta queremos saber em que pontos temos energia para produzir ATP ADP + Pi ATP + H2O Go'= +7,3 kcal /mol, precisamos, portanto, liberar no mínimo esta energia. Pela tabela temos que as etapas onde isto é possível são as escritas em negrito. temos 3 sítios onde é possível a formação de ATP. O gráfico abaixo ilustra a resolução do problema. 2. A uma solução 1 M de NAD+, NADH, Piruvato e Lactato, adicionou-se lactato desidrogenase: Lactato + NAD+ Piruvato + NADH + H+ Eo' (NAD+/NADH) = -0,32 V Eo' (Piruvato/Lactato) = -0,19 V a) Em que sentido a reação ocorrerá? Sempre o par com Eo' mais negativo doa elétrons para o par com Eo' mais positivo portanto: NADH + H+ NAD+ + 2H+ + 2 e (doação de 2 e). Piruvato + 2H+ + 2e Lactato (recebimento de 2 e. ------------------------------------------------------------- +---Piruvato + NADH + H+ Lactato + NAD+ Este é o sentido da reação. b) À medida que a reação ocorre, como variam esses potenciais redox? Para resolver este problema temos que aplicar a equação: E=Eo' + (2.303RT/nF) log [ forma oxidada]/[forma reduzida] E0’1 e E1 = potencial padrão e potencial de eletrodo para o par NAD+ /NADH E0’2 e E2= potencial padrão e potencial de eletrodo para o par Piruvato/Lactato Para o par piruvato/lactato temos: E2=Eo2' + (2.303RT/nF) log [piruvato]/[lactato] com o decorrer da reação a concentração de piruvato vai diminuir e a concentração de lactato vai aumentar, portanto o termo log [piruvato]/[lactato] tende a ficar negativo e E2 vai ficando menor que Eo'2. para o par NAD+/NADH temos: E1=Eo'1 + (2.303RT/nF )log [NAD+]/[NADH] com o decorrer da reação a concentração de NADH vai diminuir e a concentração de NAD+ vai aumentar, portanto o termo log [NAD+]/[NADH] tende a ficar mais positivo e E1 vai ficando maior que Eo'1. c) Quando a reação atingirá o equilíbrio? Qual o valor do potencial redox (E) nessa situação? E1=E01' + (2.303RT/nF) log [NAD+]/[NADH] (equação 1) E2=E02' + (2.303RT/nF) log [piruvato]/[lactato] (equação 2) No equlíbrio [NAD+]=[Lactato] e [NADH]=[Piruvato] Vamos rearranjar a equação 2 invertendo a fração do termo logarítmico: E2=E02' - (2.303RT/nF) log [Lactato]/[Piruvato] (equação 2 rearranjada) Somando as equações 1 e 2 rearranjada: E1=E01' + (2.303RT/nF) log [NAD+]/[NADH] (equação 1) E2=E02' - (2.303RT/nF) log [Lactato]/[Piruvato] (equação 2 rearranjada) --------------------------------------------------------------------------------------+-E1 +E2 = E01' + E02' , uma vez que os termos que contém os logs das frações se cancelam. Portanto, E1 +E2 = -0.19 + (-0.32) = - 0.51 V como no equilíbrio E1 = E2, o potencial de ambos os eletrodos é igual a -0.255 V, não há passagem de corrente elétrica entre os eletrodos. Portanto, E = 0. 3. Citar as consequências dos seguintes fatores para o funcionamento da cadeia respiratória e da fosforilaçåo oxidativa: a) Presença de KCN ou CO KCN e CO são inibidores da cadeia de transporte de elétrons, como os dois processos estão acoplados, inibindo a cadeia de transporte de elétrons temos a inibição da fosforilação oxidativa. b) Carência de Pi c) Carência de ADP ADP e Pi são necessários para a fosforilação oxidativa, como os dois processos estão acoplados, inibindo a fosforilação oxidativa temos a inibição da cadeia de transporte de elétrons d) Presença de DNP (dinitrofenol) O DNP é um desacoplador da fosforilação oxidativa. Ele desfaz o gradiente de protóns na mitocondria. A cadeia de transporte de elétrons não é afetada e temos supressão da fosforilação oxidativa. e) Carência de Pi e/ou ADP em presença de DNP Neste caso como os processos estão desacoplados, a cadeia de transporte de elétrons não é afetada e temo supressão da fosforilação oxidativa, mesmo na ausência de ADP e/ou Pi. f) Presença de oligomicina A oligamicina é um inibidor da fração Fo da ATP sintetase, como os dois processos estão acoplados, inibindo a fosforilação oxidativa temos a inibição da cadeia de transporte de elétrons g) Presença de oligomicina + DNP Neste caso como os processos estão desacoplados, a cadeia de transporte de elétrons não é afetada e temos supressão da fosforilação oxidativa ( o efeito do DNP sobrepõem-se ao efeito da oligomicina). 4. Uma droga X inibe o consumo de O2 e a síntese de ATP em uma suspensão de mitocôndrias. Que tipo de droga deveria ser adicionada para se determinar o modo de ação da droga X? Como não sabemos se o inibidor funciona inibindo a cadeia de transporte de elétrons ou a fosforilação oxidativa, devemos colocar um desacoplador, por exemplo DNP. Neste caso podemos obter dois resultados: Resultado 1: Não se verifica consumo de oxigênio. Mesmo na presença de DNP continuamos a verificar a inibição dos dois processos. Neste caso a droga X é um inibidor da cadeia de transporte de elétrons. Resultado 2: Verifica-se consumo de oxigênio. Na presença de DNP verificamos que a cadeia de transporte de elétrons funciona e a fosforilação oxidativa é suprimida. Neste caso a droga X é um inibidor da fosforilação oxidativa não interfirindo na cadeia de transporte quando desacoplada.. 5. Calcular o número de moléculas de ATPs formadas na oxidação total de: I. glicose (uma molécula) O cálculo pode ser obtido à partir das etapas em que o processo se divide, ou seja: a-oxidação de glicose a 2 piruvato b-oxidação de 2 piruvato a 2 acetil-CoA c-oxidação de 2 acetil-CoA pelo ciclo de Krebs d-oxidação das coenzimas pela cadeia respiratória coenzimas produzidas a 2NADH b 2NADH c 6NADH 2FADH2 (a+b+c) 10NADH 2FADH2 ATP 30 4 fosforilação ao nível substrato 2ATP 2GTP 4ATP 4 -----------------------------------------------------------------------------------------------------------------------TOTAL = 38ATP Em algumas células ( tecido muscular) a oxidação aeróbica de glicose produz 36 ATP, pois o NADH produzido no citossol é transferido para a mitocôndria pela lançadeira glicerol fosfato. NADH + H+ + Diidroxiacetona fosfatoglicerol 3-fosfato + NAD+ (citossol) O glicerol 3-fosfato chega até a face externa da membrana interna da mitocôndria, onde se localiza uma outra glicerol fosfato desidrogenase que contém FAD como grupo prostético Glicerol 3-fosfato + FADDiidroxiacetona fosfato + FADH2 (mitocôndria) Portanto os NADH do citossol vão gerar FADH2 mitocondrial. Nas células que ocupam a lançadeira malato-aspartato temos o rendimento de 38 ATPs pois, neste caso temos regenerado NADH mitocondrial Oxaloacetato + NADH + H+Malato + NAD+ (citossol) Malato + NAD+ oxaloacetato + NADH + H+ (mitocôndria) II. ácido palmítico (16C) (uma molécula) a-ativação: b-espiral de Lynen c-oxidação de 8 acetil-CoA pelo ciclo de Krebs d-oxidação das coenzimas reduzidas pela cadeia respiratória a-gasto de 2 ligações ricas em energia (1 ATP + 1 PPi) =2ATP b-em cada volta são produzidos 1NADH e 1 FADH2, como são 7 voltas temos 7 NADH e 7 FADH2. c-na espiral são produzidos 8 acetil-CoA cada um produz no ciclo de Krebs 3 NADH, 1FADH2 e um GTP temos que multiplicar por 8, resultando em 24 NADH, 8 FADH2 e 8 GTP. d-na cadeia respiratória Coenzimas ATPs formados 7 NADH (espiral) 21 7 FADH2 (espiral) 14 24 NADH (Krebs) 72 8 FADH2(Krebs) 16 ----------------------------------------------------------------------total 123 devemos acrescentar + 8 GTP (Krebs) 123 ATP + 8 GTP= 131 ATP subtraindo as duas ligações ricas em energia consumidas na ativação temos: 131 ATP - 2 ATP= 129 ATP a) Qual seria o destino da energia não armazenada sob a forma de ATP? É liberada na forma de calor. Esta liberação de energia torna o Go'0 deixando o processo geral irreversivel. b) Qual seria o resultado na presença de dinitrofenol? Na presença de DNP, não existe formação de ATP pela fosforilação oxidativa, só aqueles formados à nível de substrato. Teríamos portanto a formação só de 8GTP. Descontando os ATPs utilizados na ativação: 8 ATP - 2 ligações ricas em energia= 6 ATPs. 6. Discutir o funcionamento do ciclo de Krebs, beta-oxidação e via glicolítica em uma suspensão de células hepáticas na presença dos seguintes compostos: antimicina Na presença de antimicina temos a inibição da cadeia respiratória (transporte de elétrons). Por consequência as vias de metabolismo que dependem do oxigênio estão desativadas: ciclo de Krebs e beta-oxidação ( não há reoxidação das coenzimas reduzidas), funciona apenas a glicólise anaeróbica ( glicose lactato), produzindo 2 moléculas de ATP por molécula de glicose). Oligomicina Na presença deste inibidor de fosforilação oxidativa temos também inibição do transporte de elétrons (processos acoplados). Por consequência as vias de metabolismo que dependem do oxigênio estão desativadas: ciclo de Krebs e beta-oxidação ( não há reoxidação das coenzimas reduzidas), funciona apenas a glicólise anaeróbica ( glicose lactato), produzindo 2 moléculas de ATP por molécula de glicose). Dinitrofenol É um desacoplador, desfaz o gradiente de prótons permitindo a ocorrência da cadeia respiratória sem síntese de ATP. Haverá metabolismo aeróbico de glicose, oxidaçã e ciclo de Krebs, porém, serão formados apenas ATPs ao nível de substrato. Antimicina + dinitrofenol Seguindo o raciocínio acima, na presença de DNP, continuamos com os dois processos inibidos, uma vez que a antimicina continua inibindo o transporte de elétrons. Como no caso de antimicina sozinha, as vias de metabolismo que dependem do oxigênio estão desativadas: ciclo de Krebs e beta-oxidação ( não há reoxidação das coenzimas reduzidas), funciona apenas a glicólise anaeróbica ( glicose lactato), produzindo 2 moléculas de ATP por molécula de glicose). oligomicina + dinitrofenol. Neste caso, a presença de DNP desacopla o processo, e como não temos inibidores da cadeia de transporte de elétrons, ela vai ocorrer, ficando a fosforilação oxidativa inibida. Como os elétrons chegam até o oxigênio, ocorrem o ciclo de Krebs e beta-oxidação, porém só se formam ATP ao nível de substrato. A glicólise vai até piruvato. 7. A membrana externa da mitocôndria é permeável à maioria dos solutos de baixo peso molecular. A membrana interna, entretanto, possui seletividade, sendo impermeável por exemplo a coenzimas, nucleosídeos, etc. De posse dessas informações responder as seguintes indagações: a) Como os acil-CoA produzidos após ativação dos ácidos graxos podem ser degradados na beta-oxidação? b) Como o NADH produzido na via glicolítica pode ser reoxidado na cadeia respiratória? c) Como o ATP produzido na cadeia respiratória pode ser utilizado nas biossínteses que ocorrem no citoplasma? Prestar atenção no tranportador 6. Ele é inibido por uma droga chamada atractilosídeo. 8. Um microorganismo aeróbico facultativo é cultivado em meio líquido glicosado com aeração e sem aeração. Em qual das duas culturas o consumo de glicose pelas células é maior? Justificar a resposta em termos de regulação metabólica. com aeração: glicose CO2 + H2O + 38 ATPs sem aeração:glicose Lactato + 2 ATPs o rendimento de ATP/glicose é muito maior no caso aeróbico. O consumo de glicose é portanto, menor no meio aerado. No caso do metabolismo aeróbico a economia no consumo de glicose é explicada pela alta relação ATP/ADP. ADP baixo deixa de estimular a cadeia respiratória e também a isocitrato desidrogenase, o que acarreta um acúmulo de citrato. Citrato e ATP altos no citossol inibem alostericamente a fosfofrutoquinase 1. 9. Aceita-se que a oxidação de NADH ao nível de cadeia respiratória produz, em média, 3 ATP. É conhecido que existem "sítios" de produção de ATP (quais?). Discutir a relação estequiométrica e a existência de "sítios" à luz da teoria do acoplamento quimiosmótico. (Ver na página seguinte) METABOLISMO DE AMINOÁCIDOS Proteinas da dieta Proteinas endogenas AMINOÁCIDOS Compostos nitrogenados não-proteicos Cadeia Carbônica NH3 UREIA 1+ NADPH + H + NH4 + Glutamato desidrogenase + -Cetaglutarato Glutamato + NADP+ + H2O. Transaminase A.A. + -Cetoglutarato -Cetoácido + Glutamato Sendo as reações reversíveis, o que vai determinar a sua direção é a disponibilidade de reagentes e a remoção contínua dos produtos formados. 2. Oxidação de Lactato LactatoPiruvato Piruvato Acetil-CoA Acetil-CoA CO2 Equiva. Redutor NADH ATP produzido 3ATP NADH 3NADH FADH2 3ATP 9ATP 2ATP 1ATP [GTP] ------18ATP Alanina TRANSAMINASE Alanina + -Cetaglutarato Piruvato + Glutamato Glutamato DESIDROGENASE. Glutamato + NAD+ + H2O NADH + H+ + NH4+ + -Cetaglutarato ___________________________________________________________________ Alanina + NAD+ + H2O NADH + H+ + NH4+ + Piruvato Alanina Piruvato Acetil-CoA Piruvato Acetil-CoA CO2 NADH e !![NH4+] NADH 3NADH FADH2 3ATP 3ATP 9ATP 2ATP 1ATP [GTP] ------18ATP !!!!!!Remoção de Nitrogênio 2ATP para Carbamoil-P 2ATP (ATP+PPi) para Citrulina/Aspartato CO2 + 2 NH4+ + 4 ATP + 2 H2O UREIA + 4 ADP + 4 Pi (I) Portanto, utilizamos 4 ATP para remover o nitrogênio como uréia. Notar que na equação acima temos 2 NH4+ , consideramos que temos aspartato para doar o outro amino grupo. Neste caso o rendimento para a oxidação da alanina é: 18 ATP - 4 ATP= 14 ATP. Outra maneira de resolver é pensando que só temos 1 molécula de alanina ( sem considerar o aspartato). Neste caso dividimos a equação I por dois, pois só temos 1 NH4+ para remover. Temos neste caso o gasto de 2 ATP e o rendimento de oxidação da alanina fica: 18 ATP - 2 ATP=16 ATP. 3 Esquema Apostila (Músculo, Sangue, Figado) 4. a/ PROTEINA Fenilalanina Fenilalanina 4-monooxigenase TIROSINA Melanina TRANSAMINASE Fenilpiruvato Fenilactato b/ O metabolismo normal de fenilalanina Tirosina está bloqueado levando a um aumento na concentração de fenilalanina que será excretada na urina. c/ Fenilalanina é convertida em fenilpiruvato via reação de fenilalanina transaminase. Desde que a constante de equilíbrio é igual a 1, a reação é deslocada para a formação de fenilpiruvato quando aumenta a concentração de fenilalanina. d/ Tirosina e precursor da sintese de melanina que da pigmentação à pele e cabelo. Uma deficiência em tirosina acarreta em deficiência em melanina. 5. Em um primeiro caso , imaginamos que a dieta contem todos os amonoácidos essencias só que em baixa quantidade. Neste caso a ingestão de proteínas deveria ser em is quantidade maior para obter um nivel de A.A. essenciais para a sintese de proteinas. Em outro caso, a dieta não contem todos os aminoácidos essenciais. Neste caso, para previnir sintomas de desnutrição, deveria haver complementação alimentar com outro tipo de alimento, ou diretamente com os aminoácidos que estão em falta. BALANÇO NITROGENADO (BN) Ingestão de Nitrogenio proteico = perda de Nitrogenio pelas Fezes e urina BN negativo Excreta mais que absorve ex: Febre alta, doença degenerativa, velhice. BN positivo Absorve mais que excreta ex: crescimento, gravidez, lactação, recuperação de uma doenca +
Download