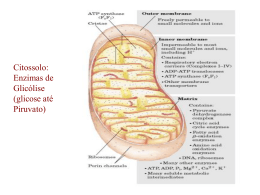
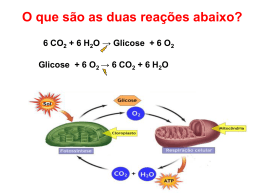
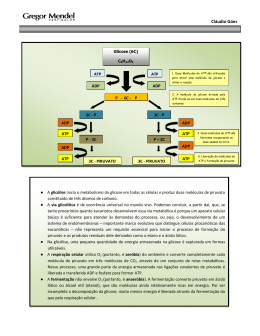
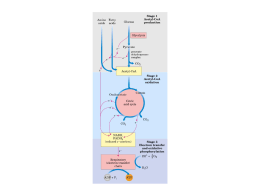
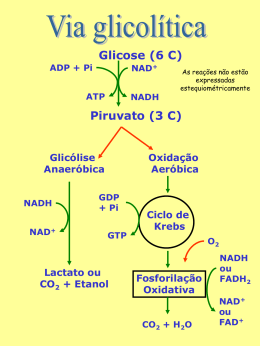
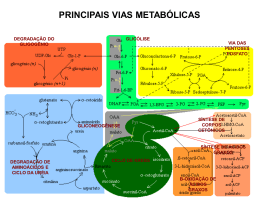
Bioquímica Nutricional Profa. Ana Maria Feoli Profa. Sônia Alscher Curso de Especialização em Terapia Nutricional Parenteral e Enteral – FAENFI/ PUCRS • Dia 29/04: Metabolismo Energético; Metabolismo dos Carboidratos; • Dia 12/05: Tópicos especiais em Carboidratos; • Dia 13/05: Metabolismo dos Lipídios e das Proteínas; • Dia 26/05: Inter-relação Metabólica ; • Dia 27/05: Solidificando conhecimentos adquiridos – Estudo dirigido; Metabolismo dos Carboidratos Frutose MONOSSACARÍDEOS Dissacarídeos Sacarose POLISSACARÍDEOS: amido glicogênio fibras Estado Alimentado ACETILCOA Glicólise Mg2+ Mg2+ * Gasto * Gasto 2x Produçã o Produçã o Mg2+ * Mg2+ Todas as células utilizam Glicose para gerar ATP Glicólise Oxidação da glicose em piruvato Características da Glicólise Ocorre no citosol das células; Gera ATP; Reduz o NAD para NADH; Fase Aeróbica x Fase Anaeróbica Glicose 2ADP + Pi 2 ATP 2 NAD+ 2 NADH + 2H+ (2) Piruvato O2 (2) Lactato Sem ou pouco O2 Muitas células são parcialmente ou total mente dependentes de glicose. 120 gramas de glicose / dia = 480 Kcal (2) Piruvato (2) Lactato Lactato desidrogenase Sem ou pouco O2 Hemácias – só fazem glicólise anaeróbica – Não têm mitocôndria. Demais tecidos – fazem glicólise aeróbica conforme a sua capacidade mitocondrial e disponibilidade de oxigênio. Presença de Oxigênio Ciclo de Krebs Cadeia Respiratória Piruvato Complexo Piruvato Desidrogenase Acetil Coa CK Tiamina (B1) Ácido lipóico FAD (B2 – Riboflavina) COASH (vitamina B5 ou ácido pantotênico) NAD (vitamina B3 ou nicotinamida) Ciclo de Krebs Descoberta CK - 1937 2X 3 ATP * 3 ATP * * 2 ATP 3 ATP * Glicose 2 NADH 6 ATP 2 ATP Total 38 ATP Piruvato 2 NADH Acetil CoA CK 6 NADH 6 ATP 18 ATP 2 FADH2 4 ATP 2 GTP 2 ATP Reações Anapleróticas Cadeia Respiratória Coenzima Q Também chamada Ubiquinona. Transfere dois elétrons e dois prótons.. Citocromos São proteínas transportadoras de elétrons. Apresentam um grupo prostético, com Ferro. Os citocromos têm estruturas e propriedades distintas. Deficiência de ferro Transporte de Elétrons O transporte de elétrons da C.R. inicia quando o substrato entrega 2 elétrons e 2 prótons para o NAD e termina quando estas partículas são entregues ao oxigênio formando água. CURIOSIDADES Inibidores São substâncias que atuam sobre os componentes da Cadeia Respiratória impedindo o transporte de elétrons. Inibidores Inibidor Rotenona Amital Local de Atuação NADH CoQ oxidada Antimicina A Cianeto Monóxido de Carbono Cit c oxidado Cit a1e a3 oxidado Cit a1e a3 reduzido Inibidores Desacopladores São substâncias que destroem o acoplamento existente entre o transporte de elétrons e a fosforilação. Em presença de desacopladores o transporte de elétrons se processa normalmente e a síntese de ATP está diminuída. Tecido Adiposo Marrom • Possui muitas mitocôndrias; • Proteína Termogenina; • Os prótons H+ retornam para matriz mitocondrial pelo canal existente nesta proteína; • Energia do retorno produz calor. Estado Alimentado = Anabolismo INSULINA Síntese proteínas Glicólise Glicogênese Lipogênese Glicogênese Insulina Depósito de carboidrato Fonte de energia primária Glicogênio Estoque de glicose; Ligações alfa- 1,4 e alfa 1,6; Estrutura ramificada; Fígado e músculo esquelético. JEJUM = Catabolismo Glicogenólise Glucagon e Epinefrina Glicogênio Fígado x Músculo X Fígado: manutenção da glicemia; síntese (insulina) e degradação (glucagon e epinefrina). Glicogênio - Músculo Trabalho muscular; Regulado por: cálcio - contração muscular, epinefrina - hormônio “luta ou fuga”. Fosforilase Enzima desramificadora e glucagon Gliconeogênese “Glicos” = doce “Neo” = novo “Gênese” = origem Gliconeogênese Jejum Glucagon O principal destino do lactato é a conversão a glicose pela GLICONEOGÊNESE Lactato produzido pelo músculo esquelético ( e outros tecidos) é captado pelo fígado e é convertido em glicose. Ciclo de Cori Acidose Láctica Estado patológico; O acúmulo de ácido lático no sangue, alterando seu pH (menor que 7,2); Origens: da oxidação do piruvato via piruvato desidrogenase; Comprometimento do CK; Sr. Martini chegou ao hospital com falência cardíaca. Após os exames laboratoriais e a anamnese alimentar a equipe de saúde detectou que o Sr. Martini tinha uma dieta deficiente em tiamina e a função alterada (diminuída) das seguintes enzimas: piruvato desidrogenase, alfa cetoglutarato desidrogenase e alfa ceto ácido desidrogenase Dica: A tiamina é uma das vitaminas requeridas na dieta. O seu “turnover” é muito rápido em humanos, e os sintomas de sua deficiência podem se desenvolver após somente 2 semanas de uma dieta pobre em tiamina. Atualmente a deficiência de tiamina está freqüentemente associada com o alcoolismo. O mecanismo para a absorção de tiamina é diretamente e fortemente inibido pelo álcool. Entretanto, a deficiência na absorção pode persistir por muitos meses após o abandono do consumo de álcool. Pergunta: Qual a relação da tiamina e da alteração das enzimas (principalmente a alfa cetoglutarato desidrogenase) na falência cardíaca? A Biotina é uma vitamina. A deficiência de biotina é muito rara em humanos porque ela é requerida em quantidades muito pequenas e é sintetizada pelas bactérias intestinais. Entretanto, a deficiência pode ocorrer em pessoas que têm uma alimentação composta por clara de ovo crua. Os ovos contêm biotina ligada a uma proteína chamada avidina. Se esta proteína não for desnaturada pela cocção ela pode depletar a biotina da dieta, pois interfere em sua absorção. Pergunta: Qual (is) a (s) conseqüência (s) da deficiência de biotina? Explique com base nas reações bioquímicas. Por que a deficiência das vitaminas pantotenato, riboflavina, niacina e tiamina resulta em fadiga? Os hormônios da tireóide modulam a produção e utilização de energia. Um dos efeitos desses hormônios é aumentar a transcrição do genes envolvidos na síntese de enzimas/proteínas. Por exemplo, se ocorrer um aumento da síntese das enzimas mitocôndriais, todas as enzimas do ciclo de krebs e as proteínas da fosforilação oxidativa estarão aumentadas. Qual a relação dessas alterações (hipertiroidismo) com o metabolismo oxidativo? Maria foi admitida na emergência de um hospital de Porto Alegre com acidose lática. Seus níveis plasmáticos de ácido lático estavam elevados e seu pH arterial diminuído. A descompensação acido-básica foi causada pela severa redução na quantidade de oxigênio pela respiração celular (hipóxia). Algumas causas contribuíram para a falta de oxigênio: a brusca queda de pressão sanguínea causada pela hemorragia de uma úlcera gástrica – a hipoperfusão – ou reduzida ‘entrega” de oxigênio para os tecidos. Além disso, a existência prévia de DPOC (doença pulmonar obstrutiva crônica) – onde a capacidade em retirar oxigênio partir do ar inspirado e tranferir para o sangue arterial está reduzida (saturação de oxigênio baixa). Explique como a DPOC e a hipóxia podem causar acidose lática. Obrigada, Até a próxima aula! Ana e Sônia
Download