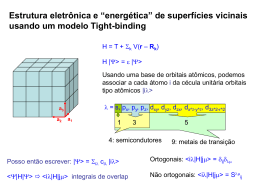
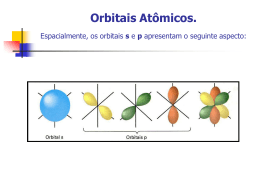
Geometria Molecular e Teorias de ligação Antonio Paulo Rossignolli de Lima Vinícius Renó de Paula nº. 16991 nº. 17032 Curso: Engenharia de Produção Mecânica Importância da Geometria Molecular O estudo da geometria molecular é importante para : • Reações bioquímicas • Sensações de olfato e visão • Abordagens físicas e químicas das substâncias • Entre outros. 15/04/2009 Antonio Lima / Vinícius R. Paula 2 Formas Espaciais Moleculares • Importância da estrutura de Lewis Lewis: bidimensional 15/04/2009 Forma tridimensional Antonio Lima / Vinícius R. Paula 3 Exemplos de Formas Espaciais Moléculas ABn : Moléculas do tipo AB2 15/04/2009 Moléculas do tipo AB3 Antonio Lima / Vinícius R. Paula 4 Exemplos de Formas Espaciais • Cinco geometrias fundamentais 15/04/2009 Antonio Lima / Vinícius R. Paula 5 Exemplos de Formas Espaciais • Estruturas espaciais adicionais 15/04/2009 Antonio Lima / Vinícius R. Paula 6 O Modelo de Repulsão dos Pares de Elétrons no Nível de Valência •Ligação simples, ligação múltipla, par não-ligante => DOMÍNIO DE ELÉTRON • Os domínios de elétrons se repelem • Força de repulsão do domínio: Par não-ligante > Ligação Múltipla > Ligação Simples 15/04/2009 Antonio Lima / Vinícius R. Paula 7 CO2 BF3 CH4 15/04/2009 NO 2- NH3 Antonio Lima / Vinícius R. Paula H2O 8 PCl5 SF6 15/04/2009 SF4 XeF2 ClF3 BrF5 Antonio Lima / Vinícius R. Paula XeF4 9 O Modelo RPENV • Como encontrar a geometria molecular : Exemplo: 15/04/2009 Antonio Lima / Vinícius R. Paula 10 Formas de Moléculas Maiores • Exemplo : Ácido acético 15/04/2009 Antonio Lima / Vinícius R. Paula 11 Polaridade Molecular • Momento dipolar total: soma vetorial dos dipolos de ligação Soma = 0 => molécula apolar Soma ≠ 0 => molécula polar Exemplos: 15/04/2009 Antonio Lima / Vinícius R. Paula 12 Teoria da Ligação de Valência • Noções de ligações por pares de elétrons + idéia de orbitais atômicos => Teoria da ligação de valência • Superposição de orbitais: orbitais compartilham uma região do espaço 15/04/2009 Antonio Lima / Vinícius R. Paula 13 Orbitais Híbridos • Hibridização: Processo de combinação dos orbitais atômicos, variando-os à medida que os átomos se aproximam para formar ligações. Nesse processo formam-se os chamados ORBITAIS HÍBRIDOS Número de orbitais atômicos combinados = Número de orbitais híbridos, onde os orbitais híbridos obtidos são equivalentes, mas apontam para direções diferentes. • Orbitais híbridos sp: 15/04/2009 BeF2 : Antonio Lima / Vinícius R. Paula 14 Orbitais Híbridos (ilustrações): 15/04/2009 Antonio Lima / Vinícius R. Paula 15 Orbitais Híbridos • Orbitais híbridos sp² • Orbitais híbridos sp³ • Também ocorre hibridização envolvendo orbitais d: sp³d, sp³d² 15/04/2009 Antonio Lima / Vinícius R. Paula 16 Orbitais Híbridos e Geometria • 2 sp Linear • 3 sp² Trigonal Plana • 4 sp³ Tetraédrica • 5 sp³d Bipiramidal Trigonal • 6 sp³d² Octaédrica 15/04/2009 Antonio Lima / Vinícius R. Paula 17 Ligações Múltiplas • Ligações sigma (σ): ligações covalentes nas quais a densidade eletrônica concentra-se no eixo internuclear • Ligações pi (π): superposição de dois orbitais p, posicionados de forma perpendicular ao eixo internuclear Ex: Uma ligação σ Uma ligação σ Duas ligações π 15/04/2009 Antonio Lima / Vinícius R. Paula 18 Ligações Múltiplas (ilustrações) • Exemplo: etileno (C2H4) 15/04/2009 Antonio Lima / Vinícius R. Paula 19 Ligações π Delocalizadas • Ligações pi que não podem ser totalmente associadas a dois átomos • Aparecem em moléculas que têm duas ou mais estruturas de ressonância • Exemplo: benzeno (C6H6) 15/04/2009 Antonio Lima / Vinícius R. Paula 20 Orbitais Moleculares • Superposição de orbitais atômicos => Orbitais Moleculares (OM) O número de orbitais atômicos combinados é igual ao número de OM formados Molécula de Hidrogênio (H2 ) : Dois orbitais 1s => formam: um OM ligante e um OM antiligante Diagramas de níveis de energia 15/04/2009 Antonio Lima / Vinícius R. Paula 21 Orbitais Moleculares • Ordem de Ligação: relaciona-se com a estabilidade de uma ligação Ordem de ligação = ½ ( nº de elétrons ligantes – nº de elétrons antiligantes) Se a ordem de ligação =1 ligação simples =2 ligação dupla =3 ligação tripla Se for = 0, significa ligação inexistente 15/04/2009 Antonio Lima / Vinícius R. Paula 22 Orbitais Moleculares - Moléculas diatômicas do segundo Período Orbitais Moleculares para Li 2 e Be 2 : Li2 : Ordem de ligação do 15/04/2009 Be 2 0, portanto, não existe Antonio Lima / Vinícius R. Paula 23 Orbitais Moleculares • Orbitais moleculares a partir de orbitais atômicos 2p Diagrama de níveis de energia 15/04/2009 Antonio Lima / Vinícius R. Paula 24 Orbitais Moleculares • Diagrama de energia para os orbitais moleculares B2,C2,N2 15/04/2009 O2,F2,Ne 2 Antonio Lima / Vinícius R. Paula 25 Orbitais Moleculares •Moléculas diatômicas heteronucleares: Óxido de nitrogênio (NO) : 15/04/2009 Antonio Lima / Vinícius R. Paula 26 Paramagnetismo e Diamagnetismo Paramagnetismo: ocorre em substâncias com elétrons desemparelhados Diamagnetismo: ocorre em substâncias sem elétrons desemparelhados 15/04/2009 Antonio Lima / Vinícius R. Paula 27 Referências Bibliográficas • Química – A Ciência Central, Theodore Brown; edição nº. 9; editora Pearson; ano 2007; Capítulo 9 , páginas: 289 à 327 • http://www2.iq.usp.br/docente/gcazzell/7_LigacaoCovalente_OM.pdf 15/04/2009 Antonio Lima / Vinícius R. Paula 28
Download