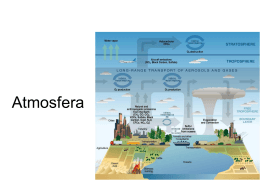
Atmosfera da Terra Dividida em 4 regiões: • Troposfera - limite a tropopausa (12km e 215K) • Estratosfera - limite estratopausa (50km e 275K) • Mesosfera – limite mesopausa (85km) • Termosfera – acima de 85km • 99,9% da massa da atmosfera está localizada na Troposfera e Estratosfera sendo que 75% está na Troposfera Temperatura X Altitude Pressão Atmosférica x Altitude 120 Altitude Pressão Altitude (km) 100 80 60 Pressão (thor) Pressão (thor) 40 20 0 0 200 400 600 Pressão Atmosférica (torr) 800 Composiçao da atmosfera Composição do ar seco próximo do nível do mar Componente Teor (fração em qtde de matéria) Massa molar Nitrogênio 0,78084 28,013 Oxigênio 0,20948 31,998 Argônio 0,00934 39,948 Dióxido de carbono 0,000375 44,0099 Neônio 0,00001818 20,183 Hélio 0,00000524 4,003 Metano 0,000002 Criptônio 0,00000114 83,80 Hidrogênio 0,0000005 2,0159 Óxido nitroso 0,0000005 44,0128 Xenônio 0,000000087 16,043 131,30 Regiões externas da atmosfera •Contribui principalmente contra as precipitaçãos de radiação e de partículas de alta energia. Efeitos das precipitações: • Fotodissociação – É a quebra de uma ligação química resultante da absorção de um fóton por uma molécula Ex: O2(g) + hv →2O(g) •A energia mínima necessária para provocar a dissociação do O2 é de 495kJ/mol Exercício exemplo: Qual o comprimento de onda máximo de luz(em nanômetros) que tem energia suficiente por fóton para dissociar a molécula de O2? Resolução: Sabemos que a energia de dissociação do O2 é de 495 kj/mol , portanto : (495 x 103 J/mol)(1 mol/6,022 x 1023 moléculas) = 8,22 x 10-19 J/molécula Usando a relação de Plank E=hv calculamos a freqüência : v = E/h = 8,22 x 10-19 J/6,626 x 10-34 J/s = 1.24 x 1015 s-1 Usando a freqüência e o comprimento de onda da luz temos: λ= c/v = (3 x 108 m/s / 1.24 x 1015 s-1)(109 nm / 1m) = 242 nm Portanto a luz ultravioleta de comprimento de onda de 242nm tem energia por fóton suficiente para fotodissociar uma molécula de O2. Fotoionização – ocorre quando uma molécula absorve radiação e a energia absorvida provoca a perda de um elétron. O OZÔNIO NA PARTE SUPERIOR DA ATMOSFERA O(g) + O2(g) → O3*(g) +M(g) O3*(g) → O3(g) + M*(g) DIMINUIÇÃO DA CAMADA DE OZÔNIO 1970 – Paul Crutzen •óxidos de nitrogênio naturais destruíam cataliticamente o ozônio; 1974 – F. Sherwood Rowland e Mario Molina •identificaram que o cloro dos clorofluorcarbonos (CFCs) podem diminuir a camada de ozônio; CLOROFLUORCARBONOS (CFCs) C F2 Cl2 (g) + hv → C F2 Cl (g) + Cl (g) Cl (g) + O3 (g) → Cl O (g) + O2 (g) Cl O (g) + hv → Cl (g) + O (g) Cl 2 O3 (g) → 3 O2 (g) HIDROFLUORCARBONETOS •tem como característica o uso do hidrogênio no lugar do cloro; •alto custo para mudança dos equipamentos; •menos eficiente em relação à refrigeração; A QUIMICA E A TROPOSFERA Compostos de enxofre e chuva ácida: •Origem; •Efeitos negativos; •Soluções; Ca C O3 (s) → Ca O (s) + C O2 (g) Ca O (s) + S O2 (g) → Ca S O3 (s) MONÓXIDO DE CARBONO •Origem; •Efeitos negativos; •Soluções; ÓXIDOS DE NITROGÊNIO E NÉVOA FOTOQUÍMICA •Origem; •Efeitos negativos; •Soluções; VAPOR DE ÁGUA, DIÓXIDO DE CARBONO E CLIMA •Efeito Estufa; •Manter temperatura durante a noite; •Metano como gás do efeito estufa. O OCEANO DO MUNDO •Água do mar; •Dessalinização; ÁGUA DOCE •Oxigênio dissolvido e qualidade da água; •Tratamento de fontes de água municipais; •Abrandamento da água; Química verde Objetivo – sociedade sustentável •Promove o desenvolvimento e a aplicação de produtos e processos químicos compatíveis com a saúde humana e que preservem o meio ambiente Alguns princípios que governam a química verde são: • É melhor evitar os rejeitos do que tratá-los ou limpa-los depois de criados • Ao sintetizar novas substancias geradas devem possuir pouca ou nenhuma toxicidade a saúde humana e ao meio ambiente • Os processos químicos devem ser desenvolvidos para ser tão eficientes em termos de energia quanto possível, evitando altas temperaturas e pressões • quando possível devemos usar catalisadores contendo substancias comuns e seguras • Quando for técnica e economicamente viável as matérias-primas usadas para os processos químicos devem ser provenientes de estoques com suprimentos renováveis • As substancias auxiliares, como solventes, devem ser eliminadas ou transformadas em inoculas quando possível. Referencias Bibliográficas: Química A ciência central 9 edição cap.19 pag. 651 http://www.ufpel.tche.br/iqg/wwverde/html/Qu%EDmica_Verde.htm Acesso em 14/10/2008 http://www.simae.com.br/esquema.jpg Acesso em 14/10/2008 http://ebsco.smartimagebase.com/imagescooked/27648W.jpg Acesso em 14/10/2008
Baixar