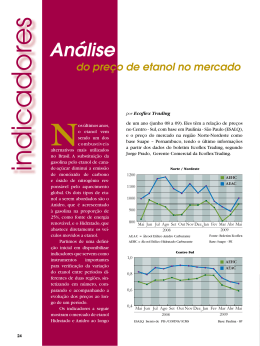
PROFA. JANA Repare no gráfico abaixo, tudo que foi escrito antes: Densidade ou massa específica. Densidade é uma propriedade física e expressa a quantidade de matéria existente em um certo volume. d = massa volume A densidade de líquidos e sólidos são geralmente dadas em 3 g/cm ou em g/mL, que se equivalem. Também pode ser dada em kg/L que se mantém o valor. A densidade do álcool é 0,8 3 g/cm ou 0,8 kg/L, tanto faz. Exemplos de algumas substâncias a 25ºC e 1 atm. O tetracloreto de carbono (CCl4) tem comportamento igual ao das outras substâncias, a temperatura aumenta e a densidade diminui. Mas repare que a densidade do CCl4 é maior que da água, em torno de 1,6 g/mL. Dos haletos, os monofluoretos e monocloretos são menos densos que a água, já os brometos e iodetos são mais densos. Os polihaletos, em geral são bastante densos. Em particular, o CH2I2 é o líquido mais denso (d = 3,32 g/mL) conhecido na química orgânica (ele é usado como líquido de contraste no estudo de minerais ao microscópio). 3 Material Nitrogênio Xenônio Acetona Álcool Água Alumínio Ferro Mercúrio Ouro Densidade em g/cm ou kg/L 0,00125 0,00580 0,8 0,8 1 2,7 7,8 13,6 19,3 Os gases possuem uma densidade muito pequena em g/mL, por isso, normalmente é apresentada em g/L. Nitrogênio Xenônio Densidade de uma mistura A densidade de uma substância composta ou de uma mistura, é a média ponderada das densidades dos componentes desta mistura, calculada a partir das proporcões (das concentrações), como por exemplo das porcentagens em massa de cada um dos componentes. Os fenômenos de interações entre os átomos, as moléculas e íons nas misturas, podem afetar estes cálculos, como por exemplo, o que acontece com a mistura de etanol e água (onde ocorre contração do volume). 1,25 g/L 5,80 g/L A densidade da água depende da temperatura (com qualquer outra substância) e consideramos ela como 1 g/mL, mas sabemos bem que esse valor não é atingindo nem na temperatura de 4ºC, seu maior valor. Exemplo: Considere que ar atmosférico seco tem 78% de N2, 21% de O2 e 1% de Ar. Qual a densidade do ar atmosférico? Temperatura (°C) Densidade (g/cm³) 100 0,9584 80 0,9718 60 0,9832 40 0,9922 30 0,9956 25 0,9970 22 0,9977 20 0,9982 Aparelhos que medem a densidade: 15 0,9991 10 0,9997 4 0,9999 0 0,9998 Picnômetro: é uma vidraria especial utilizada na picnometria, que possui baixo coeficiente de dilatação. A picnometria é uma técnica laboratorial utilizada para fazer a determinação da massa específica de líquidos. Também pode-se determinar a densidade de sólidos, devendo antes ser dissolvido. densidade do N2: 28 g./22,4 L = 1,25 g/L densidade do O2: 32 g./22,4 L = 1,42 g/L densidade do Ar: 40 g./22,4 L = 1,78 g/L densidade do ar: 1,25 x 78 + 1,42 x 21 + 1,78 x 1 = 1,29 g/L. 100 A diminuição da densidade da água de 4 a 0ºC e no estado sólido em relação ao estado líquido, dev-se as ligações de hidrogênio que se intensificam e ocupam um volume maior. Química Densímetro: é um aparato que tem por objetivo medir a massa específica de líquidos. O densímetro foi inventado por Hipátia, grande matemática e filósofa grega. 1 Densidade PROFA. JANA Uma das utilidades do densímetro é inferir propriedades dos líquidos através da inspeção de sua massa específica, principalmente quando os líquidos são misturas de substâncias. Nestes casos é possível inferir se a composição da mistura é a esperada ou não a partir do valor esperado para a massa específica da mistura. Picnômetro que durou meses na plataforma Deepwater Horizon, da British Petroleum, pode ter derramado 4,5 milhões de barris de petróleo no mar. Considerando que um barril corresponde a 159 litros e -1 que a densidade do petróleo é de 0,88 kg.L , qual é a quantidade de matéria (em mols) aproximada de carbono presentes no petróleo derramado? Assuma que a composição -1 do petróleo é de alcanos de fórmula geral CnH2n+2. (M (g.mol ): H = 1,008; C = 12,01) Assinale a alternativa correta. densímetro 10 a) 4,4 × 10 . 2 b) 4,5 × 10 . 23 c) 6,02 × 10 . 200 d) 1,0 × 10 . 6 e) 4,6 × 10 . 3. Misturam-se 100 g. e 200 g. respectivamente de dois líquidos 3 A e B, obtendo-se uma mistura homogênea, com 400 cm de volume total. Calcule a densidade da mistura. 3 a) 0,75 g/cm . 3 b) 1,75 g/cm . 3 c) 1,33 g/cm . 3 d) 0,50 g/cm . 3 e) 1,50 g/cm . Exercícios 1. Vendas fracas de diesel S50 preocupam ANP 4. . (Ita 2011) A 25°C, as massas específicas do etanol e da –3 –3 água, ambos puros, são 0,8 g cm e 1,0 g cm , respectivamente. Adicionando 72 g de água pura a 928 g de 3 etanol puro, obteve-se uma solução com 1208 cm de volume. Assinale a opção que expressa a concentração desta solução em graus Gay-Lussac (°GL). Às vésperas de completar o primeiro mês de obrigatoriedade de oferta do óleo diesel S50, com menor teor de enxofre em sua composição (no caso, 50 partes por milhão, em massa), a demanda, ainda tímida, pelo produto, principalmente entre veículos pesados, preocupa o setor. A medida faz parte do Programa de Controle da Poluição do Ar por Veículos Automotores (Proconve), criado em 2009. Entre as razões elencadas para a baixa procura pelo novo diesel, a mais citada é o prazo dado aos fabricantes de veículos pesados para entregar, até março, os veículos vendidos e faturados em 2011, cujos motores podem funcionar com qualquer dos três tipos de óleo diesel à disposição no país. Como o diesel S50 é o tipo mais caro ainda não consegue estimular a adesão dos consumidores, mesmo sendo menos poluente. Suponha que em um posto de combustíveis, o tanque de estocagem de óleo diesel S50 possua capacidade volumétrica 3 de 30 m a) 98 b) 96 c) 94 d) 93 e) 72 5. (Mack) Num recipiente calibrado contendo 485 mL de água (d 3 = 1g/cm ) colocou-se um objeto (feito de um único material) de massa igual a 117 g. Observou-se que o objeto imerge e que o nível da água no recipiente passa a ser de 500 mL. Com esses 3 dados e consultando a tabela abaixo (d em g/cm ), pode-se afirmar que o objeto pode ser feito de: Material Chumbo Ferro Osso Cortiça Pedra Densidade 11,3 7,8 2,0 0,3 5,0 e esteja cheio desse combustível, cuja densidade é 3 de 0,85 g cm . Sendo assim, é correto afirmar que a massa máxima de enxofre contida no combustível armazenado nesse tanque é de a) chumbo. b) osso. c) ferro. d) cortiça. e) pedra. a) 1275 g. b) 2550 g. c) 3825 g. d) 5100 g. e) 6375 g 6. Um carro possui um tanque de gasolina com capacidade de 40 L. Sabendo-se que com o tanque cheio o carro pesa 530 kg, qual será seu peso quando o tanque estiver vazio? ( Dado: densidade da gasolina = 0,8 g/mL) 2. . (Ufpr 2011) Este ano ocorreu um terrível acidente ambiental com o vazamento de petróleo no Golfo do México. O vazamento, Química 2 Densidade PROFA. JANA a) 32 b) 498 c) 562 d) 40 e) 490 7. (ENEM) Pelas normas vigentes, o litro de álcool hidratado que abastece os veículos deve ser constiuído de 96% de álcool puro de 4% de água (em volume). As densidades desse componentes são dadas na tabela I. No que se refere as densidades destes líquidos, é correto afirmar que: a) o líquido X é o mais denso dos 3. b) o líquido Y tem densidade intermediária entre X e Z. c) o líquido Z é o menos denso dos três. d) os líquidos X e Z tem a mesma densidade. e) os líquidos X e Y têm a mesma densidade. Um técnico de um órgão de defesa do consumidor inspecionou cinco postos suspeitos de vender álcool hidratado fora das normas. Colher uma amostra do produto em cada posto, mediu a densidade de cada uma, obtendo a tabela II. tabela I Substância Água Álcool tabela II Posto I II III IV V 10. Para o estudo de densidade de líquidos, um professor utilizou o seguinte experimento: introduziu uma bolinha de 3 densidade igual a 1 g/cm em quatro frascos. Estes frascos continham volumes iguais de líquidos diferentes. Densidade (g/L) 1000 800 Densidade do combustível (g/L) 822 820 815 808 805 O resultado observado foi o seguinte: A partir da posição da bolinha nos líquidos contidos nos quatro frascos, assinale a alternativa correta: A partir desses dados, o técnico pode concluir que estavam com o combustível adequado somente os postos: a) I e II. b) I e III. c) II e IV. d) III e V. e) IV e V. a) Os líquidos contidos nos frascos A e B apresentam 3 densidades menores que 1 g/cm . 3 b) O líquido contido no frasco D é mais denso que 1 g/cm . c) O líquido contido no frasco C é menos denso que o líquido contido no frasco D. d) Os líquidos contidos nos frascos A e B são menos densos que o líquido contido no frasco D. e) Os líquidos contidos nos frascos A e B são mais densos que o líquido contido no frasco D. 8. (Ufrgs) Em vazamentos ocorridos em refinarias de petróleo, que extravasam para rios, lagos e oceanos, verifica-se a utilização de barreiras de contenção para evitar a dispersão do óleo. Nesses casos, observa-se a formação de um sistema heterogêneo onde o petróleo fica na superfície desses recursos hídricos. Sobre o sistema acima descrito é correto afirmar que a água e o petróleo não se misturam porque 11. (Unifenas) Se em um copo contendo água for colocada uma bolinha de naftalina (naftaleno), observa-se que a mesma afunda. Acrescentando-se a esse sistema sal de frutas, a naftalina passa a boiar. Esse fenômeno se deve ao fato de que: a) se apresentam em estados físicos diferentes. b) apresentam densidade diferentes, e o petróleo fica na superfície devido a sua maior densidade. c) apresentam moléculas com polaridade diferentes, e o petróleo fica na superfície devido a sua menor densidade. d) a viscosidade da água é maior que a do petróleo. e) a elevada volatilidade do petróleo faz com que este fique na superfície. a) a naftalina torna-se menos densa, pois começa a se dissolver na água. b) há formação de gás carbônico, o qual interage com a naftalina, deixando-a menos densa. c) com a adição do sal de fruta, gera-se uma solução mais densa que a naftalina, fazendo com que esta boie. d) a naftalina tem uma grande facilidade para sofrer o processo de sublimação. e) forma-se uma mistura heterogênea instável que tende a se tornar homogênea com a expulsão da naftalina do meio, facilitando sua sublimação. 9. (Ufrgs) Um pequeno cubo de plástico (C), é colocado sucessivamente em três recipientes contendo líquidos X, y ou Z, diferentes entre si. Esse cubo fica em equilíbrio mecânico nas posições ilustradas nas figuras: Química 3 Densidade PROFA. JANA 15. O gráfico e a tabela, a seguir, contêm informações sobre a densidade, d, de alguns metais, a 20°C. No gráfico, estão indicadas relações entre massa e volume dos metais X, Y e Z. 12. Considere as seguintes propriedades de três substâncias líquidas: Densidade Solubilidade (g/mL a 20ºC) em H2O Hexano 0,659 insolúvel Tetracloreto de carbono 1,595 insolúvel Água 0,998 – Misturando-se volumes iguais de hexano, tetracloreto de carbono e água, será obtido um sistema Substância a) monofásico. b) bifásico, no qual a fase sobrenadante é o hexano. c) bifásico, no qual a fase sobrenadante é o tetracloreto de carbono. d) trifásico, no qual a fase intermediária é o tetracloreto de carbono. e) bifásico ou trifásico, dependendo da ordem de colocação das substâncias durante a preparação da mistura. 13. (UFV) Três tubos de ensaio contêm, separadamente, amostras de 4 mL dos líquidos clorofórmio, etanol e gasolina. A cada um destes tubos foi adicionado 1 mL de água. As densidades destes líquidos estão abaixo relacionadas A seqüência correta das amostras contidas nos tubos é, em presença da água: a) I- clorofórmio, II- etanol, III- gasolina. b) I- clorofórmio, II- gasolina, III- etanol. c) I- etanol, II- gasolina, III- clorofórmio. d) I- etanol, II- clorofórmio, III- gasolina. e) I- gasolina, II- etanol, III- clorofórmio. Considerando esse gráfico e essa tabela, é incorreto afirmar que: 3 a) a densidade de Y é, aproximadamente, 5 g/cm . b) a densidade de Y é cerca de duas vezes maior que a de X. c) o metal X é o magnésio. d) o metal X tem menor densidade que Z. e) os volumes ocupados por 10,0 g de Y e Z são diferentes. 14. Considere os elementos químicos e algumas de suas propriedades físicas: PF (ºC) PE (ºC) d (g/mL) Cobalto (Co) 1495 2900 8,9 Mercúrio (Hg) – 38 357 13,6 Xenônio (Xe) – 112 – 108 0,003 Pode-se dizer corretamente que: 16. (UFSC) Uma medalha, supostamente de ouro puro, foi testada pelo deslocamento do volume de água contido em uma 3 proveta (recipiente cilíndrico de vidro graduado em cm ). Para isso,a medalha, cujo peso era de 57,9 gramas, foi colocada 3 numa proveta de 50 cm que continha 3 25 cm de água e mediu-se o volume de água deslocado na proveta. Sabendo-se que a densidade do ouro puro é de 19,3 3 3 g/cm , qual será o volume final lido na proveta em cm se a medalha for de ouro puro? Assinale no cartão-resposta o resultado numérico encontrado. a) à temperatura ambiente, dois são líquidos. b) na temperatura de fusão de gelo, dois são gases. c) na temperatura de ebulição da água, dois são sólidos. d) volumes iguais dos três têm massas decrescentes na ordem Hg, Co, Xe. e) massas iguais dois três têm volumes decrescentes na ordem Hg, Co, Xe. Química 4 Densidade PROFA. JANA 50 mL foram colocados 25 mL de areia de praia lavada, decantada e seca. A massa da areia foi de 40,6 g. A areia foi então transferida para proveta contendo os 25 mL de água e o volume total foi de 39 mL. Com relação ao experimento descrito acima: o volume ocupado pelos grãos de areia (mL); o volume ocupado pelo ar entre os grãos na areia seca (mL); e a −1 densidade dos grãos de areia (g.mL ). 17. (Enem) A gasolina é vendida por litro, mas em sua utilização como combustível, a massa é o que importa. Um aumento da temperatura ambiente leva a um aumento no volume da gasolina. Para diminuir os efeitos práticos dessa variação, os tanques dos postos de gasolina são subterrâneos. Se os tanques não fossem subterrâneos: I. Você levaria vantagem ao abastecer o carro na hora mais quente do dia, pois estaria comprando mais massa por litro de combustível. II. Abastecendo com a temperatura mais baixa, você estaria comprando mais massa de combustível para cada litro. III. Se a gasolina fosse vendida por quilograma em vez de por litro, o problema comercial decorrente da dilatação da gasolina estaria resolvido. Dessas considerações, somente: a) I é correta. b) II é correta. c) III é correta. d) I e II são corretas. e) II e III são corretas. 20. (UFSC) As medalhas dos Jogos Olímpicos de Londres em 2012 possuem massas que variam entre 375 e 400 g, com 85 mm de diâmetro e 7,0 mm de espessura. As medalhas são moldadas com a seguinte composição: 18. (Fuvest) Água e etanol misturam-se completamente, em quaisquer proporções. Observa-se que o volume final da mistura é menor do que a soma dos volumes de etanol e de água empregados para prepará-la. O gráfico a seguir mostra como a densidade varia em função da porcentagem de etanol (em volume) empregado para preparar a mistura (densidades medidas a 20 ºC). “Medalha de ouro”: 92,5% (em massa) de prata e 1,34% (em massa) de ouro. O restante é cobre. Medalha de prata: 92,5% (em massa) de prata e o restante de cobre. Medalha de bronze: 97,0% (em massa) de cobre, 2,5% (em massa) de zinco e 0,50% (em massa) de estanho. Com base no texto apresentado, é CORRETO afirmar que: 01. considerando que a medalha seja um cilindro regular, a densidade de uma medalha de 375 g é de aproximadamente 9,4 3 g/cm . 02. uma “medalha de ouro” de 400 g possui 24,6 g de cobre 04.o número de mol de átomos de ouro presente em uma “medalha de ouro” é maior que o número de mol de átomos de zinco presente em uma medalha de bronze de mesma massa. 08.uma medalha de bronze de 400 g possui 0,017 mol de átomos de estanho. 16. a medalha de bronze é formada apenas por metais de transição. 32. os átomos constituintes da medalha de prata unem-se por meio de ligações metálicas, ao passo que os átomos constituintes da medalha de bronze unem-se por meio de ligações metálicas e de ligações iônicas Gabarito: 1.a 2.a 3.a 4.b 5.c 6.b 7.e 8.c 9.a 10.e 11.c 12.e 13.c 14.d 15.c 16.28 17.e 18.e 19. 28 20.11 Se 50 mL de etanol forem misturados a 50 mL de água, a 20 oC, o volume da mistura resultante, a essa mesma temperatura, será de, aproximadamente, a) 76 mL b) 79 mL c) 86 mL d) 89 mL e) 96 mL 19. (UFSC) Considere o seguinte experimento: em uma proveta de 50 mL foram colocados 25 mL de água. Em outra proveta de Química 5 Densidade PROFA. JANA Compare as unidades de medida para comprimento, área e volume. Começamos pelas unidades de comprimento: Unidades de medidas Para calcular a densidade existem alguns pré-requisitos básicos, como o domínio das unidades de massa e volume. Vamos para algumas unidades e prefixos básicos: Múltiplo Nome Massa é a quantidade de matéria dos corpos. Unidades, múltiplos e submúltiplos Múltiplo Nome 0 10 1 10 grama Símb. Múltiplo Nome g –1 decagrama dag 10 hectograma hg 10 quilograma kg 10 megagrama Mg 10 gigagrama Gg 10 12 teragrama Tg 10 15 petagrama Pg 10 2 10 3 10 6 10 9 10 10 10 18 10 exagrama Eg –2 –3 –6 –9 dg centigrama cg miligrama mg micrograma µg nanograma ng picograma –15 femtograma fg –18 attograma –21 zeptograma zg –24 yoctograma yg 10 zettagrama Zg 10 24 yottagrama Yg 10 10 decigrama –12 21 10 Símb. pg Símb. 10 0 metro 10 1 decâmetro dam 10 2 10 3 10 6 10 9 10 12 10 15 10 18 10 21 10 24 –1 decímetro –2 centímetro cm –3 milímetro –6 micrômetro µm –9 nanômetro nm –12 picômetro –15 femtômetro fm –18 atômetro –21 zeptômetro zm –24 10 ioctômetro ym Em cm 100 cm 2 2 100 cm 2 3 100 cm Em mm 1000 mm 2 2 1000 mm 3 3 1000 mm 10 10 quilômetro km 10 megâmetro Mm terâmetro petâmetro exâmetro zetâmetro iotâmetro Símb. m hectômetro hm gigâmetro Múltiplo Nome 10 Gm 10 Tm 10 Pm 10 Em 10 Zm 10 Ym dm mm pm am Comparando com área e volume: ag 1m 2 1m 3 1m OBSERVAÇÕES LINGUÍSTICAS: 1. As grafias quilo, kilo e kilograma são comuns, mas somente quilograma é a correta, incorporada aos dicionários. 2. O quilograma é informalmente abreviado por quilo, mas uma ordem de grandeza não deveria ter plural por ela não ser uma unidade de medida propriamente dita. 3. Outro erro muito comum é abreviar quilograma com a primeira letra maiúscula, resultando em Kg, símbolo que no SI representa kelvin-grama. O símbolo de quilograma é kg, com a primeira letra minúscula. Em dm 10 dm 2 2 10 dm 3 3 10 dm Vejamos agora a comparação com litros. 1 L = 1000 mL 3 Importante: 1 L = 1 dm . (Lê-se: Um litro é igual a um decímetro cubico) 3 3 e como 1 dm = 1000 cm . 3 logo: 1 mL = 1 cm . (Lê-se: Um mililitro é igual a um centímetro cubico) 3 3 3 E também: 1 m = 10 dm , 3 logo: 1 m = 1000 L. (Lê-se: Um metro cúbico é igual a mil litros) Exemplos legais: Existem massas muito pequenas, como a de átomos e moléculas. −24 A massa de um átomo de hidrogênio é 1,67.10 g. ou 1,67 yg. −23 A massa de uma molécula de água é 3.10 g. ou 0,03 zg. Mas existem também massas muitos grandes, como dos satélites naturais, planetas e estrelas: 22 A massa da Lua é de 7,35.10 kg. ou ou 73,5 Zg. 24 3 A massa do planeta Terra é de 6.10 kg. ou 6.10 Yg. 30 A massa do Sol é de 2.10 kg. ou 2 000 000 Yg. Volume é a extensão do espaço ocupado por um corpo. Química 6 Densidade
Baixar