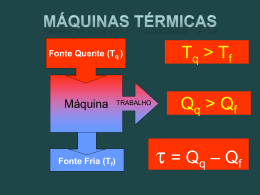
1 Entropia e a Segunda Lei da Termodinâmica Introdução Muitos processos termodinâmicos ocorrem naturalmente em um dado sentido, mas não ocorrem em sentido oposto. Por exemplo, o calor sempre flui de um corpo quente para um corpo frio, nunca em sentido contrário. O fluxo de calor de um corpo frio para um corpo quente não viola a primeira lei da termodinâmica, a energia seria conservada. Porém, isso não ocorre na natureza. Por que não? É fácil converter completamente a energia mecânica em calor; isto ocorre sempre que usamos o freio para parar um carro. Indo no sentido inverso, existem muitos dispositivos que convertem parcialmente o calor em energia mecânica (por exemplo, o motor de um automóvel). Porém, nunca nenhum inventor conseguiu construir uma máquina capaz de converter completamente uma quantidade de calor em energia mecânica. Por que não? A resposta para estas duas perguntas diz respeito aos sentidos dos processos termodinâmicos é dada pela segunda lei da termodinâmica. Esta Lei determina limites fundamentais para o rendimento de uma máquina ou de uma usina elétrica. Ela também estipula limites para a energia mínima que deve ser fornecida a um refrigerador. Logo, a segunda lei da termodinâmica é diretamente relevante para muitos problemas práticos importantes. Podemos também enunciar a segunda lei em termos do conceito de entropia, uma grandeza que mede o grau de desordem de um sistema. A idéia de entropia ajuda a entender por que a tinta que se mistura com água não pode jamais ser separada espontaneamente e qual á a razão pela qual uma grande quantidade de processos aparentemente possíveis nunca ocorre na natureza. Processos Reversíveis e Irreversíveis Os processos termodinâmicos que ocorrem na natureza são todos processos irreversíveis. Estes processos são aqueles que ocorrem em um determinado sentido porém não ocorrem no sentido contrário. Um processo reversível é aquele cujo sentido pode ser invertido por mudanças infinitesimais nas condições do processo. Um processo reversível é também processo de equilíbrio. Consideremos um sistema em equilíbrio, e apenas nessas circunstâncias podemos caracterizar um estado termodinâmico e, nesse estado podemos atribuir valores para as funções termodinâmicas de estado tais como temperatura, pressão, energia interna, etc. Quando um sistema sofre variações através de absorção de calor ou trabalho, ele sai momentaneamente do estado de equilíbrio, e depois de um certo tempo de relaxação encontra outro estado de equilíbrio. Quando a variação sofrida pelo sistema for infinitesimal, as suas funções termodinâmicas também sofrerão variações infinitesimais. E podemos caracterizar os novos valores das funções termodinâmicas para essa nova situação de equilíbrio. Essas transformações infinitesimais são chamadas às vezes de transformações quasi-estáticas. Quando submetemos um sistema a várias transformações quasiestáticas, podemos definir uma seqüência de valores para suas funções de estado, que irão caracterizar cada uma das pequenas transformações. Podemos desse modo executar a mudança de um sistema físico entre dois estados termodinâmicos afastados, utilizando uma seqüência de pequenas transformações quasi-estáticas. 2 Um exemplo dessa situação seria considerar um gás em equilíbrio, contido em um êmbolo, que está mantido nessa posição por uma certa quantidade de pequenos pesos. À medida que retiramos um pequeno peso, a pressão exercida no êmbolo diminui infinitesimalmente, fazendo com que o gás encontre outra situação de equilíbrio, infinitesimalmente próxima da situação de equilíbrio anterior. Quando terminarmos de retirar os pesos, o gás encontra-se em um estado termodinâmico final distante do estado termodinâmico inicial. E o gás alcançou o estado final seguindo um percurso de estados intermediário que foram sendo conhecidos enquanto ele sofria as transformações infinitesimais. Se quisermos fazer o gás retornar ao estado inicial pelo mesmo percurso, será necessário apenas ir recolocando paulatinamente os pesos em sues lugares originais, e o sistema voltará usando os mesmos estados do percurso de ida. Fig.1 Consideremos o mesmo sistema anterior, no mesmo estado inicial. A única diferença da configuração seria que os pequenos pesos foram substituídos por um único peso de mesma massa. Quando esse peso é retirado, o sistema sofre uma mudança brusca até atingir o equilíbrio. Durante esse processo, para as funções termodinâmicas de estado tais como temperatura, pressão, energia interna; ficam indefinidas, pois são caracterizadas apenas em situações de equilíbrio. Como não estamos limitando as possibilidades de interação entre o gás e o ambiente, as quantidades de calor e trabalho envolvidas no percurso de volta podem ser diferentes das quantidades do percurso da vinda. No percurso inicial, quando retiramos o peso, o gás enfrentou um processo de forte desequilíbrio no qual não é possível definir as funções termodinâmicas. Essa é a essência de um processo irreversível: a impossibilidade de definir os estados intermediários de uma transformação termodinâmica. Como não podemos conhecer o percurso utilizado, não podemos reverter o processo pelo mesmo caminho. Fig.2 Definição de Variação de Entropia A variação de entropia ∆S que ocorre quando um sistema fechado muda de um estado inicial bem definido para outro, igualmente bem definido, através de um processo que pode ser descrito como reversível, é definida por f ∆S = ∫ i dQ T onde T é a temperatura absoluta. A entropia depende somente do estado do sistema e a variação de entropia entre um dado estado final e um dado estado inicial é sempre a mesma para qualquer processo que faça o sistema sair do estado inicial e chegar ao estado final. O enunciado da segunda lei da termodinâmica usando o conceito de entropia S é: a entropia de um sistema isolado pode crescer, mas nunca pode diminuir. Quando um sistema interage com suas vizinhanças, a variação total de entropia do sistema e do ambiente nunca pode diminuir. Quando a interação envolve apenas processos reversíveis, a entropia total é constante e ∆S = 0; quando existe um processo irreversível, a variação total da entropia aumenta e ∆S > 0. Segunda Lei da Termodinâmica – Em qualquer processo termodinâmico que vai de um estado de o sinal > para processos irreversíveis. equilíbrio para outro, a entropia do conjunto sistema ∆S ≥ 0 + ambiente aumenta ou permanece o sinal = para processos reversíveis. constante Portanto, Máquinas Térmicas Máquina térmica ou motor é um dispositivo que extrai energia do ambiente, na forma de calor, e realiza trabalho útil. No interior de toda máquina térmica está uma substância de trabalho, que sofre as transformações termodinâmicas que possibilitam as mudanças de forma da energia. Para que uma máquina funcione de maneira permanente é necessário que ela opere em ciclos, ou seja: a substância de trabalho passa por diversas transformações termodinâmicas até retornar ao estado inicial, completando um ciclo. De modo geral as máquinas térmicas operam em ciclo entre duas fontes térmicas com temperaturas diferentes. Uma máquina térmica retira calor da fonte quente e rejeita parte desse calor para uma fonte fria e transforma essa diferença de energia em trabalho mecânico. Uma máquina de Carnot Em um ciclo de uma máquina de Carnot a substância de trabalho passa por quatro processos diferentes, onde dois processos são isotérmicos (ab e cd) e os outros dois processos são adiabáticos (bc e da). Fig.3 – Ciclo de Carnot O sistema absorve uma quantidade de calor Q2 isotermicamente a uma temperatura T2 quando vai do estado a para o estado b . E de maneira equivalente, o sistema rejeita uma quantidade de calor Q1 isotermicamente a uma temperatura T1 quando vai do estado c para o estado d . As transformações entre os estados b e c , bem como entre os estados d e a acontecem adiabaticamente, ou seja, sem que ocorra troca de calor com o ambiente. Fig.4 3 4 O ciclo de Carnot mostrado em um gráfico temperatura-entropia. A entropia varia durante os processos ab e cd, mas não variam durante os processos bc e da. O gráfico terá sempre uma forma retangular independente da substância de trabalho. Rendimento de uma Máquina de Carnot Fig.5 O propósito de uma máquina é transformar o calor Q2 retirado do reservatório quente no máximo de trabalho. Este resultado é medido em termos da chamada eficiência ou rendimento térmico ε, definida por ε= W energia obtida (trabalho efetivo) = energia fornecida (calor absorvido) Q2 Aplicando a primeira Lei da Termodinâmica: Da primeria lei, dEint = dQ + dW para um ciclo ⇒ dEint = 0 W = Q2 − Q1 , portanto ε = N trabalho resultante Calor resultante Do diagrama T-S, temos ∆S 2 = −∆S1 ⇒ Q2 T2 = Q2 − Q1 Q2 Q1 T1 ⇒ ⇒ ε = 1− Q1 Q2 Q1 T1 = Q2 T2 Logo, o rendimento de uma máquina de Carnot é dada por: ε = 1 − T1 < 100% pois T1 < T2 T2 Entropia e Rendimento de Máquinas Máquina térmica ou motor é um dispositivo que extrai energia do ambiente, na forma de calor, e realiza trabalho útil. No interior de toda máquina térmica está uma substância de trabalho, que sofre as transformações termodinâmicas que possibilitam as mudanças de forma de energia. Para que uma máquina funcione de maneira permanente é necessário que ela opere em ciclos, ou seja: a substância de trabalho passa por diversas transformações termodinâmicas até retornar ao estado inicial, completando um ciclo. De modo geral as máquinas térmicas operam em ciclo entre duas fontes térmicas com temperaturas diferentes. Uma máquina térmica retira calor da fonte quente e rejeita parte desse calor para uma fonte fria e transforma essa diferença de energia em trabalho mecânico. A Busca da Máquina “Perfeita” Segunda Lei da Termodinâmica - Primeira Forma: Não é possível, com nenhuma série de processos, retira-se calor de uma fonte térmica e transformá-lo completamente em trabalho. Não existem máquinas perfeitas. Fig.6 5 Máquina de Stirling (1816) A figura ao lado mostra um diagrama p-V para um idealizado motor Stirling que utiliza um gás ideal. O trabalho resultante feito pelo sistema durante o ciclo é representado pela região sombreada. Q2 representa o calor adicionado ao sistema durante a expansão isotérmica ab. Q1 representa o calor perdido pelo sistema durante a contração isotérmica cd. (Durante o processo a volume constante bc, energia térmica é armazenada em uma parte do motor, em geral uma rede metálica. A mesma quantidade de energia é retirada da rede durante o processo a volume constante da. O motor percorre o ciclo no sentido horário. O rendimento da máquina de Stirling é menor que o da máquina de Carnot. Fig.7 Entropia e Desempenho de Refrigeradores Refrigerador é um dispositivo cuja função é transferir calor de um reservatório térmico em uma temperatura mais baixa para um outro reservatório térmico em uma temperatura mais alta. Em um processo natural o calor se transfere de um reservatório com temperatura mais alta para outro com uma temperatura mais baixa. Para conseguir realizar uma transferência de calor num sentido contrário ao sentido natural, o refrigerador necessita executar trabalho na substância de trabalho. A região onde são armazenados os alimentos no interior de uma geladeira doméstica é o reservatório frio, e o reservatório quente é o ambiente que rodeia a geladeira. Para um ar-condicionado o reservatório frio é o interior do aposento onde ele está instalado, e o reservatório quente é o ambiente externo a esse aposento. De maneira semelhante a uma máquina térmica ideal, em um refrigerador ideal todos os processos são reversíveis. Em um refrigerador de Carnot temos um ciclo passando pelos mesmos estados de uma máquina de Carnot, mas com uma seqüência de transformações em um sentido contrário, como mostra a figura ao lado. Fig.8 O equivalente à eficiência de uma máquina térmica é definido como coeficiente de desempenho de um Refrigerador K. K= Q1 Q1 = W Q2 − Q1 Para um refrigerador de Carnot temos que: K= T1 T2 − T1 Fig.9 6 Segunda Lei da Termodinâmica -Segunda Forma: Não é possível um processo cujo único resultado seja a transferência de calor de um reservatório a uma temperatura para outro reservatório a uma temperatura mais baixa. Não existem refrigeradores perfeitas. As Eficiências de Máquinas Reais Teorema: Nenhuma máquina real, operando entre duas temperatura, pode ter uma eficiência maior do que uma Máquina de Carnot operando entre as mesmas duas temperaturas. Para demonstrar o teorema, suponha que um inventor de fundo de quintal alegue que construiu uma Máquina X, cuja eficiência εX > εC (onde εC a eficiência da máquina de Carnot) Vamos acoplar a máquina X à máquina de Carnot operando no sentido inverso, como um refrigerador ( figura ao lado). Ajustando o refrigerador de Carnot de tal maneira que o trabalho que necessita por ciclo é justamente o fornecido pela máquina X. Se εX > εC é verdadeiro, então (∗) W W > Q2′ Q2 ⇒ Q2 > Q2′ Fig. 10 Como o trabalho realizado pela máquina X é igual ao executado sobre o refrigerador de Carnot, temos Q2 − Q1 = Q2′ − Q1′ ⇒ Q2 − Q2′ = Q1 − Q1′ = Q com Q > 0 A comparação da equação (*) com a figura 10 mostra que o efeito resultante da máquina X e do refrigerador de Carnot, trabalhando em conjunto, é o de transferir energia térmica Q do reservatório de baixa temperatura para o reservatório de alta temperatura sem necessidade de trabalho. Assim, o conjunto age como refrigerador perfeito, violando a segunda Lei da Termodinâmica. A primeira lei da termodinâmica incorpora ao princípio geral da conservação da energia o reconhecimento de que calor é uma forma de energia. Qualquer processo cuja energia total seja conservada é compatível com a primeira lei da termodinâmica. No entanto, existem processos que só acontecem em um sentido, são os processos irreversíveis. A segunda lei da termodinâmica dá consta desta questão, assim como das possíveis maneiras de transformar calor em trabalho. 7 Outras formas de enunciar a 2a da Termodinâmica: I) Entropia é uma variável de estado cuja variação dS é dada pelo calor dQ (transferido reversivelmente) dividido pela temperatura T à qual o calor é transferido. dQ dQ ⇒ ∆S = S f − S i = ∫ T T ∆S = 0 (para qualquer processo ciclico) dS = Entropia e a segunda Lei da Termodinâmica ∆S universo = ∆Ssistema + ∆Sambiente “Para qualquer processo, a entropia do universo ou aumenta (se o processo é irreversível) ou permanece a mesma (se o processo é reversível ” ∆S universo ≥ 0 II) Postulado: Existe uma função (chamada de ENTROPIA) das parâmetros extensivos de qualquer sistema composto, definida para todos os estados de equilíbrio com a seguinte propriedade. “Os valores assumidos pelos parâmetros extensivos na ausência de um vínculo interno são aqueles que maximizam a entropia sobre a variedade de estados de equilíbrio possíveis. Observações: 1) A entropia só e definida para estados de equilíbrio; 2) Estado de equilíbrio: 2) Parâmetros intensivos: são aqueles independentes do número de partículas no sistema 3) Parâmetros extensivos: São linearmente proporcional ao número de partículas no sistema. Uma Abordagem Estatística da Entropia 8 Uma amostra de um gás comum contém um número muito grande de átomos ou moléculas. Para termos uma idéia da ordem de grandeza de quão grande é esse número basta lembrarmos que em um mol de hidrogênio (2 gramas) existem 1023 moléculas (número de Avogadro). Para lidar com grande quantidade de moléculas vamos introduzir conceitos de probabilidade e estatística, e para tal vamos analisar um gás composto por pouquíssimas partículas. Consideremos um gás com apenas duas moléculas idênticas, que ocupam um recipiente dividido em duas partes; à parte da esquerda e a parte da direita. Quais as possíveis configurações que esse gás pode apresentar? A A - As duas moléculas ocupam o lado esquerdo do recipiente. B B - Uma molécula ocupa o lado esquerdo do recipiente enquanto a outra molécula ocupa o lado direito. C C - As posições são invertidas, D D - As duas moléculas ocupam o lado direito do recipiente. Mas afinal, esse gás de duas moléculas se apresentará em qual configuração? Essa situação se apresenta de uma forma nova, pois o gás pode se apresentar em qualquer uma das configurações. A pergunta deve ser feita de uma maneira diferente: qual a probabilidade do gás se apresentar em cada uma das configurações? Para responde a essa pergunta vamos construir uma tabela: Temos dois estados equivalentes, e são aqueles associados com as configurações B e C. O total de estados acessíveis para as duas moléculas, nestas circunstâncias, é 2N = 22 = 4 . Considerando que cada uma das configurações são igualmente prováveis, a probabilidade de encontrar o sistema em cada uma delas é 1/4 . Como temos duas configurações equivalentes (B e C), a probabilidade de encontrar sistema em uma delas é 2.(1/4) = 1/2 . As duas configurações são equivalentes (B e C) por que são indistinguíveis, não se pode distinguir em qual das configurações o sistema está. 9 Para tentar entender o comportamento de um gás real, devemos analisar um gás com um número cada vez maior de moléculas. Nesse sentido, vamos refazer os cálculos anteriores considerando dessa vez um gás com 4 moléculas. Na tabela ao lado, usamos a notação N N! w= = n n !( N − n)! número de microestados É possível generalizar os resultados obtidos para a situação onde o sistema é composto por um número N de moléculas. As probabilidades calculadas para cada uma das situações têm a forma: N 1 P (nE , nD ) = N nE 2 Como mostra a figura abaixo na medida que aumenta o número N de moléculas do gás o máximo em torno de nE = nD vai se tornando cada vez mais agudo. Podemos entender que quando N for pequeno, não são muito diferentes as probabilidades do sistema ocupar um de seus estados acessíveis. No entanto, quando N assume valores apreciáveis, existe uma grande quantidade de estados equivalentes em torno de nE = nD e desse modo existe uma grande probabilidade do sistema ocupar um estado onde nE = nD onde o número de moléculas na parte esquerda do recipiente é igual ao número de moléculas na parte direita do recipiente. O Físico austríaco Ludwig Boltzmann deduziu uma relação entre a entropia S de um sistema e a multiplicidade (número de micro-estados) w , e essa relação tem a forma: S = k B ln w na qual kB = 1,38 ×10-23J/K é a constante de Boltzmann.
Baixar