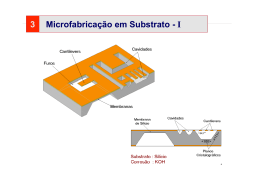
Corrosão Anisotrópica de Silício em Soluções Alcalinas Fundamentos e Aplicações Cyro Ketzer Saul Departamento de Física Centro Politécnico Universidade Federal do Paraná Jardim das Américas, 81531-990, Curitiba, PR CP 19044 Fone: (041) 3361-3404 / 3361-3003 (lab) Fax : (041) 3361-3418 e-Mail: [email protected] Referencia Bibliográfica: Cyro Ketzer Saul "Corrosão Anisotrópica de Silício em Soluções Alcalinas: Fundamentos e Aplicações" Sensores y Microsistemenas - Vol I - Tecnologias de Fabricacion CYTED - Subprograma IX – Microelectronica Red IX.I - Tecnologias para el Desarrollo de Sensores y Microsistemas pag.: 45-76 Fev 2004 Ed. Liliana B. Fraigi - Coordinador Internacional - Red IX Teseo Buenos Aires - Argentina 1 Introdução ................................................................................................... 3 O Silício........................................................................................................ 3 Propriedades do Silício ............................................................................................4 Estrutura Cristalina.................................................................................................5 Orientação Cristalina das Lâminas........................................................................8 Corrosão Anisotrópica de Silício............................................................... 9 Hidrazina...................................................................................................................9 EDP ............................................................................................................................9 TMAH......................................................................................................................10 Soluções de Hidróxidos Alcalinos .........................................................................10 Solução de KOH .....................................................................................................11 A Reação................................................................................................................................11 Anisotropia ............................................................................................................................12 Parâmetros de Corrosão.........................................................................................................13 Processo empregando KOH ..................................................................................18 Projeto de Máscaras para KOH .............................................................................................18 Alinhamento ..........................................................................................................................19 Controle da profundidade da corrosão...................................................................................20 Etapas do processo empregando corrosão com KOH ...........................................................22 Equipamento...........................................................................................................23 Banho Térmico ......................................................................................................................23 Recipiente da Solução ...........................................................................................................23 Controle da Temperatura .......................................................................................................24 Agitação da Solução ..............................................................................................................24 Exemplos de estruturas............................................................................ 26 Canais ......................................................................................................................26 Membranas .............................................................................................................27 Cantilevers ..............................................................................................................28 Conclusões ................................................................................................. 29 Referências Bibliográficas ....................................................................... 29 Apêndice A – Processo de Limpeza de Lâminas ................................... 30 Limpeza Preliminar ...............................................................................................30 Remoção de contaminantes orgânicos residuais e certos metais (SC-1)...........30 Remoção do filme de óxido formado ....................................................................31 Remoção dos contaminantes atômicos e iônicos (SC-2) .....................................31 Secagem das lâminas de Si. ...................................................................................31 2 Introdução A microfabricação em silício é uma das áreas que apresentou maior crescimento nas últimas décadas do século XX. Esta técnica conhecida internacionalmente pela sigla MEMS (MicroElectroMechanical Systems) é referida por alguns autores como o próximo passo lógico na revolução do silício [1][2]. Este crescimento é impulsionado pela necessidade de miniaturização de dispositivos sensores e atuadores cada vez mais requisitados nas áreas de monitoração ambiental, automobilística, biotecnologia, aeroespacial e industrial. Tendo nascido dentro da indústria microeletrônica, a adoção de métodos e processos de fabricação foi natural. Entretanto alguns processos novos foram desenvolvidos tendo em vista as necessidades específicas desta tecnologia emergente, principalmente no que se refere à definição tridimensional dos dispositivos. Considerando suas características, os processos de definição tridimensional em silício podem ser inicialmente divididos em duas categorias: os processos a seco onde a formação das espécies reativas ocorre dentro de um plasma de baixa temperatura; e os processos úmidos, onde as espécies reativas estão dissolvidas em uma solução. Em ambas as categorias o processo pode ser isotrópico, isto é, não possuí direções preferenciais de ataque, ou anisotrópico, onde o ataque depende de fatores estruturais da amostra ou de características específicas do processo. No caso do silício os processos de corrosão úmida anisotrópica apresentam uma forte dependência da orientação cristalina das faces da amostra expostas à solução. Baseado na existência de anisotropia dependente de orientação cristalina é possível fabricar estruturas tridimensionais como membranas, cantileveres, canais, pontes e cavidades com controle excelente e qualidade superficial que pode chegar à níveis atômicos. A utilização destas estruturas sozinhas ou combinadas possibilita a fabricação de uma inúmera variedade de dispositivos sensores, atuadores, microfluídicos, etc. Neste trabalho será efetuada uma abordagem dos processos de corrosão úmida de silício em soluções alcalinas com um enfoque particular no processo empregando soluções aquosas de hidróxido de potássio em função de suas vantagens em termos de custo e baixa periculosidade. O Silício O silício por se tratar do segundo elemento mais abundante, correspondendo a 25,7% do peso da crosta terrestre, sempre foi empregado pela humanidade em seu processo evolutivo. Seu emprego remonta os primórdios da civilização onde lascas de silex (óxido de silício em forma vitrificada) eram empregadas na confecção de armas e ferramentas cortantes. Em 1811 Joseph Louis Gay-Lussac e Louis Jacques Thénard conseguiram obter silício a partir de SiF4 na presença de potássio aquecido. O SiF4 foi obtido previamente dissolvendo sílica em ácido fluorídrico. Entretanto o crédito da descoberta foi dado à Jons Jacob Berzélius em 1824 por ter obtido o silício com maior pureza. Posteriormente, em 1854, Etienne Henri Sainte-Claire Deville obteve silício na forma cristalina por meio da eletrólise de cloreto de sódio alumínio com aproximadamente 10% de silício. No início do século XX o estudo da interação entre sílica e carbono possibilitou o desenvolvimento do principal processo de obtenção de silício puro empregado até os dias de hoje. O processo atual consiste em reagir quartzito (areia) com carbono, na forma de carvão, em um forno de arco à 2000oC, conforme a reação SiO2 + 2C → Si + 2CO . O material obtido desta forma é 98% puro, conhecido como silício de grau metalúrgico. Como a pureza exigida nas aplicações eletrônicas é muito elevada, (melhor que 1 parte em 108) o silício é moído e reagido com ácido clorídrico gasoso formando tricloro-silano, conforme a reação 3 Si + 3HCl( g ) → SiHCl3 + H 2 , o qual é um líquido com alta pressão de vapor que ferve à 32oC. Assim como o silício, a grande maioria das impurezas existentes inicialmente também reage formando compostos clorados altamente estáveis e com pontos de ebulição distintos do tricloro-silano. Desta forma, é possível separar o composto de interesse com extrema pureza mediante destilação fracionada. Em uma reação posterior, o tricloro-silano puro é reagido com hidrogênio em elevada temperatura, formando o silício de grau eletrônico, conforme a reação SiHCl3 + H 2( g ) → 2Si + 3HCl . Ainda que extremamente puro, o silício obtido está policristalino, o que não é apropriado para fabricação de dispositivos, e portanto, é necessário “crescer” um cristal monocristalino a partir do pó policristalino. Este processo de crescimento de cristal é conhecido como processo Czochalski (CZ) e envolve o derretimento do silício policristalino em um forno apropriado em ambiente inerte. A inserção de uma “semente” cristalina com a orientação desejada na superfície do silício derretido provoca a agregação lenta de material cristalinamente orientado de acordo com mesma. A rotação lenta associada à extração da semente provoca o surgimento de uma barra monocristalina de diâmetro controlado, conforme mostra a figura 1. Um segundo processo para obtenção de silício monocristalino, conhecido como processo de “Float Zone” (FZ), também está disponível. Neste processo, uma barra de silício policristalino é passada lentamente por uma bobina de indução alimentada com radio freqüência (RF) de elevada potência em uma atmosfera inerte ou de elemento dopante. Neste caso, a semente é inserida no início da barra a fim de determinar a orientação desejada do monocristal a ser obtido. Figura 1 - Barra de silício monocristalino. Nas aplicações do silício na indústria de microeletrônica e de sensores as barras de silício são cortadas formando as lâminas que posteriormente passam por processos de polimento mecânico e químico de acordo com as especificações do mercado. Com a evolução da qualidade dos processos e a necessidade de aumentar a produtividade das fabricas de componentes, as laminas fabricadas atualmente chegam à 300 mm de diâmetro. Propriedades do Silício Nos primórdios da indústria eletrônica as propriedades do silício que mais interessavam eras suas propriedades elétricas. O estudo destas propriedades à exaustão tornou possível à uma pessoa comum a compra de um computador pessoal com capacidade de processamento de alguns MFLOPS (milhões de operações de ponto flutuante por segundo). Até a década de 70 a posse de um computador pessoal era inimaginável para as pessoas comuns, e os MFLOPS eram o sonho e a meta dos cientistas que dependiam de poder computacional para seus estudos. Por outro lado, 4 as propriedades mecânicas do silício foram deixadas de lado até aproximadamente a década de oitenta com o início dos estudos de estruturas eletromecânicas [3]. Considerando a importância do silício como matéria prima no desenvolvimento de diversos tipos de dispositivos, a tabela I a seguir apresenta os valores das principais propriedades do silício [4]. Tabela I - Principais propriedades do silício. Propriedade Permissividade elétrica Permissividade elétrica relativa Largura da banda proibida Mobilidade n Mobilidade p Campo elétrico para ruptura Função trabalho Concentração de portadores Densidade de estados efetiva na banda de condução Densidade de estados efetiva na banda de valência Massa efetiva (elétrons) Massa efetiva (lacunas) Resitividade Comprimento de Debye Peso atômico Isótopos Número atômico Raio atômico Raio iônico Densidade Densidade atômica Densidade de átomos superficiais Número de átomos por célula unitária Estrutura cristalina Constante da rede cristalina Comprimento da ligação Propriedades Térmicas Condutividade térmica Calor específico Capacidade térmica molar Difusividade térmica Ponto de fusão Ponto de ebulição Temperatura crítica Pressão de vapor Coeficiente de expansão térmica linear Módulo de Young (E) Razão de Poisson Módulo de Cisalhamento Propriedades Elétricas Valor 1,04 x 10-10 F/m 11,75 1,124 eV (1,170 à 0K) 1350 V/s 480 V/s 3 x 107 V/m 4,15 eV 1,45 x 1010 /cm3 3,22 x 1019 / cm3 1,83 x 1019 / cm3 0,26 me 0,38 me 2,3 x 105 Ω.cm 24 µm Propriedades Químicas 28.0855 g 28 – 92,23% 29 - 4,67% 30 - 3,10% 14 177 pm 40 pm 2,33 g/cm3 4,995 x 1022 /cm3 (100) 6,78 x 1014 /cm2 (110) 9,59 x 1014 /cm2 (111) 7,83 x 1014 /cm2 8 diamante 5,431 Å 2,36 Å 1,412 W/cm.K 0,70 J/g.K 20,00 J/mol.K 0,9 cm2/s 1683 K 2628 K 5159 K 1 x 10-7 Torr (1050oC ) 1 x 10-5 Torr (1250oC ) Propriedades Mecânicas 2,6 x 10-6/K 155,8 GPa C11 = 165,7GPa C12 = 63,9 GPa C44 = 79,6 GPa 0,2152 64,1 GPa Observação -2,3 x 10-4 eV/K cm V . s cm cm V . s cm intrínseco Temperatura ambiente intrínseco intrínseco ligação covalente sólido sólido Estrutura Cristalina O silício apresenta estrutura tipo diamante com parâmetro de rede a = 5,43 Å. Basicamente esta estrutura cristalina pode ser representada por duas redes Cúbicas de Face Centrada (CFC-FCC) 5 deslocadas de ¼ do comprimento da diagonal principal da rede de referência conforme mostra a figura 2 abaixo. Nesta figura as duas redes CFC estão representadas com tons diferentes à fim de facilitar a visualização. Figura 2 - Representação da estrutura cristalina do silício como duas redes CFC deslocadas. Quando se fala em processos de corrosão anisotrópica, onde a anisotropia está associada à orientação cristalina dos planos atômicos do cristal, torna-se necessário definir os planos principais de uma rede cúbica e indexá-los de acordo com os índices de Miller, conforme mostra a figura 3. Figura 3 - Principais planos cristalinos em uma rede cúbica. Em corrosão, quando se especifica a taxa de corrosão em uma determinada direção, [100] por exemplo, isto significa que o processo se dá em uma direção normal ao plano cristalino correspondente, conforme está mostrado na figura 4. Figura 4 - Exemplo de plano cristalino e orientação cristalina. 6 A observação de um cristal de silício em cada uma destas direções preferenciais, mesmo sem indicar a presença das ligações químicas entre os átomos, é possível verificar que apenas o espaçamento entre os átomos já fornece indícios sobre o comportamento da corrosão em cada uma das direções referidas. Na figura 5 estão representadas as visões de cada uma das direções principais de uma rede cristalina de silício. As posições atômicas estão dimensionadas conforme o parâmetro de rede do silício, entretanto os raios atômicos estão fora de escala por uma questão de facilitar a visualização. Figura 5 - Vista da rede cristalina do silício de cada uma das três principais direções. A primeira vista nota-se que o grau de compactação atômica difere em cada uma das orientações e este fato tem conseqüências diretas sobre as taxas de corrosão. Fica evidente que nas orientações [100] e [110] a taxa de corrosão deve ser superior à da orientação [111]. Considerando agora as ligações químicas incompletas (“dangling bonds”) existentes na superfície, novamente se verifica a existência de uma maior densidade destas ligações nos planos (100) e (110) do que no plano (111), como pode ser constatado na figura 6. Outro fator importante é o grau de exposição das ligações à solução de corrosão, pois em princípio na reação a ligação entre dois átomos vizinhos é rompida pela presença de um radical OH que se encontra próximo. Como a - ligação com o radical OH provoca um desbalanceamento na distribuição das nuvens eletrônicas do silício ao qual se ligou, fica mais fácil romper as demais ligações. Assim quanto maior o número de ligações expostas à solução tanto mais fácil é remover o átomo de silício da rede cristalina. No caso da direção [111] verifica-se que existe apenas uma ligação disponível na superfície enquanto as demais estão bastante afastadas, e portanto protegidas pelos átomos vizinhos que também só apresentam uma ligação exposta. Assim sendo fica fácil explicar porque é tão difícil corroer planos (111). Figura 6 - Célula unitária do silício mostrando as ligações químicas entre os átomos. Estão representados os planos (100), (110) e a direção [111]. 7 Orientação Cristalina das Lâminas Após o processo de crescimento das barras de silício com a orientação desejada as lâminas são cortadas seguindo um padrão que permite identificar visualmente a orientação principal da mesma, isto é, a orientação normal ao plano da superfície, assim como permite saber como estão orientados os principais planos cristalinos no plano da lâmina. A figura 7 mostra as principais direções cristalinas em uma lâmina de silício [100] em relação ao chanfro principal (“primary flat”). É importante ressaltar que as orientações não estão sendo escritas seguindo as regras dos índices de Miller por uma questão de simplificação. Com base nesta figura é possível efetuar a orientação das máscaras apropriadamente a fim de obter os resultados desejados no final do processo. Com exceção da orientação [100], que é normal à superfície da lâmina, todas as demais orientações estão paralelas à superfície da lâmina. Figura 7 - Principais orientações cristalinas no plano de uma lâmina de Si[100]. A figura 8 mostra um exemplo das principais orientações cristalinas de uma lâmina de silício [110] em relação ao chanfro principal. O principal problema das lâminas [110] é que a orientação do chanfro varia de fabricante para fabricante, o que pode causar alguns transtornos durante o processo, portanto é interessante criar uma máscara de teste com diversas estruturas e alinha-la com o chanfro para estudar o resultado. Figura 8 - Principais orientações cristalinas no plano de uma lâmina de Si[110]. 8 Corrosão Anisotrópica de Silício Os primeiros estudos relativos aos efeitos de anisotropia durante o processo de corrosão do silício foram efetuados no final dos anos sessenta, associados ao crescimento da indústria eletrônica. Nesta época o maior interesse estava associado ao processo de isolação e contato elétrico dos dispositivos. O processo anisotrópico apresentava como principal vantagem sua reproducibilidade. Em seu trabalho D.B. Lee [5] mostrou algumas estruturas obtidas durante o processo de corrosão do silício em uma solução a base de hidrazina empregando máscaras de alumínio. Neste trabalho foram analisadas as orientações cristalinas dos planos remanescentes do processo. Posteriormente na década de setenta E. Bassous [6] estudou o processo de corrosão empregando uma solução à base de etilenodiamina e pirocatecol na fabricação de canais e orifícios em lâminas de silício. Neste trabalho é mostrado o processo de fabricação de microcanais similares aos empregados até os dias de hoje em impressoras de jato de tinta. Atualmente o processo de corrosão anisotrópica pode ser efetuado com diversas soluções que apresentam vantagens e desvantagens específicas. Dentre as mais conhecidas estão soluções à base de metais alcalinos do grupo Ia, à base de Etileno Diamina (EDP), de Tetra-Metil Hidróxido de Amônio (TMAH) e à base de Hidrazina. A seguir serão abordados cada um dos processos com suas características básicas, vantagens e desvantagens. Hidrazina O uso de soluções de hidrazina no processo de corrosão de silício é bastante reduzido em função dos cuidados necessários no manuseio deste tipo de composto. A hidrazina é um oxidante poderoso comumente empregado como combustível líquido de foguetes, e portanto perigoso e de difícil obtenção. Ao reagir com o oxigênio do ar, forma nitrogênio e água conforme a reação N 2 H 4 + O2 → N 2 + 2 H 2 O . Além das suas características explosivas, o produto ainda apresenta elevado grau de toxidez, com TLV = 1 ppm para contato com a pele. TLV que é a sigla para “Threshold Limit Value” corresponde à concentração máxima permissível de um material. Assim como o TMAH, a hidrazina não ataca o alumínio o que permite seu emprego em pósprocessamento de dispositivos com contatos de alumínio. Um estudo recente desta característica da solução a base de hidrazina foi desenvolvido por M.A. Gajda et al. [7]. EDP As soluções de Etilenodiamina-Pirocatecol são outra alternativa para a o processo de corrosão anisotrópica de silício. Os primeiros e mais completos estudos sobre esta solução foram efetuados por A. Reisman et al. [8] e posteriormente por H. Seidel et al.[9]. As soluções de EDP são geralmente empregadas em temperaturas elevadas próximo ao ponto de ebulição (~118oC para a solução B [8]). A pirazina pode ser adicionada em pequenas quantidades para aumentar as taxas de corrosão e melhorar a seletividade. Em temperaturas mais baixas a solução produz resíduos insolúveis e tende a “envelhecer” rapidamente. A presença de oxigênio na solução que é responsável pelo processo de envelhecimento e pelo aumento das taxas de corrosão, pode ser evidenciada pela mudança de cor da solução do ambar para o vermelho escuro. Entretanto o uso de atmosfera de argônio [8] ou nitrogênio [9] no recipiente reduz estes efeitos. Borbulhar argônio na solução aquecida também promove a remoção do oxigênio. Segundo H. Seidel et al.[9] as taxas de corrosão da solução de EDP tipo S [9][8], à 50 oC, para as direções [100]:[110]:[111] do silício são aproximadamente (5):(9):(0,06) micrômetros por hora, o que implica em uma anisotropia de (83):(150):(1), e a razão das taxas de corrosão 9 Si/SiO2, na mesma temperatura, é de aproximadamente 105. O que confirma uma anisotropia razoável e uma excelente eficiência do SiO2 como máscara. Metais nobres também podem ser empregados como máscara pois não são atacados pela solução, entretanto o alumínio é fortemente atacado, o que impede sua aplicação em pósprocessamento CMOS. A reduzida taxa de corrosão em silício dopado com boro [10] na solução de EDP abre margem para o uso de técnicas de “etch -stop” durante o processo. Suas principais desvantagens são: o elevado grau de toxidez [10]; se trata de um produto carcinogênico; é e altamente corrosivo para os metais não nobres. A tabela II mostra um exemplo de solução EDP. Tabela II - Composição da solução S (“slow”) estudada por Seidel [9] e Reisman [8]. Composto Etileno-Diamina Pirocatecol Água Pirazina Quantidade 1000 ml 160 g 133 ml 6g TMAH A solução de Tetrametil Hidróxido de Amônia é a única que apresenta total compatibilidade com os processos MOS e CMOS pois não contém metais alcalinos em sua formula, conforme mostra a figura 9. Usualmente o TMAH é um dos compostos presentes nas soluções de revelação de fotoresiste empregados no processo de litografia. CH3 H3C N OH H3C CH3 Figura 9 - Molécula de TMAH. Outro fator de compatibilidade do TMAH com os processos MOS e CMOS se deve ao fato de não atacar o alumínio significativamente. As soluções de TMAH não apresentam a toxidez do EDP e inflamabilidade da hidrazina, mas em se tratando de uma base forte é necessário tomar algumas precauções, principalmente em relação aos olhos [10]. Segundo Tabata et al.[11] as taxas de corrosão da solução de 20% de TMAH, à 60 oC, para as direções [100]:[110]:[111] do silício são aproximadamente (30):(15):(1,4) micrômetros por hora. Isto implica em uma anisotropia de (21):(11):(1). Nestas condições a taxa de corrosão do SiO2 é de aproximadamente 12 nm/h o que implica em uma razão de 2,5 x 103, a qual é bem menor que a da solução de EDP, mas também viabiliza o uso de mascara de óxido. Soluções de Hidróxidos Alcalinos Em princípio todos os hidróxidos alcalinos podem ser empregados no processo de corrosão anisotrópica de silício, dentre eles os mais empregados são o NaOH e o KOH por sua facilidade de obtenção, baixo custo e reduzida toxidez. A única desvantagem do emprego do NaOH está 10 vinculada à elevada mobilidade dos íons de sódio dentro do SiO2 , muito maior que a do potássio, devido às reduzidas dimensões do primeiro. O trabalho de I. Zubel et al. [12] apresenta um comparativo entre os processos de corrosão empregando NaOH e KOH. Em função desta pequena desvantagem do sódio em relação ao potássio e da existência de uma grande quantidade de informações sobre o segundo composto este trabalho será orientado para sua aplicação. Solução de KOH As soluções alcalinas à base de KOH são com certeza as mais estudadas em sua aplicação para definir estruturas tridimensionais em silício. Um dos primeiros estudos a mencionar o uso de soluções a base de KOH foi publicado na década de 70 por K.E. Bean [13]. Posteriormente na década de 90 o trabalho de H. Seidel et al.[9] desenvolveu um dos mais completos estudos sobre anisotropia e taxas de corrosão em função da concentração e da temperatura da solução. Neste trabalho foram apresentados resultados comparativos com a solução EDP e a adição de IPA (Álcool Isopropílico) na solução de KOH. Os resultados obtidos são citados mundialmente tornando este artigo uma das principais referências quando se fala em corrosão anisotrópica de silício. A Reação A reação do silício em soluções alcalinas é razão de bastante discussão e, até o momento, não é perfeitamente compreendida. Diversos autores estudaram a reação e existem diferentes propostas. Segundo O.A.Ohlweiler [14] a reação do Silício em solução alcalina obedecia a reação Si + 4OH − → SiO 4 −4 + 2H 2 que implicava na formação de silicatos e hidrogênio na forma de gás. Posteriormente Raley et al. [15] sugeriram que a reação devia ser do tipo +2 Si + 2OH − → Si (OH ) 2 + 4e − +2 −2 Si (OH ) 2 + 4e − + 4 H 2O → Si (OH ) 6 + 2 H 2 onde estão evidenciados: a formação de um hidróxido de silício; hidrogênio na forma de gás; e por último a existência de uma carga elétrica que promove o surgimento de um potencial negativo do silício em relação à solução. Mais recentemente H. Seidel [16] propôs uma nova equação para a reação em três etapas que consiste de: +2 Si + 2OH − → Si (OH ) 2 + 4e − 4 H 2O + 4e − → 4OH − + 2 H 2 +2 −2 Si (OH ) 2 + 4OH − + 2 H 2O → SiO2 (OH ) 2 + 2 H 2O e cuja soma dá: 11 −2 Si + 2OH − + 2 H 2O → SiO2 (OH ) 2 + 2 H 2 . Neste modelo, a taxa de corrosão é limitada pela reação (redox) das moléculas de água que estão adsorvidas à superfície do silício e pela formação da dupla camada de carga na interface Si-solução. Os elétrons necessários para a reação são produzidos pela reação dos íons hidroxila com o silício e são injetados na banda de condução do semicondutor. Todos estes resultados indicam a natureza eletroquímica da reação do silício em solução alcalina, e isto é efetivamente empregado no controle da espessura de membranas durante o processo de corrosão [17]. A abordagem mais específica do aspecto eletroquímico da reação, suas possíveis implicações e aplicações fogem ao escopo deste trabalho. Anisotropia O principal mecanismo para estudo da anisotropia desenvolvido por Seidel consiste de uma máscara em forma de “Wagon Wheel” conforme mostrado na figura 10. Na prática os ângulos dos “raios” da roda devem ser menores ou iguais à 1 o a fim de permitir a visualização detalhada da anisotropia. Ao ser aplicada sobre a lâmina o processo de corrosão fica restrito às áreas não protegidas cuja orientação varia entre 0 e 360o. Como o processo de corrosão, na direção perpendicular ao plano da superfície, é homogêneo em toda a superfície não protegida, os efeitos do mascaramento serão sentidos apenas no processo de corrosão das paredes laterais, isto é, no processo de corrosão sob a máscara. O resultado disto é o surgimento de uma figura polar que indica visualmente as direções mais atacadas e as menos atacadas. Figura 10 - Exemplo de máscara tipo “Wagon Wheel”. O resultado da corrosão de lâminas de silício orientadas na direção [100] e [110], mascaradas com o padrão “w agon wheel”, estão mostrados nos gráficos da figura 11. Os gráficos normalizados foram feitos com base nos dados de Seidel et al. [9] para uma solução de KOH. Figura 11 - Taxas de corrosão lateral em lâminas de silício [100] e [110]. 12 O padrão observado para uma solução de EDP é praticamente idêntico quando se trata de uma lâmina [100] e apresenta uma alteração apreciável no caso da lâmina [110] [9]. Parâmetros de Corrosão Com base nos dados obtidos por H. Seidel et al.[9] foram elaborados diversos gráficos que facilitam a determinação do conjunto de parâmetros mais apropriados para o processo em função das taxas de corrosão nos planos [100], [110] e da máscara de SiO2, que é a mais empregada. A figura 12 mostra as taxas de corrosão do silício na direção [100] para diferentes temperaturas e concentrações de KOH. É importante ressaltar que as concentrações são em percentual de massa. Figura 12 - Taxa de corrosão de silício na direção [100] em função de temperatura e concentração de KOH. A fim de facilitar o uso da informação as figuras 13a e 13b mostram a variação das taxas em função da temperatura e da concentração respectivamente. Na figura 13a estão representadas apenas quatro concentrações para evitar a sobreposição dos pontos no gráfico. 13 [100] [100] Taxa de Corrosão (µm/h) 10 o ( C) 20 30 40 50 60 70 80 90 100 10 1 10 Temperatura 100 Taxa de Corrosão (µm/h) Concentração (% KOH) 10 40 50 60 100 1 20 30 40 50 60 70 80 90 100 110 10 o 20 30 40 50 60 Concentração (% KOH) Temperatura ( C) (a) (b) Figura 13 - Variação da taxa de corrosão do silício na direção [100] em função da temperatura para diversas concentrações (a) e em função da concentração para diversas temperaturas (b). A figuras 13a,b evidenciam uma forte dependência com a temperatura que permite variar a taxa de corrosão de até duas ordens de grandeza na faixa entre 20 e 100oC o que não é surpresa pois a temperatura tem efeito direto sobre a cinética da reação. A variação de concentração por sua vez não apresenta efeito tão marcante sobre as taxas de corrosão. Notase a existência de um máximo próximo da concentração de 20% e uma posterior redução para concentrações maiores. Segundo Seidel et al.[9] para concentrações maiores a taxa de corrosão apresenta uma proporcionalidade com a quarta potência da concentração de água na solução. A literatura também ressalta que para concentrações reduzidas (< 20%) em temperaturas da ordem de 70oC o processo de corrosão apresenta aumento da rugosidade final da superfície [18]. Este tipo de rugosidade conhecido como texturização é bastante empregado na fabricação de células solares, nas quais o aumento de área implica em aumento de eficiência [19]. Entretanto, é interessante ressaltar que em estudos efetuados com concentrações de 10% em temperaturas de 50oC não foi observada a rugosidade citada por I. Zubel [18], conforme mostra a figura 14. Figura 14 - Resultado de um processo de corrosão empregando solução de KOH 10% à 50oC . Na direção [110] as taxas não variam muito em função dos mesmos parâmetros conforme mostra a figura 15. A anisotropia média entre as direções [110] e [100] é de [110] ≅ 1,5 [100] 14 para toda a faixa dos parâmetros apresentados. Figura 15 - Taxa de corrosão do silício na direção [110] em função da temperatura e da concentração de KOH. Como no caso da direção [100] as figuras 16a e 16b mostram a variação das taxas de corrosão na direção [110] em função da temperatura e da concentração respectivamente. Como no caso anterior a figura 16a apresenta apenas quatro concentrações para evitar a sobreposição dos pontos no gráfico. [110] Concentração (% KOH) 10 40 50 60 100 10 1 10 Temperatura Taxa de Corrosão (µm/h) Taxa de Corrosão (µm/h) [110] o ( C) 100 20 30 40 50 60 70 80 90 100 10 1 20 30 40 50 60 70 o Temperatura ( C) 80 90 100 110 10 20 30 40 50 60 Concentração (% KOH) (a) (b) Figura 16 - Variação da taxa de corrosão do silício na direção [110] em função da temperatura para diversas concentrações (a) e em função da concentração para diversas temperaturas (b). 15 Conhecidas as taxas de corrosão nos dois principais planos cristalinos é fundamental analisar as taxas de corrosão do SiO2 , que é a principal máscara no processo de corrosão. O nitreto de silício também é bastante empregado, mas sua deposição direta sobre o silício provoca elevados níveis de “stress” mecânico nas lâminas. A figura 17 mostra as taxas de corrosão para uma camada de SiO2 crescida térmicamente em presença de vapor de água (óxido térmico úmido). Como o SiO2 é um material amorfo não existe sentido em falar sobre a direção da corrosão. Também é importante salientar que as taxas estão expressas em nanômetros por hora. Figura 17 - Taxa de corrosão do SiO2 em função da temperatura e da concentração de KOH. Como no caso das direções [100] e [110] a dependência com a temperatura apresenta um evidente aumento da taxa de corrosão com o aumento da temperatura, novamente por se tratar de uma reação cuja cinética depende diretamente deste parâmetro. No caso do efeito de variação da concentração nota-se claramente uma mudança no comportamento quando a concentração ultrapassa os 30% de KOH. Este comportamento é linear com a concentração até os 30% e acima destes valores decai aproximadamente com o quadrado da concentração molar de água na solução [9]. Nas figuras 18a e 18b estão representadas as taxas de corrosão como função da temperatura e da concentração respectivamente. Como existe um valor máximo para taxa de corrosão em função da concentração o gráfico da figura 18a apresenta apenas tr6es conjuntos de pontos para evitar a superposição dos dados. 16 SiO2 SiO2 Concentração (% KOH) 10 30 60 100 10 1 10 Atenção: Existe um Máximo para a Concentração de 30% 20 30 40 50 60 70 o Temperatura ( C) 80 90 100 110 1000 Temperatura o Taxa de Corrosão (nm/h) Taxa de Corrosão (nm/h) 1000 ( C) 20 30 40 50 60 70 80 90 100 100 10 1 10 20 30 40 50 60 Concentração (% KOH) (a) (b) Figura 18 - Variação da taxa de corrosão do SiO2 em função da temperatura para diversas concentrações (a) e em função da concentração para diversas temperaturas (b). Como o SiO2 é o principal material de mascaramento das estruturas torna-se fundamental o conhecimento do grau de anisotropia existente entre a taxa de corrosão do silício e a taxa de corrosão do óxido. Para evidenciar o grau de anisotropia existente a figura 19 mostra a razão entre a taxa da direção [100] e a taxa de corrosão do SiO2 em função da temperatura e da concentração da solução. Figura 19 - Anisotropia na taxa de corrosão entre a direção [100] do silício e o SiO2 empregado como máscara. A partir dos dados aqui compilados é possível estimar os resultados de um processo de corrosão empregando solução de KOH, desde que sejam mantidas as estabilidades de temperatura e da concentração durante o processo. 17 Processo empregando KOH As características agressivas da solução de KOH impedem seu uso após a conclusão dos processos de microeletrônica necessários para criar as estruturas responsáveis pela excitação e pelo sensoreamento no dispositivo. Portanto o processo de corrosão KOH deve ser executado antes de todos os demais processos e existem cuidados específicos a serem adotados para garantir o sucesso do mesmo. A seguir serão analisadas as principais etapas do processo de corrosão. Projeto de Máscaras para KOH Quando se trabalha com KOH o processo de corrosão, a ser efetuado no início do processo, se restringe à parte de trás da lâmina, pois a existência de qualquer irregularidade na sua superfície frontal impediria etapas posteriores de aplicação de fotoresiste, a menos que fossem empregadas técnicas diferentes da aplicação com “spinner”. Neste caso a dispersão do fotoresiste se torna irregular, o que prejudica o processo posterior de mascaramento e revelação. Quando se trabalha com o lado posterior da lâmina é muito interessante utilizar lâminas de dupla face (polida em ambos os lados), pois isto facilita o alinhamento da máscara posterior. Outro cuidado importante está associado com a marca de alinhamento, que também ficará na parte posterior da lâmina. O cuidado se refere ao fato de que quando as máscaras são desenhadas em programa gráfico apropriado o desenho é feito sempre visualizando a estrutura pela parte da frente da lâmina. Quando a máscara é aplicada na face posterior a marca de alinhamento da máscara subsequente fica espelhada, conforme mostra a figura 20. Marcas de Alinhamento Máscara 1 Lado posterior (KOH) Máscara 2 Lado anterior (Metal) Máscaras Superpostas no Projeto A marca de alinhamento ficou espelhada após a aplicação na parte posterior da lâmina. Resultado na Amostra Tentativa de alinhamento da segunda máscara no Projeto Figura 20 - Problema de alinhamento da máscara anterior em relação à máscara subsequente devido ao fato da primeira sera plicada na face posterior da lâmina. 18 A solução para este problema é colocar as marcas de alinhamento da primeira e da segunda máscara em posição simétrica em relação ao dispositivo que está sendo fabricado, conforme mostra a figura 21. Marcas de Alinhamento Máscara 1 Lado posterior (KOH) Máscara 2 Lado anterior (Metal) Máscaras Superpostas no Projeto e na Amostra Figura 21 - Correção do problema de alinhamento colocando as primeiras marcas de alinhamento em posição simétrica ao dispositivo. Alinhamento Quando não se dispõe de uma máquina de alinhamento de dupla face torna-se necessário desenvolver um processo alternativo que permita um alinhamento razoável entre as partes posterior e anterior da lâmina. Isto pode ser alcançado com uma marca feita em ambos os lados da lâmina com bom alinhamento, mas neste caso ambas as máscaras deverão ser alinhadas a olho nu, o que implica em um alinhamento precário. Outro processo consiste em montar um dispositivo mecânico que sustente ambas as máscaras alinhadas e que permita introduzir a lâmina com fotoresiste em ambos os lados para a fase de sensibilização. Neste caso a sensibilização e a revelação de ambos os lados ocorre simultaneamente, o que não é nada simples sob o aspecto de manuseio. Por fim, é necessário proteger a parte frontal da lâmina do processo de corrosão, o que também não é uma tarefa simples. Este processo permite um alinhamento consideravelmente melhor que o anterior mas é mais complexo. Mesmo quando se dispõe de uma máscara de alinhamento, o processo da primeira máscara, no lado posterior da lâmina, é efetuado com alinhamento visual da máscara em relação ao chanfro da lâmina. Mesmo que este processo não seja preciso a anisotropia da corrosão garante um resultado satisfatório. Isto ocorre pois o processo de corrosão apresenta um fenômeno de auto-alinhamento em relação à lâmina, conforme mostrado no esquema da figura 22. 19 Figura 22 - Efeito de auto-alinhamento do processo de corrosão para uma máscara mal alinhada em relação ao chanfro da lâmina. Como o auto-alinhamento ocorre em relação à rede cristalina da lâmina fica garantido o alinhamento das estruturas obtidas no processo de corrosão. Com isto fica garantido o alinhamento das próximas máscaras em relação à estrutura cristalina da lâmina. O alinhamento da segunda máscara tem que ser efetuado em uma alinhadora com câmera de infravermelho que permite visualizar as estruturas existentes na parte de trás da lâmina através da mesma. Em alguns casos o alinhamento pode ser efetuado com lâminas de apenas uma face polida, mas isto dificulta bastante o alinhamento e conseqüentemente diminuí a qualidade dos resultados. Controle da profundidade da corrosão O controle de profundidade do processo de corrosão, para a obtenção de membranas e ou de cantileveres, pode ser feito de diversas maneiras que variam em sofisticação e consequentemente em precisão. A primeira técnica, extremamente simples, consiste em estimar o tempo de processo de corrosão com base no conhecimento das taxas de corrosão do sistema e da solução empregada. Medindo o tempo de corrosão nas condições onde a taxa é bem conhecida é possível determinar a profundidade da cavidade pela equação P = β .t , onde β é a taxa de corrosão em micrômetros por hora e t é o tempo em horas. Neste caso é indispensável a caracterização da taxa de corrosão assim como manter a estabilidade do processo e a homogeneidade da solução. A segunda técnica de controle requer medidas ao longo do processo, o que implica na retirada das amostras limpeza em água DI e secagem para a análise posterior. Esta técnica foi desenvolvida para estruturas fabricadas em lâminas [100] na fabricação de membranas. O processo está baseado no fato de o ângulo entre o plano (100) e o plano (111) em uma lâmina [100] é de 54,74o, conforme mostra a figura 23. 20 54,74o x P (111) Silício [100] (100) Figura 23 - Esquema para determinação de profundidade de corrosão em uma lâmina de Si[100]. Neste caso a profundidade da cavidade é determinada pela equação P = 1,4144.x , onde x é a largura da parede correspondente ao plano (111) medido na horizontal. Esta medida é efetuada empregando o retículo do microscópio óptico. Como a profundidade de foco (DOF) dos microscópios ópticos é reduzida quando comparada com as profundidades das cavidades medidas, torna-se necessário focalizar e medir a borda superior do plano (111) e posteriormente focalizar e medir a borda inferior do plano (111), no fundo da cavidade. Esta técnica também permite determinar a espessura da membrana, e para isto basta medir a espessura total da lâmina com um micrômetro. Então a espessura da membrana (EM) será dada pela equação EM = EL − P = EL − 1,4144.x , onde EL corresponde à espessura da lâmina. A terceira técnica de controle de profundidade consiste na alteração química e/ou física da lâmina a partir de uma determinada profundidade a fim de que naquela região a corrosão cesse completamente ou sofra uma redução apreciável. No caso do silício isto pode ser obtido de duas maneiras. A primeira consiste em dopar o silício com boro em pregando processos convencionais de dopagem a fim de transformar uma determinada região em Si-p++. É sabido que as taxas de corrosão diminuem apreciavelmente para o silício dopado com boro em soluções de KOH. Entretanto a redução mais drástica aparece para dopagens acima de 1020/cm3 que é uma dopagem considerável, tendo em vista que qualquer material tem aproximadamente 1023/cm3 (átomos) [17]. Já as soluções de EDP são mais sensíveis pois sofrem uma redução drástica para dopagens de boro acima de 2 x 1019/cm3 [17]. Entretanto a dopagem com boro provoca “stress”, e defeitos como conseqüência, que impedem o uso da camada em dispositivos eletrônicos [17]. O uso de implantação iônica para dopar a lâmina com boro oferece melhor controle do perfil de dopagem com a profundidade mas as implantações profundas exigem elevadas energias dos íons o que aumenta bastante o dano provocado no processo e que posteriormente tem que ser eliminado através de tratamentos térmicos. Outro fator que limita o emprego de implantação iônica de boro, é a elevada dose exigida, que implica em aumento do dispendioso tempo de uso da máquina. Ainda dentro da terceira técnica podemos considerar a técnica SOI (Silicon On Insulator) onde uma camada de óxido (SiO2) é fabricada em uma profundidade específica da lâmina. Existem diversas técnicas de formação de camadas SOI das quais as mais conhecidas são a soldagem anódica de uma lâmina oxidada de Si em uma lâmina não oxidada, e a implantação de oxigênio no silício com posterior tratamento térmico. Por último existe a opção de compra de lâminas SOI no mercado que tem custo bastante elevado. As grandes vantagens desta técnica são a redução considerável do “stress” residu al e drástica redução da taxa de corrosão das diversas soluções. Por último é importante citar o processo eletroquímico de controle de profundidade. Neste processo são necessárias lâminas com camadas n+ sobre um substrato p. Empregando a 21 técnica de quatro eletrodos desenvolvida por Kloeck et al. [20] o processo de corrosão para exatamente na junção p-n formada na lâmina em função da amostra estar polarizada acima do potencial de passivação do silício na solução de KOH. A grande dificuldade deste processo está na necessidade de existirem contatos elétricos na lâmina durante o processo de corrosão, o que implica na construção de um porta-amostra que isole quimicamente a fiação e as metalizações de contato da solução. Etapas do processo empregando corrosão com KOH A seguir será abordada uma seqüência de processamento usualmente empregada para efetuar o processo de corrosão anisotrópica de silício. Esta seqüência não é única e pode variar dependendo das exigências de limpeza do processo e de contaminação do laboratório onde ocorrem as etapas posteriores de processamento das lâminas. Outro fator crucial na determinação das etapas do processo tem há ver com os equipamentos disponíveis para a execução de cada uma das etapas. • Limpeza das lâminas O processo de limpeza das lâminas é indispensável antes de cada etapa de fabricação a fim de evitar contaminações nas etapas posteriores e a fim de remover resíduos dos processos litográficos. O processo mais conhecido é o processo de limpeza RCA detalhado no apêndice deste trabalho. Esta etapa de limpeza é fundamental sempre que as lâminas venham a ser submetidas à elevadas temperaturas, como nos processos de difusão e oxidação. Os contaminantes tem a tendência de se difundirem para o interior da lâmina e isto pode levar à falhas elétricas posteriores. • Formação da camada de máscara O processo mais comum para a formação da máscara para o processo de corrosão com KOH é a oxidação do silício em atmosfera úmida. Os parâmetros de oxidação estão disponíveis na literatura especializada. Outro material que resiste ao ataque da solução é o nitreto de silício (SixNy) que pode ser obtido por processos de deposição química de vapor (CVD). As camadas de nitreto de silício dependendo da temperatura de deposição sobre as lâminas de silício apresentam elevados níveis de “stress” mecânico. Quanto maior a temperatura de deposição maior o tensionamento da camada. Isto pode provocar a curvatura de estruturas delicadas e impedir o processamento posterior. Eletricamente o “stress” da camada pode redu zir as tensões reversas de diodos e transistores bipolares fabricados posteriormente sobre a lâmina. Em geral o crescimento da camada de nitreto sobre uma fina camada de SiO2 reduz consideravelmente o “stress” da camada. • Definição das estruturas na máscara O processo de definição das estruturas na máscara se da em geral por processo litográfico convencional. A imagem da máscara é transferida para o resiste orgânico depositado sobre a lâmina. Após da revelação da camada de resiste vem a etapa de abertura da camada de proteção a fim de expor a superfície do silício a ser atacada quimicamente pela solução de KOH. No caso do material da máscara ser o SiO2 o processo de abertura da camada se da com ácido fluorídrico buferizado (BHF) que corroe o SiO2 com uma taxa bem conhecida em função da temperatura da solução ou do ambiente. Já no caso de emprego de nitreto de silício o processo de abertura deve ser efetuado preferencialmente em um sistema de corrosão à plasma, empregando SF6 como gás reagente, por exemplo. O BHF ataca o nitreto muito lentamente e a existência de uma camada de SiO2 sob o nitreto provoca efeitos catastróficos durante o processo de corrosão. Quando o BHF ultrapassa a camada de nitreto e alcança o SiO2 a taxa de 22 corrosão lateral observada é muitas vezes maior que a taxa de corrosão vertical provocando “undercuts” extensos que inutilizam a camada de mascaramento. • Limpeza das lâminas Esta etapa inicia com a remoção do resiste empregando solventes orgânicos. Posteriormente é interessante executar a primeira etapa do processo RCA a fim de eliminar os resíduos orgânicos de resiste e dos solventes empregados na limpeza. • Processo de corrosão Em geral o processo de corrosão com solução de KOH deve ser efetuada fora da sala limpa, principalmente se existir alguma etapa de processos CMOS dentro das mesmas. Isto ocorre porque o íon de potássio funciona como carga móvel dentro do óxido de porta de transistores CMOS provocando variações de parâmetros que inviabilizam os dispositivos. • Limpeza das lâminas A limpeza das lâminas após o processo com KOH somente é crítica se as lâminas forem ser levadas para o interior de um laboratório onde são fabricadas estruturas CMOS. Caso contrário basta executar a etapa inicial do processo de limpeza, que remove a maior parte dos resíduos de potássio das lâminas. Equipamento O equipamento básico consiste de um banho térmico com temperatura controlada, um sistema de agitação da solução e um porta-amostra. A seguir serão abordados os principais fatores a serem considerados na construção do sistema para garantir a reproducibilidade dos resultados e a fim de evitar ao máximo os problemas inerentes às características do processo. Banho Térmico Consiste de um recipiente que contém a solução de corrosão a qual pode ser aquecida e mantida na temperatura desejada com a maior estabilidade possível Uma configuração interessante é o Banho-Maria, onde o recipiente que contém a solução é colocado no interior de um segundo que contém água ou outro líquido e um resistor blindado para aquecimento. A blindagem não é obrigatória mas evita o risco de choques elétricos. Este tipo de configuração garante uma elevada inércia térmica, o que implica em grande estabilidade da temperatura. Recipiente da Solução O recipiente que contém a solução de corrosão deve ser de PIREX pois dependendo da configuração do sistema de aquecimento podem ocorrer gradientes térmicos elevados o suficiente para quebrar o recipiente. Como se trata de uma solução aquecida é importante evitar o aumento de pressão no interior da câmara e para isto basta deixar um orifício para saída dos vapores. Algumas aplicações empregam saídas com serpentinas de água circulante a fim de evitar a perda de água do sistema. A perda de água implica em variação da concentração da solução e consequentemente das taxas de corrosão durante o processo. Desta forma se a saída de vapor for pequena as perdas podem ser desprezadas dentro de um processo. Entretanto se o sistema for empregado regularmente as perdas deixarão de ser desprezíveis em médio prazo. Uma solução simples para corrigir este problema economizando material é fazer uma marcação de nível no recipiente que contém a solução de corrosão e completar com água DI sempre que for necessário. Outro ponto a ser considerado tem a ver com o fato de que a reação gera hidrogênio. Quando as temperaturas de operação e as quantidades de material a ser corroído são pequenas não há problemas pois qualquer abertura no recipiente possibilita o escape do gás para o ambiente sem riscos. Caso contrário é necessário o escape do gás com segurança pois o hidrogênio explode muito facilmente. 23 Controle da Temperatura O controle de temperatura deve ser preferencialmente automático tendo em vista os tempos de processo que podem ultrapassar 24 h dependendo do que é desejado. Em muitos casos o banho térmico vem equipado com controle automático de temperatura. Entretanto a qualidade do controle é diretamente proporcional ao custo do equipamento. Uma saída econômica para este problema é montar um sistema que consiste de um controlador do tipo PID de baixo custo um termopar encapsulado em vidro e uma resistência blindada para submersão no banho térmico. Estes tipos de controles permitem ajustes, muitas vezes automáticos, que permitem adaptar o controle às características do sistema banho térmico solução de corrosão. Desta forma é possível obter estabilidade dentro de ±1oC o que leva á uma excelente reprodutibilidade de taxas de corrosão, e consequentemente dos resultados obtidos com a corrosão. Agitação da Solução A agitação da solução é de extrema importância pois o fluxo das espécies ativas e remove os resíduos facilitando aumentando a eficiência da reação [18]. Entretanto, este parâmetro é extremamente crítico principalmente quando estão sendo fabricadas estruturas sensíveis como cantileveres e membranas. A viscosidade elevada da água faz com que turbulências possam destruir as estruturas durante o processo de corrosão. Por outro lado a não agitação provoca o surgimento de um gradiente de temperatura e de concentração na solução o que provoca corrosão irregular em amostras grandes com muitos dispositivos. A solução para este inconveniente é adotar uma agitação lenta que possibilite uma circulação mínima da solução. A formação de hidrogênio na superfície do silício durante o processo também deve ser considerada pois as bolhas de gás, mostradas na figura 24 (a), tendem a se concentrar sob as protuberâncias das estruturas gerando tensões mecânicas fortes o suficiente para rompe-las, conforme mostrado na figura 24 (b). Além da tensão mecânica as bolhas funcionam com o polo positivo de uma micro-bateria que por estar muito próxima da superfície do silício, que está negativamente carregada, provocam o surgimento de grandes campos elétricos localizados. Nestas regiões as taxas de corrosão são incrementadas podendo perfurar a lâmina de lado a lado em pouco tempo. (a) (b) Figura 24 - (a) Bolhas de hidrogênio acumuladas na superfície de pequenos cubos de Si. (b) Rachaduras na membrana de SiO2 provocadas pela acumulação de bolhas de hidrogênio. Existem algumas alternativas para minimizar este problema e algumas delas funcionam ao mesmo tempo como agitação mecânica da solução. A mais simples é empregar um portaamostra que entre e saia regularmente da solução, desta forma, quando a amostra sai para a atmosfera as bolhas de H2 se rompem e escapam para o ar. Além disto a regularidade do movimento impede o crescimento das bolhas. A figura 25 mostra um exemplo deste tipo de equipamento, onde estão visíveis o sistema digital de controle de temperatura, o banho térmico, o recipiente da solução e o sistema de movimentação do porta-amostra. A movimentação do porta-amostra é efetuado por um motor AC (6 RPM) adaptado à um 24 excêntrico de acrílico. Um fio de nylon que desliza no eixo do excêntrico passa por um orifício de alinhamento até chegar ao porta-amostra. Desta forma o movimento resultante se dá apenas na vertical. Note-se que o recipiente da solução tem uma tampa na qual existem dois orifícios, um para o cateter de vidro que protege o termopar e um para a passagem do fio e da extremidade do porta-amostra. Figura 25 - Exemplo de equipamento para corrosão anisotrópica com KOH, com fotos em detalhe do controle de temperatura, do recipiente da solução e do sistema de movimentação do porta-amostra. Este tipo de configuração pode apresentar problemas de homogeneidade no processo quando as amostras são posicionadas verticalmente no porta-amostra, conforme mostra o esquema da figura 26, pois durante o processo de entrada e saída da amostra da solução não será o mesmo para a extremidade inferior e a superior da mesma. Com isto a parte inferior da amostra fica mais tempo na solução e portanto é mais atacada. Isto implica em uma variação da profundidade das cavidades, ou na variação da espessura da lâmina na direção de movimentação. 25 Lâmina b a b inicio final a Vista lateral da lâmina Porta-Amostra Figura 26 - Diagrama esquemático representando o efeito do posicionamento vertical da amostra sobre o resultado do processo de corrosão. Quando possível, o posicionamento da amostra na horizontal elimina os efeitos adversos ilustrados. Outra solução é mudar a posição da lâmina no porta-amostra com uma certa regularidade. Outro processo alternativo à movimentação mecânica é o uso de ultra-som, que provoca agitação da solução e provoca o deslocamento das bolhas. Entretanto se a potência empregada for elevada pode ocorrer cavitação com o colapso das bolhas, o que gera ondas de choque mecânicas suficientemente fortes para arrancar material localizado próximo do local da explosão. Como vantagem, o uso de ultra-som melhora a uniformidade da superfície e reduz o número de defeitos [21] Por último pode ser considerado de compostos tensoativos que reduzem a tensão superficial da solução facilitando o desprendimento das bolhas da superfície do silício. Entretanto antes do emprego deve ser verificada a compatibilidade do tensoativo com a solução de KOH que reage com praticamente tudo que é orgânico. Exemplos de estruturas A principal aplicação do processo de corrosão anisotrópica é a definição de estruturas tridimensionais no silício. Com base nos parâmetros apresentados e nas possíveis variantes dos mesmos fica evidente o potencial da técnica. A variedade de estruturas que podem ser obtidas e suas aplicações tem como principal limitação a criatividade do projetista. Atualmente existem “softwares” capazes de predizer os tipos de estruturas obtidas em função dos parâmetros empregados [22], entretanto a especialização implica em custo elevado. A seguir serão abordados alguns tipos de estruturas bastante comuns obtidas com corrosão anisotrópica e que podem ser empregados na fabricação de diversos dispositivos. Canais Os canais em geral são empregados para o transporte de fluídos e/ou para o estudo do comportamento dos mesmos quando as dimensões características das estruturas são muito reduzidas. Uma possibilidade muito interessante é a confecção de dispositivos que permitem construir dispositivos lógicos baseados no controle de fluxo de gases. Estes dispositivos são conhecidos como lógica fluídica [23]. Outra área que tem extremo interesse na aplicação de microcanais é a biotecnologia, para a qual o uso de dispositivos de dimensões microscópicas implica em grandes reduções nos custos dos reagentes para processos como PCR (“Polimerase Chain Reaction”) empregados em processos de identificação por DNA. Neste caso a meta principal é o desenvolvimento do Laboratório em Um Chip (“Lab -on-a-chip”) que consiste em uma estrutura como todos as etapas de amostragem, separação, reação e análise em um “chip” d e silício. De preferência esta estrutura deverá ser descartável. 26 A figura 27 abaixo mostra um canal obtido por corrosão anisotrópica em uma lâmina de silício [100]. O canal está orientado na direção [100] da lâmina de forma que as paredes laterais também tem orientação [100]. Na extremidade do canal estão planos (111). A rugosidade observada na lâmina se deve ao processo de corrosão ter sido efetuado na parte de trás (não polida) da mesma. É interessante notar que a rugosidade não se reproduz nas regiões atacadas. Figura 27 - Canal aberto na direção [100] de uma lâmina de silício [100]. O comprimento do canal é de aproximadamente 2 mm. Se o canal estiver orientado na direção [110] da lâmina é possível obter estruturas similares às apresentadas na figura 28. É interessante lembrar que os planos (111) apresentam reduzida taxa de corrosão e portanto podem ser empregados para determinar a dimensão final do canal, quando houver a necessidade de dimensões dentro de uma tolerância reduzida. (111) (111) (100) Vista em corte Figura 28 - Vista em corte de canais orientados na direção [110]. Membranas As membranas são as estruturas mais empregadas em dispositivos sensores como acelerômetros, sensores de pressão e sensores térmicos. As membranas podem ser de silício ou compostas do material empregado como máscara no processo de corrosão. Esta definição depende muito do tipo de aplicação do dispositivo empregado. Membranas de silício muito finas são de difícil obtenção pois o controle do processo se torna crítico e qualquer descontrole implica 27 na perda das mesmas. Métodos de controle de espessura, comentados anteriormente, também apresentam dificuldades ou desvantagens posteriores. Portanto, quando se deseja membranas muito finas é interessante empregar membranas baseadas no material da máscara. Quando o processo de corrosão é executado no início da fabricação e existem etapas posteriores para fabricação de outras estruturas é interessante manter a membrana espessa o suficiente para resistir as etapas de colocação de resiste em “spinners” nos quais a lâmina é presa por vácuo. Isto evita o rompimento das membranas. A forma final da membrana depende muito da lâmina empregada e da orientação da máscara sobre a mesma. A figura 29 mostra diversas cavidades abertas na parte posterior da lâmina de silício de forma a constituir membranas na parte anterior da mesma. As cavidades estão orientadas na direção [110] da lâmina e suas paredes laterais são planos (111) do silício. Logo neste tipo de estrutura as dimensões finais são facilmente previsíveis. Figura 29 - Cavidades empregadas para a fabricação de membranas na parte anterior da lâmina. As cavidade mostradas tem dimensão da ordem de 1 x 1 mm. Cantilevers Os cantileveres, como as membranas, também tem suas características definidas de acordo com a sua aplicação. O processo de obtenção dos cantileveres é muito similar ao da obtenção das membranas. A aplicação mais notória de cantileveres microfabricados em silício é a das ponteiras dos microscópios de força atômica (AFM). Outra aplicação interessante corresponde aos acelerômetros baseados em cantilevers e estruturas similares. A figura 30 mostra um exemplo de cantilever obtido por corrosão anisotrópica em duas etapas. A primeira na parte posterior da lâmina e a segunda na parte anterior. O que chama mais atenção nesta estrutura é o comprimento do braço do cantilever (~3 cm) e a sua espessura ~10 µm. Dada a grande dimensão a fotografia mostrada foi montada a partir de diversas fotografias obtidas com microscópio eletrônico de varredura. 28 Figura 30 - Cantilever obtido por processo de corrosão com KOH. Comprimento ~3 cm e espessura do braço ~10 µm. Conclusões Os processos de corrosão anisotrópica em silício já podem ser considerados como tecnologia sedimentada e de uso comum na definição tridimensional de dispositivos microfabricados. Entretanto isto não significa que a não exista mais campo para pesquisa nesta área, muito pelo contrário, as respostas até o momento obtidas ainda propõem um grande número de desafios tanto no aspecto científico quanto no aspecto tecnológico. Este trabalho foi idealizado como uma introdução para alunos e pesquisadores que tenham interesse em empregar esta técnica ou que tenham interesse em orientar seus esforços de pesquisa nesta direção. Referências Bibliográficas [1] - Jay Jakubczak, “Vision for MEMS” http://www.sandia.gov/mstc/technologies/micromachines/vision.html [2] - Jiantao Pan, “MEMS and Reliability” http://www.ece.cmu.edu/~koopman/des_s99/mems/index.html Carnegie Mellon University (1999) [3] – Kurt E. Petersen, “Dynamic micromechanics on silicon: techniques and devices.” , IEEE Trans. Electron Devices, ED-25 (1978) 1241-1250 [4] – Tom Knight, “Silicon Properties”, http://www.ai.mit.edu/people/tk/tks/silicon.html (1994) [5] – D.B. Lee, Anisotropic etching of silicon. Journal of Applied Physics, 40 (1969) 4569- 4574 [6] – E. Bassous, Fabrication of novel three-dimensional microstructures by the anisotropic etching of (100) and (110) silicon. IEEE Trans. Electron Devices, ED-25 (1978) 1178-1185 [7] – M.A. Gajda, H. Ahmed, J.E.A. Shaw and A. Putnis, Anisotropic etching of silicon in hydrazine, Sensors and Actuators A, 40 (1994) 227 [8] – A. Reisman, M. Berkenblit, S.A. Chan, F.B. Kaufman and D.C. Green, The controlled etching of silicon in catalized ethylenediamine-pyrocatechol-water solutions, J.Electrochem.Soc., 126 (1979) 1406 [9] - H.Seidel, L.Csepregi, A.Heuberger and H.Baumgärtel, Anisotropic Etching of Crystalline silicon in Alkaline Solution, J.Electrochem.Soc., 137 (1990) 3612-3626 [10] – M. Elwenspoek and H. Jansen, Silicon Micromachining, Cambridge University Press, Cambridge - UK (1998) 29 [11] – O. Tabata, R. Asahi, H. Funabashi, K. Shimaoka and S. Sugiyama, Anisotropic etching of silicon in TMAH solutions, Sensors and Actuators A, 34 (1992) 51 [12] – I. Zubel and I. Barycka, Silicon anisotropic etching in alkaline solutions I: The geometric description of figures developed under etching Si(100) in various solutions, Sensors and Actuators A, 70 (1998) 250 [13] – K.E. Bean, Anisotropic etching of silicon. IEEE Trans. Electron Devices, ED-25 (1978) 1185-1193 [14] – O.A. Ohlweiler, Química Inorgânica, Edgar Blücher, S.P. (1971) Vol.1, pp. 265 [15] – N.F. Raley, Y. Sugiyama, T. Vanduzer, (100) silicon etch-rate dependence on boron concentration in ethylenediamine-pyrocatechol-water solutions, J.Electrochem.Soc., 131 (1984) 161-171 [16] – H. Seidel, in: A. Heuberger (Ed.), Mikromechanik, Springer-Verlag, 1991, pp. 151 [17] – S.D. Collins , Etch stop techniques for micromachining, J.Electrochem.Soc., 144 (1997) 2242 [18] – I. Zubel, Silicon anisotropic etching in alkaline solutions II: On the influence of anisotropy on the smoothness of etched surfaces, Sensors and Actuators A, 70 (1998) 260 [19] – Z. Xi, D. Yang, D. Que, Texturization of monocrystalline silicon with tribasic sodium phosphate, Solar Energy Materials & Solar Cells 77 (2003) 255–263 [20] – B. Kloeck , S.D. Collins, N. deRooji and R.L. Smith, Study of Electrochemical Etch-Stop for High Precision Thickness Control of Silicon Membranes, IEEE Trans. Electron Devices, ED-36 (1989) 663-669 [21] – J. Chen, L. Liu, Z. Li, Z. Tan, Q. Jiang, H. Fang, Y. Xu, Y. Liu “Study of anisotropic etching of (100) Si with ultrasonic agitation” Sensors and Actuators A 96 (2002) 152–156 [22] – http://www.corningintellisense.com/productsservices/products/anise.asp [23] – R.Furlan and J.N. Zemel, Behavior of microfluidic amplifiers, Sensors and Actuators A, 51 (1995) 239 Apêndice A – Processo de Limpeza de Lâminas O procedimento aqui apresentado é conhecido como processo RCA usualmente empregado em laboratórios de microfabricação. Este processo tem como características o elevado consumo de reagentes alto grau de atividade dos resíduos. Embora nas plantas industriais o processo empregado seja um descendente menos poluente do processo RCA, os princípios são exatamente os mesmos. Limpeza Preliminar Inicialmente o excesso de resiste (quando presente) deve ser removido com plasma de oxigênio ou por imersão em removedor de resiste. Após esta etapa as lâminas devem ser fervidas em uma mistura (1:2) de H2O2 : H2SO4 a 120oC durante 10 minutos, observando as precauções de segurança. (400cc de H2O2 + 800cc de H2SO4) – ATENÇÃO – Esta mistura é conhecida como “Piranha” por razões óbvias. Lavar com água deionizada (DI) em tanque de esgotamento superior (“overflow tank”) por 5 minutos. Remoção de contaminantes orgânicos residuais e certos metais (SC-1) Preparar uma nova mistura de H2O-H2O2-NH4OH (5:1:1) em um becker ou em um recipiente de sílica fundida. a. 5 partes de água DI (1000 cc) b. 1 parte de H2O2 (30% não estabilizada / grau eletrônico) (200 cc) c. 1 parte de NH4OH (29% grau eletrônico) (200 cc ) 30 Mergulhar o suporte com as lâminas de Si na solução fria e colocar o becker na chapa quente. Aquecer entre 75 e 80°C, então reduzir o aquecimento para manter a solução a 80°C por mais 10 minutos (o borbulhamento vigoroso se deve à evolução de oxigênio; a solução não deve ser fervida para evitar a decomposição do H2O2 e a volatilização da amônia). Remover o suporte com as lâminas de e coloca-lo no tanque de água DI com esgotamento superior para lavagem por 5 minutos. Remoção do filme de óxido formado Mergulhar o suporte com as lâminas diretamente em uma mistura de 1 parte de HF (49% grau eletrônico) e 50 partes de água DI. Manter as lâminas na solução em torno de 15 segundos, até que a solução de HF pare de molhar a superfície do Si. (A superfície é hidrofóbica quando não existe óxido nativo) Lavar em água DI durante 20 ou 30 segundos com agitação para remover a solução de HF. Transferir imediatamente as lâminas, sem secar, para a solução já aquecida SC-2. Remoção dos contaminantes atômicos e iônicos (SC-2) Preparar uma nova mistura de H2O-H2O2-HCl (6:1:1) em um becker ou recipiente de sílica fundida. a. 6 partes de água DI (1200 cc) b. 1 parte de H2O2 (30% não estabilizada / grau eletrônico) (200 cc) c. 1 parte de HCl (37% grau eletrônico) (200 cc) Colocar o becker em uma chapa quente e aquecer entre 75 e 80°C. Mergulhar as lâminas de Si ainda úmidas na solução quente. Manter a solução a 80°C por mais 10 a 15 minutos. Remover o suporte com as lâminas e colocar imediatamente no tanque de água DI e lavar por 10 minutos. Secagem das lâminas de Si. O processo ideal de secagem é empregando um equipamento de lavagem/secagem automática tipo “Rinser and Dryer”. No qual as lâminas são lavadas com medição de resistividade da água de saída até o valor chegar a 15MΩ-cm, quando então inicia o processo de secagem com N2 aquecido. Uma alternativa barata é empregando um “spiner” dentro de uma capela com fluxo laminar. A lâmina é girada até secar completamente. 31
Baixar