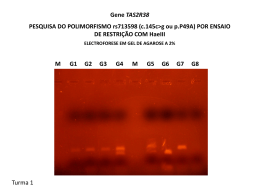
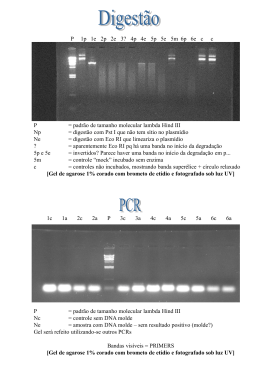
Caracterização molecular e fenotípica de plantas transgênicas de citros visando resistência à Xanthomonas citri. Bolsista Júlio César Gomes de Sousa Filho. Estudante de Biotecnologia da Universidade Federal de São Carlos. Orientador Dr. Celso Eduardo Benedetti / LNBio. CNPEM | LNLS CTBE LNBio LNNano 2 Caracterização molecular e fenotípica de plantas transgênicas de citros visando resistência à Xanthomonas citri. Bolsista Júlio César Gomes de Sousa Filho. Estudante de Biotecnologia da Universidade Federal de São Carlos. Orientador Dr. Celso Eduardo Benedetti / LNBio. Campinas, 2012. 3 “We keep moving forward, opening new doors, and doing new things, because we're curious and curiosity keeps leading us down new paths.” Walter Elias “Walt” Disney 4 AGRADECIMENTOS À minha Família que sempre me apoiou e comemorou minhas conquistas, incluindo essa tão importante; Ao CNPEM/ABTLuS pela realização do programa que me permitiu desenvolvimento científico e pessoal de imensa valia; Ao Roberto (Patriarca dos Teiús) e a querida e doce Tati pela organização e coordenação do programa, estando sempre disponíveis para ajudar e nos divertindo sempre. Muito Obrigado! Ao Celso Benedetti pela oportunidade, pela escolha, por dedicar parte do seu tempo à minha orientação, pela atenção e pela grande contribuição ao desenvolvimento científico. Muito Obrigado! À Bruna por sempre me acompanhar na bancada, nas risadas, nos almoços e nas conversas sobre Walt Disney World. À Malu pelas boas risadas, preciosas dicas e por ceder o clone da proteína WRKY bem como as plantas transformadas que foram a base do trabalho realizado. À Adriana pelas ajudas, “helps” quase constantes, bons toques, diversões, almoços, salvamentos para que não perdesse o ônibus, pela MEGA ajuda na extração de RNA e na entrega deste relatório. À Jaque pelas dicas, broncas, diversão constante, pelo empréstimo de seu “cavalo de fogo”, por conseguir uma membrana de PVDF em tempo recorde e por receber algumas broncas em nome do “Júlio do LPP”. À Mariane pelas dicas, protocolos, risadas, almoços, ajuda na revisão deste trabalho. Caio pela companhia em experimentos, pelas discussões científicas, pelo incentivo, almoços e risadas. Vocês do LPP foram essenciais. Muito Obrigado! Aos funcionários do CNPEM e membros do LNBio pela receptividade e auxílio dispensados sempre que preciso. Cito aqui alguns como: Cris do ABC que me salvou uma noite e deu preciosas dicas, Rosângela da biblioteca, Cláudia e Di da lavagem, e Priscila do LMA. Aos professores doutores Dulce Helena, Iran Malavazi, Andrea Fuentes, Anderson Cunha e Mônica Rosas, por me apresentarem o mundo científico. Como já dito a alguns de vocês, sem vocês eu não estaria aqui. Muito Obrigado! Aos bons amigos, Marina Salles, Kátia, Carol, Adriano, Henry, Heber e Dani por estimularem meus passos acadêmicos e por compartilharem comigo bons momentos. Muito Obrigado! Agradeço especialmente à Juliana Poltronieri, que me acompanhou até nessa boa aventura. Aos Bolsistas, um a um, pela companhia, risadas, almoços, passeios e troca de experiência incrível. Em especial aos companheiros de LNBio: Andrea, Mariana, Vinícius e Felipe. Muito Obrigado! A todos que contribuíram direta ou indiretamente para a realização deste trabalho. Muito Obrigado! 5 RESUMO O Cancro Cítrico, causado por Xanthomonas citri é uma doença bacteriana que afeta a maioria das variedades comerciais de citros levando a perdas econômicas. Buscando produzir plantas de citros resistentes à X. citri nosso laboratório está desenvolvendo linhagens transgênicas para porta-enxertos e variedades copa de citros. Baseado em uma análise de expressão gênica em larga escala realizada pelo grupo anteriormente, duas estratégias para a produção de plantas de citros resistente à X. citri estão sendo utilizadas. A primeira envolve a super expressão de um fator de transcrição WRKY conhecido por regular resposta de defesa basal em plantas. A segunda estratégia envolve a expressão de efetor bacteriano ativador de transcrição do tipo III, ou efetor TAL, o qual age como modulador da expressão gênica no hospedeiro. A expressão dos transgenes será avaliada por PCR e Western Blot. Plantas transformadas foram desafiadas com X. citri para o desenvolvimento dos sintomas do cancro, que são caracterizados pela formação de pústulas na superfície da folha. Os níveis de expressão de alguns genes de defesa que são alvos dos efetores de Xanthomonas também serão avaliados nos transgenes. Palavras Chave: Xanthomonas citri, efetores TAL, WRKY ABSTRACT Citrus canker, caused by Xanthomonas citri, is a bacterial disease that affects most of the commercial citrus varieties leading to economic losses. With the aim of producing citrus plants resistant to X. citri our laboratory is developing transgenic lines for citrus rootstock and scion varieties. Based on a large scale gene expression analysis undertaken by the group previously, two strategies for the production of citrus plants resistant to X. citri are being used. The first involves the overexpression of a WRKY transcription factor known to regulate basal defense responses in plants. The second strategy involves the expression of a bacterial type III transcription activator effector, or TAL effector, which acts as a modulator of gene expression in the host. The expression of the transgenes will be evaluated by PCR and Western blot analysis. Transformed plants were challenged with X. citri for the development of canker symptoms, which are characterized by the formation of raised pustules on the leaf surface. The expression levels of a number of defense-related genes as direct targets of the Xanthomonas TAL effector will also be examined in the transgenes. Keywords: Xanthomonas citri, TAL effectors, WRKY. 6 SUMÁRIO LISTA DE FIGURAS ................................................................................................... 7 1 REVISÃO DE LITERATURA ................................................................................... 8 O cancro cítrico .................................................................................................... 8 Interação Planta Patógeno .................................................................................. 9 Efetores TAL ...................................................................................................... 10 Fatores de transcrição do tipo WRKY ................................................................. 11 Estratégias para obtenção de plantas resistentes ao cancro cítrico. .................. 12 2 OBJETIVOS .......................................................................................................... 13 3 MATERIAIS E MÉTODOS .................................................................................... 13 Detecção de plantas geneticamente modificadas por PCR.. .............................. 13 Subclonagem, expressão e purificação do fator de transcrição do tipo WRKY. . 14 Análise da expressão dos transgenes. ............................................................... 16 Avaliação dos níveis transcricionais de genes de interesse. .............................. 18 Desafio das plantas com Xanthomonas citri e avaliação fenotípica ................... 19 4 RESULTADOS E DISCUSSÃO ............................................................................ 20 Detecção de plantas geneticamente modificadas por PCR.. .............................. 20 Subclonagem, expressão e purificação do fator de transcrição do tipo WRKY. . 23 Análise da expressão dos transgenes.. .............................................................. 25 Avaliação dos níveis transcricionais de genes de interesse. .............................. 29 5 CONCLUSÃO E PERSPECTIVAS ....................................................................... 30 6 REFERÊNCIAS BIBLIOGRÁFICAS ..................................................................... 31 7 LISTA DE FIGURAS Figura 1: Lesões características do Cancro Cítrico em frutos e folhas. .................................. 8 Figura 2 - Esquematização de um efetor TAL.. .................................................................... 10 Figura 3 - Representação dos aminoácidos da porção N-terminal de um fator WRKY de Arabdopsis thaliana ........................................................................................................... 122 Figura 4A – Eletroforese em gel de agarose 1% de extrações de DNA por metodologia convencional (CTAB). 4B -Eletroforese em gel de agarose 1% de extrações de DNA por metodologia convencional tratadas com RNAse Mix (Fermentas) ....................................... 20 Figura 5 - Eletroforese em gel de agarose 1% de reação de PCR para detectar plantas transformadas com efetores TAL. ..................................................................................... 21 Figura 6 - Eletroforese em gel de agarose 1% de reação de PCR para detectar plantas transformadas com efetores TAL/ Platinum Taq Polimerase (Invitrogen) e DNA tratado com RNAse.. ............................................................................................................................... 22 Figura 7 - Eletroforese em gel de agarose 1% de reação de PCR de Gradiente de temperatura para otimizar a PCR para amplificação dos efetores TAL em plantas trasnformadas. ..................................................................................................................... 22 Figura 8 - Eletroforese em gel de agarose 1% de PCR para identificação de plantas transformadas com efetores TAL nas condições otimizadas ................................................ 23 Figura 9 - Eletroforese em gel de agarose 1% de digestões para subclonagem. ................. 23 Figura 10 - Eletroforese em gel de agarose 1% de PCR de colônias de E.Coli DH5α transformadas com a construção pET28a/WRKY. ............................................................... 24 Figura 11 - Análise da expressão e purificação da proteína WRKY em E. Coli BL21 (DE3) por SDS-PAGE 13%. ........................................................................................................... 25 Figura 12 – Análise da extração de proteínas totais de folhas transformadas por SDS-PAGE 10% e 13%. ......................................................................................................................... 26 Figura 13 – Western Blot das proteínas de interesse em plantas transformadas. ................ 26 Figura 14 – Western Blot para avaliação de alíquotas de anticorpo anti-PthA disponíveis.. 27 Figura 15 – Western Blot para teste de detecção de anticorpo anti-WRKY.......................... 27 Figura 16 - Correlação entre Western Blot de plantas transformadas com fator WRKY e fenótipo das plantas desafiadas com X. citri ..................................................................... 28 Figura 17 – Correlação entre Western Blot de plantas transformadas com fator WRKY e fenótipo das plantas desafiadas com X. citri .................................................................... 29 Figura 18 – Eletroforese de RNA em gel de agarose 1% desnaturante.. ............................. 30 8 1 REVISÃO DE LITERATURA O Cancro Cítrico O setor da citricultura é um dos mais expressivos dentro do agronegócio no Brasil: suas exportações renderam, em 2009, 2,15 milhões de toneladas de produtos e US$ 1,84 bilhão em receita, representando cerca de 3% das exportações do agronegócio do país (NEVES et al., 2009). Uma das maiores ameaças à citricultura é o Cancro Cítrico, causado por duas linhagens de bactérias gram-negativas do gênero Xanthomonas: Xanthomonas citri (Xac) e Xanthomonas aurantifolii (Xaa). Os dois grupos causam sintomas bem parecidos em seus hospedeiros, sugerindo um mecanismo comum de patogenicidade (BRUNINGS; GABRIEL, 2003). Os sintomas mais evidentes do cancro são decorrentes de hiperplasia (aumento da divisão celular) e hipertrofia (aumento do volume celular), desencadeadas pelo patógeno ao alterar a transcrição de alguns genes do hospedeiro (CERNADAS et al., 2008), levando à formação de lesões circulares, inchadas e encharcadas nas folhas, frutos e galhos. Tecidos jovens como folhas de brotações e frutos nas primeiras fases de crescimento são mais susceptíveis a infecção com Xanthomonas citri (BRUNINGS & GABRIEL, 2003). Figura 1: Lesões características do Cancro Cítrico em frutos e folhas.(BRUNINGS & GABRIEL, 2003). A entrada da Xanthomonas citri no tecido vegetal ocorre por aberturas como estômatos, hidatódios e feridas provocadas por espinhos e/ou larva mineradora dos citros. A Xac se instala no mesófilo e em estágio avançado da doença as lesões podem romper a epiderme liberando bactéria no ambiente contribuindo para a disseminação, que é facilitada por ventos, chuvas, insetos, além de equipamentos de colheita e manutenção das plantas (AMARAL, 2003; BRUNINGS; GABRIEL, 2003). 9 Trata-se de uma doença economicamente importante e por tal a bactéria causadora é alvo de estudos moleculares buscando desenvolvimento de ferramentas para controle desta e/ou produção de plantas resistentes para reduzir perdas de produção (AMARAL, 2003). Interação Planta - Patógeno. As plantas estão constantemente sujeitas a infecção por patógenos. Uma das formas de reconhecer e responder a infecção envolve a percepção de padrões moleculares associados a microrganismos/patógenos (microbial- or pathogenassociated molecular patterns ou MAMPs/PAMPs), isto é, moléculas que são conservadas e essenciais (exemplos são: flagelina e lipossacarídeos) nos microrganismos, são detectadas por receptores presentes na superfície celular do hospedeiro. Esses receptores costumam possuir domínios citoplasmáticos que sinalizarão à célula o reconhecimento feito no meio extracelular, como é o caso do receptor da flagelina cujo domínio citoplasmático ativa uma cascata de sinalização por MAPKs (Mitogen-activated protein kinases) que resultará em resposta de defesa. Trata-se de um processo lento (JONES; DANGL, 2006). Uma “segunda linha” de defesa ocorre dentro da célula do hospedeiro através da expressão de genes de resistência (R) cujos produtos proteícos costumam possuir domínios de ligação a nucleotídeo (Nucleotide Binding ou NB) e domínios ricos em leucina (leucine rich repeat ou LRR), sendo esses últimos importantes para realização de interações proteína-proteína. Essas proteínas podem, na célula do hospedeiro, reconhecer proteínas do patógeno ditas de avirulência (avr), que são geralmente responsáveis pelo desencadeamento da patologia e foram translocadas para o ambiente celular do hospedeiro. Esse reconhecimento lembra uma interação do tipo receptor-ligante e desencadeia respostas de defesa que promovem a rápida morte celular no local da infecção para conter o avanço do patógeno em um evento chamado resposta de hipersensibilidade (hypersensitive response ou HR). Caso o patógeno não avance temos uma interação planta-patógeno incompatível. Em contrapartida, quando a interação avr/R não ocorre, possivelmente por ausência do gene R correspondente no hospedeiro, o fator Avr fica livre para agir na célula vegetal, provavelmente desencadeando os sintomas por consequência de mediar 10 modificações na célula do hospedeiro. Essa interação é dita compatível (FEBRES et al., 2009; DOMINGUES, 2011). Efetores TAL Após se instalar no mesófilo do hospedeiro, a bactéria transloca para as células vegetais algumas moléculas ditas efetoras. Essa translocação é mediada pelo sistema de secreção tipo III (T3S). Os efetores podem suprimir respostas de defesa, desencadear os sintomas da patologia e alterar a bioquímica do ambiente celular. Efetores de Xanthomonas citri da família AvrBs3/PthAs são efetores que em especial modulam a expressão gênica do hospedeiro. Esses efetores ativadores de transcrição (transcription activator-like ou TAL) são compostos estruturalmente por: um domínio central de 34/35 resíduos de aminoácidos que se repetem em tandem sendo as repetições de número variável; domínios de localização nuclear (nuclear localization signals ou NLS) e de ativação transcricional (acidic transcription activator-like domain ou AAD). (Figura 2). Figura 2 - Esquematização de um efetor TAL. Estão representados os domínios internos repetitivos, o domínio rico em leucina (LRR), os sinalizadores nucleares (NLS) e o domínio ácido de ativação transcricional (AAD). Na porção N-terminal também é comum a existência de sinalizadores para o sistema secretório tipo III (TS3). Após sua translocação pelo T3S estes são endereçados ao núcleo após reconhecimento da região do NLS por uma α-importina, que com o apoio de uma βimportina promovem a importação do efetor para o núcleo. No núcleo esses efetores vão modular a expressão gênica do hospedeiro contribuindo para o desenvolvimento do cancro e suprimindo respostas de defesa basais da planta. Estudos já demonstraram que a expressão transiente de PthA (um efetor TAL de X. citri) em citros é suficiente para induzir hiperplasia e hipertrofia (KAY; BONAS, 2009; BOGDANOVE et al., 2010). O mecanismo molecular de ligação dos efetores TAL ao DNA foi elucidado e depende da participação dos domínios repetitivos de 33/34 aminoácidos, onde os 11 aminoácidos das posições 12/13 são resíduos variáveis (RAV) e há um código para o reconhecimento específico de uma sequência de nucleotídeos sendo cada diferente par de aminoácidos 12/13 reconhecedor de um nucleotídeo específico . Esses estudos possibilitaram predizer alvos de ligação dos efetores TAL através da análise dos RAVs contidos em suas regiões repetitivas (BOCH et al., 2009). X. aurantifolii apresentam efetores equivalentes aos PthAs de X.citri. Nosso grupo levantou possíveis genes de laranja alvos desses efetores TAL de X. aurantifolii, constatamos dentre estes alguns genes relacionados ao sistema de defesa. Sabendo que infecção de X. aurantifolii em laranja induz uma série de genes relacionados à resposta de defesa com pouco ou nenhum desenvolvimento de sintomas (CERNADAS et al., 2008) sugerimos a ocorrência de transativação de genes de defesa pelos efetores de X. aurantifolii. Esse trabalho busca avaliar os níveis transcricionais de alguns desses genes possivelmente transativados em plantas transformadas com os efetores TAL de X. aurantifolii. Esses estudos serão feitos por q-RT PCR. Fatores de transcrição do tipo WRKY Proteínas do tipo WRKY são fatores de transcrição bem distribuídos no Reino Vegetal. Sua estrutura é marcada por um domínio (WRKY - triptofano; arginina; lisina; tirosina) de aproximadamente 60 aminoácidos com atividade de ligação ao DNA e em especial uma sequência denominada W-BOX (C/T)TGAC(T/C). Para realizar essa ligação, o fator depende do motivo invariável WRKY e dos resíduos cisteína e histidina do domínio WRKY que participam da formação de um zinc finger característico (Figura 3) (ULKER; SOMSSICH, 2004; RUSHTON et al., 2010). Estudos evidenciaram a presença de W-BOXES (sítios de ligação dos fatores WRKY em DNA) nas regiões promotoras de clusters de genes expressos em condições de reação de defesa sistêmica, sugerindo participação desses fatores de transcrição nos processos de defesa das plantas. Recentemente alguns fatores 12 Figura 3 - Representação dos aminoácidos da porção N-terminal de um fator WRKY de Arabdopsis thaliana. Em negrito, está destacada a sequência WRKY bem conservada. Com asteriscos estão indicados os resíduos de cisteína e histidina que participam da formação do zinc finger (ULKER; SOMSSICH, 2004). WRKY foram associados a MAPK (Mitogen-activated protein kinases) cujas cascatas podem culminar na ativação da transcrição de fatores WRKY (OSORIO, 2010) (PANDEY; SOMSSICH, 2009). Além disso, a transcrição de genes WRKY é forte e rapidamente ativada pela ocorrência de feridas, infecção por patógenos e condições de estresse abiótico. Estudos demonstraram que a super expressão de fatores WRKY em Arabidopsis thaliana e Oryza sativa resultaram na indução de genes de defesa. Estes aparecem, portanto, como potenciais candidatos na produção de culturas com resistência aumentada a patógenos (LIU et al., 2007; HWANG, S.-HEE et al., 2011). Estratégias para obtenção de plantas resistentes ao cancro cítrico. Esse trabalho analisa plantas que foram transformadas com dois efetores TAL de X. aurantifolii separadamente. e um fator de transcrição WRKY endógeno, sempre As construções feitas colocam os genes sob controle de um promotor levantado pelo grupo que é sensível ao dano e à infecção com X. citri. As plantas sofreram transformação mediada por Agrobacterium. Sugerimos a transativação de genes de defesa pelos efetores TAL nas plantas transformadas com estes, podendo resultar em linhagens mais resistentes ao patógeno. Nas plantas transformadas com o fator WRKY sugerimos que a super expressão deste, pode conferir às linhagens um maior nível de resistência ao patógeno (PANDEY; SOMSSICH, 2009). A susceptibilidade das plantas transformadas foi avaliada por desafio das plantas com o patógeno. 13 2 OBJETIVOS - Verificar a expressão das proteínas de interesse em plantas transgênicas de citros transformadas com as construções para tal; - Correlacionar a expressão transgênica do fator de transcrição e dos efetores em estudo com o desenvolvimento do Cancro Cítrico; 3 MATERIAIS E MÉTODOS 3.1. Detecção de plantas geneticamente modificadas por PCR. Extração de DNA genômico Uma primeira extração de DNA genômico das plantas e reação subsequente de PCR foram realizadas com REDExtract-N-Amp™ Plant PCR Kit (Sigma Aldrich) seguindo as recomendações do fabricante e utilizando primers que amplificam uma parte (800bp) da região C-terminal de efetores TAL de Xanthomonas citri. Alternativamente, para extração de DNA genômico por metodologia convencional utilizando CTAB (Brometo de cetil trimetil amônio) como detergente, uma folha foi recolhida e congelada em nitrogênio líquido em tubo de 2 mL. O material foi macerado com bastão de vidro. Ao pó obtido foi adicionado Tampão de Extração (CTAB 0,8%; NaCl 800 mM; EDTA 22 mM; Tris-HCl pH 8,0 220 mM; βmercaptoetanol 0,2%) e solução 24:1 de clorofórmio : álcool isoamílico. As amostras foram vortexadas e incubadas a 55ºC por 10 minutos. A amostra foi centrifugada, o sobrenadante transferido e a ele adicionado isopropanol para precipitação do DNA. O pellet foi lavado com etanol 70%. O DNA foi ressuspendido em tampão TE (10 mM Tris, pH 7.5 – 8.0, 1 mM EDTA) (Sigma Aldrich). A suspensão foi tratada com RNAse Mix (Fermentas) seguindo as recomendações do fabricante. A qualidade da extração foi aferida por eletroforese em gel de agarose 1%. 14 Reação de PCR Protocolo 1: Utilização de DNA extraído por metodologia convencional (1µL), oligos de interesse que amplificam uma região de 800 bp dos efetores TAL e enzima DreamTaq Polimerase (Fermentas), seguindo as recomendações do fabricante. A temperatura de annealing foi 55ºC. Protocolo 2: Utilização de DNA extraído por metodologia convencional, tratado com RNAse Mix (Fermentas) (1µL), oligos de interesse que amplificam uma região de 800 bp dos efetores TAL e enzima Platinum™ Polimerase (Invitrogen),uma Hot Start, seguindo as recomendações do fabricante. A temperatura de annealing foi 55ºC. Protocolo 3: PCR de gradiente de temperatura nas condições do protocolo 2, variando apenas a enzima: TrueStart Hot Start Taq Polimerase (Fermentas). O DNA utilizado havia sido tratado com RNAse Mix (Fermentas) e as temperaturas de annealing testadas foram: 55ºC, 55.9ºC, 57ºC, 58.3ºC, 59.3ºC e 59.9ºC Protocolo Final: PCR utilizando 2µL de DNA extraído por metodologia convencional, tratado com RNAse Mix (Fermentas) , oligos de interesse que amplificam uma região de 800 bp dos efetores TAL e enzima TrueStart Hot Start Taq Polimerase (Fermentas) seguindo as recomendações do fabricante. A temperatura de annealing foi 60ºC. 3.2. Subclonagem, expressão e purificação do fator de transcrição do tipo WRKY. Subclonagem do gene de fator do tipo WRKY. A construção pGEM/WRKY (cedida pela pesquisadora Maria Luiza Oliveira) e o vetor de expressão pET28a (Novagen) foram digeridos com as enzimas de restrição (Fermentas) NcoI (CCATGG) e SacI (GAGCTC) e o produto da digestão avaliado por eletroforese em gel de agarose 1%. As bandas de interesse foram excisadas e purificadas a partir do gel com o kit QIAquick Gel Extraction (QIAGEN) seguindo as recomendações do fabricante. 15 Os produtos da purificação: vetor linearizado e região gênica codificante, foram postos à ligação nas proporções 1:3 e 1:5 na presença da enzima ligase (Fermentas) em reação de aproximadamente 14 horas mantida a 16ºC, seguindo as recomendações do fabricante. A ligação em vetor pET28a permitiu fusionamento da proteína de interesse à cauda 6xHis, permitindo posterior purificação por cromatografia de afinidade. O DNA ligado foi transformado por choque térmico em células de E.coli DH5α quimiocompetentes. A transformação se deu por incubação da reação em banho de gelo por meia hora, choque térmico de 1 minuto e 30 segundos em banho-maria a 42ºC seguido de 1 minuto em banho de gelo. Procedeu-se adição de meio LB (Triptona 1%; Extrato de Levedura 0,5%; NaCl 1%; pH 7,5) e incubação celular a 37ºC e 200 rpm para restabelecimento e divisão celular. As células foram plaqueadas em meio LB sólido suplementado com canamicina (25 µg. mL-1) e incubado a 37ºC por 18 horas. Foram picadas 13 colônias dentre as obtidas, fervidas em 40 µL de água tipo 01. Uma alíquota do fervido foi utilizada como template para PCR de colônia (DreamTaq Polimerase / Fermentas) utilizando os oligos do gene em estudo. Duas colônias “PCR positivas” foram incubadas overnight em 10 mL de meio LB a 37ºC e 200 rpm. Foi feita minipreparação de 3 mL de cultura, com o kit QIAprep Mini Prep Kit (QIAGEN), seguindo as recomendações do fabricante, para isolamento da construção plasmidial de interesse. A construção pET28a/WRKY foi transformada por choque térmico em células de E. coli BL21(DE3) quimiocompetentes. O produto de transformação foi plaqueado em meio LB suplementado com canamicina (25 µg. mL-1) e incubado a 37ºC por 18 horas. Uma colônia crescida na placa foi picada e incubada overnight em 5 mL de meio LB suplementado com canamicina (25 µg. mL-1) a 37ºC e 200 rpm. Expressão e purificação da proteína WRKY. Um pré-inóculo foi diluído em 0,5 L de meio LB também suplementado com canamicina (25 µg. mL-1) e incubado a 37ºC até que a O.D. 600 (optical density) da cultura a 600 nm atingisse 0.9. A cultura foi induzida com 0,4 mM de IPTG (Isopropyl β-D-1-thiogalactopyranoside) e incubada por 4 horas a 30ºC sob agitação de 200 rpm. A cultura foi pelletada em centrífuga refrigerada. Alíquotas da cultura foram 16 feitas antes e ao fim da indução para posterior análise por SDS PAGE (sodium dodecyl sulfate polyacrylamide gel electrophoresis) (LAEMMLI, 1970). Uma alíquota do pellet obtido foi ressuspendido em Tampão A ( 20 mM TrisHCl pH 8.0; 5 mM Imidazol; 200 mM NaCl; 1 mM PMSF; Glicerol 2%). O conteúdo foi tratado com lisozima e sonicado em banho de gelo com intensidade de 24% e pulsos curtos. A amostra foi centrifugada por uma hora a 4ºC para obtenção do sobrenadante. Alíquotas das fases foram feitas para posterior análise. A purificação do sobrenadante por cromatografia de afinidade foi feita em resina TALON® Metal Affinity Resin (Clontech). A coluna foi equilibrada com 15 volumes Tampão A, o sobrenadante foi aplicado na coluna e esta foi lavada com 15 volumes de Tampão B (20 mM Tris-HCl pH 8.0; 200 mM NaCl; 1 mM PMSF; Glicerol 2%). A eluição foi realizada com 2 volumes de Tampão C (20 mM Tris-HCl pH 8.0; 250 mM Imidazol; 200 mM NaCl; 1 mM PMSF; Glicerol 2%). Alíquotas de expressão e purificação da proteína WRKY foram analisadas em SDS PAGE 13%. (LAEMMLI, 1970). 3.3. Análise da expressão dos transgenes. Extração das proteínas totais de tecido vegetal A extração de proteínas totais se deu em 03 condições diferentes: 1) a partir de 04 discos de folha de diâmetro 6.5 mm; 2) a partir de 06 discos de folha de 6.5 mm de folha “machucada”; 3) A partir da folha inteira. As folhas retiradas das plantas foram postas em tubos de 2 mL, que foram mantidos em gelo até o momento da extração. Foi escolhida dentre as 03 condições já citadas a mais adequada para cada construção e o material foi macerado em cadinho embebido em água tipo 01, procedeu-se a adição de 400 µL de SDS PAGE Sample Buffer 2X (200 mM β Mercaptoetanol; SDS 4% (p/v); Azul de bromofenol 0,2% (p/v); Glicerol 20% (v/v); 100 mM Tris HCl pH 6.8) (SAMBROOK & RUSSELL,2001 ) A extração foi verificada por SDS PAGE 10% e 13% (LAEMMLI, 1970) . 17 Imunodetecção por Western Blot As proteínas totais foram separadas por SDS PAGE (LAEMMLI, 1970) utilizando géis 10% e 13% em corrida de aproximadamente 1 hora sob corrente constante de 15 mA por gel. A transferência destas para membrana de PVDF (Millipore) foi realizada em tampão de transferência gelado (Tris 48mM; Glicina 39 mM; SDS 0,0037%; Metanol 20%) sob corrente constante de 350 mA por 1 hora e 15 minutos. A membrana foi bloqueada à temperatura ambiente por uma hora e meia sob agitação com solução TBS-T (20 mM Tris-HCl; 150mM NaCl; 0,05% Tween20, pH 7,5) + 5% (p/v) de leite em pó desnatado. Em seguida a membrana foi incubada sob agitação, por toda a noite a 4ºC, com solução TBS-T pH 7,5 + 5% leite em pó desnatado contendo o anticorpo primário na titulação mais conveniente. No dia seguinte foram feitas 03 lavagens sob agitação, de 10 minutos cada, com 15 mL de TBS-T. Incubou-se a membrana, sob agitação e a temperatura ambiente, com solução TBS-T + 5% de leite desnatado em pó com anticorpo secundário Anti-Rabbit (GE-Health Care) também na titulação desejada (geralmente 1:3000). Foram repetidas as 03 lavagens com TBS-T, como descrito anteriormente. A detecção foi feita por quimiluminescência com o kit ImmunoCruz™: Western Blotting Luminol Reagent (Santa Cruz Biotechnology) em filme de alta performance Amersham Hyperfilm™ ECL (GE Health Care), sempre seguindo as recomendações dos fabricantes. (MACPHEE, 2010) Stripping de membrana Algumas membranas de PVDF foram recuperadas com Stripping Buffer (100mM β-mercaptoetanol ; 62,5 mM Tris-HCl pH 6.7; SDS 2%), onde 50 mL do tampão foram incubadas com a membrana a 60ºC sob agitação. Seguiram-se 03 lavagens sob agitação, de 10 minutos cada, com 15 mL de TBS-T (20 mM Tris-HCl; 150mM NaCl; 0,05% Tween20, pH 7,5) + 5% (p/v) de leite em pó desnatado. Após o procedimento repetiram-se os passos do Western Blot partindo do bloqueio da membrana. 18 3.4. Avaliação dos níveis transcricionais de genes de interesse Desenho de oligonucleotídeos para reação de qRT-PCR Oligonucleotídeos correspondentes a vários genes de citros, identificados como alvos diretos de efetores TAL de Xanthomonas aurantifolii foram desenhados utilizando o software Primer Express 3.0 (Life Technologies). Extração de RNA de tecido vegetal e síntese de cDNA Uma folha jovem foi congelada e macerada em nitrogênio líquido utilizando cadinho previamente incubado com água oxigenada. Ao pó claro obtido foi adicionado reagente TRIzol® (Invitrogen) e o conteúdo incubado a temperatura ambiente e vortexado. Adicionou-se clorofórmio. Foi realizada centrifugação refrigerada e a fase aquosa obtida, contendo RNA, foi recuperada. Adicionou-se a essa 2-propanol e o conteúdo foi centrifugado a 4ºC para precipitação do RNA. O pellet foi lavado com Etanol 75% gelado e centrifugado. Esperou-se até a secagem do pellet para posterior ressuspensão em água DEPC (Diethylpyrocarbonate) 0,1%. Para atestar a qualidade da extração e a integridade do material extraído, foi realizada eletroforese em gel de agarose desnaturante. O gel foi preparado por fundição da agarose em água e posterior adição de tampão MOPS (200 mM MOPS; 60 mM Acetato de Sódio; 10 mM EDTA; pH 7.0) A qualidade do RNA extraído foi aferida por eletroforese em gel de agarose 1% desnaturante, com MOPS 1X (MOPS 20 mM; Acetato de Sódio 5 mM; EDTA 1 mM pH 7.0 em água DEPC 0,1%) e formaldeído 5%. O RNA foi quantificado em espectrofotômetro (SAMBROOK & RUSSELL,2001 ) por medida da absorbância da amostra, diluída em água DEPC 0,1%, nos comprimentos de onda 260 e 280 nm. Foi utilizada cubeta UVette® (Eppendorf) RNA free. Síntese de cDNA. O RNA quantificado foi tratado com DNAse I (Fermentas) seguindo as recomendações do fabricante e em seguida foi realizada síntese de fita simples de cDNA utilizando The Maxima® First Strand cDNA Synthesis Kit (Fermentas) partindo de aproximadamente 2,5 µg de RNA total. 19 qRT – PCR e análise dos dados. A reação de qRT – PCR foi realizada em plataforma 7500 Real-Time PCR System (Applied Biosystems) utilizando diluições específicas do cDNA produzido para avaliar a quantidade necessária para detecção dos transcritos. O qRT – PCR foi feito com Maxima® SYBR Green/Fluorescein qPCR Master Mix (2X) (Fermentas) com adição do cDNA de interesse e dos primers para cada gene analisado mais dois genes endógenos de controle em concentração final aproximada de 0,3 µM, seguindo as recomendações do fabricante. 3.5. Desafio das plantas com Xanthomonas citri e avaliação fenotípica. Cultura permanente de Xanthomonas citri 306 foi plaqueada em meio LB sem sal (Triptona 1%; Extrato de Levedura 0,5%; Ágar 1,5%) suplementado com Ampicilina (25 µg.mL-1) e incubada a 30ºC por 48 horas. Para desafio das plantas foi preparada solução aquosa de Xanthomonas citri 306 de O.D600 = 0.28, o que corresponde a aproximadamente 2.105 UFC/mL . Na infiltração foram injetados entre 20 e 50 µL de solução bacteriana em folhas jovens e maduras das plantas envolvidas no projeto. Diluições da solução utilizada foram plaqueadas e incubadas para contagem celular e avaliação das bactérias inoculadas. O desenvolvimento dos sintomas foi acompanhado com o tempo. A cepa de X. citri utilizada também foi plaqueada em meio LB sem sal suplementado com o inseticida Decis 25 EC 0,1% (Bayer Environmental Science) para avaliar o efeito deste no desenvolvimento da bactéria, em vista da utilização do mesmo na manutenção dos insetos no ambiente das plantas. O desenvolvimento dos sintomas foi acompanhado por fotos a partir do décimo dia pós-inoculação. Quando de quinze dias do desafio das plantas com Xanthomonas as folhas foram recolhidas e fotos das lesões foram tiradas em lupa com magnitudes de 10X e 20X de ampliação. 20 4 RESULTADOS E DISCUSSÃO 4.1. Detecção de plantas geneticamente modificadas por PCR. Extração de DNA genômico A extração de DNA genômico de folhas por metodologia convencional, utilizando CTAB como detergente, foi bem sucedida (Figura 4A) e permite visualização de bandas superiores e majoritárias, que correspondem ao DNA genômico extraído. Alguns rastros também são perceptíveis e indicam contaminações com RNA. O tratamento das extrações com RNAse Mix (Figura 4B) (Fermentas) limpou os rastros e melhorou a condição do material para PCR. Figura 4A – Eletroforese em gel de agarose 1% de extrações de DNA por metodologia convencional (CTAB). As amostras 1-28 correspondem à extração de DNA genômico de plantas possivelmente transformadas com efetores TAL de Xanthomonas aurantifolii. 4B -Eletroforese em gel de agarose 1% de extrações de DNA por metodologia convencional tratadas com RNAse Mix (Fermentas) – 1-14: Amostras de DNA genômico (4A) pós tratamento com RNAse Mix (Fermentas). M: MassRuller™ DNA Ladder Mix (Fermentas). Tentativas de extração de DNA genômico e amplificação, com o REDExtractN-Amp™ Plant PCR Kit não foram bem sucedidas. Análise por eletroforese em gel de agarose 1% evidenciou baixa ou não extração de DNA com o kit. O produto do PCR obtido com o kit também foi avaliado por eletroforese em gel de agarose 1% e não apresentou amplificado. Reação de PCR 21 Eletroforese em gel de agarose 1% do primeiro protocolo de reação PCR (Figura 5) apresentou muitos amplicons inespecíficos, não permitindo detecção dos efetores de forma eficiente. Supondo influência da contaminação com RNA, o DNA extraído por metodologia convencional foi tratado com RNAse MIX (Fermentas). A seta (Figura 5) indica amplificado de 800 bp, como esperado, no controle positivo. Figura 5 - Eletroforese em gel de agarose 1% de reação de PCR para detectar plantas transformadas com efetores TAL. M: MassRuller™ DNA Ladder Mix (Fermentas). 1-27: plantas testadas. C-: plantas controle não transformadas. C+: PthA clonado em vetor pET (controle positivo). Eletroforese em gel de agarose 1% do produto de PCR do segundo protocolo (Figura 6) apresentou diminuição das amplificações inespecíficas, mas estas ainda atrapalhavam a identificação de plantas transformadas com os efetores TAL. 22 Figura 6- Eletroforese em gel de agarose 1% de reação de PCR para detectar plantas transformadas com efetores TAL/ Platinum Taq Polimerase (Invitrogen) e DNA tratado com RNAse. M: MassRuller™ DNA Ladder Mix (Fermentas). 1-12: plantas testadas. C-: plantas controle não transformadas. C+: PthA clonado em vetor pET (controle positivo). O protocolo de PCR com gradiente de temperatura (Figura 7) indicou 59.9ºC/60ºC como a melhor temperatura de annealing para o protocolo em questão porque minimizou as amplificações inespecíficas no controle negativo (1) e permitiu amplificação notável na planta positiva (3) e no controle positivo (2). Figura 7 - Eletroforese em gel de agarose 1% de reação de PCR de gradiente de temperatura para otimizar a reação para amplificação dos efetores TAL em plantas transformadas. M: MassRuller™ DNA Ladder Mix (Fermentas). 1: planta controle não transformada 2: PthA clonado em vetor pET (controle positivo). 3: planta transformada identificada como possível PCR positiva em análise anterior. A temperatura de annealing utilizado para cada reação está indicada acima das canaletas. O protocolo de PCR final, congregando as otimizações, praticamente eliminou as amplificações inespecíficas e possibilitou identificar como positivas (transformadas) as plantas 11, 16, 17,22 e 24. (Figura 8). Infelizmente algumas das plantas PCR positivas estavam pequenas impossibilitando desafio com X. citri. 23 Figura 8 – Eletroforese em gel de agarose 1% de PCR para identificação de plantas transformadas com efetores TAL nas condições otimizadas M: MassRuller™ DNA Mix Ladder (Fermentas). C-: Plantas não transformadas (controles negativos) . 1-26: Plantas testadas. C+: PthA clonado em vetor pET (controle positivo). 4.2. Subclonagem, expressão e purificação da proteína WRKY. Subclonagem do gene de WRKY. Visando obter controle positivo para procedimentos de Western Blot, o gene WRKY foi subclonado e expresso. A construção inicial pGEM/WRKY e o vetor pET28a foram digeridos com sucesso pelas enzimas NcoI e SacI (Figura 9). A banda única em 1 apresenta o vetor pET28a linearizado. A banda em destaque em 2 mostra o inserto livre do vetor de propagação. Figura 9 - Eletroforese em gel de agarose 1% de digestões preliminares para subclonagem. M: MassRuller™ DNA Mix Ladder (Fermentas). 1: Vetor pET28a digerido com as enzimas NcoI e SacI (5260 bp). 2: Construção pET28a/WRKY digerida com as enzimas NcoI e SacI. O fragmento de interesse está em destaque (1kB). 24 A transformação da ligação em E. coli submetidas a PCR de colônia (Figura 10) DH5α gerou colônias que foram que resultou em amplificação do fragmento de interesse (1 kB) em quase todas as colônias. A amplificação no controle positivo está indicada pela seta (Figura 10) Figura 10 - Eletroforese em gel de agarose 1% de PCR de colônias de E.Coli DH5α transformadas com a construção pET28a/WRKY. M: MassRuller™ DNA Mix Ladder (Fermentas). 1-12 : PCR de colônias (para amplificação do gene WRKY : 1kB) de E.Coli DH5α crescidas em LB Canamicina após transformação química com a construção pET28a/WRKY. C+: Construção pGEM/WRKY (controle positivo). Expressão e purificação da proteína WRKY Células de E. Coli BL21 (DE3) transformadas e crescidas foram préinoculadas, diluídas no dia seguinte e induzidas. A cultura induzida por IPTG e purificação da proteína WRKY em E. Coli BL21 (DE3) foram avaliadas em SDSPAGE 13% (LAEMMLI, 1970) (Figura 11) que evidencia os maiores níveis de proteína 4 horas após a indução (canaleta 2) e ainda mostra a indução da expressão da proteína de interesse clonada em vetor pET28a sob controle do promotor T7. A figura 11 também relata a prevalência da proteína de interesse na fração insolúvel após sonicação (canaleta 3). Apesar disto, procedeu-se com a purificação em coluna de gravidade com 0,5 mL de resina. A eluição com imidazol (canaleta 7) não tem banda aparente no gel de SDS PAGE 13%, contudo, analises posteriores de Western Blot detectaram a proteína nessa fração. 25 Figura 11 - Análise da expressão e purificação da proteína WRKY em E. Coli BL21 (DE3) por SDS-PAGE 13%. MM: Marcador de peso molecular Unstained Molecular Weight Marker (Fermentas). 1. Amostra de extrato celular da cultura não induzida (T 0) . 2. Amostra de extrato celular de cultura 4 horas após a indução (T4). 3. Fração insolúvel. 4. Fração solúvel. 5. Lavagem da coluna de purificação. 6. Flow da coluna de purificação 7. Eluição com Imidazol 250 mM. Experimentos de otimização da expressão e purificação da proteína podem ser realizados futuramente para estudos estruturais. 4.3. Análise da expressão dos transgenes. Extração das proteínas totais de tecido vegetal Os melhores protocolos de extração de proteínas totais foram aqueles que forneceram maior quantidade de material biológico, isto é, aquele que utilizava a folha inteira como material. Contudo, blots que detectaram super expressão foram feitos com extração de 5 discos de folha. A figura 12 mostra géis SDS PAGE de extrações em diferentes condições onde é possível perceber a diferença de quantidade proteica. A qualidade da extração geralmente foi associada à identificação qualitativa da banda correspondente à enzima Rubisco, abundante em plantas e que se apresenta de forma marcante na separação de proteínas totais de plantas em eletroforese em gel de poliacrilamida. 26 Figura 12 – Análise da extração de proteínas totais de folhas por SDS-PAGE 10% e 13%. Imunodetecção por Western Blot A detecção por Western Blot passou por adequações de protocolo até detecção das proteínas de interesse nas plantas transformadas. A figura 13 mostra blot onde a titulação do anticorpo e a quantidade de proteínas totais não foram suficientes para a detecção, sendo notável apenas as proteínas recombinantes utilizadas como controle positivo. Em 13A e 13 B vemos um PthA recombinante detectado. Em 13C e 13D visualizamos a deteccção da WRKY recombinante produzida. Para estes casos foram utilizadas titulações 1:3000 e 1:1000 de anticorpos primários. Figura 13 – Western Blot das proteínas de interesse em plantas transformadas. A e B: Tentativa de detecção de efetores TAL em plantas transformadas. C e D: Tentativa de detecção do fator WRKY em plantas transformadas. 27 Como alternativa, utilizamos para as duas vertentes de detecção uma titulação de 1:500 de anticorpo primário correspondente. Foi possível detecção das proteínas de interesse, mas notou-se background alto quando do uso de algumas alíquotas de anticorpo anti-PthA (utilizado para detectar os efetores TAL). Buscando amenizar o background testamos alíquotas diferentes do anticorpo na detecção de proteína recombinante. A figura 14 mostra 3 alíquotas de anticorpo diferentes detectando PthA recombinante. As três alíquotas foram classificadas como satisfatórias. Uma dessas alíquotas foi aplicada na tentativa de detecção dos efetores em plantas transformadas, contudo não alcançamos detecção satisfatória. Figura 14 – Western Blot para avaliação de alíquotas de anticorpo anti-PthA disponíveis. 1,2,3: PthA recombinante detectado com diferentes alíquotas (1,2, e 3) de anticorpo anti PthA. Testamos o anticorpo anti-WRKY disponível detectando a proteína recombinante na fração insolúvel, além de 4 diluições seriadas de 10x desta fração para aferir a amplitude de detecção. Foram também postas a detecção alíquotas do Flow e da eluição, como mostra a figura 15. Visualizamos a banda majoritária de aproximadamente 37,5 kDa, correspondente a proteína WRKY fusionada a cauda 6x His Tag na eluição e em outras canaletas, atestando a qualidade do anticorpo. Partindo para a detecção das proteínas em plantas transformadas com o fator Figura 15 – Western Blot para teste de detecção de anticorpo anti-WRKY. P: amostra da fração insolúvel obtida no ensaio de expressão. D1,D2,D3 e D4: diluições seriadas (10x) da fração insolúvel obtida no ensaio de expressão. FT: flow through . EL: Eluição da proteína recombinante. 28 WRKY temos na figura 16 um Western Blot onde nota-se que os níveis da proteína nas plantas testadas chegam a ser levemente menores que o controle. É importante notar que a quantidade de proteína no controle é maior que nas canaletas das plantas testadas, como mostra o gel blotado (16D). A figura 16C mostra a aparência da lesão nas folhas das respectivas plantas transgênicas expressando o fator WRKY 16 dias após o desafio, apresentando menor desenvolvimento dos sintomas, apesar da pouca quantidade da proteína quando comparado ao controle representado em 16B. Sugerimos aqui um retardamento no desenvolvimento do cancro por decorrência da super expressão do fator WRKY. Cabe ainda a repetição dos experimentos para a confirmação dos resultados. Figura 16 - Correlação entre Western Blot de plantas transformadas com fator WRKY e fenótipo das plantas desafiadas com X. citri A: Western Blot de plantas transformadas com a construção WRKY. C-: controle negativo (planta não trasnformada) WRKY: WRKY recombinante fusionado a 6xHis Tag (~36 kDa); 1-6: plantas transformadas com WRKY. B-C: Lesões características de cancro cítrico ( 10 x ampliadas) após 16 dias da inoculação com X. citri. B: planta controle; C: planta 02 D: Gel SDS PAGE 13% idêntico ao blotado para o Western representado em A. A Figura 17 mostra outro Western Blot para detecção de fator WRKY em plantas controle e transformadas. Em particular, as plantas transgênicas de 3 a 5 mostram aumento dos níveis de proteína de WRKY em relação aos controles, sugerindo que eles estão, de fato, super expressando a WRKY. Curiosamente, é 29 possível correlacionar os níveis mais elevados de expressão nas plantas WRKY 3, 4 e 5 com uma redução no desenvolvimento do cancro em relação ao controle (17B), como indicado na Figura 17C, D e E, respectivamente. Sugerimos que esses níveis proteicos correspondem a super expressão e esta contribuiu para menor desenvolvimento dos sintomas. Figura 17 – Correlação entre Western Blot de plantas transformadas com fator WRKY e fenótipo das plantas desafiadas com X. citri A: Western Blot de plantas transformadas com a construção WRKY. C e C’: controles negativos (plantas não transformadas) WRKY: WRKY recombinante fusionado a 6xHis Tag (~36 kDa); 1-6: plantas transformadas com WRKY. B-E: Lesões características de cancro cítrico (10 x ampliadas) após 16 dias da inoculação com X. citri. B: planta controle; C: planta 3; D: planta 4; E: planta 5. F: Gel SDS PAGE 13% idêntico ao blotado para o Western representado em A. 4.4. Avaliação dos níveis transcricionais de genes de interesse Extração de RNA de tecido vegetal e síntese de cDNA As extrações de RNA foram realizadas com sucesso (Figura 18), fato evidenciado pelas bandas ribossomais e a ausência de rastros que indicariam degradação do material. As amostras foram quantificadas por espectrofotometria e estão em concentração de aproximadamente 2,5 µg/µL. A razão entre as absorbâncias em 260nm e 280nm é de aproximadamente 1.55. 30 O cDNA foi sintetizado e um experimento preliminar de qRT-PCR foi realizado na tentativa de analisar os níveis transcricionais de genes tidos como alvos moleculares do efetores transformados. Figura 18 – Eletroforese de RNA em gel de agarose 1% desnaturante. 1: RNA de concentração conhecida (7µg/µL). 2-5: Extração de RNA das amostras de interesse. 5 CONCLUSÃO E PERSPECTIVAS Nossos resultados mostraram que a proposta de super expressão de um fator WRKY visando resistência ao cancro cítrico pode ser interessante, com base no observado em plantas com maiores níveis dessa proteína, onde houve menor desenvolvimento dos sintomas do cancro. Cabem estudos moleculares mais intensos para validar a proposta. Sobre as plantas transformadas com os efetores TAL, o trabalho permitiu consolidar alguns procedimentos da análise que facilitarão estudos mais avançados das características dessas plantas transgênicas. A análise da influência da expressão desses transgenes nos níveis transcricionais de genes de defesa de citros como alvos de desses efetores é uma perspectiva do trabalho. A continuação das análises será possível após crescimento das plantas utilizadas, o que vai facilitar os trabalhos pela maior disponibilidade de material vegetal. 31 6 REFERÊNCIAS BIBLIOGRÁFICAS AMARAL, A. M. DO. Cancro Cítrico: permanente preocupação da citricultura no Brasil e no mundo. Comunicados Técnicos, 2003. Brasília - DF: Embrapa. BOCH, J.; SCHOLZE, H.; SCHORNACK, S. et al. Breaking the code of DNA binding specificity of TAL-type III effectors. Science, v. 326, n. 5959, p. 1509-12, 2009. BOGDANOVE, A. J.; SCHORNACK, S.; LAHAYE, T. TAL effectors : finding plant genes for disease and defense. Current Opinion in Plant Biology, v. 13, n. 4, p. 394-401, 2010. BRUNINGS, A. M.; GABRIEL, D. W. Xanthomonas citri: breaking the surface. Molecular Plant Pathology, v. 4, p. 141-157, 2003. CERNADAS, R. A.; CAMILLO, L. RODRIGUES; BENEDETTI, C. E. Transcriptional analysis of the sweet orange interaction with the citrus canker pathogens Xanthomonas axonopodis pv. citri and Xanthomonas axonopodis pv. aurantifolii. Molecular Plant Pathology, 2008. DOMINGUES, M. N. Caracterização de proteínas de Citrus sinensis que interagem com a proteína efetora PthA, indutora do cancro cítrico, 2011. UNICAMP. FEBRES, V. J.; KHALAF, A.; GMITTER, F. G.; GLORIA, J. Production of Disease Resistance in Citrus by Understanding Natural Defense Pathways and Pathogen Interactions. Molecular and Cellular Biology, 2009. HWANG, S.-HEE; WON, S.; HWANG, D.-JU. Plant Science Heterologous expression of OsWRKY6 gene in Arabidopsis activates the expression of defense related genes and enhances resistance to pathogens. Plant Science, v. 181, n. 3, p. 316-323, 2011. JONES, J. D. G.; DANGL, J. L. The plant immune system. Nature, v. 444, n. 7117, p. 323-9, 2006. 32 JOSEPH SAMBROOK; DAVID. W. RUSSELL. Molecular Cloning: A Laboratory Manual. 3rd ed.. New York: Cold Spring Harbor Lab Press, 2001. KAY, S.; BONAS, U. How Xanthomonas type III effectors manipulate the host plant. Current Opinion in Microbiology, p. 1-7, 2009. LAEMMLI, U. K. Cleavage of Structural Proteins during the Assembly of the Head of Bacteriophage T4. Nature, v. 227, p. 680-85, 1970. LIU, X.; BAI, X.; WANG, X.; CHU, C. OsWRKY71 , a rice transcription factor , is involved in rice defense response. , v. 164, 2007. MACPHEE, D. J. Methodological considerations for improving Western blot analysis. Journal of pharmacological and toxicological methods, v. 61, n. 2, p. 171-7, 2010. NEVES, M. F.; TROMBIN, V. G.; MILAN, P. et al. O retrato da citricultura brasileira. 1st ed. Ribeirão Preto: Markestrat - CitrusBR, 2009. OSORIO, M. B. Análise funcional de genes que codificam proteínas WRKY, responsivos ao ataque do fungo Phakopsora pachyrhizi Sydow, agente causador da ferrugem asiática em soja [Glycine max (L.) Merrill], 2010. UFRGS. PANDEY, S. P.; SOMSSICH, I. E. The role of WRKY transcription factors in plant immunity. Plant physiology, v. 150, n. 4, p. 1648-55, 2009. RUSHTON, P. J.; SOMSSICH, I. E.; RINGLER, P.; SHEN, Q. J. WRKY transcription factors. Trends in Plant Science, v. 15, n. 5, p. 247-258, 2010. ULKER, B.; SOMSSICH, I. E. WRKY transcription factors: from DNA binding towards biological function. Current opinion in plant biology, v. 7, n. 5, p. 491-8, 2004.
Download