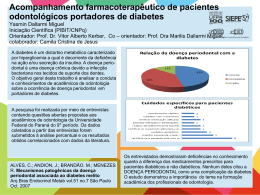
R. Periodontia - Setembro 2008 - Volume 18 - Número 03 PRODUTOS FINAIS DE GLICOSILAÇÃO AVANÇADA (AGE) E A EXACERBAÇÃO DA DOENÇA PERIODONTAL EM DIABÉTICOS – REVISÃO DE LITERATURA Advanced glycation end products (AGE) and the exacerbation of periodontal disease in diabetics patients - Review Warley David Kerbauy1, Fernando Reno de Lima1, Fernando Augusto Perrella2, José Benedito Oliveira Amorim3 RESUMO Os estudos sobre a patogênese das complicações do diabete têm se direcionado a investigar o papel de compostos biologicamente ativos formados através de ligação da glicose com proteínas ou lipídios, conhecido como AGEs (produtos finais de glicosilação avançada) e a interação com receptores específicos na superfície de membrana celulares (RAGE). Esses compostos e seus receptores estão drasticamente aumentados em indivíduos diabéticos e possuem um papel biopatológico extremamente importante no desenvolvimento e na exacerbação das complicações diabéticas. Sendo o diabete uma condição sistêmica considerada um fator de risco na prevalência e severidade da doença periodontal, faz-se necessário entender os mecanismos dessa interação entre essas doenças e as possíveis alternativas de tratamento. O objetivo desse trabalho é esclarecer o mecanismo de formação de AGEs, bem como suas implicações no processo inflamatório, inclusive na patogenia da doença periodontal e enfatizar as pesquisas que visam interferir na formação ou interação dessas moléculas, a fim de minimizarmos os efeitos da condição sistêmica dos diabéticos. UNITERMOS: Diabete melito, periodontite, complicação diabética, fator de risco, produtos finais de glicosilação. R Periodontia 2008; 18:20-27. Recebimento: 23/11/07 - Correção: 04/03/08 - Aceite: 26/06/08 20 INTRODUÇÃO O diabetes mellitus ou diabete melito (DM) é uma doença crônica evolutiva que se caracteriza pelas alterações dos metabolismos de carboidratos, gorduras e proteínas devido à falta de insulina ou de sua capacidade de agir na transferência de glicose do plasma para o citoplasma das células. Atinge aproximadamente 5% da população mundial (THE EXPERT COMMITTEE ON THE DIAGNOSIS AND CLASSIFICATION OF DIABETES MELLITUS, 2002) e, em 1980, segundo dados do Ministério da Saúde, a sua prevalência no Brasil era de 7,6% (MALERBI & FRANCO, 1992), porém, dados internacionais sobre a projeção dessa doença no século XXI revelam quadro alarmante (ZIMMET, 2003). Atualmente, o DM está classificado, de acordo com a American Diabetes Association (ADA), 1997, em dois tipos principais, o tipo 1 e o 2, além do gestacional e tipos específicos (THE EXPERT COMMITTEE ON THE DIAGNOSIS AND CLASSIFICATION OF DIABETES MELLITUS, 2002). O DM tipo 1 ocorre geralmente nas crianças e jovens e se caracteriza pela absoluta falta de insulina, em geral decorrente de destruição das células beta (tipo 1 a), havendo necessidade de sua reposição nesses pacientes. O tipo 2, previamente conhecido como R. Periodontia - 18(3):20-27 não-insulino dependente, corresponde a aproximadamente 85% dos casos e caracteriza-se como uma doença poligênica, além de estar relacionada com o moderno estilo de vida, em que a obesidade constitui um dos principais fatores de risco. O DM gestacional é caracterizado pelo seu aparecimento durante a gravidez e após o parto requer reclassificação. Outros tipos específicos de DM são raros e de naturezas variadas (ZAMBON et al., 1988). O resultado dessas alterações metabólicas do diabete se define como uma elevação crônica da glicose no sangue (hiperglicemia) e está associada à disfunção em longo prazo e danos em vários órgãos, especialmente rins, olhos, coração, nervos e vasos sangüíneos (MEALEY, 2000). Está bem estabelecido que o diabete é um fator de risco para o desenvolvimento de doença periodontal em humanos. Estudos em grandes populações, como as realizadas na comunidade indígena Pima do Arizona, onde há a maior prevalência de diabete tipo 2 do mundo, foram claros ao demonstrar que pacientes diabéticos apresentavam maior perda de inserção e perda óssea alveolar quando comparados aos controles não-diabéticos em todas as idades (EMRICH et al., 1991; SHLOSSMAN et al., 1990). PAPAPANOU, 1996, através de meta-análise que incluiu um total de 3.524 adultos com mais de 18 anos de idade, chegou a conclusão que havia associação significativa entre as doenças, sendo que o diabete pode influenciar não apenas a prevalência e a gravidade da periodontite, como também o progresso da doença. A doença periodontal é caracterizada pela perda de tecido conjuntivo ao redor dos dentes e atualmente é considerada multifatorial. Embora esteja amplamente comprovado que o agente causador é o biofilme bacteriano e seus subprodutos, está muito claro que a resposta imunoinflamatória do hospedeiro é de fundamental importância para a progressão da doença. Não havendo diferenças entre a composição do biofilme bacteriano entre pacientes diabéticos e não diabéticos (SASTRAWIJOTO et al., 1989; ZAMBOM et al., 1988), o mecanismo pelo qual pacientes diabéticos apresentam maiores índices de perda de inserção e perda óssea resume-se à resposta do hospedeiro. Desta maneira, a doença periodontal é similar às clássicas complicações do diabete. Estudos que objetivam entender os mecanismos de interação do diabete com suas complicações têm se voltado aos AGEs (Produtos finais de glicosilação avançada), que compreendem vários compostos biologicamente ativos resultantes da ligação não enzimática entre carboidratos e proteínas, carboidratos e lipídeos, de forma irreversível, intimamente relacionada com a hiperglicemia e que se depositam no plasma e nos tecidos dos indivíduos, inclusive no tecido gengival (GROSSI & GENCO, 1998). A interação entre os AGEs e seus receptores (RAGE) na superfície de determinadas células parece ser um dos maiores responsáveis pelas complicações do diabete, tanto nas macrovasculares, como a aterosclerose e acidentes cardiovasculares e cerebrovasculares prematuros, como nas microvasculares, como a retinopatia e a insuficiência renal. Várias células já mostraram apresentar esses receptores em suas superfícies, como as células endoteliais, macrófagos e fibroblastos, e cada tipo celular apresenta uma resposta diferente, mas todas alteram a resposta inflamatória e cicatricial normal do hospedeiro (PEPPA & VLASSALA, 2005). Uma vez que o DM é um fator de risco para as doenças periodontais e estas para a saúde global do indivíduo, nesta revisão procuramos esclarecer o processo de formação dos AGEs e sua interação com seus receptores (RAGE) nas superfícies das membranas celulares, bem como suas conseqüências no periodonto e os novos rumos das pesquisas nessa área, já que muitos resultados parecem promissores. Mecanismo de formação e implicações biológicas dos AGEs No último século, acreditava-se que não havia relação causal entre a hiperglicemia e as complicações do diabete. Entretanto, nas últimas três décadas, estudos epidemiológicos em modelos animais e estudos bioquímicos sugeriram fortemente que essa relação existe (BROWNLEE & CERAMI, 1981; GROOP et al., 2005; TANGI et al., 2000). Embora saiba-se que o grau de hiperglicemia está diretamente correlacionado com a extensão das complicações do diabete, os estudos estão apenas no início da compreensão dos mecanismos desses processos. Atualmente, porém, muitos autores já afirmam que os produtos finais de glicosilação avançada (AGEs) têm o papel principal na patogênese das complicações do diabete. A formação dos AGEs inicia-se com a ligação nãoenzimática da glicose com o grupo amina das proteínas e formam uma base Schiff instável. Através de um processo bioquímico lento, estes produtos são convertidos em glicoseproteína aduzida estável, mas, ainda sim reversível, conhecido como Amadori product. Um exemplo é a conhecida Hemoglobina glicosilada (Hbc) utilizada na mensuração da glicose. Nesse estágio, se houver uma diminuição dos níveis glicêmicos, o processo pode ser interrompido e não há a formação de AGEs; entretanto, na manutenção da hiperglicemia, os Amadori products tornam-se altamente estáveis e formam AGEs (MEALEY, 2000). (Fig 1) 21 R. Periodontia - 18(3):20-27 Glicose + proteína Base Schiff Tabela 1 PROPRIEDADES QUÍMICAS PATOLOGICAMENTE RELEVANTES DOS AGES (proteína glicada) (VLASSARA, 1997) A formação de AGEs ocorre em proteínas, lipídeos e ácidos nucléicos AGEs (Produtos finais de glicosilação avançada) A formação de AGEs com proteínas confere uma alta resistência a digestão proteolítica xx Amadori product Fig.1. Formação dos AGEs. A glicose liga-se à parte final do radical amino das proteínas para formar uma base Schiff instável. Em semanas, esse produto se estabiliza porém ainda de forma irreversível sendo chamado de Amadori product. Na permanência de hiperglicemia, esse Amadori product se rearranja e torna-se um AGE irreversível. Extraído de Mealey BL. Diabetes Mellius. In: Medicina Periodontal. Rose LF, Genco RJ, Mealey BL, Cohen DW. Hamilton, Ontário, BC: Ed. Santos Jr, 2000: 121-150. De acordo com WALTIER & GUILLAUSSEAU, 2001, além da formação endógena, os AGEs podem ser gerados em inúmeras condições, como na fermentação, no cozimento de alimentos ou apenas na oxidação da atmosfera. Várias moléculas já foram encontradas, entretanto, em humanos, os principais AGEs descritos são a carboximetil-lisina (IKEDA et al., 1996) e a pentosidina (SELL & MONNIER, 1989). Os AGEs são irreversíveis: uma vez formados mantêmse ligados às proteínas por toda a sua meia-vida e, mesmo que a hiperglicemia retorne á normalidade, os níveis de AGEs nos tecidos afetados são mantidos. Constantemente são formados AGEs no organismo de indivíduos saudáveis, de forma lenta, desde o período embrionário, acumulando-se com a idade; porém, em indivíduos diabéticos, devido a maior disponibilidade de glicose, formam-se de maneira acelerada (PEPPA & VLASSALA, 2005). Estudos histoquímicos em animais, utilizando anticorpos AGE-específicos mostraram que a amostra de ratos diabéticos tinha de 10-45 vezes mais AGEs do que amostra não diabética após 45 dias de indução do diabete (MITSUHASHI et al., 1993). Da mesma forma, indivíduos diabéticos com bom controle glicêmico demonstraram apresentar menor formação de AGEs e menos complicações que indivíduos diabéticos hiperglicêmicos crônicos (SEPPÄLÄ et al., 1997). Algumas propriedades químicas dos AGEs foram relatadas na tabela 1. Basicamente, três são os mecanismos principais pelos quais os AGEs podem interferir na patogênese das complicações do diabete. Primeiramente, os AGEs podem reagir com o colágeno da matriz extracelular formando uma reação cruzada (cross-linking), resultando na formação de 22 A modificação por AGEs é irreversível AGEs são substâncias altamente reativas que causam a) Formação cruzada (cross-linking) entre polipetídeos da mesma proteína, por exemplo, colágeno b) Capturação de proteínas não glicosiladas, como imunoglobulinas, LDL A formação de AGEs com lipídeos induz oxidação desses lipídeos AGEs inativam quimicamente o óxido nítrico (NO) macromoléculas de colágeno altamente estáveis e que são resistentes à degradação enzimática normal e às modificações teciduais (MONNIER et al., 1996). Esta reação ocorre nas paredes tanto dos vasos maiores, favorecendo a formação de placas de ateromas, quanto dos vasos menores, alterando o transporte difusional normal através da membrana basal desses vasos (BROWNLEE, 1994). Outro processo decorrente da formação de AGEs é a sua ligação com receptores específicos na membrana de diferentes tipos celulares, principalmente macrófagos, linfócitos, fibroblastos e células endoteliais. Esses receptores são conhecidos como RAGE (receptor de produtos finais de glicosilação avançada) e a sua expressão está aumentada nos indivíduos diabéticos (BRETT et al., 1993). A interação dos AGEs com RAGE nas superfícies celulares amplificam suas respostas inflamatórias frente ao desafio microbiano, como ocorre na doença periodontal e outras doenças crônicas. Isso ocorre basicamente porque as células, como macrófagos, fibroblastos e endoteliais, quando ativadas pelos AGEs, produzem maior quantidade de citocinas como IL-1 (interleucina 1), IL-6 (interleucina 6) e TNF-α (fator de necrose tumoral alfa), além de enzimas como as MMPs (metaloproteinases de matriz), responsáveis pela reabsorção óssea. Ao se ligar ao seu receptor na célula, os AGEs alteram o metabolismo celular, causando liberação de radicais de oxigênio, induzindo o chamado estado de estresse oxidativo celular, responsável, em parte, por injúrias vasculares e também pelo aumento da expressão da molécula de adesão VCAM-1, capaz de agregar monócitos na parede endotelial, aumentando a chance de formação de trombos e aterosclerose R. Periodontia - 18(3):20-27 Tabela 2 PRINCIPAIS PROPRIEDADES BIOLÓGICAS PATOLOGICAMENTE RELEVANTE DOS AGES (VLASSARA, 1997) AGEs induzem migração transendotelial de monócitos e macrófagos AGEs estimulam liberação de citocinas e fatores de crescimento pelos macrófagos AGEs ligam-se a moléculas não glicosiladas, levando a formação de complexos imunes, ativação de complemento AGEs, na presença de co-estimulantes, induzem liberação de Interferon-y pelos linfócitos-T AGEs aumentam a permeabilidade das células endoteliais e sua atividade pró-coagulante dos em vários órgãos de animais, como retina, rim, nervos e artérias apresentando bons resultados (BROWNLEE, 1994; SOULIS-LIPAROTA et al., 1991; VLASSARA, 1994). Recentemente outros compostos têm sido estudados na inibição da formação dos AGEs e suas conseqüências sobre os tecidos, como a piridoxamina, que inibe a formação de AGEs a partir dos Amadori products, a pimagedina, que reage com produtos intermediários da glicose e o alagebrium que quebra a ligação cruzada (cross-linking) com o colágeno (WILLIAMS, 2004). Nenhum estudo com substâncias inibidoras de AGEs foi testado para se avaliar redução da doença periodontal em diabéticos, em modelo animal ou humano. AGEs aumentam a síntese de componentes da matriz extracelular AGEs aumentam proliferação celular (células musculares lisas, fibroblastos) AGEs aumentam taxa de mutação de DNA (SCHMIDT et al., 1996). SCHMIDT et al., 1996, comprovaram aumento de heme-oxigenase (marcador de aumento de estresse oxidativo) em biópsias de tecido gengival de diabéticos, quando comparadas as de indivíduos normais. Os autores sugeriram que esse aumento de estresse oxidativo relacionado com AGEs está relacionado com o aumento da resposta inflamatória do hospedeiro na doença periodontal, acelerando seu processo disfuncional em pacientes diabéticos. O terceiro mecanismo através do qual os AGEs podem influir na resposta do hospedeiro é quando ocorre a sua formação dentro do citoplasma de algumas células. A glicosilação intracelular não é exclusiva da glicose; outros carboidratos, como a frutose, podem reagir para formar AGEs (NASSAR et al., 2007). A formação intracelular de AGEs ocorre mais rapidamente que a extracelular. A união dos carboidratos às proteínas dentro das células pode alterar profundamente a função da proteína alvo, sendo muito deletéria em alguns casos na resposta imunoinflamatória. A tabela 2 relaciona algumas propriedades biológicas patologicamente importante dos AGEs. Estudos com inibidores de AGEs estão sendo desenvolvidos e os resultados têm sido promissores. O primeiro a ser estudado foi a aminoguanidina, um pequeno composto derivado da hidrazina, que não previne a formação de Amadori products, mas inibe sua transformação em produtos finais de glicosilação (AGEs). Os efeitos desta molécula na patogênese das complicações do diabete foram investiga- AGE-RAGE na doença periodontal Durante muitos anos tentou-se explicar os motivos pelos quais pacientes diabéticos apresentavam doença periodontal de uma forma mais acelerada e severa que pacientes não diabéticos. Várias hipóteses foram pesquisadas no intuito de se estabelecer uma relação biológica para essa exacerbação da doença em diabéticos (LALLA et al., 1998; SALVI et al., 1998). Atualmente, com o avanço nas pesquisas com os AGEs e suas implicações na patogenia das complicações do diabete, pode-se afirmar que o aumentos dos AGEs nos diabéticos e sua relação com seus receptores é o principal fator de amplificação da resposta imunoinflamatória pelo hospedeiro frente ao desafio microbiano na doença periodontal (LALLA et al., 2001; NASSAR et al., 2007). Dentre os mecanismos patológicos dos AGEs, o que está mais relacionado às doenças periodontais é a sua interação com seu receptor, RAGE, na superfície de algumas células, alterando a resposta celular. LALLA et al., 1998, criaram um modelo animal onde foram induzidos diabete e doença periodontal em ratos, e perceberam que ratos diabéticos apresentavam uma aceleração da doença periodontal, maior acumulação de AGEs e maior expressão de RAGE nas células inflamatórias. Os autores afirmaram que o aumento de AGE e RAGE no tecido gengival é potencialmente um mecanismo de maior destruição periodontal em diabéticos. O receptor para AGE (RAGE) é um membro das superfamílias das imunoglobulinas da superfície celular e é altamente expressivo em células vasculares e inflamatórias de diabéticos (RITTHALER et al., 1995). KATZ et al., 2005, avaliando a expressão de RAGE em gengiva de pacientes diabéticos e saudáveis, relatou que diabéticos apresentavam um aumento de 50% na expressão de mRNA para RAGE comparado com o controle. Concomitante ao aumento do acúmulo de AGEs nos tecidos dos diabéticos, há também um aumento na expressão de seu receptor (RAGE) na superfície de algumas células desses mesmos tecidos (SCHIMDT 23 R. Periodontia - 18(3):20-27 et al., 1995a). Tem sido proposto que a interação de AGEs com o receptor celular (RAGE) resulta na perturbação das propriedades celulares, muitas das quais associadas ao desenvolvimento de doenças vasculares, bem como à sustentação do processo inflamatório observado em defeitos de cicatrização de feridas e doenças inflamatórias crônicas, como a doença periodontal avançada (LALLA et al., 2001). Nas células endoteliais, o aumento da interação AGERAGE resulta em hiperpermeabilidade vascular e aumento da expressão de moléculas de adesão pró-inflamatórias, como VCAM-1, visto como fator de risco para o desenvolvimento de doenças vasculares no diabético (SCHMIDT et al., 1995b). Isto pode ocorrer também na microcirculação, como nos capilares periodontais e de acordo com LALLA et al., 1998, a interação de AGEs com RAGE das células endoteliais poderia resultar, em parte, na perpetuação do processo inflamatório periodontal, devido ao aumento da expressão de VCAM-1, que aumentaria a migração e saída dos monócitos para o periodonto. Os macrófagos, portanto, sofrem um estímulo na migração para locais onde há aumento de AGEs, imobilizamse nesses locais e podem interagir com o AGE disponível, através de seu receptor (RAGE). Essa interação provoca distúrbios intra-celulares, levando a um aumento da liberação de citocinas pró-inflamatórias (IL-1α, IL-6, TNFα), além de alterar a capacidade dos macrófagos de realizar renovação tecidual (LALLA et al., 1998; WEHBA et al., 2004). Esses dados corroboram com o estudo de SALVI et al., 1998, que provaram que macrófagos de pacientes diabéticos apresentavam níveis mais elevados de secreção de TNFα (4.6-fold), IL-1α (4.4-fold) e PGE2 (prostaglandina E2) (4.2-fold) no fluido gengival crevicular. Além disso, os autores afirmaram que em presença de LPS (lipopolissacárides) de Porphyromonas gingivalis, pacientes diabéticos tinham secreção anormal de monócitos inflamatórios em relação a pacientes não-diabéticos periodontais. Em estudo animal, SCHIMDT et al., 1996, relacionou a formação de AGEs com o aumento de estresse oxidativo na gengiva. A infusão de albuminas-AGE em ratos gerou um aumento no nível de TBARS (substâncias reativas ao ácido tiobarbitúrico), um marcador molecular indicativo de estresse oxidativo, comparado ao grupo em que foi aplicado apenas albumina não glicosilada. No entanto, esse processo foi inibido quando foram utilizados bloqueadores de RAGE ou agentes antioxidantes. Entretanto, de acordo com LALLA et al., 2001, a ligação dos RAGE com a doença periodontal pode ser ainda mais complexa. Isto porque este grupo de pesquisadores identificou que o RAGE é o receptor principal de superfície celular 24 para uma molécula denominada EN-RAGE (proteínas extracelulares recém-identificadas de ligação ao RAGE) e para outros membros da S100/calgranulina (família das citocinas pró-inflamatórias). Essas proteínas intracelulares localizamse em células-chaves na resposta inflamatória (como leucócitos polimorfonucleares e monócitos) e podem ter acesso ao espaço extracelular num ambiente inflamatório. Uma vez liberadas, estas moléculas têm habilidade de interagir com o RAGE celular e isto parece ser importante na propagação e sustentação da perturbação celular e injúria tecidual crônica, mesmo em normoglicemia (HOFMANN et al., 1999). Todas essas alterações celulares, mediadas pela interação de AGEs e outras moléculas, com o EN-RAGE e a S100/ calgranulina ao receptor celular RAGE, contribuem para a exacerbação do processo inflamatório e danos teciduais em resposta à infecção bacteriana na doença periodontal em diabéticos. Apesar de ainda não estar exatamente determinado o papel destes receptores no processo inflamatório das complicações do diabete, muitas pesquisas começam a investigar se bloqueadores de RAGEs podem atenuar o aparecimento dessas complicações. Pode-se intervir nos receptores de diversas maneiras, porém a forma mais pesquisada atualmente é a utilização de RAGE solúvel extracelular. RAGE solúvel ou sRAGE é a parte ligante extracelular do receptor original e serve como um chamariz para AGE e outras moléculas, que ao se unirem, acabam reduzindo a interação destas com os RAGEs das superfícies celulares (LALLA et al., 2001). RAGE solúvel são desenvolvidos em laboratórios e são espécies-específicos. Estudos in vivo em animais têm mostrado resultados animadores. O bloqueio da interação com RAGE utilizando sRAGE em animais diabéticos apontou diminuição da hiperpermeabilidade vascular e suprimiu aterosclerose acelerada em ratos (HOFMANN et al., 1999; PARK et al., 1998; WALTIER et al., 1996). GOOVA et al., 2001, observaram que ratos diabéticos tiveram uma cicatrização tecidual acelerada quando administrado sRAGE, comparado ao placebo. Esses resultados levaram os pesquisadores a investigar se todas as complicações do diabete eram reduzidas, ou no mínimo amenizadas, ao se utilizar dos bloqueadores de RAGE. Em periodontia não foi diferente: LALLA et al., 1998, criaram um modelo animal em ratos de diabete e doença periodontal, utilizando estreptozotocina, um agente que causa uma destruição seletiva das células beta do pâncreas, responsáveis pela produção de insulina, análogo ao diabete tipo 1 em humanos, e inoculando nesses animais cepas de Porphyromonas gingivalis, um dos patógenos da doença periodontal. Observaram ao fim da pesquisa que animais R. Periodontia - 18(3):20-27 do grupo-teste apresentaram maior perda óssea alveolar, maior acumulação de AGEs nos tecidos e maior expressão de RAGE nas células gengivais, quando comparados aos grupo-controle. Uma segunda etapa deste trabalho foi avaliar o efeito da administração de sRAGE nesse modelo animal de diabete e doença periodontal. A equipe de pesquisadores chegou a conclusão que ratos do grupo-teste (diabete + periodontite + sRAGE) apresentaram menor perda óssea, menor expressão de citocinas pró-inflamatórias, como o TNFα e IL-6 e redução da produção de metaloproteinases da matriz, enzimas responsáveis pela destruição óssea e conjuntiva na periodontite, quando comparado aos ratos do grupo-controle (diabete + periodontite) (LALLA et al., 2000). CONSIDERAÇÕES FINAIS Sendo o diabete uma doença de considerável prevalência e de alta morbidade e que influencia varias especialidades na área médica e odontológica, é de grande valia todos os esforços da ciência para a melhoria da qualidade de vida desses indivíduos. Dessa forma a elucidação da patogênese das complicações diabéticas vem contribuir para uma melhor investigação dos seus mecanismos, sendo o objetivo chegar a uma terapia eficaz. A intervenção na formação dos AGEs e o bloqueio dos receptores RAGE tanto para AGEs quanto para outros ligantes como S100/calgranulina, além de ter grande plausibilidade biológica, tem obtido bons resultados in vivo em animais (LALLA et al., 2001; KIM et al., 2005). Entretanto, não foram realizados estudos em humanos, portanto, nenhum protocolo terapêutico foi testado e, segundo BROWNLEE, 2005, a patogenia das complicações do diabete depende de outros fatores além dos AGEs e receptores, sendo um mecanismo altamente complexo. Embora muito ainda deva ser pesquisado no intuito elucidar o papel dos AGEs e receptores nas complicações do diabete, afirmamos que futuramente existirão drogas capazes de inibir sua formação e interação, minimizando assim as doenças crônicas que são agravadas pelo diabete, inclusive a doença periodontal, melhorando a qualidade de vida desses pacientes. ABSTRACT The complications of diabetes mellitus have been extensively investigated by studies on the pathology of this disease, with the purpose to understand the role of AGEs (advanced glycation end products), active biological components formed through association of glucose with proteins or lipids, as well as their interaction with specific receptor localized in the cellular membrane (RAGE). It has been shown that the AGE-RAGE system increased remarkably in diabetic conditions and has an important participation in the development or exacerbation of diabetic complications. Since the diabetic status is a risk factor in the prevalence and severity of periodontal disease, efforts are necessary to understand the cellular mechanisms involved with AGEs and RAGE in the periodontal disease and possible alternatives of dental treatment. Thus, the aim of this review addresses concerns about how the AGE-RAGE system is produced as well as its implications in the inflammatory process, including the pathogenesis of periodontal disease. We emphasize the ongoing research concerning the formation or interaction of the AGE-RAGE system in order to improve quality of life among patients in the diabetic status. UNITERMS: Diabetes mellitus, periodontal disease, diabetes complications, risk factor, Advanced Glycation End Products. 25 R. Periodontia - 18(3):20-27 REFERÊNCIAS BIBLIOGRÁFICAS 1- Brett J, Schmidt AM, Yan SD, Zou YS, Weidman E, Pinsky D et al. Survey of the distribution of a newly characterized receptor for advanced glycation end products in peripheral occlusive vascular disease. Am J Pathol 1993; 143:1699-1712. 2- Brownlee M, Cerami A. The biochemistry of the complication of diabetes mellitus. Annu Rev Biochem 1981; 50:385-432. 3- Brownlee M. Glicosylation and diabetes complications. Diabetes 1994; 43:836-841. 4- Brownlee M. The pathobiology of diabetes complications. Diabetes 2005; 54:615-1625. 5- Emrich LJ, Shlossman M, Genco RJ. Periodontal disease in non-insulin dependent diabetes mellitus. J Periodontol 1991; 62:123-30. 6- Groop PH, Forsblom C, Thomas MC. Mechanism of disease: Pathwayselective insulin resistance and microvascular complications of diabetes. Nat Clin Pract Endocrinol Metab 2005; 1(2):100-110. Clin Invest 2000; 105(8):1117-1124. 16- Lalla E, Lamster IB, Stern DM, Schmidt AM. Receptor for advanced glycation end products, inflammation, and accelerated periodontal disease in diabetes: Mechanisms and insight therapeutic modalities. Ann Periodontol 2001; 6(1):113-118. 17- Malerbi DA, Franco LG. Multicenter study of the prevalence of Diabetes Mellitus and impaired glucose tolerance in urban brazilian population aged 30-69 year. Diabetes Care 1992; 15:1509-1516. 18- Mealey BL. Diabetes Mellius. In: Medicina Periodontal. Rose LF, Genco RJ, Mealey BL, Cohen DW. Hamilton, Ontário, BC: Ed. Santos Jr, 2000: 121-150. 19- Mitsuhashi T, Nakayama H, Itoh H, Kuwajima S, Aoki S, Atsumi T et al. Immunochemical detection of advanced glycation end products in renal cortex from STZ induced diabetic rat. Diabetes 1993; 42:826833. 7- Grossi SG, Genco RJ. Periodontal disease and diabetes mellitus: a two way relationship. Ann Periodontol 1998; 3: 171-177. 20- Monnier VM, Gollub M, Elgawish A, Sell DR. The mechanism of collagen cross-linking in diabetes. A puzzle nearing resolution. Diabetes 1996; 45(Suppl 3): S67-72. 8- Goova MT, Li J, Kinslinger T, Qu W, Lu Y, Bucciarelli LG et al. Blockade of receptor for advanced glycation end-products restores effective wound healing in diabetic mice. Am J Pathol 2001; 159(2):513-525. 21- Nassar H, Kantarci A, Van Dyke TE. Diabetic periodontitis: a model for activated innate immunity and impaired resolution in inflammation. Periodontology 2000 2007; 43: 233-244 9- Hofmann MA, Drury S, Fu C. RAGE mediates a novel proinflammatory axis: a central cell surface receptor for S100/ calgranulin polypeptides. Cell 1999; 97:889-901. 22- Papapanou PN. 1996 World Workshop in Clinical Periodontics. Periodontal diseases: epidemiology. Ann Periodontol 1996; 1:1-36. 10- Ikeda K, Higashi T, Sano H, Jinnouchi Y, Yoshida M, Araki T et al. N(carboxymethyl) lysine protein adducts is a major immunological epitope in protein modified with advanced glycation and products of the Maillard reaction. Biochem 1996; 35: 8075-8083. 11- Katz J, Bhattacharyya I, Farkhondeh-Kish F, Perez FM, Caudle RM, Heft MW. Expression of the receptor of advanced glycation end products in gingival tissues of type 2 diabetes patients with chronic periodontal disease: a study utilizing immunohistochemistry and RT-PCR. J Clin Periodontol 2005; 32:40-44. 23- Park L, Raman KG, Lee KJ, Lu Y, Ferran LG, Chow WS et al. Supression of accelerated diabetic atherosclerosis by the soluble receptor for advanced glycation end products. Nature Med 1998; 4:1025-1031. 24- Peppa M, Vlassala H. Advaced glycation end products and diabetic complications: a gen.ral overview. Hormones 2005; 4(1):28-37. 25- Ritthaler U, Deng Y, Zhang Y, Greten J, Abel M, Sido B et al. Expression of receptors for advanced glycation endproducts in peripheral occlusive vascular disease. Am J Pathol 1995; 146: 688-694. 26- Salvi GE, Beck JD, Offenbacher S. PGE2, IL-1â and TNF-á responses in 12- Kim W, Hudson BI, Moser B, Guo J, Rong LL, Lu Y et al. Receptor for advanced glycation end products and its ligands. A journey from the complications of diabetics to its pathogenesis. Ann NY Acad Sci 2005; 1043:553-561. 13- Lalla E, Lamster IB, Schimidt AM. Enhanced interactions of advanced glycation end products with their cellular receptor Rage: Implications for the pathogenesis of accelerated periodontal disease in diabetes. Ann Periodontol 1998; 3(1): 13-19. 14- Lalla E, Lamster IB, Feit M, Huang L, Schmidt AM. A murine model of accelerated periodontal disease in diabetes. J Period Res 1998; 33:387399. 15- Lalla E, Lamster IB, Feit M, Huang L, Spessot A, Qu W et al. Blockade of Rage supresses periodontitis-associates-bone loss in diabetic mice. J 26 diabetic as modifiers of periodontal expression. Ann Periodontol 1998; 3(1):40-50. 27- Sastrowijoto SH, Hillemans P, Steenbergn TJ, Abraham-Inpijin L, de Graaff J. Periodontal condition and microbiology of healthy and diseased periodontal pockets in type 1 diabetes mellitus patients. J Clin Periodontol 1989; 16:316-22. 28- Sell DR, Monnier V. Structure elucidation of a senescence cross-link from human extracellular matrix. Implication of pentoses in the aging process. J Biol Chem 1989; 264: 21597-21602. 29- Schimdt AM, Yan SD, Stern D. The dark side of glucose. Nat Med 1995; 1-1002-1004. 30- Schmidt AM, Hori O, Chen J, Li JF, Crandall J, Zhang J et al. Advanced R. Periodontia - 18(3):20-27 glycation end products interacting with their endothelial receptor induce expression of vascular cell adhesion molecule-1 (VCAM-1): a potencial mechanism for the accelerated vasculopathy of diabetes. J Clin Invest 1995; 96:1395-1403 31- Schmidt AM, Weidmam E, Lalla E, Yan SD, Hori O, Cao R et al. Advanced glycation endproducts (AGEs) induce oxidant stress in the gingiva: a potencial mechanism underlying accelerated periodontal disease associates with diabetes” J Periodont Res 1996; 31:508-515. 32- Seppälä B, Sorsa T, Ainamo J. Morphometric analysis of cellular and vascular changes in gingival connective tissue in long-term insulin dependent diabetes. J Periodontol 1997; 68(12): 1237-45. 33- Shlossman M, Knowler WC, Pettit DJ, Genco RJ. Type 2 diabetes mellitus and periodontal disease. J Am Dent Assoc 1990; 121:532-6. 34- Soulis-Liparota T, Cooper M, Papazouglou D, Clarke B, Jerums G. Retardation by aminoguanidine of development of albuminuria, mesangial expansion, and tissue fluorescence in streptozocin-induced diabetic rat. Diabetes 1991; 40:1328-1335. 35- Tangi N, Markowitz GS, Fu C, Kislinger T, Taguchi A, Pischertsrieder M, Schimidt AM et al. Expression of advanced glycation end products and their cellular receptor RAGE in diabetic nephropathy and nondiabetic renal disease. J Am Soc Nephrol 2000; 11:1656-1666. 36- The Expert Committee on the Diagnosis and Classification of Diabetes Mellitus, Report of the Expert Committee on the Diagnosis and Classification of Diabetes Mellitus. Diabetes Care; 25(supp 2002):520. 37- Vlassara H. Recent progress on the biologic and clinical significance of advanced glycosylation end products. J Lab Clin Med 1994; 124(1):19-30. 38- Waltier JL, Zoukourian C, Chappey O, Waltier MP, Guillausseau PG, Cao R et al. Receptor-mediated endothelial cell dysfunctionin diabetic vasculopathy. Soluble receptor for advanced glycation end products blocks hyperpermeability in diabetic rats. J Clin Invest 1996; 97:238243. 39- Waltier JL & Guillausseau PJ. Advanced glycation end products, their receptors and diabetic angiopathy. Diabetes Metabol 2001; 27: 535542. 40- Wehba C, Rodrigues AR, Soares FP. Diabetes e doença periodontal: uma relação bidirecional. In: Periodontia Médica. 2004 Brunetti MC São Paulo Ed. Senac: 171-196. 41- Williams EM. Clinical studies of advanced glycation end products inhibitors and diabetic kidney disease. Curr Diab Reports 2004; 4:441446. 42- Zambon JJ, Reynolds F, Fisher JG, Shlossman M, Dunford R, Genco RJ. Microbiological and immunological studies of adult periodontitis in patients with non-insulin dependent diabetes mellitus. J Periodontol 1988; 59:23-31. 43- Zimmet P. The burden of Type 2 diabetes: Are We doing enough? Diabetes Metabolism 2003; 29(6): 9-18. Endereço para correspondência: Warley David Kerbauy Universidade Estadual Paulista/UNESP – Faculdade de Odontologia de São José dos Campos Departamento de Diagnóstico e Cirurgia Disciplina de Periodontia Av. Francisco José Longo, 777 CEP: 12245-000 - São José dos Campos – SP E-mail: [email protected] 27
Baixar