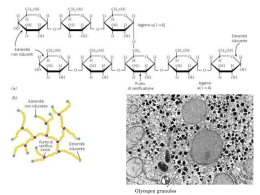
-11- INTRODUÇÃO 1.1- O Carrapato Rhipicephalus (Boophilus) microplus e sua importância econômica Os carrapatos são artrópodes ectoparasitos hematófagos classificados em três famílias: Argasidae, Ixodidae e Nuttalliellidae (Keirans, 1992; Keirans & Robbins 1999; Horak et al., 2002). Argasídeos são carrapatos que procuram o hospedeiro para sugar sangue, abandonando-o em seguida e alimentando-se mais de uma vez em seu ciclo de vida. As fêmeas efetuam várias posturas, alternando ovoo0posição com repasto sangüíneo. Cada postura pode variar de 50 à 600 ovos, totalizando um número realmente pequeno quando comparado aos ixodídeos. Nos Ixodídeos a alimentação dura um tempo mais prolongado e é feita uma única vez em todo o ciclo de vida e a ovoposição resulta num grande número de ovos (de várias centenas a 23.000 ovos por fêmea) e depois morrem, sendo estas as diferenças mais marcantes entre estas famílias (Flechtmann, 1977, Klompen, 2005). Os carrapatos são transmissores de patógenos que afetam população animal e humana (Estrada-Peña & Jongejan, 1999; Parola & Raoult, 2001). A família Nuttalliellidae é representada por apenas uma espécie, na qual pouco se sabe sobre a sua biologia e aparentemente não possui importância médico – veterinária (Klompen, 2005). O carrapato Rhipicephalus (Boophilus) microplus é um ixodídeo responsável por grandes perdas econômicas para a pecuária de regiões tropicais e subtropicais. Este carrapato é um ectoparasita hematófago originário da Ásia, cujo principal hospedeiro é o bovino. Sua incidência é maior em grandes rebanhos da América, África, Ásia e Austrália, sendo considerado o carrapato de maior impacto em perda econômica nos rebanhos da América do Sul (Gonzales, 1995; Nari, 1995). Apartir de 2002, Rhipicephalus (Boophilus) microplus se tornou a nomenclatura para o carrapato Boophilus microplus de acordo com estudos taxonômicos. O gênero Rhipicephalus tem sido considerado parafilético ao gênero Boophilus, assim este se tornou um subgênero de Rhipicephalus. Assim, o carrapato Rhipicephalus (Boophilus) microplus pode ainda ser chamado de B.microplus, mas esta nomenclatura será substituída de acordo com o reflexo do conhecimento de filogenia e da evolução desse carrapato (Barkel & Murrell, 2002). -2R. microplus é um parasita que precisa obrigatoriamente passar por um período sobre o bovino, ingerindo substratos teciduais e principalmente sangue (Pereira, 1982), sendo um dos principais transmissores dos parasitas Babesia bovis e Babesia bigemina, causadores da piroplasmose bovina. Esta doença, popularmente conhecida como tristeza bovina, afeta gravemente o desenvolvimento do gado, podendo levá-lo à morte em poucos meses (McKosker, 1981). Alguns membros da família dos ixodídeos são vetores de duas doenças para humanos conhecidas como tifo e doença de Lyme, uma borreliose. Anteriormente julgava-se que apenas os carrapatos da família dos argasídeos eram capazes de transmitir Rickettsia e Borrelia (Beaty & Marquardt, 1996). Devido aos diversos danos econômicos acarretados pelo R. microplus, que atingem a ordem de um bilhão de dólares no Brasil (Labruna &Veríssimo, 2001), este se tornou o principal alvo de programas de controle e erradicação nos rebanhos da América do Sul (Nari, 1995). Um carrapato bovino suga, em média, de 2 a 3mL de sangue do seu hospedeiro (Gonzáles, 1975), o que reflete em grandes perdas na produção de leite e carne (Sutherst et al., 1983) e danos no couro causados por reações inflamatórias nos locais de fixação do carrapato (Seifert et al., 1968). Após o ingurgitamento uma fêmea de R. microplus aumenta em até 100 vezes o seu próprio peso inicial (Sonenshine, 1991) (Figura 1). O controle das infestações tem sido dificultado devido ao fato dos carrapatos possuírem poucos predadores naturais. Os métodos de controle tradicionais aos carrapatos fazem uso de vários tipos de carrapaticidas químicos (Hopkins et al., 1985; Cramer et al., 1988). Contudo, a aplicação destes carrapaticidas tem limitada eficácia na redução da infestação e frequentemente vem acompanhada por vários danos, incluindo a seleção de carrapatos resistentes ao carrapaticida, contaminação do ambiente, como também do leite e da carne com resíduos da droga. Além do mais, o desenvolvimento de novos carrapaticidas é um processo longo e de alto custo, no qual reforça a necessidade de novas alternativas para o controle da infestação de carrapato (Graf et al., 2004). Recentemente têm sido desenvolvidas vacinas que induzem a proteção imunológica de hospedeiros vertebrados contra a infestação de carrapato. A possibilidade do controle da infestação de carrapato através da imunização de bovinos foi demonstrada com o desenvolvimento de vacinas que reduzem a infestação de Boophilus spp em bovinos (de la -3Fuente & Kocan, 2003; Willadsen, 2004). O desenvolvimento destas vacinas pode permitir a inclusão de múltiplos antígenos que tem como alvo o combate ao carrapato e também à prevenção da transmissão de patógenos (de la Fuente & Kocan, 2006) 1cm cm ♂ ♀ Figura 1: Carrapato bovino Rhipicephalus (Boophilus) microplus. Fêmea ingurgitada (esquerda) e macho (direita) (Flechtmann, 1977). Em nosso grupo de trabalho foi desenvolvida uma vacina (Leal et al.,2006) que tem como antígeno uma glicolipoproteína de 54 kDa isolada de ovos, chamada de BYC (Boophilus Yolk Catepsin), que parece atuar na degradação da vitelina, a principal proteína de reserva dos ovos do carrapato (Logullo et al., 1998, Abreu et al., 2004). O princípio desta vacina está baseado no bloqueio do desenvolvimento dos ovos. Quando bovinos imunizados com BYC foram desafiados com larvas infestantes, houve uma redução no número de teleóginas, na capacidade de postura e na fertilidade dos ovos, com eficácia variando entre 14% e 36% em dois experimentos independentes. Os níveis de anticorpos declinaram gradualmente após a infestação e responderam positivamente a um reforço vacinal, aplicado 11 meses após a infestação, indicando a existência de memória imunológica para esse antígeno (Vaz Jr. et. al., 1998). -41.2-Ciclo de vida do carrapato R. microplus O carrapato R. microplus apresenta duas etapas distintas no seu ciclo de vida (Figura 2): uma fase parasitária durante um período médio de 22 dias sobre um único hospedeiro e uma fase não parasitária que ocorre no solo que pode durar de dois a três meses, dependendo fundamentalmente das condições climáticas existentes (Gonzales et al., 1974). Na fase parasitária, o carrapato apresenta três variações morfológicas distintas: larva, ninfa e adulto. A larva apresenta três pares de patas, é bastante ativa, pois necessita encontrar o hospedeiro para nele se fixar, e sobrevive das reservas energéticas acumuladas na fase de ovo. Fixa-se em locais específicos utilizando algumas importantes estruturas, como as quelíceras, as quais seccionam a pele para a introdução do hipostômio, órgão responsável pela fixação da larva na pele do bovino (Gonzales et al., 1974). A larva alimenta-se e inicia o processo de desenvolvimento e crescimento tegumentário. Passa por um período de inércia entre o quarto e quinto dia e atinge a fase de metalarva. Em torno do sexto dia, adquire uma nova estrutura, com um outro tegumento, mais um par de patas e uma fileira de dentição do hipostômio entre outras alterações: é a fase de ninfa. Esta fase dura em média dois a quatro dias e ao continuar seu desenvolvimento, uma nova alteração no exoesqueleto se processa, havendo um período igual de inatividade, denominado de metaninfa. Ao final do processo surja o indivíduo adulto, sexualmente diferenciado. Isto acontece em torno do décimo segundo dia. A partir dessa fase, inicia-se o processo de maturação dos machos e das fêmeas. Em torno do décimo sétimo dia os machos já estão aptos à cópula. As fêmeas, após serem fecundadas, passam de metaninfa para neógina num período médio de 17 dias. Em seguida, em um período de três dias, passam a partenógena (parcialmente ingurgitada) e em mais dois dias, a teleógina (ingurgitamento máximo) (Gonzales et al., 1974). Nota-se um crescimento mais acentuado do tegumento nessa fase, e nas últimas horas próximas ao ingurgitamento completo, a alimentação intensifica-se, ao ponto das fêmeas apresentarem um tamanho cerca de 10 vezes superior ao dos machos. -5- Figura 2: Representação esquemática do ciclo de vida do carrapato R. microplus. (Gonzales et al., 1974). Na fase de vida parasitária as larvas se alimentam e sofrem diferenciação sexual. Na fase de vida livre, as fêmeas ingurgitadas caem ao solo e iniciam a ovoposição. Aos 22 dias, a maioria das fêmeas cai ao solo. Os machos podem permanecer no bovino por mais de 38 dias fecundando inúmeras fêmeas (Gonzales et al., 1974). A fase não parasitária compreende os estágios de fêmea adulta (teleógina), ovo e larva infestante. A fêmea adulta fecundada, ao desprender-se do bovino procura um local no solo para efetuar a postura. Em condições adequadas de temperatura (26-28ºC) e umidade (~80%) a postura se inicia no terceiro dia após a queda. Após a postura, a fêmea apresenta uma coloração mais amarelada chegando à morte após o término da ovoposição. A eclosão dos ovos inicia a partir da quarta semana após o inicio da postura. No meio ambiente, este processo pode ser longo, sendo uma forma estratégica de sobrevivência do parasito frente às adversidades climáticas. As larvas necessitam de um -6período de maturação médio de uma semana para estarem aptas a fixarem-se no hospedeiro e continuarem o desenvolvimento. Após esse período, deslocam-se às extremidades da vegetação para alcançarem mais facilmente o bovino. Nessa fase de larva infestante, elas podem sobreviver por até 60 dias (Gonzales et al., 1974). 1.3- Modificações metabólicas durante o desenvolvimento de invertebrados Em animais ovíparos, um fator determinante para a perpetuação de espécies é a ovogênese. Durante este processo, os ovócitos em desenvolvimento apresentam uma elevada taxa de crescimento inicial, em um estágio denominado vitelogênese (Salerno et al., 2002), que ocorre devido ao acúmulo de grandes quantidades de proteínas, lipídeos e glicogênio (Salerno et al., 2002; Logullo et al., 2002). Essas moléculas serão fontes de energia e unidades de construção para o desenvolvimento dos embriões (Salerno et al., 2002). Deste modo, após a postura dos ovos com o conteúdo vitelínico, os embriões se desenvolvem fora do organismo materno tendo acesso somente aos nutrientes armazenados no ovo durante a ovogênese. Os embriões de carrapato desenvolvem-se formando um sincício, com abrupta celularização, semelhante ao processo observado na mosca Drosophila melanogaster (Bate & Marquardt, 1993). Nos carrapatos a embriogênese, em condições controladas, leva em média 20 dias desde a postura dos ovos até a eclosão. A literatura sobre a morfologia de embriões de carrapatos é precária, devido a problemas relacionados à permeabilização dos ovos, que dificulta a entrada de agentes fixadores utilizados em microscopia óptica ou eletrônica. Resultados prévios do nosso grupo descrevem morfologicamente alguns momentos marcantes na embriogênese do R. microplus, como a formação do sincício no quarto dia, do blastoderma celular no quinto dia e a segmentação do embrião no sétimo dia do desenvolvimento (Campos et al., 2006) (Figura 3). -7- Figura 3: Etapas do desenvolvimento carrapato R microplus. A- 1 dia, B- 3 dias (blastoderma sincicial), C- 5 dias (blastoderma celular), D- 7 dias (embrião segmentado), E- 12 dias (Campos et. al., 2006). Recentemente foi demonstrado por Moraes et al. (2007), que uma das estratégias metabólicas utilizadas pelo carrapato R. microplus, para a formação de seu embrião, é degradar inicialmente glicogênio (Figura 4). Sugerindo então, que este metabólito poderia estar de algum modo suportando energeticamente a diferenciação celular e a formação de proteínas. Esta sugestão baseia-se nos dados de determinação da concentração de vitelina (Logullo et al., 2002), no não aparecimento do produto de excreção catabólica de aminoácidos em aracnídeos (guanina) (Moraes et al., 2007) e na constatação da formação do blastoderma celular (Campos et al., 2006). Vimos ainda que após a formação das estruturas celulares, e conseqüentemente protéicas, do embrião no quinto dia do desenvolvimento é iniciada uma intensa degradação de aminoácidos, ocorrendo um acúmulo de guanina (Campos et al., 2006; Moraes et al., 2007) (Figura 5c). Verificamos que concomitantemente ocorre aumento dos níveis de glicogênio e glicose nesta fase (Figuras 4 e 5a). Desta forma, os embriões desta espécie de carrapato são capazes de gerar glicose a partir do catabolismo de aminoácidos, possivelmente associado a uma ativação da gliconeogênese, como também uma significativa re-síntese de glicogênio nos ovos a partir do sexto dia do desenvolvimento. -8- Figura 4: Conteúdo de glicogênio durante o desenvolvimento do carrapato R. microplus. A quantidade de glicogênio em homogenatos de ovos foi determinada por digestão com α-amiloglucosidase e glicose liberada foi medida utilizando kit comercial (Moraes et al., 2007). -9- Figura 5: Via Gliconêogenica durante o desenvolvimento do carrapato R. microplus. (A) Concentrações de glicose medidas em homogenatos de ovos. (B) Atividade específica de PEPCK medidas em homogenatos de ovos. (C) concentrações de guanina determinadas por HPLC, como coluna interação hidrofóbica (C-18) (Moraes et al.,2007). Logullo e colaboradores (2007) mostraram que a expressão de fosfoenolpiruvato carboxicinase (PEPCK) aumenta a partir do 5º dia do desenvolvimento do carrapato R. microplus, resultado coerente com os dados de re-síntese de glicogênio e glicose (Figuras 4 e 5a), como também atividade da PEPCK (Figura 5b) (Moraes et al., 2007). A PEPCK é uma enzima chave da gliconeogênese e que em mamíferos sua expressão é regulada pela - 10 via da insulina (Liao et al., 1998). A via da insulina desencadeia uma cascata que fosforila e inativa a Glicogênio Sintase Quinase (GSK-3) via fosforilação por proteína cinase B (Galetic et al., 1999, Hanada et al., 2003). Já foi descrito que a atividade da GSK-3 estaria regulando a ativação de alguns fatores de transcrição envolvidos na expressão da PEPCK (Finlay et al., 2004; Lochhead et al., 2001). Foi sugerido de acordo com estes dados, que a via gliconeogênica seria ativada durante o desenvolvimento do carrapato a partir do estágio de blastoderma celular, aumentando a concentração de glicose nos ovos, onde parte deste seria utilizada no metabolismo do embrião e o restante seria estocado como glicogênio (Moraes et al., 2007). 1.4- Glicogênio Sintase Quinase (GSK-3) e sua participação durante a diferenciação celular A enzima Glicogênio Sintase Quinase-3 (Glycogen Synthase Kinase-3, GSK-3) foi descrita originalmente como reguladora do metabolismo de glicogênio, uma proteína quinase que fosforila e inativa a Glicogênio Sintase (GS) (Embi et al., 1980), enzima final da biossíntese do glicogênio (Figura 6). Porém, atualmente já são descritas mais de 40 enzimas fosforiladas pela GSK-3, incluindo 12 fatores de transcrição. O mau funcionamento da GSK-3 está ligada a um número surpreendente de doenças em humanos (Jope e Johnson, 2004). A GSK-3 é uma serino/tirosina quinase que possui duas isoformas: GSK-3α e GSK3β (Mukai et al., 2002). Suas atividades são reguladas por fosforilação nos resíduos serina e tirosina (Grimes & Jopes, 2001). A atividade da GSK-3 é reduzida por fosforilação de um resíduo N- terminal de serina (Ser9 em GSK-3β e Ser21 em GSK-3α). Várias quinases podem fosforilar estes resíduos de serina, incluindo a PKB (Akt), PKA, p90Rsk, entre outras (Jope & Johnson, 2004). Em oposição à regulação inibitória pela fosforilação dos resíduos de serina, atividade da GSK-3 é facilitada por fosforilação da tirosina 216 em GSK-3β e da tirosina 279 em GSK-3α, que pode ocorrer por autofosforilação ou por outras quinases, em um processo pouco entendido (Frame & Cohen, 2001; Grimes & Jope, 2001). As isoformas, GSK-3α e GSK-3β, possuem alta homologia dentro dos seus - 11 domínios quinases e propriedades bioquímicas (Hoeflich et al., 2000). Porém, existem algumas diferenças entre as regiões N- e C- terminais em que sugerem que a regulação e função de ambas isoformas de GSK-3 não são sempre idênticas. Por exemplo, a interrupção da isoforma GSK-3β em camundongos resulta em uma letalidade embrionária, onde a isoforma GSK-3α não é capaz de compensar a perda da isoforma GSK-3β (Hoeflich et al., 2000). Figura 6: Insulina estimula síntese de glicogênio e síntese protéica via inibição de GSK-3. A ligação da insulina ao seu receptor dispara uma cascata de sinalização mediada por substratos receptores de insulina (IRS), PI-3quinase e PKB (Akt) que inibe GSK-3 por fosforilação. Como resultado, resíduos da glicogênio sintase e do fator de iniciação eucariótico(eIF2B) sofrem desfosforilação aumentando suas atividades e assim estimulam respectivamente a síntese de glicogênio e proteínas (Frame & Cohen, 2001). A GSK-3 também é descrita como uma quinase essencial na especificação do destino de células em embriões, através da via Wnt, em estudos conduzidos em - 12 Drosophila, Xenopus e mamíferos. Um sinal extracelular libera β-catenina pela dissociação de um complexo GSK-3, APC (adenomatous poliposis coli) e AXN (Axin) (Wang & Wynshaw-Boris, 2004). A β-catenina liberada se dirige para o núcleo onde ativa fatores de transcrição, ativando os genes de padronização de segmentos (Frame & Cohen, 2001). A via Wnt é altamente conservada entre Drosophila, Xenopus e vertebrados (Wang & Wynshaw-Boris, 2004) (Figura 7). Figura 7: Componentes da via de sinalização Wnt altamente conservados entre diversos organismos. O esquema acima representa componentes desta via em diferentes organismos, mostrando seus componentes e efeitos específicos sobre a expressão gênica (Frame & Cohen, 2001). A regulação via GSK-3 está envolvida em outros papéis como a regulação da proliferação celular, diferenciação celular, dinâmicas de microtúbulos e motilidade celular, componentes do ciclo celular, fatores de transcrição de proteínas envolvidas na formação - 13 de microtúbulos e adesão celular (Frame & Cohen, 2001). Vários trabalhos associam a GSK-3 com a hipertrofia muscular (Hardt & Sadoshima, 2002; Haq et al., 2003), câncer (Manoukian & Woodgett, 2002 ; Hill & Hemming, 2002), distúrbio bipolar (Klein & Melton,1996; Jope, 1999), esquizofrenia (Kozlovsky et al.,2002), doença de Alzheimer (Grimes & Jope ,2001) e diabetes (Eldar-Finkelman, 2002; Nikoulina et al., 2000). Devido a isto, drogas que inibem a GSK-3 têm emergido potencial alvo tratamentos de doenças. Lítio é um inibidor da GSK-3, por isso, sua propriedade farmacológica tem sido usada em terapia para distrofia bipolar. A inibição de GSK-3 por Li+ é do tipo competitiva com Mg++ e não competitiva pelo substrato (Ryves & Horwood, 2001). Contudo, o Li não é um inibidor específico de GSK-3, inibindo também outras enzimas, incluindo polifosfato-1 fosfatase, caseina kinase II, proteína kinase -2 ativada por MAP (MAPKAP-K2) e quinase ativada e fosforilada por p38 (Berrigde et al., 1989; Davies et al., 2000). Por isso moléculas que inibem especificamente GSK-3 têm sido desenvolvidas. As moléculas SB-216763 e SB-415286 são pequenas moléculas do tipo maleimidas desenvolvidas para funcionarem como potentes e seletivos inibidores de GSK-3 que competem com o ATP (Coghlan et al., 2000). As alsterpaullones fazem parte de outro grupo de inibidores de GSK-3. A inibição da GSK-3 por esta molécula também é por competição ao sítio de ligação de ATP. Alsterpaulone inibe a fosforilação de tau in vivo, na região que é tipicamente fosforilado por GSK-3 na doença de Alzheimer. Assim esta especificidade da alsterpaulone pode ser uma poderosa ferramenta para os estudos e possibilidades de tratamento de doenças neurodegenerativas (Leost et al., 2000). 1.5- GSK-3 e a sua função em mitocôndria e núcleo A GSK-3 é tradicionalmente considerada uma proteína citosólica, mas também foram descritas isoformas presentes em núcleos e mitocôndrias, as quais exibem atividades mais elevadas que a observada na GSK-3 citosólica (Bijur & Jope, 2001). Em relação à regulação dos níveis de glicogênio em núcleos, Caracciolo e colaboradores (1998) demonstraram atividade de GSK-3 em núcleos de células embrionárias de Xenopus laevis. Nesta mesma espécie, núcleos funcionais podem ser reconstituídos a partir de DNA purificado na presença de frações citosólicas, membranares - 14 e uma terceira fração rica em glicogênio (Hartl et al., 1994). Junto a esta fração rica em glicogênio foi identificada a presença de GSK-3, que estaria ativando PP- 1 (Proteína Fosfatase -1), enzima que degrada glicogênio (Caracciolo et al., 1998). Além desta função na formação de núcleos, a GSK-3 estaria presente neste compartimento atuando na fosforilação, ativando ou inativando vários fatores de transcrição (Frame e Cohen, 2001). Em mitocôndrias, a GSK-3 tem papel na regulação de vias apoptóticas relacionada à liberação de citocromo c. A apoptose neuronal frequentemente ocorre por translocação de Bax, uma proteína membro pró apoptótico da família Bcl-2, para a mitocôndria, que sinaliza a formação de poros na membrana externa, liberando citocromo c (Zong et al., 2001). Em cultura de células neuronais foi demonstrado que Bax é um substrato de GSK3β que regula a sua localização subcelular (Linsemam et al., 2004). A inibição da GSK-3β reduz os efeitos do infarto e melhora as funções pos-isquémias. Entre todos os fatores que causam morte celular, períodos prolongados de hipóxia seguido de reoxigenação causam as mais perigosas e irreversíveis conseqüências (Tong et al., 2002). Juhaszova e colaboradores (2004) demonstraram que a inativação de alguns tipos de canais mitocondriais é um possível mecanismo que conduz a proteção de tecidos cardíacos e concluiu que o mecanismo geral de proteção converge para a via de inibição de GSK-3, limitando a permeabilidade da mitocôndria. - 15 - 2- OBJETIVOS Neste trabalho tivemos como objetivo principal a caracterização de uma GSK-3β na embriogênese do carrapato bovino Rhipicephalus (Boophilus) microplus. Para isso definimos os seguintes objetivos específicos: 1) Detectar a atividade enzimática de GSK-3β em homogenatos de ovos e em frações de núcleo e mitocôndria durante o desenvolvimento; 2) Determinar a distribuição de glicogênio em frações de núcleo e mitocôndrias; 3) Estudar o efeito de inibidores de GSK-3β em fêmeas ingurgitadas, na distribuição de glicogênio nos ovos postos; 4)Clonagem da GSK-3β de ovos do carrapato Rhipicephalus (Boophilus) microplus. - 16 3- MATERIAIS E MÉTODOS 3.1- Ovos de carrapatos Os carrapatos da espécie Rhipicephalus (Boophilus) microplus foram criados em bovinos na Faculdade de Veterinária da Universidade Federal do Rio Grande do Sul. Os carrapatos se desenvolveram em bovinos isolados em estábulos, livres de qualquer contato com o campo. As larvas foram colocadas no dorso dos bovinos e após 21 dias, no período modal de queda das teleóginas, o estábulo foi lavado e as fêmeas adultas coletadas com auxílio de peneiras. As fêmeas de carrapato foram utilizadas para postura de ovos usados nos experimentos. Para isso, foram mantidas à temperatura de 28ºC e umidade de 80%. 3.2- Manutenção dos ovos Durante o período de ovoposição, os ovos postos são separados das fêmeas diariamente. Os ovos foram mantidos à temperatura de 28ºC e umidade de 80%. Nestas condições, a eclosão é próxima de 100%, em aproximadamente 20 dias. A idade dos ovos, ao longo da embriogênese é contada a partir do dia em que estes são coletados e o desenvolvimento dos ovos interrompido por congelamento à -20°C. 3.3- Obtenção de homogenatos de ovos Os homogenatos de ovos foram obtidos por maceração com pestilo de plástico em microtubos, na presença de inibidores de proteases (PMSF 2mM, Pepstanina 1µM, Leupeptina 50 µM, EDTA 5mM) e inibidores de fostase (Molibdato de Amônio 1µM e Vanadato de Sódio 20µM). O material obtido foi centrifugado a 200 x g por 5 min e o sobrenadante foi utilizado. - 17 3.4- Isolamento de frações de núcleo e mitocôndria 1g de ovos de carrapato foi homogeneizado em 5 mL de tampão de lise (sacarose 12,5%, MOPs-KOH 20 mM, pH 7,2) contendo inibidores de proteases (PMSF 2mM, Pepstanina 1µM, Leupeptina 50 µM, EDTA 5mM) e inibidores de fostase (Molibdato de Amônio 1µM e Vanadato de Sódio 20µM). O homogenato foi centrifugado a 200 x g por 5 min a 4ºC. O sobrenadante foi coletado e novamente centrifugado a 2000 x g por 10 min a 4ºC. O precipitado foi coletado como fração nuclear e o sobrenadante foi novamente centrifugado a 8000 x g por 15 min a 4ºC. O sobrenadante foi descartado e o precipitado (fração mitocondrial) ressuspenso em 50µL de tampão de lise. 3.5- Dosagem de proteínas As proteínas foram quantificadas pelo método de Bradford (1976), utilizando albumina bovina (Sigma) como padrão. 3.6- Western blot As amostras das frações de núcleo e mitocôndria (100 µg de proteína) foram submetidas à eletroforese em gel de poliacrilamida 10%, com SDS. A transferência das proteínas para membrana de PVDF (Towbin et al., 1979) foi feita em tampão Tris-glicina 25mM, pH 8,3 contendo metanol 20% por 1 hora a 0,8mA por cm2. A membrana foi corada com uma solução 0,5% de vermelho de Ponceau, para verificar a eficiência da transferência. A membrana foi incubada por 4 horas com uma solução de Tris-HCl 10mM, pH 7,2 contendo 5% de leite em pó desnatado e 0,01% de Tween 20, para bloqueio e depois novamente incubada com o mesmo tampão contendo o anticorpo primário antiGSK-3β monoclonal (Sigma), numa diluição de 1:2000 por 2 horas. A membrana foi então lavada 5 vezes no mesmo tampão de incubação e novamente incubada com o anticorpo secundário (anti-IgG de coelho) conjugado com peroxidase (Sigma) em uma diluição de 1:5.000 por 1 hora. A membrana foi lavada por 5 vezes com tampão de incubação. A - 18 membrana foi revelada por reação de peroxidade em Tris-HCl 40mM pH 7,2, Imidazol 10mM, DAB 0,1% e H2O2 0,1%. 3.7- Quantificação de glicogênio Alíquotas (90 µg de proteínas) das amostras foram incubadas com αamiloglicosidase (0,336 U/tubo) (Sigma), em tampão acetato de sódio 0,2 M, pH 4,8 (volume final 200 µL), por 4 horas a 40°C. Foi feito um controle sem a enzima amiloglicosidase e submetidos às mesmas condições acima. A reação foi interrompida pela adição de 300 µL de PBS pH 7,4 e a glicose livre formada foi determinada com um kit enzimático para o diagnóstico de glicose (Glucox® 500, Doles). Após 10 minutos de incubação a 37°C, as amostras foram lidas em espectofotômetro a 510 nm. Foi feito uma curva padrão de glicogênio, a qual foi submetida às mesmas condições das amostras. As D.O. dos controles foram subtraídos às dos ensaios. 3.8- Injeção de inibidores de GSK-3 em teleógenas Teleógenas foram separadas em 4 grupos de 20 indivíduos por grupo. As injeções foram realizadas na região dorsal com uma microsseringa (Hamilton) de 25 microlitros de capacidade. No grupo controle foi injetado 1µL de DMSO. O segundo, o terceiro e quarto grupos foram injetados com o mesmo volume de soluções de SB 415286 10mM (inibidor específico de GSK-3), LiCl 10M e insulina 1,6mM, respectivamente. As soluções de SB 415286 e insulina foram preparadas em DMSO. Os grupos foram mantidos a 28°C com 80% de umidade em estufa. Os ovos de cada grupo foram coletados somente 3 dias após as injeções e mantidos nas mesmas condições. Alíquotas foram separadas no primeiro, quinto e décimo primeiro dias de desenvolvimento para a dosagem de glicogênio. Os dados de concentração de cada inibidor foram feitos considerando o volume de cada teleógena de 200 µL. Assim a concentração final de inibidor por indivíduo foi 50µM de SB415286, 8µM de insulina e 50mM de LiCl. - 19 3.9- Imunoprecipitação de GSK-3β β em homogenato de ovos Alíquotas dos homogenatos (100 µg de proteína) foram incubadas com 2 µL de anticorpo comercial anti-GSK-3β (Sigma) por 30min em banho-de-gelo, sendo agitadas a cada 10 min. Após esta incubação, foram adicionados 5 µL de proteína A-Agarose e incubada novamente por 10 min em gelo. O precipitado foi lavado e centrifugado á 200 x g por 5 min por 3 vezes com 20 µL de TBS pH 7,0. O precipitado final foi ressuspenso em 50 µL de TBS pH 7,0 e separado em duas alíquotas. 3.10- Atividade da GSK-3β Atividade da GSK-3β foi determinada em imunoprecipitados de homogenatos totais e em frações de núcleo e mitocôndria (50µg de proteína) de ovos de carrapato em diferentes dias do desenvolvimento. As frações foram incubadas em tampão Tris-HCl 20 mM, MgCl2 10 mM e DTT 5 mM, pH 7.5, mais o substrato específico, CREBtide® (Calbiochem) 50 µM, ATP 100 µM e [γ-32P] ATP (Amersham Biosciences) 500-3000 CPM/pmol em um volume final de 100 µL. Foram feitos frações controles para cada amostra sem o substrato da reação. As reações foram mantida à 370C por 30 minutos. Logo após, alíquotas de 20µL em quadriplicatas foram aplicadas em papel fosfocelulose Whatman P81, lavados com 50mL de ácido fosfórico 75 mM por filtração à vácuo. Depois de secos, os papéis foram colocados em “vials” de poliuretano, com 500µL de líquido de cintilação (POPOP 55µM e PPO 27mM) e analisados no cintilador (1600 TR Tricarb- Packard). 3.11- Extração de RNA total de ovos de carrapato 1g de ovo de 6º dia de desenvolvimeto foi macerado em 10mL de reagente Trizol® (Invitrogen) em N2 líquido. O homogenato foi aliquotado em microtubos (1 mL), e centrifugado a 12000 g por 10 min a 4ºC. Os sobrenadantes foram separados, e adicionou-se 500 µL de clorofórmio, com agitação por inversão 3 vezes e centrifugado a 12000 g por 15 min a 4ºC. Após a centrifugação, a fase aquosa dos sobrenadantes foi - 20 coletada separadamente e adicionou-se 1mL de isopropanol. A mistura foi incubada a 20ºC por 2 horas. Após a incubação foram centrifugados a 12000rpm por 10 min a 4º C. Os sobrenadantes foram removidos e os precipitados lavados com 500 µL de etanol 70%. Os precipitados foram secos a temperatura ambiente e posteriormente ressuspensos em 20 µL de água estéril e utilizados imediatamente. 3.12- Amplificação do gene da GSK-3β por RT-PCR Foram utilizados 5 µL do RNA total extraído, para a síntese do cDNA. O cDNA correspondente foi sintetizado com “kit SUPERSCRIPT® II (GibcoBRL), de acordo com as especificações do fabricante.. Para a amplificação dos cDNAs por PCR utilizou-se o primers específicos, sendo o primer “forward” 5’-ATG AGT GGA CGG CCG AGG AC- 3’ e o primer “reverse” 5’-TTA CAC GGG CCC GCT GTT TG -3’ para a seqüência completa do gene em R. microplus. As condições para amplificação foram: 94 ºC por 5 min; 35 ciclos de 94 ºC por 30s, 63 ºC por 30 s, 72 ºC por 30s; 72 ºC por 7min. O produto do PCR foi observado por eletroforese de DNA em gel de agarose 0,8% e um fragmento com aproximadamente 1200 pb correspondente ao cDNA de GSK-3β. 3.13- Clonagem e sequenciamento do gene da GSK-3β Para a clonagem utilizou-se o fragmento de DNA de 1200 pb, amplificado por RTPCR. O produto do RT-PCR foi precipitado com a adição de 1mL de etanol absoluto gelado, mais 40µL de acetato de sódio 3M e incubado à -20 ºC por 2 horas. Após a incubação o meio foi centrifugado à 12.000 rpm por 20 min à 4ºC. O sobrenadante foi descartado, o precipitado foi lavado com 500µL de etanol absoluto gelado e novamente centrifugado a 12.000 rpm por 5min à 4ºC. O sobrenadante foi descartado e o precipitado secou por uma hora. O precipitado foi ressuspenso em 5µL de água estéril e submetido em gel de agarose 0,8%. O fragmento foi purificado do gel de agarose, utilizando-se o “kit GLASSMILK®” (Sigma) de acordo com as normas do fabricante. Após a purificação, o fragmento foi inserido no vetor plasmidial pGEM®-T Easy (Promega) com T4 DNA ligase. - 21 A transformação bacteriana de E. coli foi promovida por eletroporação. As células eletrocompetentes foram retiradas do freezer -70ºC, colocadas no gelo e juntamente com as cubetas de eletroporação. Aproximadamente 25ng do vetor com o inserto foi adicionado às células eletrocompetentes em microtubos e imediatamente transferidos para a cubetas, evitando a formação de bolhas. Em seguida, as cubetas foram submetidas à eletroporação, com um pulso elétrico de 25µF de capacidade (2500V) e 200 ohm de resistência. Após a remoção da cubeta da câmara adicionou-se 1ml de meio SOC e as células foram suspensas cuidadosamente. Transferiu-se a suspensão celular para um microtubo e incubou-se a 37ºC por 1h. O meio foi centrifugado a 12.000 rpm por 5 min. 800µL do meio foi descartado e volume restante foi usado para plaquear placas contendo meio LB mais ampicilina e incubadas overnight a 37ºC. Após o crescimento, os clones positivos foram selecionados e incubados novamente em meio LB e ampicilina a 37ºC, overnight. Para a purificação do DNA plasmidial, foi utilizado o Plasmid Midi Kit (QIAGEN) e o sequenciamento foi realizado em um seqüenciador de nucleotídeos BigDye Terminator v3.0, modelo ABI 377XL (AppliedBiosystems). - 22 4- RESULTADOS 4.1- Estudo cinético da GSK-3β na embriogênese de R. microplus Sendo a GSK-3 uma enzima envolvida na regulação da expressão de PEPCK (Lochhead et al., 2001) e na regulação da síntese de glicogênio (MacAulay et al., 2005), resolvemos estudar o seu papel no metabolismo de glicogênio durante o desenvolvimento do nosso modelo de estudo, o Rhipicephalus (Boophilus) microplus. A caracterização da atividade de GSK-3β em ovos de R. microplus foi realizada em imunoprecipitados obtidos de homogenatos de ovos de diferentes estágios, ao longo da embrigênese (Figura 8). Foi observado que a atividade de GSK-3β, ensaiada a partir da hidrólise de [γ-32P] ATP, e incorporação do isótopo radioativo em um peptídeo comercial (CREBtide®, Calbiochem), varia durante a embriogênese. A maior contribuição da atividade se apresentou nos dias próximo ao período de transição do blastoderma sincicial para o celular. A partir desse momento se observa uma queda nos valores de atividade nos estágios finais da embriogênese. (Figura 8). Este resultado demonstra que a atividade de GSK-3β, pode estar regulando os níveis de glicogênio em homogenatos de ovos durante o desenvolvimento como demonstrado por Moraes e colaboradores (2007) (Figura 4). Atividade GSK-3β (%) - 23 - 100 90 80 70 60 50 40 30 20 10 0 0 2 4 6 8 10 12 14 16 Dias após a ovoposição Figura 8: Atividade de GSK-3β em homogenatos de ovos durante o desenvolvimento do R. microplus. Após a imunoprecipitação usando anticorpo anti GSK-3β, a atividade foi medida usando os pontos de maior atividade como percentual máximo de incorporação do radioisótopo [P32] no substrato específico (CREB). Os dados são médias de quatro experimentos diferentes (Logullo et al., 2007) 4.2- Atividade de GSK-3β em frações subcelular de ovos de R.microplus Diante das evidências da presença de GSK-3 em compartimentos subcelulares (Maurer et al., 2006; Caracciolo et al.,1998) e da sua fundamental participação em núcleos para desenvolvimento embrionário de vários modelos, inclusive invertebrados (Frame e Cohen, 2001), frações de núcleo e mitocôndria de ovos de Rhipicephalus (Boophilus) microplus foram obtidos para detecção imunológica de GSK-3 e de sua atividade. Por ensaio de western blot, foi detectada a presença de GSK-3, em frações de núcleos (Figura 9), usando anticorpo anti-GSK-3β (Sigma) que reconhece uma região C- - 24 terminal de um peptídeo de GSK-3β humanos. Logullo e colaboradores (2007) demonstraram que a GSK-3β encontra-se constitutivamente expressa durante todos os dias do desenvolvimento do carrapato R. microplus. Assim foi utilizado homogenato de ovos de 6º dia de desenvolvimento para se obter um perfil de comparação na detecção da proteína. A distribuição de GSK-3 nas frações nucleares mostrou-se heterogênea ao longo da embriogênese. No segundo dia de desenvolvimento foi detectada maior quantidade da proteína (Figura 9). A determinação de glicogênio nessas mesmas frações (Figura 10) mostrou que há uma queda nos níveis de glicogênio do segundo dia de desenvolvimento até o sétimo, com posterior re-síntese de glicogênio, a partir do 7º dia. Também foi detectado um forte sinal da presença de GSK-3β nos estágio finais da embriogênese (Figura 9). A atividade de GSK-3β nas frações de núcleo (Figura 11) demonstra ser coerente com as dosagens de glicogênio nesta fração (Figura 10), havendo uma elevação progressiva da atividade enzimática do 1º ao 12º dia do desenvolvimento. Posteriormente, no 15º e 19º dias, há uma diminuição da atividade e uma retomada, respectivamente. Assim, em momentos iniciais do desenvolvimento (1º e 6º dia) há uma diminuição dos níveis de glicogênio concomitante ao aumento da atividade da GSK-3β, que atinge o seu máximo por volta do 12º dia de desenvolvimento (Figura11). Após esse momento, a resíntese de glicogênio parece ser retomada e a atividade da GSK-3β volta a diminuir. GSK-3β β 2 9 12 15 21 H Dias após a ovoposição Figura 9: Detecção de GSK-3β β em frações de núcleos durante o desenvolvimento do embrião de R. microplus Amostras de fração de núcleo dos dias de desenvolvimento 2, 9, 12, 15, 21 e homogenato de ovo do dia 6 foram resolvidas em gel 10 % SDS-PAGE e transferidas para membrana de PVDF. Foi usado o anticorpo Anti- GSK-3β para análise. ng glicogênio/ µ g ptn - 25 - 1.4 0.9 0.4 0 2 4 6 8 10 12 14 16 18 20 Dias após a ovoposição Figura 10: Conteúdo de glicogênio em frações de núcleo durante o desenvolvimento do embrião de R. microplus A quantidade de glicogênio foi determinada por digestão com α-amiloglicosidase e o conteúdo de glicose foi medido utilizando o kit Glucox® 500 (Doles). Os resultados são representativos de quatro experimentos diferentes. 19 15 12 6 90 80 70 60 50 40 30 20 10 0 1 Atividade GSK-3β (%) em frações de núcleo - 26 - Dias após a ovoposição Figura 11: Atividade de GSK-3β em frações de núcleo durante o desenvolvimento do R. microplus. A atividade GSK-3β foi medida por percentual máximo de incorporação do radioisótopo [γ-32P] ATP no substrato específico (CREB). Os dados são representativos de três experimentos diferentes. - 27 - A GSK-3β foi identificada nas frações mitocondriais, sendo mais significativa nos 2º e 15º dias da embriogênese, ainda que nos dias restantes, o sinal tenha sido positivo, porém heterogêneo (Figura 12). Os níveis de glicogênio nas frações foram dosados, porém não foi observada a presença deste. Apesar disto, foi detectado atividade de GSK3β em alguns dias do desenvolvimento nas frações de mitocôndria (Figura 13). Assim se pode observar atividade de GSK-3β no 6º e no 19º dias do desenvolvimento, indicando uma possível ativação de fatores apoptóticos envolvidos na diferenciação celular. Nos outros dias do desenvolvimento observa-se uma atividade negativa, devido ao fato de os controles terem apresentados maior incorporação do radioisótopo γ[P32] do o ensaio. GSK-3β β Dias 2 9 12 15 21 H Dias após a ovoposição Figura 12: Detecção de GSK-3β β em frações de mitocôndria durante o desenvolvimento do embrião de R. microplus Amostras de fração de mitocôndria dos dias de desenvolvimento 2, 9, 12, 15, 21 e homogenato de ovo do dia 6 foram resolvidas em gel 10 % SDS-PAGE e transferidas para membrana de PVDF. Foi usado o anticorpo Anti-GSK-3β para análise. 80 60 40 20 19 15 6 -20 12 0 1 Atividade GSK-3β (%) - 28 - -40 Figura 13: Atividade de GSK-3β em frações de mitocôndria durante o desenvolvimento do R. microplus. A atividade GSK-3β foi medida por percentual máximo de incorporação do radioisótopo [γ-32P] ATP no substrato específico (CREB). 4.3- Efeitos da Injeção de inibidores de GSK-3 em teleógenas de R. microplus A injeção em teleógenas de substâncias que interferem no desenvolvimento do embrião tem sido uma alternativa para se simular os efeitos destes compostos in vivo. Assim a partir dos dados que detectaram a presença e a atividade de GSK-3 em ovos de carrapato, foi proposta a administração de inibidores (SB415281, Insulina, LiCl) anteriormente descritos. Os efeitos das injeções destes inibidores foram observados na mortalidade e na ovoposição das fêmeas injetadas (tabela1). Os grupos em que foram injetados 50µM de SB415281 e 8µM Insulina tiveram uma mortalidade de 5% e 10% - 29 respectivamente, sete dias após a injeção. O grupo que foi injetado com a solução 50mM de LiCl a mortalidade atingiu 80% no sétimo dia após a injeção e as teleógenas sobreviventes não foram capazes de fazer a ovoposição. Nos grupos controle e nos injetados com SB415281 e Insulina não foram observado diferenças no efeito da injeção em relação a massa de ovos postos. Os ovos foram coletados 3 dias após a injeção e o desenvolvimento foi acompanhado nos dias 1, 5, 11 , onde foram tomadas alíquotas para a verificação dos efeitos dos inibidores de GSK-3 na distribuição de glicogênio nestes ovos (Figura 14). O conteúdo de glicogênio nos ovos de 1º dia nos grupos onde foram injetados inibidores teve um aumento quando comparados com o controle, principalmente o grupo em que foi injetado insulina, de aproximadamente 26%. Na dosagem de glicogênio nos ovos de 5º de desenvolvimento houve um aumento do conteúdo de glicogênio no grupo que foi injetado com insulina se comparados com o controle. No 11º dia de desenvolvimento não foi detectada diferença no conteúdo de glicogênio. Teleógenas vivas 1ºdia após injeção 3ºdia após injeção 7ºdia após injeção Mortalidade (%) mg ovos/ teleógena DMSO 20 20 20 0 93,55 SB415281 20 20 18 10 105,88 Insulina 20 19 19 5 94,10 LiCl 18 15 4 80 0 Inibidores Tabela 1: Efeitos da injeção de inibidores de GSK-3β β na mortalidade de teleógenas e na ovoposição. - 30 - ng glicogênio /µ g ptn 2.5 DMSO 50µM SB415281 8µM Insulina 2.0 1.5 1.0 0.5 0.0 1 5 11 Dias após a ovoposição Figura 14: Dosagem de glicogênio em ovos de teleógenas injetadas com inibidores de GSK-3 Os ovos foram coletados 3 dias após a injeção e alíquotas no 1º, 5º, 11º dias do desenvolvimentos para a dosagem de glicogênio A quantidade de glicogênio foi determinada por digestão com α-amiloglicosidase e o conteúdo de glicose foi medido utilizando o kit Glucox® 500 (Doles). 4.4- Clonagem de GSK-3β de ovos de R. microplus Os primers “forward” e “reverse” específicos para a região ORF do gene de GSK-3β foram desenhados a partir da seqüência de um fragmento de 600 pb de GSK-3β de R. microplus clonado. O primer “forward” possui um seqüência para o ATG inicial e um sítio para a enzima de restrição NdeI. O primer “reverse” possui uma seqüência de stop códon, uma cauda de histidina (para futura purificação da proteína recombinante) e um sítio para a enzima de restrição EcoRI. Um fragmento de aproximadamente 1200 pb foi amplificado (Figura 15). Então, o produto do PCR foi clonado no vetor pGEMT-Easy e as bactérias E. coli foram transformadas. Os clones positivos foram selecionados e seqüenciados (Figura 16). - 31 A seqüência deduzida de aminoácidos mostrou marcada similaridade com GSK-3. A seqüência completa do cDNA contem uma região ORF de 1200 bp (número de acesso GenBank EF142066). A seqüência foi analisada usando o programa ScanProsite. Dois possíveis sítios de fosforilação, serina 9 e tirosina 215 envolvidos na ativação e na inativação de GSK-3β estão presentes na seqüência de GSK-3β de R. microplus, indicados pelas setas vermelhas. A presença destes sítios de fosforilação podem propor que o mecanismo de regulação da GSK-3β de R. microplus seja similar aos já descrito para esta enzima em outros modelos, devido da sua alta identidade. A comparação das seqüências de aminoácidos GSK-3β de R. microplus mostrou identidade de 76% com a de D. rerio, 76% com a de A. mellifera, 75% com a de M. musculus, 75% com de B. Taurus, 75% com a de X. laevis e 62% com a de D. melanogaster. 23130 9416 6557 4361 2322 2027 ~1200 pb 564 1 2 3 Figura 15: Amplificação por RT-PCR do cDNA de GSK-3β. (1, 3) Amplificado de R. microplus, (2) controle negativo, PCR sem cDNA. As amostras foram submetidas à eletroforese de DNA em gel de agarose 0,8 % com cloreto de etídio. - 32 - Firura 16: Alinhamento comparativo da seqüência de aminoácido de GSK-3β β de R. microplus, D. melanogaster, D. rerio, A. mellifera, B. taurus, X. leavis, M. musculus analizado por Blast. Os resíduos comuns entre as todas as sete proteínas são marcados em pretos e o restante em gradiente de cinza de acordo com o número de resíduos em comum. As setas vermelhas indicam os resíduos de fosforilação que regulam a atividade. - 33 5- DISCUSSÃO O carrapato bovino Rhipicephalus (Boophilus) microplus se alimenta exclusivamente de sangue bovino, o que suporta a manutenção de suas atividades, incluindo a ovogênese e posteriormente o desenvolvimento de seus embriões. Como conseqüência da digestão, o alimento processado é utilizado para síntese de vitelina (VT), proteína responsável pelo suporte energético do ovo para formação do embrião (Sonenshine, 1991). Estudos sobre o metabolismo do desenvolvimento deste carrapato demonstraram que os níveis de proteína se matêm constantes, desde os estágios iniciais até a formação do embrião (Campos et al., 2006). Por outro lado, conteúdo de glicogênio é consumido até o sexto dia para dar suporte à intensa celularização do sincício. A partir deste momento, há uma re-síntese do conteúdo de glicogênio, com formação de guanina e ativação de PEPCK (Moraes et al., 2007). A GSK-3β é descrita como uma das enzimas envolvidas na regulação da expressão de PEPCK, por ativar alguns fatores de transcrição, sendo o CREB um deles (Finlay et al., 2004; Lochhead et al., 2001). Esta enzima já foi descrita em mais de uma centena de modelos experimentais, sendo bastante conservada em todos (Frame & Cohen, 2001). Possui um sítio quinase que representa mais de 30% de sua seqüência, onde se encontram os principais sítios de regulação (Dajani et al., 2001). A clonagem desta enzima em R. microplus revelou que sua seqüência de aminoácidos traduzida obedece aos parâmetros de similaridades com as GSK-3β de outros modelos (Figura 16). No R. microplus, Logullo e colaboradores (2007) identificaram a isoforma GSK-3β e demonstraram que esta é constantemente expressa durante o desenvolvimento dos embriões. Ainda neste trabalho sugere-se um envolvimento da GSK-3β na regulação de expressão de PEPCK. A partir daí surgiu o interesse em estudar o envolvimento da enzima GSK-3β no controle da gliconeogênese e principalmente com o fenômeno de reabastecimento de glicose que culmina no acúmulo de glicogênio nestes ovos (Moraes et al., 2007). A GSK-3β é uma quinase que é inibida por fosforilação por PKB (ou Akt) quando a via de sinalização por insulina é ativada (Frame & Cohen, 2001). Outros inibidores que mimetizam o efeito da insulina são capazes de inibirem a GSK-3β (Coghlan et al., 2000; Leost et al., 2000). A inibição da GSK-3β está diretamente envolvida com a regulação da - 34 síntese de glicogênio, permitindo que a GS se torne ativa (MacAulay et al., 2005). Assim em momentos em que a GSK-3β está inibida, a GS não é mais fosforilada por esta quinase, se tornando ativa. Coerentemente com este fenômeno, observamos que o perfil de atividade da GSK-3β (Figura 8) em homogenatos de ovos R. microplus é inversamente proporcional ao conteúdo glicogênio ao longo do desenvolvimento (Figura 4) (Moraes et al., 2007). Ainda nesse trabalho, há a sugestão de uma correlação entre re-síntese de glicogênio com a ativação da via de gliconeogênese, por aumento da atividade da PEPCK, principal enzima desta via. Esta hipótese foi corroborada quando se demonstrou o envolvimento da atividade de GSK-3β com a expressão de PEPCK (Logullo et al., 2007). Sendo assim, há correlações entre atividades da GSK-3β e síntese de glicogênio em homogenatos totais e em frações de núcleos de ovos durante o desenvolvimento do carrapato R. microplus (Figuras 4, 8, 10 e 11) que corroboram com as hipóteses propostas por Moraes e colaboradores (2007) e Logullo e colaboradores (2007). Caracciolo e colaboradores (1998) demonstraram que o glicogênio é um elemento fundamental na formação de núcleo e que existe o envolvimento de GSK-3β neste processo. Dessa forma a GSK-3β poderia estar regulando a síntese de glicogênio por inibição da GS ou a degradação de glicogênio por ativação da PP-1 (Caracciolo et al., 1998). Outros autores também demonstraram a presença e envolvimento de GSK-3β no controle de expressão gênica (Wang e Wynshaw, 2004; Frame & Cohen, 2001). Uma outra abordagem em relação a GSK-3, é o seu envolvimento com a ativação de fatores apoptóticos em mitocôndrias (Maurer et al., 2006), fenômeno importante na diferenciação celular durante a embriogênese (Freitas et al.,2007). A partir daí iniciou-se estudos sobre a presença e a atividade de GSK-3β em frações de núcleo e mitocôndria no modelo experimental o carrapato R. microplus. Observa-se a presença desta enzima apenas em alguns estágios embrionários tanto em núcleo quanto em mitocôndrias (Figuras 9, 12). Diferentemente, Logullo e colaboradores (2007) observaram que em homogenatos totais há uma distribuição constante da expressão de GSK-3, tanto por western-blot quanto por RT-PCR, neste mesmo modelo. Também foi descrito que em P. falciparum a expressão de GSK-3β é constante em vários estágios de (Droucheaua et al., 2004), mas para Xenopus a expressão deste gene não é constante durante a embriogênese (He et al., 1995). - 35 A dosagem do perfil de glicogênio em frações de núcleo (Figura 10) demonstrou que há uma diminuição dos níveis desse composto até o sétimo dia do desenvolvimento do embrião. Provavelmente esta reserva pode estar abastecendo energeticamente a intensa divisão mitótica que marca a fase de formação do sincício (Campos et al., 2006). Sugere-se então que o glicogênio nuclear poderia estar envolvido tanto na formação de núcleos como no controle das reservas energéticas durante a formação destes embriões. Já nas frações de mitocondriais não foi possível detectar o glicogênio. Por outro lado, foi detectada a presença de GSK-3β (Figura 12). Porém, as frações de 2º e 21º dias apresentaram maior quantidade da proteína, o que não condiz com o ensaio de atividade GSK-3β nesse compartimento (Figura13). A GSK-3β demonstrou ser mais ativa no 6º dia e posteriormente no final do desenvolvimento, no 19º dia. Não se sabe ainda qual seria a função da GSK-3β nas frações mitocondriais do modelo R. microplus, mas também poderia estar regulando a apoptose de acordo com alguns autores (Juhaszova et al., 2004; Maurer et al., 2006). Estudo de injeção em hemocele de R. microplus de anticorpos ou por RNAi para verificar o efeito na embriogênese, representa uma alternativa que permite os estudos in vivo, mas é altamente dificultado devido a impermeabilidade dos ovos. Por outro lado a injeção afeta a sobrevivência, o peso e a ovoposição desses carrapatos (de la Fuente e Kocan, 2006). A injeção de inibidores de GSK-3β para ensaiar os seus efeitos durante a embriogênese, permite que estes inibidores sejam absorvidos pelos tecidos ovarianos do carrapato e transportados para os ovócitos, precursores dos ovos ainda permeáveis. No grupo de teleógena em que foi injetado uma solução de 50mM LiCl, os carrapatos fêmeas não foram capaz de fazer a ovoposição. Em recombinantes de GSK-3β de Dictyostelium (ameba) que possuem 71% de identidade em seus sítios catalícos com GSK-3β de humanos, a atividade é totalmente inibida com 100mM de LiCl (Ryves & Harwood, 2001). Por isso, é possível que a concentração de LiCl tenha sido alta suficientes para interferir no mecanismo de ovoposição, não permitindo que pudesse ser analisado os seus efeitos no metabolismo do glicogênio no carrapato, além de inibir outras enzimas kinases (Berrigde et al., 1989; Davies et al., 2000). Por outro lado, em experimento anterior de injeção de inibidores, 50µM de LiCl não apresentou diferença significativa nos níveis de glicogênio durante o desenvolvimento (dados não mostrados). Quanto ao efeito dos outros - 36 inibidores (Figura 14), SB415281 e insulina, os níveis de glicogênio aumentaram no 1º dia do desenvolvimento para ambos. Assim, esses inibidores demonstram estar afetando de alguma forma a síntese de glicogênio neste compartimento. Já no 5º dia do desenvolvimento, foi visto aumento dos níveis de glicogênio somente no grupo em que foi injetada insulina o que indica que o efeito do SB415281 esteja sendo de alguma forma inibido no que diz respeito ao metabolismo de glicogênio no ovo desse carrapato. Pelo mesmo motivo não foi detectado diferença nos ovos 11º dia do desenvolvimento em nenhum dos grupos. Quanto a eclosão dos ovos em que foi injetado os inibidores, percebeu-se uma diminuição na eficiência de eclosão, porém esse dado não foi avaliado estatisticamente. Em perspectivas futuras, pretende-se estudar o efeito da inibição de GSK-3β em cultura de células embrionárias no metabolismo de glicogênio, como na ativação da GS e das vias gliconeogênicas, incluindo a ativação de fatores de transcrição envolvidos nestes mecanismos. Uma alternativa para o estudo da inibição GSK-3β é a alimentação artificial, utilizando capilares, em carrapatos fêmeas na fase paternógena de desenvolvimento (de la Veja et al., 2000). Esta seria a forma mais próxima da via natural de alimentação, sem causar efeitos colaterais como os causados pela injeção, como o extravasamento de hemolinfa e corpo gorduro, que por si só refletiriam efeitos na formação e no desenvolvimento desses ovos. Outro aspecto importante é a obtenção da GSK-3 recombinante, que se encontra em estágio avançado. Com isso, poderemos fazer um estudo detalhado de fatores regulatórios envolvidos em sua atividade. - 37 6- CONCLUSÕES Diante de resultados dos obtidos nesta dissertação, pode- se concluir que: A GSK-3β de R. microplus apresenta alta identidade com os modelos D. menalogaster, D. rerio, A. melífera, B. taurus, X. laevis, M. muculus, incluindo os seus sítios de regulação de atividade; Existe uma correlação entre atividade de GSK-3β e o níveis glicogênio durante o desenvolvimento do carrapato R. microplus; A GSK-3β está presente e ativa em frações de núcleo e mitocôndria em homogenatos de ovos de R. microplus; A injeção de inibidores de GSK-3β em teleógenas de R. microplus pode alterar o desenvolvimento do embrião. - 38 - 7- REFERÊNCIAS BIBLIOGRÁFICAS Abreu, L. A., Valle, D., Manso, P. P., Façanha, A. R., Pelajo-Machado, M., Masuda, H., Masuda, A., Vaz, I. S. Jr., Lenzi, H., Oliveira, P. L., Logullo, C. (2004) Proteolytic activity of Boophilus microplus Yolk pro-Cathepsin D (BYC) is coincident with cortical acidification during embryogenesis. Insect Biochem Mol Biol. 34:443-449. Barker S. C., Murrell, A. (2002) Phylogeny, evolution and historical zoogeography of ticks: a review of recent progress. Experimental and Applied Acarology 28: 55-68. Bate, M., Marquardt, W. C. (1993) The development of Drosophila melanogaster. Cold Spring Harbor Laboratory Press, New York. Beaty, B. J., Marquardt, W. C. (1996) The biology of disease vectors, University Press of Colorado. Berridge, M. J., Downes, C. P., Hanley, M. R. (1989) Neural and developmental actions of lithium: a unifying hypothesis. Cell 59:411- 419. Bijur, G. N., Jope, R. S. (2001) Proapoptotic stimuli induce nuclear accumulation of glycogen synthase kinase-3 beta. J. Biol. Chem. 276: 37436-37442. Bradford, M. M. (1976) A rapid and sensitive method for the quantification of microgram quantities of protein utilizing the principle of protein-dye binding. Anal. Biochem., 72: 248254. Campos, E., Moraes, J., Façanha, A. R., Moreira, E., Valle, D., Abreu, L., Manso, P. P. A., Nascimento, A., Pelajo-Machado, M., Lenzi, H., Masuda, A., Silva Vaz Jr. I., Logullo, C. (2006) Metabolic activity of Boophilus microplus during embryonic development: a comparison with morphogenetic movements. Veterinary Parasitology 138: 349–357. - 39 - Caracciolo, M. R., Berlin, W. K., Miller, M. W., Hanover, J.A. (1998) Nuclear Glycogen Synthase Kinase 3. Biochim. Biophys. Acta 249: 422-427. Coghlan, M. P., Culbert, A. A., Cross, D. A., Corcoran, S. L., Yates, J. W., Pearce, N. J., Rausch, O. L., Murphy, G. J., Carter, P. S., Roxbee, C. L. (2000) Selective small molecule inhibitors of glycogen synthase kinase-3 modulate glycogen metabolism and gene transcription. Chem. Biol. 7: 793-803. Cramer, L. G., Carvalho, L. A. F., Bridi, A. A., Amaral, N. K., Barrick, R. A. (1988) Efficacy of topically applied ivermectin against Boophilus microplus in cattle. Vet. Parasitol. 29: 341-349. Dajani, R., Fraser, E., Roe, S. M.,Young, N., Good, V., Dale, T. C., Pearl, L. H. (2001) Crystal Structure of Glycogen Synthase Kinase 3: Structural Basis for Phosphate-Primed Substrate Specificity and Autoinhibition Cell, Cell Press 105: 721–732. Davies, S. P., Reddy, H., Caivano, M., Cohen, P. (2000) Specificity and mechanism of action of some commonly used protein kinase inhibitors. Biochem. J. 351, 95-105. de la Fuente, J., Kocan, K. M. (2006) Strategies for development of vaccines for control of ixodid tick species. Parasite Immunol. 28: 275-283. de la Fuente, J., KocanK, M. (2003) Advances in the identification and characterization of protective antigens for development of recombinant vaccines against tick infestations. Exp. Rev. Vaccines 2:583-593. de la Vega, R., Diaz, G., Finlay, L. (2000) Artificial feeding in Boophilus microplus (Acari:Ixodidae) through micropipettes. Ann N Y Acad Sci 916: 315-319. - 40 Droucheaua, E., Primota, A., Thomasa, V., Matteib, D., Knockaerta, M., Richardsonc, C., Sallicandrod, P., Alanod, P., Jafarshade, A., Barattea, B., Kunickf, C., Parzyg, D., Pearlc, L., Doerige, C., Meijera, L. (2004) Plasmodium falciparum glycogen synthase kinase-3: molecular model, expression, intracellular localization and selective inhibitors. Biochemical et Biophysica Acta 1697 181– 196. Eldar-Finkelman, H. (2002) Glycogen synthase kinase 3: an emerging therapeutic target. Trends Mol. Med. 8:126–132. Embi, N., Rylatt, D. B., Cohea, P. (1980) Glycogen synthase kinase-3 from rabbit skeletal muscle. Separation from cyclic-AMP-dependent protein kinase and phosphorylase kinase. Eur. J. Biochem, 107: 519-527. Estrada-Penã, A., Jongejan, F. (1999) Ticks feeding on humans: a review of records on humans- biting Ixodidoidea with special references to pathogen transmission. Exp Appl. Acarol 23: 685-715. Finlay, D., Patel, S., Dickson, L. M., Shpiro, N., Maerquez, R., Rhodes, C. J., Sutherland, C. (2004) Glycogen Synthase Kinase-3 regulates IGFBP-I gene transcription through thr Thymine- rich Insulin Response Element. BMC Molecular biology 5: 15- 28. Flechtmann, C. H. W. (1977) Elementos de acarologia. Livraria Nobel, São Paulo. Frame, S., Cohen, P. (2001) GSK-3 takes centre stage more than 20 years after its discovery. Biochem.J. 359:1-16. Freitas, D. R. J., Rosa, R. M., Moura, D. J., Seitz, A. L., Colodel, E. M., Driemeier, D., Vaz Jr, I. S., Masuda, A. (2007) Cell death during preoviposition period in Boophilus microplus tick. Vet Parasitol. 144:321-327. - 41 Galetic, I., Andjelkovi, M., Meier, R., Brodbeck, D., Park, J., Hemmings, B. A. (1999). Mechanism of Protein Kinase B Activation by Insulin/ Insulin- Like growth factor-1 revealed by specific inhibitors of Phosphoinositide 3- Kinase _ Significance for Diabets and Cancer. Pharmocol. Ther. 82: 409- 425. Gonzales, J. C., Silva, N. R., Franco, N. (1974) A vida livre do Boophilus microplus. Arq. Fac. Vet. UFRGS. RG. 3: 21-28. Gonzales, J. C.; Silva, N. R.; Wagner, E. M. (1975) O ciclo parasitário do Boophilus microplus em bovinos estabulados. Arq. Fac. Vet. UFRGS, 2: 25 – 34. Gonzales, J.C. (1995) O controle do carrapato do boi, 2a ed. Porto Alegre. Edição do autor. Graf, J. F., Gogolewski, R., Leach- Bing, N. (2004) Tick control; an industry point of view. Parasitol 129: 427-442. Grimes, C. A., Jope, R. S. (2001) The multifaceted roles of glycogen synthase kinase 3 in cellular signaling. Prog. Neurobiol. 65, 391–426. Hanada, M., Feng, J., Hemmin, B. A. (2003) Structure, regulation and function of PKB/ AKT _ a major therapeutic target. BBA 1697: 3-16. Haq, S., Michael, A., Andreucci, M., Bhattacharya, K., Dotto, P., Walters, B., Woodgett, J., Kilter, H., Force, T. (2003) Stabilization of b-catenin by a Wnt-independent mechanism regulates cardiomyocyte growth. Proc. Natl. Acad. Sci. U. S. A. 100: 4610-4615. Hardt, S. E., Sadoshima, J. (2002) Glycogen synthase kinase-3b: a novel regulator of cardiac hypertrophy and development. Circ. Res. 90: 1055-1063. - 42 Hartl, P., Olson, E., Dang, T., Forbes, D. J. (1994) Nuclear assembly with lambda DNA in Fractionated Xenopus egg Extractors: an Unexpected role in formation of a Higher Order chromatin Intermediate. Jounal of Cell Biology 124:235- 248. He, X., Saint-Jeannet, J. P., Woodgett, J. R., Varmus, H. E., Dawid, I. B., (1995) Glycogen synthase kinase-3 and dorsalventral patterning in Xenopus embryos. Nature 374: 617-622. Hill, M. M., Hemmings, B. A. (2002) Inhibition of protein kinase B/Akt. Implications for cancer therapy. Pharmacol. Ther. 93: 243–251. Hoeflich, K. P., Luo, J., Rubie, E. A., Tsao, M. S., Jin, O., Woodgett, J. R. (2000) Requirement for glycogen synthase kinase-3beta in cell survival and NF-kappaB activation. Nature 406:86- 90. Hopkins, T. J.; Woodley, I. R., Blackwell, R. (1985) The safety and efficacy of flumethrin pour-on used to control Boophilus microplus on cattle in Australia. Vet. Med. Rev., 2: 112125. Horak, I. G., Camicas, J., Keirans, J. E. (2002) The Argasidae, Ixodidae and Nuttalliellidae (Acari:Ixodida): a world list of valid tick names Experimental and Applied Acarology 28: 27–54. Jope, R. S. (1999) Anti-bipolar therapy:mechanism of action of lithium. Mol. Psychiatry 4:117–128. Jope, R. S., Johnson, G. V. G. (2004) The glamour and gloom of glycogen synthase kinase-3, Trends in Biochemical Sciences 29, 95-102. Juhaszova, M., Zorov, D. B., Kim, S. H., Pepe, S., Fu, Q., Fishbein, K. W., Ziman, B. D., Wang, S., Ytrehus, K., Antos, C. L., Olson, E. N., Sollot, S. J. (2004) Glycogen synthase - 43 kinae-3β mediates convergence of protection signaling to inhibit the mitochondrial permeability transition pore. Jounal of Clinical Investigation 113: 1535-1549 Keirans, J. E. (1992). Systematics of the Ixodida (Argasidae, Ixodidae, Nuttalliellidae): An overview and some problems. In Tick Vector Biology. Medical and Veterinary Aspects (B. H. Fivaz, T.N. Petney, and I.G. Horak,) ed. Springer- Verlag, Berlin, pp. 1-21. Keirans, J.. E., Robbins, R. G. (1999) A world checklist of genera, subgenera, and species of ticks (Acari: Ixodida) published from 1973- 1997. J. Vector Ecol. 24: 115-129. Klein, P. S., Melton, D. A. (1996) A molecular mechanism for the effect of lithium on development. Proc. Natl. Acad. Sci. U. S. A. 93: 8455–8459. Klompen, H. (2005) Ticks, the Ixodida In: Marquardt, W. C., Black, W. C., Freier, J. E., Hagedorn, H. H., Hemingway, J., Higgs, S., James, A. A., Kondratieff, B., Moore, C. G. Biology of Disease Vectors. 2ºed Colorado: Elsevier Academic Presss, p. 45-55. Kozlovsky, N., Belmaker, R. H., Galila, A. (2002) GSK-3 and the neurodevelopmental hypothesis of schizophrenia. Eur. Neuropsychophar. 12:13–25. Labruna, M. B., Veríssimo, C. J. (2001) Observações sobre Boophilus microplus (Acari:Ixodidae) em bovinos mantidos em rotação de pastagem, sob alta densidade animal, Arq. Ins. Biol. USP, São Paulo, 68: 115-120. Leal, A. T., Seixas, A., Pohl, P.C.,. Ferreira, C. A. S, Logullo, C., Oliveira, P. L.,. Farias, S. E., Termignoni, C., Vaz Jr, I. S., Masuda, A, (2006) Vaccination of bovines with recombinant Boophilus Yolk pro-Cathepsin Veterinary Immunology and Immunopathology 114: 341-345. Leost, M., Schultz, C., Link, A., Wu, Y., Biernat, J., Mandelkow, E., Bibb, J. A., Snyder, G. L., Greengard, P., Zaharevitz, D. W., Gussio, R. (2000) Paullones are potent inhibitors - 44 of glycogen synthase kinase-3b and cyclin-dependent kinase 5/p25 Eur. J. Biochem. 267:5983-5994 Liao, J., Barthel, A., Natakatani, K., Roth, R. A. (1998) Activation of Protein Kinase B/ Akt is Sufficient to repress the Glucocorticoid and cAMP Induction of Phosphoenolpyruvate Carboxykinase Gene. JBC, 273: 27320- 27324. Linseman, D. A., Butts, B. D., Precht, T. A., Pheps, R. A., Le, S. S., Laessig, T. A., Bouchard, R. J., Florez-McClure, M. L., Heidenreich, K. A. (2004) Glycogen Synthase Kinase-3β Phosphorylates Bax and Promotes Its Mitochondrial Localization during Neuronal Apoptosis. Jounal Neuroscience 24: 9993-10002. Lochhead, P. A., Coghlan, M., Rice, S. Q. J., Sutherland, C. (2001) Inhibition of GSK-3 selectively reduces Glucose- 6- Phosphatase and Phosphoenolpyruvate Carboxykinase Gene. Expression. Diabets 50: 937-944. Logullo, C., Moraes, J., Dansa-Petretski, M., Vaz Jr., I. S., Masuda, A., Sorgine, M. H. F., Braz, G. R., Masuda, H., Olveira, P. L. (2002) Binding and storage of heme by vitellin fron the cattle tick Boophilus microplus. Insect Bioch. Mol. Biol., 32: 1805 –1811. Logullo, C., Vaz Jr., I. S., Sorgine, M. H. F., Paiva-Silva, G. O., Faria, F. S., Zingali, R., Lima, F. R., Abreu, L., Oliveira, E. F., Alves, E. W., Masuda, H., Gonzales, J. C., Masuda, A., Oliveira, P. L. (1998) Isolation of a aspartic proteiase precursor from the egg of a hard tick, Boophilus microplus. Parasitol. 116:525-532. Logullo, C., Witola, W. H., Andrade, C., Gomes, J., Vaz Jr., I.S., Imamura, S., Konnai, S., Ohashi, K., Onuma, M. (2007) GSK-3β positively regulates the PEPCK gene expression in tick embryos (Em Submição). MacAulay, K., Blair, A. S., Hajduch, E., Terashima, T., Baba, O., Sutherland, C., Hundal, H. S. (2005) Constitutive Activation of GSK3 Down- regulates Glycogen Synthase - 45 Abundance and Glycogen Deposition in Rat Skeletal Muscle Cells Journal Biological Chemistry 280 : 9509-9518. Manoukian, A. S., Woodgett, J. R. (2002) Role of glycogen synthase kinase-3 in cancer: regulation by Wnts and other signaling pathways.Adv. Cancer Res. 84:203–229. Maurer, U., Charvet, C., Wagman, A. S., Dejardin, E., Green, D. R. (2006) Glycogen Synthase Kinase-3 Regulates Mitochondrial Outer Membrane Permeabilization and Apoptosis by Destabilization of MCL-1 Molecular Cell 21, 749–760. McKosker, P.L. (1981) The global importance of Babesiosis. In Babesiosis. Ristic, M., J.P. Kreier, Academic Press. New York. Moraes, J., Galina, A., Alvarenga, P. H., Rezende, G. L., Masuda, A., Vaz Jr, I., Logullo, C. (2007) Glucose metabolism during embryogensis of the hard tick Boophilus microplus. Comparative Biochemistry and Physiology,146: 528–533. Mukai, F., Ishiguro, K., Sano, Y., Fujita, S. C. (2002) Alternative splicing isoform of tau protein kinase I/glycogen synthase kinase 3beta. J Neurochem. 81:1073-1083. Nari, A. (1995) Strategies for the control of one-host ticks and relationship with tickborne diseases in South America. Vet. Parasitol., 57: 153-165. Nikoulina, S. E., Ciaraldi, T. P., Mudaliar, S., Mohideen, P., Carter, L., Henry, R. R., (2000) Potential role of glycogen synthase kinase-3 in skeletal muscle insulin resistance of type 2 diabetes. Diabetes 49: 263–271. Parola, P., Raoult, D. (2001) Tick- borne bacterial diseases emerging in Europe. Clin Microbiol Infest 7:80-83. - 46 - Pereira, M.C. (1982) Boophilus microplus: Revisão Taxonômica e morfo-biológicaManual Quimio, Divisão de Veterinária. Phiel, C. J., Klein, P. S. (2001) Molecular targets of lithium action. Annu. Rev. Pharmacol. Toxicol. 41, 789–81. Ryves, W. J., Harwood, A. J. (2001) Lithium inhibits glycogen synthase kinase-3 by competition for magnesium. Biochem. Biophys. Res. Commun. 280: 720-725. Salerno, A. P., Dansa-Petretski, M., Silva-Neto, M. S. L., Coelho, H. S. L., Masuda, H. (2002) Rhodnius prolixus vitellin is composed of three different populations: comparison with vitellogenin. Insect Biochem. Molec. Biol. 32:709-717. Seifert, G. W., Springell, P. H., Tatchel, l R.J. (1968) Radioactive studies on the feeding of larvae, nymphs and adults ofthe cattle tick Boophilus microplus (Canestrini). Parasitology. 58: 415-430. Sonenshine, D. E. (1991) Biology of ticks. New York, Oxford University Press. Sutherst, R. W., Maywald, G. F., Kerr, J. D., Siegeman, D. A. (1983) The effect of the cattle tick (Boophilus microplus) on the growth of Bos indicus x Bos taurus steers. Australian Journal of Agricultural Research. 34: 317-327. Tong, H., Imahashi, K., Steenbergen, C., Murphy, E. (2002). Phosphorylation of glycogen synthase kinase-3beta during preconditioning through a phosphatidylinositol-3kinase-dependent pathway is cardioprotective. Circ. Res. 90:377–379 - 47 Towbin, H., Staehelin, T., Gordon, J. (1979) Electrophoretic transfer of proteins from polyacrilamide gels to nitrocellulose sheets: procedures and some applications, Proc. Nat. Acad. Sci., 76: 4350-4354. Vaz Jr, I. S., Logullo, C., Sorgine, M., Velloso, F. F., Lima, M. F. R., Gonzáles, J. C., Masuda, H., Oliveira, P. L., Masuda, A. (1998) Immunization of bovines with an aspartic proteinase precursor isolated from Boophilus microplus eggs Vet. Immunol. And Immunopathology 66:331-341 Wang, J., Wynshaw- Boris, A. (2004) The canonical Wnt pathway in early mammalian embryogenesis and stem cell maintenance/ differentiation Curr Opin Genet Dev 14: 1-7 Willadsen, P. (2004) Anti- tick vaccines. Parasitol 129: 267-387. Zong, W. X., Lindsten, T., Ross, A. J., MacGregor, G. R., Thompson, C. B. (2001) BH3only proteins that bind pro-survival Bcl-2 family members fail to induce apoptosis in the absence of Bax and Bak. Gene Dev 15: 1481- 1486.
Baixar