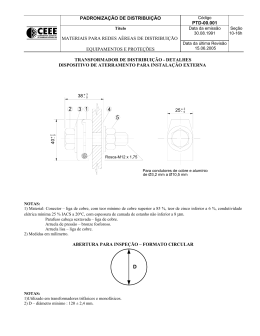
1 Medidas de Geração de espécies reativas causadas por diferentes complexos de cobre Lago C.C.Larissa 1 e Cerchiaro Giselle1 1 Universidade federal do ABC, Centro de ciências naturais e humanas, Santo André-sp, Brasil. Este trabalho analisou a formação de radicais livres devido à interação com o cobre sob diversas formas, em diferentes classes de complexos. Pode-se medir a formação de radicais totais, como também especificamente a formação de radicais hidroxila neste sistema oxidante. Os resultados obtidos foram comparados com os efeitos experimentais obtidos com os diferentes complexos de cobre no cultivo de células tumorais de mamíferos. Pode-se concluir há muitas interações diferentes atuando no meio biológico. Palavras Chave— Radicais livres, cobre, peptídeos, espectroscopia. I. INTRODUÇÃO N os últimos tempos a preocupação com a patologia ocasionada por radicais livres incentivou diversas pesquisas neste campo.1-5 Esses estudos propiciaram um melhor entendimento do assunto, levando a um avanço significativo na área. Radicais livres são caracterizados por moléculas extremamente reativas que possuem orbitais com um ou mais elétrons desemparelhados.6 As espécies reativas de oxigênio (ERO) e as espécies reativas de nitrogênio (ERN), chamados usualmente por radicais livres, influenciam no organismo causando dano celular mas também sabe-se que desempenham um importante papel fisiológico nos seres vivos.1 Os radicais livres são formados nas mitocôndrias, no citoplasma ou na membrana celular, e geralmente danificam macromoléculas como proteínas, lipídeos e DNA. Quando em excesso ERO e ERN irão causar o estresse oxidativo, o qual está sendo estudado podendo estar envolvido em algumas doenças como: diabetes, doenças neurodegenerativas, câncer e cardiopatias. Sabe-se que metais de transição, como ferro e cobre, são catalisadores de reações na oxidação de biomoléculas, logo aumentam a velocidade da geração de radicais livres.5 O Cobre é o terceiro metal traço mais abundante em mamíferos7, e possui dos dois níveis oxidativos +2 e +1. Portanto há uma grande importância de estudos feitos com o cobre. Estruturalmente os complexos de cobre utilizados do tipo base de Schiff e os complexos de cobre com ligantes estão representados na figura 1. Figura 1- Estruturas dos complexos utilizados. Materiais e métodos Materiais: Utilizou-se para este estudo os seguintes complexos de cobre: Cu(Isa-pn), Cu(Isa-en), Cu(Isa-epy), Cu(Isa-amiquin) e Sulfato de Cobre. Outros complexos com ligantes pepitídeos de baixa massa molecular também foram utilizados como: Tri-glicina (G3), Tetra-glicina (G4) e Glicinaglicina-histidina (GGH), formando complexos com Cu2+. As sondas utilizadas para identificação da formação de radicais livres foram: NADH e DHR123. Os demais reagentes utilizados foram: tampão fosfato, tampão fosfato salino(, peróxido de hidrogênio, bicarbonato de sódio, 2-deoxy-D-ribose,ácido tiobarbitúrico. Além da vidraria e materiais usualmente utilizados em laboratório utilizou-se um espectofotômetro da marca Shimadzu modelo uv-180 e cubetas de quartzo com caminho ótico igual a 1,000 cm. Métodos: A primeira etapa consistiu em analisar de oxidação do NADH mediadas pelos seguintes complexos de cobre: Cu(Isapn), Cu(Isa-en), Cu(Isa-epy), Cu(Isa-amiquin) e Sulfato de Cobre, em ambiente oxidante. Utilizou-se concentrações de complexo de cobre (50 μM), bicarbonato de sódio (25 mM), NADH (50 μM) e peróxido de hidrogênio (3 mM) e PBS(10mM, pH=7,4), misturou-se tudo em um tubo eppendorf e rapidamente pipetou-se em uma cubeta de quartzo, medindo a cinética de oxidação do NADH para NAD+ no espectofotômetro.(λ=340 nm). A segunda etapa foi feita para confirmar os resultados obtidos na primeira etapa do trabalho, portanto trocou-se a sonda utilizada por DHR123. Utilizou-se concentrações de complexo de cobre (50μM), bicarbonato de sódio(25mM), DHR123(50μM) e peróxido de hidrogênio(3mM), misturou-se tudo em um eppendorf e rapidamente pipetou-se em uma cubeta de quartzo, medindo a cinética de oxidação da DHR à rodamina no espectofotômetro.(λ=500 nm). A terceira etapa do trabalho consistiu em analisar a formação de radicais hidroxila, utilizando o método TBARS(substâncias reativas do ácido tiobarbitúrico).9 Os 2 complexos de cobre utilizados foram: Cu(Isa-pn), Cu(Isa-em), Cu(Isa-epy), Cu(Isa-amiquin) e Sulfato de Cobre. Utilizou-se das seguintes concentrações: 2-deoxy-D-Ribose (2,5 mM); tampão fosfato (50mM, pH=7,4), complexos de cobre(50 μM); bicarbonato de sódio (25 mM) e peróxido de Hidrogênio (3mM). A etapa final do trabalho consistiu em analisar a formação de radicais hidroxila, utilizando ligantes (Tri-Glicina(G3), Tetra Glicina(G4) e GlicinaGlicinaHistidina(GGH)) ligados a Cu2+. Utilizou-se das seguintes concentrações: das seguintes concentrações: 2-deoxy-D-Ribose (2,5mM); tampão fosfato (50mM,pH=7,4) , ligante com o cobre(300μM); bicarbonato de sódio (25 mM) e peróxido de Hidrogênio (3mM). II. RESULTADOS E DISCUSSÕES Ao medir a absorbância do NADH, feita na primeira parte do trabalho, foi possível descobrir a oxidação ocasionada por radicais livres. Os resultados encontram-se na figura 2. Figura 2 Gráfico da oxidação do NADH , n=5, Onde * p< 0,05. Observa-se uma linha de tendência na oxidação do NADH provocada por complexos de cobre, onde o sulfato de cobre foi o mais reativo. No entanto as barras de erros ficaram grandes e não se pode afirmar que a tendência é exatamente igual à média das vezes, então para confirmar a tendência oxidativa fez-se o mesmo processo utilizado a sonda DHR123 ao invés da sonda NADH. Os resultados obtidos encontram-se na figura 3. espécies reativas. Notou-se que claramente o sulfato de cobre é o composto mais oxidante seguido pelos outros compostos. Para entender um pouco melhor a interação dos radicais com o meio oxidante fez-se a identificação dos radicais hidroxila a partir do método TBARS.9 Os resultados Obtidos encontram-se na figura 3. Figura 4- Formação dos Radicais Hidroxila. n=3, Onde * p< 0,05 e *** p < 0,001 Pode-se notar a mesma tendência, encontrada na oxidação das sondas gerada por radicais livres. Implica que os radicais hidroxila são os que mais formam no processo. Ao comparar a estrutura de cada complexo de cobre podese notar uma similaridade entre Cu(Isa-pn) e Cu(Isa-epy), e entre Cu(Isa-em) e Cu(Isa-amiquin). Devido à semelhança entre as estruturas pode-se notar uma analogia aos níveis de oxidação provocados complexos. Biologicamente se pode observar o efeito ocorrido nos estudos.Nota-se que em experimentos feitos com células tumorais, tratamentos que utilizam Cu(Isa-pn) e Cu(Isa-epy) há uma morte celular maior que os tratamentos utilizados somente sulfato de cobre.11 Primeiramente acreditava-se que a morte celular era devido à formação de radicais livres ocasionados pelos complexos de cobre. No entanto hoje, já se sabe que esses complexos de cobre possuem uma interação lipofílica e portanto quando testados empiricamente com células, os complexos entram dentro das células e degradam a membrana mitocondrial levando a morte celular.12 Sabe-se que o cobre raramente está sozinho dentro do corpo, está na maior parte das vezes ligado a proteínas carregadoras. Aplicou-se o método TBARS utilizando cobre ligado a ligantes peptídicos simples (G4,G3 ou GGH). Os resultados obtidos encontram-se no gráfico 4. Figura 3- Gráfico da oxidação do DHR, n=3, Onde * p< 0,05 e ** p < 0,01. A partir dos resultados obtidos na primeira e na segunda etapa pôde-se notar que há uma tendência sim na formação de Figura 5- Formação de radicais hidroxila proporcionados por cobre junto ao ligante, n=3, Onde ** p< 0,01 e *** p < 0,001 3 Nessa parte do experimento a primeira amostra foi o controle. Como já se sabe que o cobre catalisa a formação de radicais5, na ausência desse metal a formação de radicais livres será bem menos intensa. Verificou-se que o cobre funciona mesmo como um catalisador na formação de espécies reativas, quando ligado a estes ligantes peptídeos. O experimento mostra que a formação de radicais possuiu maior concentração nas amostras que continham respectivamente: glicina-glicina histidina(GGH); Tetraglicina(G4); Tri-glicina(G3) e Sulfato de cobre. Biologicamente pode-se notar esse mesmo efeito em estudos feitos com células.11Estudos recentes mostram que a interação entre os radicais livres e as células tumorais podem levar a proliferação celular.11 Nota-se que o tratamento que utiliza como ligante GGH, as células se proliferaram mais do que os outros tratamentos, seguindo a mesma tendência mostrada pelo gráfico 4. Ao comparar os resultados, pode-se notar que o sulfato de cobre é a barreira intermediária entre ligantes do tipo base de Schiff associados ao cobre e os complexos de cobre com peptídeos de baixa massa molecular. Por muito tempo acreditou-se que os radicais livres eram exclusivamente prejudiciais ao organismo. Atualmente sabe-se que muitas espécies reativas são mediadoras de sinais celulares como o peróxido de hidrogênio. III. CONCLUSÕES A partir dos resultados obtidos foi possível concluir que complexos de cobre com ligantes do tipo base de Schiff geram EROs em um ambiente oxidante de maneira semelhante entre si, mas diferente dos complexos de cobre com peptídeos. Estes últimos geram muito mais EROs, e em ambiente celular levam a proliferação como resposta. Isso implica na importância dos radicais livres em meio celular. AGRADECIMENTOS Este trabalho foi financiado pelo Programa de Iniciação Científica da UFABC, e pelas agências FAPESP e CNPq. REFERÊNCIASS [1]Vasconcelos S.M.L., Goulart M.O.F., Moura J.B.F., Benfato V.M, Manfredini V., Kubota L.T. Quim. Nova(2007) Vol-30 No.1323-1338 [2]Cerchiaro G, Ferreira AMDC, J. Braz. Chem. Soc. 2006, 17 (8), 1473. [3] Ruben G. M. Moreno, María V. Alipázaga, Marisa H. G. Medeiros e Nina Coichev. Quim. Nova(2006), Vol. 29, No. 5, 1086-1093. [4] BIANCHI M.D.L.P.Lusânia, ANTUNES L.M.G. Rev. Nutr., Campinas(1999), 12(2): 123-130, maio/ago. [5]FERREIRA A.L.A., MATSUBARA L.S.. Rev Ass Med Brasil (1997); 43(1): 61-8 [6] HALLIWELL, B. & GUTTERIDGE, J.M.C. Free Radical in Biology and Medicine. 2º ed. Oxford, University Press. 1989. 543pp. [7]Adman ET, Advances in Protein Chemistry, (1991), v.42, CRC Press, 145. [8]Paul A. Cobine, Fabien Pierrel, Dennis R. Winge, Biochimica et Biophysica Acta 1763 (2006) 759–772. [9]Azellini M.A.A., Bagatin I. A., Ferreira A.M.D.C. . Redox Report(2006), vol.11, No.1 [10] Vogel A.I. Química analítica qualitativa.5ª edição. [11] Estudos realizados pelo grupo de pesquisa coordenado pela professora Dra. Giselle Cerchiaro, ainda em andamento. [12] Filomeni G., Piccirillo S., Graziani I. Cardaci S., Ferreira A.M.D.C., Rotilio G,Ciriolo M.R.. Carcinogenesis(2009) vol.30 no.7 pp.1115– 1124.
Download