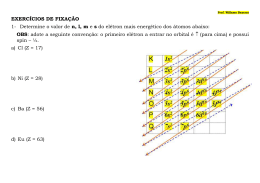
ALUNO(a): ___________________________________________ Nº: ____ SÉRIE: 1º UNIDADE: VV Valor: TURMA:_____ JC JP PC 0,0 DATA: ___/___/2013 Obs.: Esta lista deve ser entregue apenas ao professor no dia da aula de Recuperação 6 1. Um certo átomo do elemento E, genérico, apresenta o elétron mais energético no subnível 4p . Pede-se: a) Qual o período e família do sistema periódico a que pertence o elemento E? b) Quais são e qual o número atômico dos elementos que antecedem e sucedem o elemento E na mesma família do sistema periódico? 2. Um elemento que apresenta, nos últimos subníveis, a configuração 4s2, 3d2, pertence a qual família e qual período? 3. Os três elementos x, y e z têm as seguintes estruturas eletrônicas no estado fundamental: 2 2 6 2 6 2 5 x — 1s 2s 2p 3s 3p 4s 3d 2 2 6 2 6 y — 1s 2s 2p 3s 3p 2 2 6 2 6 2 10 4 z — 1s 2s 2p 3s 3p 4s 3d 4p De acordo com tais estruturas, os três elementos podem ser classificados, respectivamente, como? 4. Qual das seguintes afirmações é FALSA, a respeito da distribuição eletrônica dos elementos e sua classificação: 2 2 6 2 a) 1s 2s 2p 3s é um elemento representativo. 2 2 6 b) 1s 2s 2p é um gás nobre. 2 2 6 2 4 c) 1s 2s 2p 2s 3p é um metal. 2 2 6 2 6 2 6 d) 1s 2s 2p 3s 3p 4s 3d é um elemento de transição. 2 2 6 2 6 1 e) 1s 2s 2p 3s 3p 4s é um metal alcalino. 5. Os elementos X e Y apresentam as seguintes configurações eletrônicas 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3 e 1s2 2s2 2p6 3s2 3p6 4s1, respectivamente. O período e a família em que se encontram estes elementos são? 6. Com base na tabela periódica a seguir, em que as letras representam elementos químicos, assinale o que for correto. (01) A, B, C, D e E são metais. (02) G e H apresentam elevada eletronegatividade. (04) O elétron mais energético de E está no subnível 5p1. (08) C apresenta alta densidade. (16) F tem quatro elétrons na camada de valência. 2013_Química_1° ano_2º tri Soma das alternativas corretas ( ) 7. O elemento bromo forma compostos iônicos e moleculares. Apresente, respectivamente, um composto iônico e um molecular formado pelo bromo. 8. O iodo (I) combina-se com o hidrogênio (H), formando o ácido iodídrico. Sabendo-se que o número atômico do iodo é igual a 53 e o do hidrogênio é igual a 1, informe: a) A fórmula molecular do ácido iodídrico. b) A fórmula eletrônica (Lewis) do ácido iodídrico. c) A fórmula estrutural do ácido iodídrico. 1 9. Dentre as afirmativas abaixo, assinalar a que contém a afirmação incorreta. a) Ligação covalente é aquela que se dá pelo compartilhamento de elétrons entre dois átomos. b) O composto covalente HCℓ é polar, devido à diferença de eletronegatividade existente entre os átomos de hidrogênio e cloro. c) O composto formado entre um metal alcalino e halogênio é covalente. d) A substância da fórmula Br2 é apolar. e) A substância da fórmula CaI2 é iônica. 10. Informe os tipos de interações intermoleculares, com que tipo de moléculas ocorrem e dê exemplos. 2
Baixar