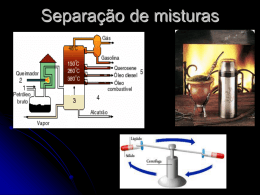
TEXTO DE APOIO Métodos de separação dos componentes de uma mistura Na natureza as substâncias raramente existem no estado "puro". Elas surgem quase sempre como componentes de uma mistura. Como no estado puro as substâncias apresentam propriedades físicas e químicas bastante diferentes é muitas vezes útil proceder à sua separação. Para isso podemos recorrer a diferentes métodos de separação! O método de separação a utilizar depende das propriedades físicas de cada componente da mistura. Para efectuar uma separação bem sucedida temos de: Conhecer as propriedades de cada um dos componentes da mistura. Conhecer as propriedades da mistura. Possuir conhecimento prévio de toda uma gama de métodos de separação de componentes de forma a escolher a mais adequada. Métodos de separação de misturas heterogéneas Filtração: Processo que permite separar as partículas sólidas que se encontram em suspensão ou depositadas num líquido. Utiliza-se um papel de filtro para reter as partículas sólidas. Estas são maiores e não conseguem atravessar os pequeninos poros do papel de filtro. Às partículas sólidas que não atravessam o papel de filtro chamamos resíduo. A parte líquida da mistura que atravessa os poros do papel de filtro designa-se por filtrado. A base física que está associada a este método de separação de componentes de uma mistura é o diferente tamanho dos constituintes da mistura. Exemplo: Separar água e grãos de pimenta ou a borra do café. 1 Decantação sólido/líquido: Processo físico que permite separar um sólido depositado no fundo de um recipiente que contém um líquido. Na decantação transfere-se o líquido de um recipiente para o outro com o auxílio de uma vareta de vidro. O uso da vareta permite controlar a quantidade de líquido a verter e evitar que o sólido depositado vá por arrasto. A base física que está associada a este método de separação de componentes de uma mistura é a diferente densidade dos componentes da mistura. A areia é mais densa do que a água e por isso fica no fundo. Exemplo: Separar água da areia. Decantação líquido/líquido: Processo que permite separar dois ou mais líquidos imiscíveis (que não se misturam), com base na diferença de densidades dos líquidos. O líquido mais denso fica por baixo. Para realizar este método de separação utiliza-se uma ampola de decantação. A base física que está associada a este método é a diferente densidade dos constituintes da mistura. Exemplo: Separar água do azeite. 2 Centrifugação: Processo que permite separar partículas sólidas de pequenas dimensões que se encontram em suspensão num líquido, contido num tubo, por acção de uma centrifugadora. Esta realiza um movimento de rotação a alta velocidade que faz com que as partículas em suspensão se concentrem no fundo do tubo como se pode verificar na figura do lado esquerdo. A base física que está associada a este método é a diferente densidade dos constituintes da mistura. A diferença em relação ao processo anterior é o facto de que aqui os componentes não são os dois líquidos. Exemplo: Separar o soro dos restantes constituintes do sangue. Peneiração: Processo que permite separar os componentes de misturas sólidas formadas por componentes que têm diâmetros diferentes, para tal utilizam-se as peneiras. A base física que está associada a este método é a diferença de diâmetro dos constituintes da mistura. Exemplo: Separar a areia da farinha. Na imagem da esquerda a malha da rede é cada vez mais apertada de forma que os componentes da mistura de maiores dimensões são logo recolhidos na parte de cima. Os de menor dimensão são recolhidos na parte de baixo. 3 Separação magnética: Processo utilizado quando um dos componentes da mistura apresenta propriedades magnéticas, ou seja é atraído por um íman. O íman separa sólidos magnéticos dos não magnéticos. A base física que está associada a este método é o facto de um dos componentes da mistura a ser atraído por um magnete ou imane. Exemplo: Separar areia de limalha de ferro. Extracção por solvente: Processo que permite separar os componentes da mistura devido ao facto de apenas um dos componentes da mistura ser solúvel em determinado solvente e os restantes não. A base física que está associada a este método é o facto de apenas um dos componentes da mistura a ser solúvel em água (solvente). Adiciona-se água agita-se para dissolver o sal e depois efectua-se uma decantação sólido/líquido. Exemplo: Separar areia de sal. ← Areia em suspensão ← Sal ← Areia Nesta mistura de areia e sal apenas o sal é solúvel em água e por isso podemos usar esse facto para efectuar a separação. 4 Métodos de separação de misturas homogéneas Ebulição do solvente: Processo usado para obter um sólido, sob a forma de pó fino, que se encontra dissolvido num solvente recorrendo à ebulição deste. Usa-se uma chama para levar o componente menos volátil (menor ponto de ebulição), a passar para o estado gasoso rapidamente e é por isso que o sólido obtido fica sob a forma de pó. A base física que está associada a este método de separação é a diferença dos pontos de ebulição dos componentes da mistura. Exemplo: Separar o sal da água de forma rápida (por ebulição). Cristalização: Processo usado para obter um sólido, sob a forma de cristais, que se encontra dissolvido num solvente recorrendo à evaporação deste. O processo é normalmente levado a cabo à temperatura ambiente. A base física que está associada a este método de separação é a diferença dos pontos de ebulição dos componentes da mistura. Exemplo: Separar o sal da água de forma lenta (por evaporação). 5 Destilação simples: Processo que permite separar dois líquidos miscíveis (que se misturam), com pontos de ebulição diferentes. Por aquecimento de uma mistura deste tipo o vapor que se forma é mais rico no componente mais volátil (menor ponto de ebulição), e por isso o líquido que se vai obter por condensação deste vapor vai ter uma maior percentagem do líquido mais volátil. O processo é tanto mais eficaz quanto maior for a diferença dos pontos de ebulição dos líquidos a destilar. A base física que está associada a este método de separação é a diferença dos pontos de ebulição dos componentes da mistura. Exemplo: Aquecer o vinho para lhe extrair o álcool que contém. O destilado vai ter maior teor de álcool do que o vinho inicial. 6 Destilação fraccionada: Processo usado para separar dois ou mais líquidos, miscíveis, com pontos de ebulição diferentes. Este método é mais eficaz do que a destilação simples pois separa melhor os dois líquidos. A base física que está associada a este método de separação é a diferença dos pontos de ebulição dos componentes líquidos da mistura. Exemplo: Aquecer o vinho para lhe extrair o álcool que contém. O destilado vai ter muito maior teor de álcool do que o vinho. 7
Baixar