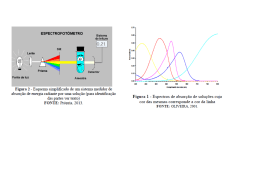
Universidade Camilo Castelo Branco Instituto de Engenharia Biomédica LEANDRO PROCÓPIO ALVES ABSORÇÃO ÓPTICA TRANSIENTE NO COMPOSTO FENOTIAZÍNICO AZUL DE TOLUIDINA TRANSIENT OPTICAL ABSORPTION IN THE PHENOTIAZINIC COMPOUND TOLUIDINE BLUE São José dos Campos, SP 2014 II Leandro Procópio Alves ABSORÇÃO ÓPTICA TRANSIENTE NO COMPOSTO FENOTIAZÍNICO AZUL DE TOLUIDINA Orientador: Prof. Dr. Egberto Munin Tese de Doutorado defendida no Programa de Pós-Graduação em Engenharia Biomédica da Universidade Camilo Castelo Branco, como complementação dos créditos necessários para obtenção do título de Doutor em Engenharia Biomédica. São José dos Campos, SP 2014 III FICHA CATALOGRÁFICA IV V DEDICATÓRIA Dedico este trabalho aos meus pais, José Alves e Odete Aparecida Procópio Alves, por todo o incentivo e dedicação buscando sempre meu crescimento pessoal, profissional e moral. Aos meus irmãos, Eliane, Danilo e Daniel que sempre me apoiaram em minhas decisões. A uma pessoa muito especial em minha vida, minha esposa Fernanda Maria Prado Braga Alves que em muito ajudou nesta etapa da minha vida. Incentivando, aconselhando, me permitindo sonhar e principalmente me fazendo acreditar nos sonhos. E principalmente a uma pessoinha muito especial que trouxe novo sentido a nossa vida, o pequeno Vinícius Braga Alves! VI AGRADECIMENTOS Primeiramente a Deus pelo dom da vida, da sabedoria, da perseverança e do amor. Em especial a meu orientador Prof. Dr. Egberto Munin, por ter me acolhido em seu laboratório com muita atenção e paciência, agradeço pela imensa ajuda, confiança e orientação em todo este percurso. Ao Prof. Dr. Renato Zângaro pela confiança e indispensável incentivo ao meu crescimento profissional. A todos os meus familiares, pelo amor e carinho. A Nídia Lucia pelo carinho, incentivo, e indispensável apoio durante o curso. A todos os colegas do IEB que de alguma forma contribuíram para a realização do meu trabalho. VII “É muito melhor lançar-se em busca de conquistas grandiosas, mesmo expondo-se ao fracasso, do que alinhar-se com os pobres de espírito, que nem gozam muito nem sofrem muito, porque vivem numa penumbra cinzenta, onde não conhecem nem vitória, nem derrota.” (Theodore Roosevelt) VIII ABSORÇÃO ÓPTICA TRANSIENTE NO COMPOSTO FENOTIAZÍNICO AZUL DE TOLUIDINA RESUMO Azul de Toluidina é um composto fotossensível com baixa toxicidade na ausência de luz e que figura em variadas aplicações na indústria, apresentando relevância clínica na medicina, tanto para diagnostico quanto para tratamentos. Neste trabalho objetivou-se registrar o comportamento transiente da absorção óptica em um composto fotossensível aplicado em Terapia Fotodinâmica. O arranjo consistiu de um laser de hélio-neônio com 12 mW de potência óptica em 632,8 nm focalizado por uma lente de 40 cm e modulado por um obturador eletromecânico, ajustado para 4 s de abertura. A amostra foi disposta em uma célula de vidro com 1,1 mm de caminho óptico, posicionada no foco da lente. A leitura do sinal transmitido e de gatilho foi realizada por dois fotodetectores, conectados a um osciloscópio de 500 MHz com armazenamento digital. Duas soluções foram preparadas variando o solvente, água destilada e etanol. A absorbância transiente para cada solução foi medida pelo sistema proposto e os dados foram processados pelo software Origin 8. Os resultados da absorção transiente para a solução agregada indicam uma redução no sinal transmitido durante os primeiros 500 ms de irradiação. Esse aumento da absorção pode estar relacionado com a conversão dímero-monômero. Para confirmar essa hipótese, foi medida a solução com baixo índice de agregação, na qual a conversão dímero-monômero pode ser considerada desprezível. Os resultados para esta solução mostraram um aumento na transmitância durante os primeiros 500 ms. Desta forma conclui-se que existe um fenômeno transiente da ordem de milissegundos cujo resultado é o aumento da absorção óptica do corante e está relacionado à conversão direta entre dímeros e monômeros. Palavras-chave: Absorção transiente, agregação, corante, laser, azul de toluidina, fenotiazina IX TRANSIENT OPTICAL ABSORPTION IN THE PHENOTIAZINIC COMPOUND TOLUIDINE BLUE ABSTRACT Toluidine Blue is a photosensitive dye with low dark toxicity, presenting a variety of applications on industry and clinical relevance on medicine, for both diagnostic and therapeutic applications. This work aimed to register the transient optical absorption on a photosensitive compound applied in Photodynamic Therapy. The setup consisted of a helium-neon laser with 12 mW of optical power at 632.8 nm focused by a 40 cm lens and modulated by an electromechanical shutter, adjusted to 4 s opening. The sample was inserted in a glass cell with 1.1 mm optical path, positioned in the focal length of the lens. The collecting of the transmitted signal and trigger was made by two photodetectors, connected to a digital storage oscilloscope with 500 MHz bandwidth. Two solutions were prepared by varying the solvent of distilled water and ethanol. The transient absorbance for each solution was measured by the proposed system and the data were processed by the Origin 8 software. The results of transient-absorption for aggregate solution indicate an increase in absorption during the first 500 ms of irradiation. This absorbance increase may be related with the monomer-dimer conversion. To confirm this hypothesis, the solution with a low level of aggregation, in which the dimer-monomer conversion can be considered negligible, was measured. The results showed an increase in transmittance during the first 500 ms, confirming the hypothesis. Thus, it could be concluded that there is a milliseconds transient phenomenon whose results is the increase in the dye optical absorption by direct dimer-to-monomer conversion. Key-words: phenothiazine Transient-absorption, aggregation, dye, laser, toluidine blue, X LISTA DE FIGURAS Figura 1: Diagrama de excitação para dímeros em diferentes arranjos geométricos de dipolos. ..................................................................................................................... 25 Figura 2: Ilustração de um sistema genérico de 3 níveis. Sm representa um estado metaestável que compreenderá a maior parte das moléculas durante o processo de branqueamento. .................................................................................................. 26 Figura 3: Estrutura molecular do Azul de Toluidina. ............................................................. 27 Figura 4: Célula para amostra líquida, construída com duas placas de vidro espaçadas por um anel de aço inox. .......................................................................................... 28 Figura 5: Diagrama da montagem experimental, onde: d1 e d2 são detectores, cp corpo de prova, s é o obturador eletromecânico, I lente convergente, a é o filtro atenuador e L laser................................................................................................... 30 Figura 6: Imagem ilustrativa da montagem experimental, onde: d1 e d2 são detectores, cp corpo de prova, s obturador eletromecânico, I lente convergente, a filtro e L laser. ........................................................................................................................ 31 Figura 7: Espectro de absorção para as amostras de Azul de Toluidina diluídas em água destilada, em diferentes concentrações.................................................................... 34 Figura 8: Aumento da absorbância pelos dímeros (λ=590 nm) e monômeros (λ=630 nm) em função do aumento da concentração. ................................................................. 35 Figura 9: Relação entre as intensidades das absorções medidas nos comprimentos de onda de pico das bandas relativas ao dímero (590 nm) e ao monômero (630 nm) em função da concentração. .................................................................................... 36 Figura 10: Espectro de absorbância para diferentes concentrações de Azul de Toluidina diluído em álcool Etílico. ........................................................................................... 37 Figura 11: Aumento da absorbância medida no pico da banda dimérica (λ=590 nm) e no pico da banda monomérica (λ=630 nm) em função da concentração para solução aquosa. .................................................................................................................... 37 Figura 12: Relação entre as intensidades de pico das bandas de absorção relativas a dímeros e monômeros em função da concentração para solução etanólica. ............ 38 Figura 13: Validação dos detectores com relação ao tempo de resposta frente ao feixe laser chaveado. Para os detectores 13DSI007 e 13DSI011 foi utilizado filtro OD 0,8. ..................................................................................................................... 39 Figura 14: Posição do feixe com relação à área da íris. ....................................................... 40 Figura 15: Curva de resposta do detector em função da potência do laser de He-Ne, comprimento de onda de 632,8 nm. Os valores de tensão na escala vertical esquerda são valores extrapolados. ......................................................................... 42 Figura 16: Avaliação da resposta do sistema experimental para Azul de Toluidina, 500 µM, em função do incremento da potência do laser. ................................................ 43 Figura 17: Distribuição espacial de energia pela secção transversal do feixe laser. ............ 44 Figura 18: Medida do perfil transversal do feixe laser. ......................................................... 45 XI Figura 19: Medida da intensidade de transmissão em função do tempo para excitação de 13,8 mW em 632,8 nm e concentração de 500 µM em água. ................................... 46 Figura 20: Exposição prolongada, 4,5 s, para a amostra de 500 µM com 13,8 mW de potência do laser. ..................................................................................................... 47 Figura 21: Absorbância transiente normalizada, para solução aquosa de azul de toluidina na concentração de 400 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). ........................................................................................................... 52 Figura 22: Delta de transmissão entre os tempos 0 e 1 s, para a solução aquosa na concentração de 400 µM. Valores obtidos a partir de curvas normalizadas de transmissão. ............................................................................................................. 52 Figura 23: Absorbância transiente para solução aquosa de azul de toluidina na concentração de 300 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). ........................................................................................................... 53 Figura 24: Delta de transmissão entre os tempos 0 e 1 s, para solução aquosa na concentração de 300 µM. Valores obtidos a partir de curvas normalizadas de transmissão. ............................................................................................................. 53 Figura 25: Absorbância transiente para azul de toluidina em solução aquosa na concentração de 200 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). ........................................................................................................... 54 Figura 26: Delta de transmissão entre os tempos 0 e 1 s, para a concentração de 200 µM, diluída em água. Valores obtidos a partir de curvas normalizadas de transmissão. ............................................................................................................. 54 Figura 27: Absorbância transiente para solução aquosa de azul de toluidina na concentração de 100 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). ........................................................................................................... 55 Figura 28: Delta de transmissão entre os tempos 0 e 1 s, para a solução aquosa na concentração de 100 µM. Valores obtidos a partir de curvas normalizadas de transmissão. ............................................................................................................. 55 Figura 29: Redução na transmissão de sinal, atribuída ao expressivo efeito de lente térmica, fazendo com que o feixe adquirisse diâmetro maior que aquele do detector. ................................................................................................................... 56 Figura 30: Transmitância transiente para o azul de toluidina em solução etanólica na concentração de 300 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). ........................................................................................................... 58 Figura 31: Delta de transmissão entre os tempos 0 e 1 s, para solução etanólica na concentração de 300 µM. Valores obtidos a partir de curvas normalizadas de transmissão. ............................................................................................................. 58 Figura 32: Coeficiente angular obtido a partir do ajuste linear aos dados de delta de transmissão. ............................................................................................................. 59 XII LISTA DE TABELAS Tabela 1: Resultados das medidas do diâmetro do feixe na posição focal da lente ............. 45 Tabela 2: Cálculo da intensidade no centro do feixe gaussiano para cada potência óptica estudada. ................................................................................................................. 48 Tabela 3: Tempo, estimado, necessário para se elevar a temperatura do meio em função da potência óptica (*)................................................................................................ 50 XIII SUMÁRIO 1. 2. 3. 4. INTRODUÇÃO.............................................................................................................. 14 1.1. Objetivo geral ........................................................................................................ 18 1.2. Objetivos específicos ............................................................................................. 18 REVISÃO BIBLIOGRÁFICA.......................................................................................... 19 2.1. Uso dos corantes associados à radiação luminosa para fins medicinais ............... 19 2.2. Compostos Fotossensíveis .................................................................................... 21 2.2.1. Compostos fotossensíveis de primeira geração.............................................. 21 2.2.2. Compostos fotossensíveis de segunda geração ............................................. 21 2.3. Agregação em Corantes ........................................................................................ 23 2.4. Fenômenos fotoinduzidos ...................................................................................... 25 MATERIAL E MÉTODOS ............................................................................................. 27 3.1. Preparo das amostras ........................................................................................... 27 3.2. Medida do espectro de absorbância ...................................................................... 28 3.3. Montagem experimental ........................................................................................ 28 3.3.1. Tempo de resposta do obturador eletromecânico ........................................... 28 3.3.2. Medida do perfil do feixe laser na posição do corpo de prova ......................... 29 3.3.3. Fotodetectores................................................................................................ 30 3.4. Definição dos parâmetros de medida..................................................................... 32 3.5. Estudo da energia acumulada na amostra ............................................................. 32 3.6. Coleta dos dados experimentais ............................................................................ 32 RESULTADOS ............................................................................................................. 34 4.1. Medida do espectro de absorbância ...................................................................... 34 4.2. Medida do tempo de resposta dos componentes do sistema................................. 38 4.3. Medida da linearidade na resposta do sistema ...................................................... 41 4.4. Medida do perfil do feixe laser na posição da amostra .......................................... 43 4.5. Tempo da aquisição .............................................................................................. 45 4.6. Calculo da energia acumulada durante a irradiação .............................................. 47 4.7. Registros para Azul de Toluidina diluído em água destilada .................................. 51 4.8. Registros para Azul de Toluidina diluído em álcool etílico...................................... 56 5. DISCUSSÃO ................................................................................................................ 60 6. CONCLUSÕES............................................................................................................. 66 REFERÊNCIAS BIBLIOGRÁFICAS ..................................................................................... 67 14 1. INTRODUÇÃO O desenvolvimento de tecnologias visando à aplicação clínica depende de inúmeros fatores que podem determinar seu sucesso ou irremediável fracasso. Dentre esses fatores pode-se destacar os estudos de biocompatibilidade (WILLIAMS, 2008), de toxicidade (GOULART et al., 2010), de eficiência terapêutica (GONZALES et al., 2010), de escalabilidade e fundamentalmente de viabilidade econômica. Porém, bem antes de uma tecnologia ser avaliada mediante esses fatores, existem outros estudos que são fundamentais na escolha do conjunto de componentes que integrará, futuramente, a tecnologia. Antecedente a uma aplicação distinta, é fundamental explorar as características dos materiais que se tem a disposição e, a partir desse conhecimento, verificar as possibilidades de associação e/ou modificações estruturais visando agregar características que podem não ser encontradas naturalmente. (WAINWRIGHT, 2005) Essa metodologia, para o desenvolvimento de tecnologias, é aplicada nas diversas áreas do conhecimento, em especial na medicina, onde a demanda por tecnologias de diagnóstico e tratamento é imprescindível. Dentre as terapias desenvolvidas para tratamento de enfermidades, pode-se destacar uma que, embora existam registros de sua aplicação nas civilizações antigas há mais de 4000 anos, somente se desenvolveu expressivamente nas últimas décadas. Essa terapia é conhecida como Terapia Fotodinâmica (TFD) e seu mecanismo depende de três componentes básicos: a presença de oxigênio, a radiação luminosa e uma molécula com características específicas, como absorção e capacidade de reação com oxigênio (GASPARETTO et al., 2010; GIROLDO et al., 2009; MUNIN et al., 2007). O sucesso que o desenvolvimento da TFD tem alcançado é resultado de um somatório de esforços na escolha de moléculas que tenham capacidade de absorver a radiação luminosa, elevar seu nível energético tornando-se reativa por si só e, quando na presença de moléculas de oxigênio, promover nestas a elevação do nível energético, agregando um nível de reatividade extremamente alto (MACDONALD; DOUGHERTY, 2001). A partir daí pode-se definir duas linhas de pesquisa independentes, porém, interconectadas quando observado pelo aspecto da terapia. A primeira linha busca, por meio de modificações em materiais conhecidos ou mesmo o desenvolvimento de novos materiais, a geração de novas fontes de 15 radiação eletromagnética nos mais variados comprimentos de onda e potência óptica (ENK; LEVI, 2012; FERRAZ et al., 2011). A segunda linha estuda diferentes moléculas buscando a máxima eficiência na absorção de radiação luminosa, mínima toxicidade intrínseca, tempo de meia-vida adequado, fácil metabolização pelo organismo e alta conversão de oxigênio molecular em oxigênio reativo (ALLISON et al., 2004; ASANO, et al., 2013; GASPARETTO et al., 2010; WAINWRIGHT; GIDDENS, 2003). Embora pareça uma tarefa simples a escolha de uma molécula que ofereça as características citadas acima e também absorva em um comprimento de onda já disponível comercialmente, torna-se complexa quando se considera o meio onde será aplicada. No caso da TFD, impreterivelmente haverá interação com algum tipo de meio biológico e essa interação restringirá as possibilidades de comprimentos de onda em função de efeitos como absorção e espalhamento, tornando a escolha da molécula muito mais delicada. Conforme relatado por Nielsen et al. (2005), a oxigenação do tumor tem grande influência na profundidade de penetração da luz no tecido. Conforme a concentração de O2 decresce, durante a TFD, a profundidade de penetração em 630 nm também decrescerá. Por sua vez, Mustafa e Jaafar (2013), simularam o comportamento de diferentes comprimentos de onda durante interação com diferentes tipos de pele e relataram que, embora a transmissão da radiação laser pela epiderme e derme ocorra, a dose muda significantemente em função da profundidade, comprimento de onda e tipo de pele. Mas não só a escolha do melhor comprimento de onda será um fator complicador, as moléculas quando em contato com o organismo poderão sofrer alguns efeitos não desejáveis durante a Terapia, tal como agregação, ou até desativação quando já em estado excitado após irradiação, o que reduzirá a eficácia da técnica. Considerando que as propriedades fotofísicas das moléculas são determinadas pela natureza e pela energia de seus estados eletronicamente excitados e ainda sofrem influência do meio sobre as energias relativas dos estados eletrônicos, várias linhas de pesquisa foram instituídas buscando prever o comportamento das moléculas. Dentre as linhas se podem citar a caracterização em diferentes meios (LIU; ZOU; UM, 2010) e concentrações (D´ILARIO; MARTINELLI, 2006), além de estudar sua eficiência fotodinâmica frente a diferentes estruturas 16 biológicas, tais como bactérias (FERRAZ et al., 2011), fungos (GASPARETTO et al., 2010), entre outros. Além dessas características amplamente estudadas, as moléculas utilizadas na TFD possuem outras características especiais e individuais que podem ser úteis tanto para a melhoria da própria TFD quanto para vislumbrar novas aplicações até então não exploradas. Exemplos desse tipo de aplicação transversal já existem em dispositivos optoeletrônicos, elementos lógicos ópticos, agentes sensibilizadores em fotografia colorida, fotocondutores, dispositivos eletroluminescentes e centros eletroopticamente ativos em sistemas fotovoltaicos, conversão de energia solar, semicondutores fotocatalíticos, controle de poluentes, preparação farmacêutica, entre outras (D´ILARIO; MARTINELLI, 2006). Uma característica presente nessas moléculas e que tem recebido grande interesse está relacionada com sua propriedade fototérmica. Quando excitada com radiação laser, com distribuição de energia Gaussiana, parte da energia incidente é absorvida pelas moléculas que estão no estado fundamental sendo excitadas para estados de maior energia. Para manter o equilíbrio, a molécula excitada precisa dissipar o excesso de energia. Uma das formas de dissipar a energia se dá por decaimento não radiativo, produzindo aumento de temperatura localizado, que induzirá um gradiente de índice de refração no meio. Desta forma o meio atuará de forma semelhante a um elemento óptico (KURIAN et al., 2003). A técnica que explora essa característica é chamada Lente Térmica. Os sinais de lente térmica são intrinsecamente não lineares na absorbância da amostra e na potência de excitação para um laser contínuo ou na energia no caso de um laser pulsado. A primeira causa para a não linearidade se origina da dependência não linear da quantia de energia absorvida com a absorbância devido à atenuação óptica do feixe de excitação ao longo do caminho óptico para amostras altamente absorvedoras. A segunda causa é que a resposta fototérmica não é sempre linear com a quantia de energia absorvida devido aos efeitos de difração causados pelo aquecimento significante da amostra (BRENNETOT; GEORGES, 1999). A não linearidade na absorção pela molécula pode estar relacionada, também, a outros fenômenos que podem ocorrer simultaneamente durante o processo de irradiação para condições que independem de concentração. Conforme relatado por Serra e Terentjev (2008), mesmo em baixas concentrações, se a 17 intensidade de iluminação superar um determinado nível de limiar, sempre produzirá um efeito dinâmico não linear equivalente ao foto branqueamento. Modificações na estrutura de uma molécula em função da interação com determinada radiação eletromagnética indica que um processo de absorção deve ter ocorrido. A absorção de radiação por uma molécula é, geralmente, o resultado de uma transição eletrônica, e pode ser estudada pela espectroscopia. Uma transição eletrônica corresponde à promoção de um elétron do estado fundamental para outro estado de maior energia durante o processo de absorção de radiação eletromagnética. A absorbância pode ser medida tanto por lente térmica quanto por transmitância. Porém, existe uma diferença importante que deve ser considerada, entre a absorbância, medida através da transmitância, e o espectro de lente térmica. O método de lente térmica mede a energia absorvida pelo material como calor, e por sua vez, o método de transmitância mede o total de energia da onda eletromagnética perdida durante a propagação pelo meio. Porém, os espectros de transmitância e de lente térmica serão iguais se não existirem efeitos adicionais além do aquecimento. No entanto, se um meio tiver alta fluorescência, Raman ou outros tipos de espalhamento de luz, o espectro de absorbância medido por transmitância poderá não ser o mesmo que o espectro de Lente Térmica (HUNG et al., 2004). Considerando a grande maioria de compostos fotossensíveis, que possuem baixa eficiência em emissões radiativas e espalhamento, em decorrência de sua capacidade de gerar espécies reativas de oxigênio, tanto a técnica de lentes térmicas quanto a técnica de transmitância serão eletivas. A técnica de transmitância para medir absorbância leva vantagem por não demandar instrumentação sofisticada e ser suficiente para registrar eventos da ordem de milissegundos. 18 1.1. Objetivo geral Registrar o comportamento transiente da absorção óptica em um composto fotossensível aplicado em Terapia Fotodinâmica. 1.2. Objetivos específicos • Identificar as condições experimentais necessárias para registrar o evento; • Registrar o comportamento transiente para solução agregada; • Registrar o comportamento transiente para solução monomérica; • Relacionar o comportamento transiente com a intensidade de agregação. 19 2. REVISÃO BIBLIOGRÁFICA 2.1. Uso dos corantes associados à radiação luminosa para fins medicinais As primeiras aplicações de corantes associados à radiação luminosa datam de aproximadamente 4000 anos. Nesta época os antigos Egípcios usavam uma combinação de extratos de uma determinada planta, Ammi majus, administrada oralmente com posterior exposição à radiação solar para tratar vitiligo. Os Gregos e Indianos também faziam tratamentos semelhantes, porém utilizando sementes de Psoralea corylifolia, para tratar psoríase além do vitiligo. Todo esse conhecimento, embora apresentasse resultados, não obteve grande repercussão por séculos, ganhando evidência apenas no final do século XIX e início do século XX, na civilização Ocidental, com o pesquisador Dinamarquês Niels Finsen e os alemães Oscar Raab e Herman Von Tappeiner (CHOUDHARY; NOURI; ELSAIE, 2009). Os primeiros experimentos científicos, envolvendo corantes e radiação luminosa, foram conduzidos por Raab e seu professor Tappeiner em 1900, quando se observou a morte de um protozoário exposto simultaneamente ao corante acridina e radiação solar. Pouco tempo depois, Von Tappeiner, em novos experimentos, demonstrou que a ocorrência da reação depende também da presença de oxigênio. Em 1907 Tappeiner e Jodlbauer introduziram o termo “ação fotodinâmica” para descrever o fenômeno. Em 1913 Meyer-Betz injetou em si próprio 200 mg de hematoporfirina sem apresentar nenhuma reação até o momento em que se expôs a luz solar, quando ficou extremamente inchado, com persistência da foto sensibilidade por diversos meses. Em 1925 Policard iniciou os estudos sobre porfirinas, avaliando a capacidade de produzir efeito foto tóxico, em observações clínicas (ACKROYD et al., 2001; STERNBERG; DOLPHIN, 1998). Embora evidências de sucesso na aplicação dessa técnica em bactérias, vírus e protozoários, tenham sido demonstradas bem antes da Segunda Guerra, seu uso foi abandonado devido à popularização das sulfonamidas e da penicilina. O retorno da aplicação antimicrobiana de agentes fotossensíveis na última década é resultado de dois fatores: a disseminação da AIDS por meio do HIV e o enorme crescimento das infecções hospitalares devido às bactérias resistentes aos fármacos (MOTTA; GIAVINA-BIANCHI, 2005). 20 A evolução microbiana é muito mais rápida que a do homem e desta forma o uso de fármacos nos hospitais promoveu a seleção natural dos mais adaptados. As bactérias patogênicas, que em pequena porcentagem são naturalmente resistentes a fármacos (tais como penicilinas), logo se tornam a população dominante. Considerando, que os agentes fotossensíveis agem via produção de oxigênio singlete e que não existe resistência microbiana natural, não importará se a cepa é resistente a uma ou muitas classes de agentes antibacterianos a TFD será efetiva (PERUSSI, 2007). Diversos estudos relataram resultados efetivos na aplicação da TFD. Como o estudo realizado por Hashimoto et al. (2009), que aplicaram a TFD em uma cepa resistente de Pseudomonas aeruginosa, utilizando como composto fotossensível o corante Hipocrelina B associado à irradiação com luz azul, e observaram efetiva redução da cepa em modelo animal. Outro estudo que investigou a possibilidade de as células bacterianas recuperarem sua atividade e desenvolver resistência póstratamento com TFD foi realizada por Tavares et al. (2010). Neste estudo foi utilizado 5,10,15-tris(1-Methylpyridinium-4-yl)-20-(pentafluorophenyl)-porphyrin triiodide (TriPy+-Me-PF) como composto fotossensível contra Vibrio fischheri e Escherichia coli. A TFD foi capaz de destruir eficientemente bactérias Gram-negativas, sem recuperação da viabilidade bacteriana, indicando que a Terapia não induz mecanismos de resistência. Existem fatores importantes que podem afetar a eficiência da TFD. Dentre eles inclui-se comprimento de onda da luz de excitação, profundidade de penetração da luz em tecidos biológicos, resposta tecidual ao oxigênio singleto, agregação e propriedades fotofísicas de compostos fotossensíveis (KOLÁROVÁ et al., 2003). A busca por uma molécula que atenda a todas estas características tem motivado diversos grupos de pesquisa a desenvolver novas opções, seja pela descoberta de novas moléculas ou pela modificação de moléculas conhecidas atribuindo características, desejáveis, que a molécula original não possuía. 21 2.2. Compostos Fotossensíveis 2.2.1. Compostos fotossensíveis de primeira geração Photofrin® e Derivados de Hematoporfirina são conhecidos como a primeira geração de compostos fotossensíveis. Possuem uma mistura complexa de estruturas monoméricas, diméricas e oligoméricas, tem o índice de máxima absorção (εmax) baixo e alto rendimento quântico (ORMOND; FREEMAN, 2013). Considerando o Photofrin® tem-se εmax para 630 nm de ~3.000 M-1 cm-1, enquanto o Azul de Toluidina apresenta εmax da ordem de 30.000 M-1 cm-1. O baixo valor de εmax indica que o Photofrin® absorve fracamente neste comprimento de onda. Basicamente, quanto maior for o valor de εmax maior será o potencial do efeito fotodinâmico. Em contrapartida, o Photofrin® possui alto rendimento quântico para oxigênio singleto, Φ∆ = 0,89, que indica alta eficiência na geração desta espécie por fóton absorvido (ORMOND; FREEMAN, 2013). Dentre as aplicações do Photofrin, aprovadas pela FDA dos Estados Unidos, estão: tratamento de câncer de bexiga, esôfago, pulmão, além de câncer localizado na cabeça, pescoço, abdômen, tórax, intestino, pele, mama e cervical (ORMOND; FREEMAN, 2013). 2.2.2. Compostos fotossensíveis de segunda geração As deficiências da primeira geração de compostos fotossensíveis, tais como fototoxicidade residual, baixa absorção na região vermelha do espectro visível, além da mistura complexa decorrente do método de síntese, direcionaram o avanço para a segunda geração de compostos fotossensíveis. Dentre os compostos fotossensíveis de segunda geração estão as Porfirinas, Clorinas, Feoforbídeos, Bacteriofeoforbideos, Texafirinas e Ftalocianinas. Embora a estrutura porfirinóide compreenda a maioria dos compostos fotossensíveis, diversos cromógenos não porfirínicos exibem atividade fotodinâmica. Estes compostos incluem Antraquinonas (COMINI et al., 2011), Xantenos (WANG et al., 2006), Cianinas (KULBACKA et al., 2011), Curcuminoides (HAUKVIK et al., 22 2009) e Fenotiazinas (GIROLDO et al., 2009; GIRONÉS et al., 2006; GONZALES et al., 2010; MUNIN et al., 2007). As fenotiazinas se destacam principalmente por sua intensa absorção na região entre 620 e 660nm, importante para TFD, pois esta faixa espectral apresenta boa penetração nos tecidos biológicos. Dos corantes pertencentes a este grupo, tem recebido grande atenção o Azul de Metileno e o Azul de Toluidina, que são compostos com estrutura química e propriedades físico-químicas similares. Os corantes fenotiazínicos são moléculas catiônicas com estrutura fundamental composta por um sistema de anel aromático tricíclico planar, que constitui um sistema altamente conjugado, funcionando como cromóforo destes compostos (BUCK, 2009). Os primeiros corantes fenotiazínicos foram sintetizados no final do século XIX, durante o que pode ser considerado o período da “corrida do ouro”, período de experimentações químicas após a descoberta dos primeiros corantes anilínicos. A síntese do corante fenotiazínico Azul de Metileno foi descrita por Caro em 1876, e sua aplicação como fármaco antimalárico por Ehrlich 15 anos depois (GUTTMANN; EHRLICH, 1960). Em termos de pesquisa de medicamentos, isso torna o sistema anel fenotiazínico um dos heterociclos estabelecidos há mais tempo e a síntese química dos fenotiazínicos é bem entendida, permitindo fácil preparação de análogos (PERUSSI, 2007). Os corantes fenotiazínicos oferecem uma abrangência maior no tratamento de enfermidades que outros tipos de corantes, e certamente maior que outros tipos de compostos fotossensíveis. Assim, corantes como o Azul de Metileno e Azul de Toluidina tem sido bastante utilizados como drogas em pesquisas contra infecção bacteriana local, devido a sua pronunciada capacidade para permear a membrana celular e realizar atividade foto-bacteriana (LIU; ZOU; UM, 2010), também é utilizado contra tuberculose, malária (AMARAL; VIVEIROS; KRISTIANSEN, 2001), infecção por fungos (SOUZA et al., 2010), tripanossomose, colonização viral do sangue (GIRONÉS et al., 2006) e câncer (JUNAID et al., 2012). Dentre outros corantes, apenas os acridinos aproximam-se de sua versatilidade. Para quaisquer compostos fotossensíveis propostos, os efeitos causados pela radiação luminosa e espécies reativas de oxigênio produzidas no composto devem ser considerados. Para o caso de aplicações terapêuticas, a decorrente fotodegradação pode ser interessante, pois minimizaria a fotosensibilidade para o 23 paciente. Porém, no caso de aplicações prolongadas, como por exemplo, em desinfecção é fundamental que a fotodegradação seja mínima para estender a eficácia do composto fotossensível. No caso do Azul de Metileno e Azul de Toluidina, a irradiação pode provocar fotodegradação, por exemplo, com a formação de produtos de degradação via mecanismos fotoquímicos. Contudo, o grau de decomposição é função da intensidade da irradiação, luz com alta intensidade irá causar maior degradação que luz de baixa intensidade, e de maneira similar, por longos períodos de iluminação comparados com períodos mais curtos. No caso de tratamentos clínicos as condições de iluminação devem, portanto, ser consideradas para simplificar o espectro toxicológico resultante e para garantir a melhor concentração do composto fotossensível (WAINWRIGHT; GIDDENS, 2003). As alterações nas propriedades espectroscópicas e eletroquímicas de moléculas orgânicas, pela interação com mediadores e moléculas biológicas têm recebido grande interesse, também, nas áreas de sensores e biosensores. As propriedades redox e fotoquímica do Azul de Toluidina também levaram a um aumento no interesse em dispositivos fotovoltaicos devido a sua possível capacidade de atuar como transdutor de luz para energia elétrica (ILANCHELIAN; RAMARAJ, 2011). 2.3. Agregação em Corantes A agregação é um fenômeno que ocorre com corantes em solução e que pode afetar as propriedades fotofísicas destes e, portanto sendo de grande importância no estabelecimento de protocolos. É conhecida a tendência de corantes iônicos formarem agregados em soluções diluídas, levando a formação de dímeros e algumas vezes agregados de ordens maiores. Neste caso a natureza molecular do corante é afetada, e, portanto, relacionada com concentração e estrutura do corante, força iônica, temperatura e presença de solventes orgânicos. Embora os corantes sejam muito individualizados como estrutura e comportamento, algumas regras gerais estão bem estabelecidas em relação à agregação em geral. A agregação pode aumentar com o aumento da concentração do corante ou força iônica, e poderá diminuir com o aumento da temperatura ou adição de solventes orgânicos (ANTONOV et al., 1999). 24 Uma das características do Azul de Toluidina relacionada à agregação é denominada metacromasia e está relacionada com a variação pronunciada de sua banda de absorção no espectro visível. Contudo as variações espectrais não são do mesmo tipo para todos os corantes, sendo possível fundamentalmente distinguir três mecanismos de agregação e, portanto, três diferentes tipos de efeitos espectroscópicos. O primeiro mecanismo é chamado agregação H e consiste de um arranjo paralelo das moléculas formando uma pilha vertical. O efeito espectroscópico decorrente de tal organização molecular é um deslocamento hipsocrômico da banda de absorção, ou seja, deslocamento para a região azul do espectro com respeito ao monômero (D´ILARIO; MARTINELLI, 2006). O segundo é a agregação J e consiste no arranjo “cabeça-cauda” das moléculas de corante formando uma pilha inclinada. Neste caso o efeito espectroscópico decorrente é um deslocamento batocrômico da banda de absorção, ou seja, deslocamento para a região vermelha do espectro com respeito ao monômero (D´ILARIO; MARTINELLI, 2006). O terceiro mecanismo consiste na geometria intermediária, obliqua, para a qual uma divisão na banda é observada, ou seja, tanto a banda no azul quanto a banda no vermelho aparecem (D´ILARIO; MARTINELLI, 2006). Quando duas moléculas idênticas ficam muito próximas uma da outra, sob irradiação, seus momentos de dipolo de transição começarão a interagir. Este fenômeno, também conhecido como acoplamento excitônico é ilustrado na Figura 1 (KASHA, 1963). 25 Figura 1: Diagrama de excitação para dímeros em diferentes arranjos geométricos de dipolos. Fonte: Adaptado de Kasha, Rawls e Ashraf El-Bayoumi (1965) Quando dois dipolos são trazidos para muito próximo um do outro, alinhados lado a lado, com orientação, tanto paralela quanto antiparalela, influenciarão a energia do monômero. Basicamente a energia do monômero, E, será dividida em dois novos estados com energia E’’ e E’, sendo que dipolos paralelos repelem um ao outro e alcançam maiores estados energéticos, enquanto dipolos antiparalelos se atraem reduzindo a energia daquele estado. Tem-se ainda que dipolos paralelos geram um momento de dipolo altamente elevado, resultando em forte absorção, enquanto dipolos antiparalelos cancelam um ao outro resultando em fraca absorção. O resultado líquido é que a banda de absorção será deslocada para o azul (maior energia). De forma similar, no arranjo cabeça-cauda o estado de energia mais baixa terá maior momento de dipolo que resultará em um deslocamento da banda de absorção para o vermelho (menor energia). Para o arranjo obliquo o resultado será o aparecimento de banda tanto para o estado mais energético quanto para o menos energético (KASHA, RAWLS, ASHRAF EL-BAYOUMI, 1965). 2.4. Fenômenos fotoinduzidos Dentre os principais fenômenos induzidos pela luz em materiais, pode-se destacar o fotoescurecimento, o fotobranqueamento, o fotocromismo e a fotocristalização. Estes fenômenos podem ser causados por quebras ou formação de ligações 26 químicas, geração e recombinação de cargas durante o processo de irradiação (BRAJATO, 2010). Dentre esses processos, o fotobranqueamento é mais facilmente induzido em meios líquidos. Para corantes em solução, pode ocorrer o decréscimo da energia relativa absorvida pela amostra com o aumento da irradiância de excitação. Isto acontece quando a taxa de excitação óptica é maior que a taxa em que as moléculas retornam para o estado fundamental. O decréscimo da absorção para altas irradiâncias originam-se por saturação óptica ou branqueamento óptico. Em um sistema de dois níveis, a saturação óptica ocorre na medida em que o estado excitado é preenchido por uma quantia significante de moléculas e a taxa de transição pela absorção se iguala a emissão estimulada. Com poucas moléculas no estado fundamental, a quantia de energia absorvida decresce (BRENNETOT; GEORGES, 1999). No sistema de três níveis, o branqueamento óptico do corante ocorre pela remoção de espécies do estado fundamental produzindo espécies metaestáveis. Considerando que a relaxação do estado metaestável é mais lenta que sua formação, tanto o estado fundamental quanto o primeiro estado excitado tenderão a se esvaziar (BRENNETOT; GEORGES, 1999), conforme ilustrado na Figura 2. Figura 2: Ilustração de um sistema genérico de 3 níveis. Sm representa um estado metaestável que compreenderá a maior parte das moléculas durante o processo de branqueamento. Fonte: Autor. 27 3. MATERIAL E MÉTODOS 3.1. Preparo das amostras Foi escolhido, como objeto de estudo, o corante fenotiazínico Azul de Toluidina devido a sua característica de absorção, com banda na região do vermelho, importante para aplicações em TFD. O corante Azul de Toluidina, para microscopia (AZUL DE TOLUIDINA-O, CI 52040, Vetec Química Fina, Duque de Caxias, Rio de Janeiro, Brasil) foi utilizado sem purificação adicional, com teor mínimo de 85 % de corante. Os experimentos foram realizados em temperatura ambiente. O corante Azul de Toluidina utilizado possui fórmula molecular C15H16Cl3N3SZn e peso molecular de 442,12. A estrutura básica é apresentada na Figura 3. Figura 3: Estrutura molecular do Azul de Toluidina. Fonte: Chemical book (online). Foram preparadas duas soluções do corante Azul de Toluidina. A primeira utilizou como solvente água destilada, com concentração resultante de 500 µM, e a segunda utilizou Álcool Etílico (Álcool Etílico Absoluto P.A.-A.C.S., LABSYNTH Produtos para Laboratórios Ltda, Diadema, São Paulo, Brasil), também com concentração resultante de 500 µM. Ambas as soluções foram homogeneizadas por agitação durante 10 min em agitador magnético (752A, Fisatom Equipamentos Científicos Ltda., São Paulo, São Paulo, Brasil) A partir dessas soluções foram preparadas diluições nas concentrações 100, 200, 300 e 400 µM para cada solvente. 28 3.2. Medida do espectro de absorbância Foram registrados espectros de absorbância, em regime de baixo sinal, para cada diluição, em um espectrômetro (MS257, Oriel Instruments, Stratford, Connecticut, Estados Unidos da América) equipado com câmera CCD intensificada com 256x1024 pixels e grade de difração de 300 linhas/mm. Como compartimento de amostra uma célula construída com duas placas de vidro paralelas, espaçadas por um anel de aço inox, resultando em um caminho óptico de 1,1 mm, conforme ilustrado na Figura 4. Figura 4: Célula para amostra líquida, construída com duas placas de vidro espaçadas por um anel de aço inox. Fonte: Autor. Os resultados da medida de absorbância foram tratados via software (Microcal OriginTM 6.0, Microcal Software, Inc., Northampton, Massachusetts, Estados Unidos da América) e apresentados em formato gráfico. A partir dos gráficos, as soluções foram avaliadas quanto à formação de agregados. 3.3. Montagem experimental 3.3.1. Tempo de resposta do obturador eletromecânico A montagem experimental empregada neste estudo consiste em um sistema de medida da porção de luz transmitida pelo corpo de prova em função do tempo, para 29 uma função de excitação do tipo degrau ascendente. O controle do feixe de excitação foi realizado por um obturador eletromecânico (Electronic Shutter, Coherent, Inc., Santa Clara, Califórnia, Estados Unidos da América), com fonte programável, posicionado próximo da amostra. O tempo de resposta foi medido utilizando um gerador de sinal (MFG-4200, Minipa, São Paulo, São Paulo, Brasil), ajustado para gerar uma onda quadrada com frequência arbitrária. A forma de onda gerada foi utilizada para disparar o funcionamento do obturador. A medição do tempo de resposta do sistema foi realizada utilizando como referência a resposta de um fotodiodo (MRD500, ON Semiconductor, Phoenix, Arizona, Estados Unidos da América), com tempo de resposta típico de 1ns, em relação à incidência de um feixe laser (He-Ne, Melles Griot, Carlsbad, Califórnia, Estados Unidos da América), λ=632,8 nm, com 13,8 mW de potência óptica. Acoplado a um osciloscópio digital (TDS 724C, Tektronix, Inc., Beaverton, Oregon, Estados Unidos da América), com 500 Mhz de largura de banda. O fotodiodo mediu a intensidade luminosa transmitida em função do tempo durante o movimento de abertura da íris do obturador eletromecânico. 3.3.2. Medida do perfil do feixe laser na posição do corpo de prova Para aumentar a densidade de energia depositada no corpo de prova, foi utilizada uma lente convergente (KPX115, Newport Corporation, Franklin, Massachusetts, Estados Unidos da América), com distância focal de 40 cm. De modo a conhecer as características do feixe laser na posição do corpo de prova foram feitas medidas de diâmetro e perfil utilizando um sistema de medida e diagnóstico de feixe (BeamMaster PC, Coherent, Inc., Santa Clara, Califórnia, Estados Unidos da América), com capacidade para medir perfis de intensidade de feixe, largura, posição, potência e forma básica de feixes provenientes de lasers contínuos. O princípio de funcionamento do dispositivo baseia-se em múltiplas bordas de lâmina que cruzam o feixe e capturam a distribuição de intensidade do laser. O dispositivo foi posicionado na distância focal da lente, de modo a estudar o feixe na mesma posição do corpo de prova. 30 O resultado da medida foi exportado em formato ASCII e imagem. O arquivo ASCII foi tratado via software (Microcal OriginTM 6.0, Microcal Software, Inc., Northampton, Massachusetts, Estados Unidos da América) e apresentado em formato gráfico para análise e medida do diâmetro do feixe, em conjunto com a imagem tridimensional do feixe. 3.3.3. Fotodetectores Para medir o sinal transmitido pelo corpo de prova e também disparar a aquisição do osciloscópio durante as medidas foram utilizados fotodiodos (13DSI007, Melles Griot, Carlsbad, Califórnia, Estados Unidos da América). Para medida do sinal foi posicionado um fotodiodo após o corpo de prova, alinhado ao feixe laser, e outro para disparar a aquisição, perpendicular ao feixe laser, entre o obturador eletromecânico de bloqueio e o corpo de prova. O disparo da aquisição se dá com a reflexão gerada por uma lâmina de vidro, com 1 mm de espessura, a 45° no caminho do feixe laser. Os dois fotodiodos foram conectados ao osciloscópio, configurado para calcular a média entre 5 medidas consecutivas. O diagrama da montagem pode ser visualizado na Figura 5 e a imagem ilustrativa na Figura 6. Figura 5: Diagrama da montagem experimental, onde: d1 e d2 são detectores, cp corpo de prova, s é o obturador eletromecânico, I lente convergente, a é o filtro atenuador e L laser. Fonte: Autor. A região linear de resposta dos detectores foi caracterizada utilizando um laser de He-Ne emitindo luz no comprimento de onda de 632,8 nm atenuado por uma associação de filtros de densidade neutra (Filtros OD, Newport Corporation, Franklin, Massachusetts, Estados Unidos da América), de modo a criar várias condições de potência óptica. A potência emitida foi coletada integralmente pelo 31 detector, que acoplado a um osciloscópio digital (TDS 724C, Tektronix, Inc., Beaverton, Oregon, Estados Unidos da América), registrou a intensidade de sinal acoplado. O resultado da medida foi exportado em formato ASCII e posteriormente tratado via software (Microcal OriginTM 6.0, Microcal Software, Inc., Northampton, Massachusetts, Estados Unidos da América) e apresentado em formato gráfico para análise. Figura 6: Imagem ilustrativa da montagem experimental, onde: d1 e d2 são detectores, cp corpo de prova, s obturador eletromecânico, I lente convergente, a filtro e L laser. Fonte: Autor. Para a avaliação do tempo de resposta dos detectores foi utilizado um laser semicondutor emitindo no comprimento de onda de 532 nm no modo chaveado, controlado por um gerador de sinal (MFG-4200, Minipa, São Paulo, São Paulo, Brasil), produzindo uma frequência em forma de onda quadrada de 43 Hz. Uma fração do feixe laser foi coletada pelos detectores que acoplados a um osciloscópio (TDS 724C, Tektronix, Inc., Beaverton, Oregon, Estados Unidos da América), registraram o tempo de decaimento do sinal. O tempo de resposta do detector com relação ao momento de chaveamento do laser, ligado para desligado, foi registrado para cada detector, processados via software (Microcal OriginTM 6.0, Microcal Software, Inc., Northampton, Massachusetts, Estados Unidos da América) e exibidos em formato gráfico para comparação. 32 3.4. Definição dos parâmetros de medida Para definir o tempo de duração da medida foi realizado um estudo preliminar com o corante Azul de Toluidina dissolvido em água destilada na concentração de 500 µM. Foram feitas medidas com janela temporal de 500 ms. Para avaliar a resposta do corante em diferentes densidades de energia, foi controlada a potência óptica emitida pelo laser através da inserção de filtros de densidade neutra (Filtros OD, Newport Corporation, Franklin, Massachusetts, Estados Unidos da América), associados de forma a possibilitar 13 condições de potência diferentes. Os filtros foram inseridos entre o laser e a lente convergente. Para aferir a potência óptica em cada condição de atenuação foi utilizado um medidor de potência (Field Master, Coherent, Inc., Santa Clara, Califórnia, Estados Unidos da América) com detector (LM-1, Coherent, Inc., Santa Clara, Califórnia, Estados Unidos da América), posicionado logo após a lente convergente. 3.5. Estudo da energia acumulada na amostra Verificou-se matematicamente uma estimativa da quantidade de energia que seria acumulada na amostra durante a irradiação. Para este cálculo foi considerado o diâmetro do feixe laser na posição da amostra, o caminho óptico percorrido pelo feixe na amostra, o tempo de irradiação e a potência óptica incidente. 3.6. Coleta dos dados experimentais Para cada concentração foi registrada uma média de 5 aquisições para cada potência óptica de excitação. Após cada variação de potência foi registrada a medida do solvente correspondente à solução como referência da transmissão máxima. A incidência do feixe laser foi concêntrica com a célula. Para minimizar eventual acúmulo de calor entre cada uma das 5 medidas consecutivas foi adotado um tempo de 30 s para acomodação térmica da amostra. Tanto para as soluções quanto para os solventes, foram registrados os sinais transmitidos e a fração refletida pela lâmina de vidro, utilizada para disparar a aquisição no osciloscópio. 33 Os dados, salvos em ASCII, foram extraídos do osciloscópio e processados via software (Microcal OriginTM 6.0, Microcal Software, Inc., Northampton, Massachusetts, Estados Unidos da América). Após o tratamento os dados foram exibidos em formato gráfico para análise. 34 4. RESULTADOS 4.1. Medida do espectro de absorbância Após o preparo e diluição das soluções, foram obtidos os espectros de absorbância em regime de baixo sinal para cada uma das diferentes diluições. Os resultados estão apresentados na Figura 7 e na Figura 10. Na Figura 7 são apresentados os espectros de absorção para as amostras de Azul de Toluidina diluídas em água destilada, incluindo a medida do solvente. Notase que o aumento da absorbância exercida pelos agregados diméricos, representada pela banda centrada em 590 nm é superior ao aumento da absorção atribuída aos monômeros, representada pela banda centrada em 630 nm. Figura 7: Espectro de absorção para as amostras de Azul de Toluidina diluídas em água destilada, em diferentes concentrações. Relacionando o valor da absorbância em função da concentração, tanto para o dímero quanto para o monômero, pode-se encontrar a relação do aumento da absorbância com a concentração. De acordo com os resultados apresentados na 35 Figura 8, tem-se que o aumento da absorção para agregados é linear para a faixa estudada, porém, para o monômero a tendência é não linear, descrevendo um polinômio de segundo grau que se afasta da linearidade logo após a concentração de 100 µM. Figura 8: Aumento da absorbância pelos dímeros (λ=590 nm) e monômeros (λ=630 nm) em função do aumento da concentração. Avaliando-se então a relação entre as absorbâncias nos comprimentos de onda característicos para dímeros e monômeros, tem-se que o aumento da absorbância da espécie monomérica tende à saturação em função do aumento da concentração da solução o que sugere um aumento da espécie dimérica superior ao da monomérica, conforme pode ser visualizado na Figura 9. 36 Figura 9: Relação entre as intensidades das absorções medidas nos comprimentos de onda de pico das bandas relativas ao dímero (590 nm) e ao monômero (630 nm) em função da concentração. Para as amostras preparadas com Azul de Toluidina dissolvido em álcool etílico PA também foram obtidos os valores de absorbância em função da concentração e os resultados estão apresentados na Figura 10, na qual se pode verificar a presença majoritária de monômeros, identificada pelo pico em 630 nm, embora ainda ocorra formação de agregados em proporção inferior, conforme apresentado na Figura 11. 37 Figura 10: Espectro de absorbância para diferentes concentrações de Azul de Toluidina diluído em álcool Etílico. Figura 11: Aumento da absorbância medida no pico da banda dimérica (λ=590 nm) e no pico da banda monomérica (λ=630 nm) em função da concentração para solução aquosa. 38 Conforme resultados encontrados para a solução em água destilada, também se verifica na solução etanólica o mesmo regime no aumento da absorbância, linear para os dímeros e não linear para os monômeros, embora em taxas de aumento diferentes. Calculando a relação de absorbancias entre os picos das bandas relativas a dímeros e monômeros tem-se uma evolução polinomial de segunda ordem, porém, naturalmente, invertida, indicando o aumento de monômeros superior ao de dímeros, como pode ser visualizado na Figura 12. Figura 12: Relação entre as intensidades de pico das bandas de absorção relativas a dímeros e monômeros em função da concentração para solução etanólica. 4.2. Medida do tempo de resposta dos componentes do sistema Duas das características dos detectores, que devem ser levadas em consideração, é o material do qual o detector foi construído e o tempo de resposta destes frente a um estímulo luminoso. Principalmente quando se deseja medir eventos rápidos. O material do qual o detector foi construído define a faixa espectral a qual esse dispositivo responderá. Como neste projeto objetiva-se medir radiação proveniente de um laser emitindo em 632,8 nm, naturalmente o detector deverá 39 responder com eficiência nesta região. Desta forma foram escolhidos detectores de silício por ter resposta espectral no intervalo de 350 a 1100 nm. Para avaliar o tempo de resposta dos detectores, foram realizadas medidas com detectores de 10 e 100 mm2 de área util. Utilizando como referência um detector com tempo de resposta típico de 1ns, MRD500, e como fonte de luz um laser de diodo com comprimento de onda de 532 nm chaveado eletronicamente. As respostas dos detectores, quando estimulados por um pulso laser, considerando o intervalo de tempo para decaimento do sinal é apresentada na Figura 13. Observa-se que conforme aumenta a área sensível do detector, diminui a velocidade de resposta do componente ao estímulo. O tempo de resposta foi de 0,93 µs para o MRD500, com área de 0,245 mm2, 5,5 µs para o 13DSI007, com área de 10 mm2, e chegando em 10,5 µs para o 13DSI011, com área de 100 mm2. Mesmo os fotodetectores, de 10 e 100 mm2, escolhidos para a experimentação terem respondido ao estímulo 5 e 10 vezes, respectivamente, mais lento que o fotodetector de referência, ainda estará a aproximadamente 1000 vezes mais rápido que o evento estudado neste trabalho. Figura 13: Validação dos detectores com relação ao tempo de resposta frente ao feixe laser chaveado. Para os detectores 13DSI007 e 13DSI011 foi utilizado filtro OD 0,8. 40 De acordo com os resultados encontrados, optou-se pelo detector 13DSI007, com área de 10 mm2, por ter tempo de resposta compatível com a velocidade dos eventos em estudo e área grande o suficiente para garantir a coleta de todo o feixe transmitido nas medidas com amostras diluídas em água. Entretanto, o detector 13DSI011 também apresenta tempo de responda adequado ao experimento. Para gerar a função excitação desejada (degrau ascendente) e para controlar o tempo de exposição do corante à radiação laser foi utilizado um obturador eletromecânico. Este sistema foi avaliado quanto ao tempo necessário para movimentar as cinco lâminas que compõem a íris, no sentido de abertura. O tempo médio medido para esse movimento foi 315 µs quando o feixe de excitação foi posicionado próximo à região central da íris. É intuitivo que a lâmina da íris atingirá velocidade máxima no final de seu movimento, ou seja, próximo da abertura total. Por este motivo, foi avaliado também o tempo de desobstrução do feixe para a condição em que este incide próximo a borda do dispositivo, conforme registrado na Figura 14. Figura 14: Posição do feixe com relação à área da íris. Fonte: Autor. 41 Nesta condição o dispositivo leva 280 µs para desobstruir o caminho do feixe de luz laser. Desta forma, esta foi a condição de trabalho escolhida, por permitir uma borda de subida mais íngreme para o sinal de excitação. Para aumentar a densidade de energia depositada no corpo de prova, foi adicionada uma lente convergente com distância focal de 40 cm (KPX115, Newport Corporation, Franklin, Massachusetts, Estados Unidos da América), com a distância focal ajustada para coincidir com a posição da amostra. Visando obter chaveamento mais rápido do feixe, o sistema eletromecânico de modulação foi posicionado próximo do foco, onde o diâmetro do feixe é menor. Desta forma, foi possível obter sinal de excitação com borda de subida da ordem de 250 µs. 4.3. Medida da linearidade na resposta do sistema Foi caracterizado o fotodetector escolhido para a montagem experimental, 13DSI007, quanto à região linear de trabalho. A curva de resposta foi medida para o comprimento de onda de 632,8 nm e os resultados podem ser visualizados na Figura 15. Avaliando a resposta do detector, que é medida em função da diferença de potencial registrada entre seus terminais, verifica-se que os 4 mW incidentes induzem uma diferença de potencial de 14 V. Apenas para valores de tensão no fotodetector inferiores a 14 V a resposta será linear e de forma a garantir que nenhuma medida extrapolasse a região linear, foi atribuído uma tolerância de 20%, limitando a região de trabalho para diferenças de potencial inferiores a 11,5 V. Considerando que a amostra será irradiada com potência óptica superior a 4 mW será necessário aumentar a faixa de trabalho com a adição de filtros de densidade neutra com atenuação conhecida e posteriormente, na etapa de processamento dos dados, corrigir os sinais matematicamente em função do filtro utilizado. Na Figura 15 tem-se dois conjuntos de medidas onde foram empregados filtros OD 0,6 e OD 1,0, para potências de excitação superiores a 4 mW. Verifica-se que o conjunto de medidas onde foi utilizado o filtro OD 1,0 apresentou um pequeno desvio da linearidade. Esse desvio se deve a grande atenuação exercida por esse filtro, considerando que a densidade óptica do filtro (OD) pode ser expressa da seguinte forma: 42 OD = −logT , onde Tλ é a transmissão para o comprimento de onda λ. Teremos, para o filtro de OD 1,0, a transmitância de 10% resultando em um nível de sinal baixo para as condições iniciais de irradiação e consequentemente de baixa resolução para o detector. Desta forma optou-se pelo filtro OD 0,6 que permite uma transmitância de 25%, estendendo a faixa de trabalho para radiação incidente e mantendo a linearidade da resposta do fotodetector. Figura 15: Curva de resposta do detector em função da potência do laser de He-Ne, comprimento de onda de 632,8 nm. Os valores de tensão na escala vertical esquerda são valores extrapolados. Foi medida também, a resposta do sistema para verificar possíveis desvios da linearidade quando no início da faixa útil do fotodetector. Como parâmetro foi utilizado o valor da amplitude inicial para cada condição de potência óptica de irradiação. Para este estudo foi coletado um conjunto de medidas a partir de uma solução preparada com água destilada na concentração de 500 µM, para simular uma condição de baixa transmissão. Essa solução foi inserida em uma célula com caminho óptico de 1,1 mm e posicionada no caminho óptico do laser, na distância focal da lente. Variou-se a 43 potência de excitação utilizando filtros de densidade neutra e para cada condição foi registrado o valor de tensão medido pelo osciloscópio. O resultado dessa medida está apresentado na Figura 16. Figura 16: Avaliação da resposta do sistema experimental para Azul de Toluidina, 500 µM, em função do incremento da potência do laser. A resposta, quando considerado o valor de intensidade no tempo zero registrado pelo osciloscópio para cada condição de potência óptica de excitação foi linear para a faixa de potência estudada. Desta forma, pode-se afirmar que mesmo para uma solução fortemente absorvedora, em alta concentração, o sistema responde linearmente. 4.4. Medida do perfil do feixe laser na posição da amostra A influência do acúmulo de energia na solução está relacionada com a geometria do feixe laser na região onde acontecerá a interação com a amostra. Desta forma, para caracterizar o feixe laser espacialmente, foi utilizado um sistema de medida e diagnóstico de feixe (BeamMaster PC, Coherent, Inc., Santa Clara, Califórnia, 44 Estados Unidos da América) com capacidade para medir o diâmetro e a distribuição espacial da energia do feixe. Com o sistema posicionado na exata posição onde será colocada a amostra, foi registrada uma média de 5 aquisições e o resultado está apresentado nas figuras, Figura 17 e Figura 18. Na Figura 17 é ilustrada tridimensionalmente a distribuição de energia na secção transversal do feixe laser. A distribuição de energia é indicada por faixas normalizadas com relação à área de maior energia. Além dessa identificação, esse gráfico facilita a rápida identificação do perfil do feixe laser. Gaussiano neste caso. O equipamento permite, também, a exportação dos dados relativos ao perfil transversal do feixe. Figura 17: Distribuição espacial de energia pela secção transversal do feixe laser. Fonte: Autor. Para o cálculo do perfil, o programa secciona o feixe em dois planos ortogonais representados pelos vetores V e W, identificados na imagem tridimensional. Desta forma pode-se calcular o diâmetro do feixe, além de verificar sua simetria radial, conforme apresentado na Figura 18, onde são apresentados os 2 perfis transversais do feixe laser. Desta forma, é possível extrair os valores numéricos de diâmetro do feixe, conforme Tabela 1. 45 Figura 18: Medida do perfil transversal do feixe laser. Tabela 1: Resultados das medidas do diâmetro do feixe na posição focal da lente Posição em relação à curva Diâmetro (µ µm) 1/e2 510,51 1/e 358,00 FWHM 292,91 (Largura plena a meia altura) 4.5. Tempo da aquisição Para ajustar o sistema em relação ao melhor período para se registrar o evento de interesse, foi registrada uma medida piloto da intensidade de luz transmitida pela amostra de Azul de Toluidina diluída em água destilada com 500 µM. O tempo da aquisição foi determinado em função da variação do sinal pelo tempo. Inicialmente optou-se por uma janela temporal com duração de 500 ms sob irradiação de uma fonte laser de 13,8 mW de potência em 632,8 nm, o resultado 46 pode ser visualizado na Figura 19. Para a amostra de Azul de Toluidina diluída em água destilada, verifica-se um rápido decaimento que descreve um decaimento exponencial de segunda ordem. Porém, este intervalo revela apenas parte do fenômeno. Figura 19: Medida da intensidade de transmissão em função do tempo para excitação de 13,8 mW em 632,8 nm e concentração de 500 µM em água. Para monitorar simultaneamente o estágio inicial de irradiação e o estágio de maior acúmulo de energia a janela temporal foi estendida. Foi definida uma nova janela temporal de 4,5 s. Considerando a mesma amostra de Azul de Toluidina diluída em água destilada com 500 µM, e mantendo a potência de excitação, foi adquirido um novo sinal transiente cujo resultado está apresentado na Figura 20. 47 Figura 20: Exposição prolongada, 4,5 s, para a amostra de 500 µM com 13,8 mW de potência do laser. Como o fenômeno de aumento da absorção, embora aconteça mais intensamente durante poucos milissegundos, tem desdobramento durante um tempo longo. Foi definida uma janela temporal de 4 s. Com este intervalo registram-se, basicamente, dois eventos distintos que ocorrem na amostra durante a irradiação. O primeiro refere-se à redução acentuada na transmissão e o segundo indica a tendência ao equilíbrio termoquímico na amostra. 4.6. Calculo da energia acumulada durante a irradiação Para promover a incidência de grande quantidade de energia na amostra são utilizadas lentes convergentes distanciadas da amostra pelo comprimento focal. A posição focal será a menor área possível e consequentemente a de maior densidade de energia. Para verificar a quantidade de energia depositada na amostra precisa-se medir o raio do feixe de luz laser nesta região. O resultado encontrado foi de 255,25 µm (1/e2). Em função da característica gaussiana do feixe laser pode-se 48 calcular a Intensidade de Pico no eixo do feixe com aplicação da seguinte equação: (QUIMBY, 2006) Iz = P 1 πω z 2 onde P é a potência total do feixe e ω é o raio do feixe na posição z. Substituindo os valores medidos, para P=1,2 mW, na equação acima ter-se-á: Iz = 1,2mW 1 255 × 10 cm 2π × = 1,17W/cm Para as demais intensidades de potência ter-se-ão as seguintes intensidades de pico: Tabela 2: Cálculo da intensidade no centro do feixe gaussiano para cada potência óptica estudada. Potência Óptica (mW) Intensidade de Pico (W/cm2) 1,2 1,17 1,4 1,37 2,3 2,25 2,8 2,74 3,7 3,62 4,8 4,69 6,1 5,96 7,0 6,84 7,6 7,43 8,2 8,01 9,5 9,28 11 10,7 12 11,7 49 Como no foco da lente o laser tem um diâmetro de 510,5 µm (1/e2) e a célula tem comprimento de 1,1 mm, então o volume cilíndrico excitado pode ser expresso por: πD V=! #×h 4 onde D é o diâmetro do cilindro e h a altura do mesmo, que corresponde à espessura da célula. Aplicando os valores para D e h ter-se-á: π510,5 × 10% m V=! # × 1,1 × 10& m = 225,15 × 10' m& 4 A massa m de água dentro deste volume irradiado é calculada por: m = ρV onde m é a massa [kg], ρ é a massa específica [kg] e V o volume por ela ocupado [m3]. Aplicando os valores para ρ (massa específica da água) e V (volume calculado) anteriormente, ter-se-á: m = )1000 kg + × 225,15 × 10' m& m& m = 225,15 × 10, kg Para elevar a temperatura da água, partindo da temperatura ambiente, Tamb=25 °C, à 100 °C, ou seja, ∆T=75 K, será necessário uma energia Q dada por: Q = mc∆T onde m é a massa da água e c o calor específico da água (4,1813 J/gK). 50 Q = 225,15 × 10% g × 4,1813 ) J + × 75K = 70,6mJ gK Considerando que a amostra foi irradiada com potências ópticas que variaram entre 1,2 e 12 mW, podemos estimar, para a situação limite em que difusão térmica e transporte de massa não sejam contabilizados, os tempos para acumular a energia acima calculada: E= P×t Tabela 3: Tempo, estimado, necessário para se elevar a temperatura do meio em função da potência óptica (*). Potência absorvida (mW) Tempo para acumular 70,6 mJ (s) Energia acumulada em 4,5 s (mJ) ∆TPI estimado 1,2 58,8 5,4 5,74 1,4 50,4 6,3 6,69 2,3 30,7 10,35 11,0 2,8 25,2 12,6 13,4 3,7 19,1 16,65 17,7 4,8 14,7 21,6 22,9 6,1 11,6 27,45 29,2 7,0 10,1 31,5 33,5 7,6 9,29 34,2 36,3 8,2 8,61 36,9 39,2 9,5 7,43 42,75 45,4 11 6,42 49,5 52,6 12 5,88 54 57,4 (pós irradiação) (°C) (*) Cálculos em primeira aproximação, não contabilizando transporte de calor e de massa e pressupondo absorção total da energia do feixe do laser pela amostra. Os cálculos mostrados na Tabela 3 sugerem que não haverá ebulição da amostra no volume irradiado. 51 4.7. Registros para Azul de Toluidina diluído em água destilada Com a definição da janela temporal para registro do evento, procedeu-se a medida de absorbância, resolvida no tempo, para cada diluição em 13 diferentes condições de potência de excitação. As amostras diluídas em água destilada compuseram o primeiro conjunto estudado. Dentre essas amostras optou-se por iniciar pela maior concentração, 400 µM, devido a sua capacidade de agregação superior. Os resultados para diferentes potências de excitação (λ=632,8 nm) variando de 1,21 a 12,3 mW estão apresentados na Figura 21. Para comparar os resultados alcançados com as diferentes concentrações, se relacionou a diferença (∆) entre o registro de transmitância inicial, tempo 0, e o registro após 1 s do início da irradiação, para cada condição de intensidade de transmissão em função da concentração. Os resultados normalizados para a concentração de 400 µM, Figura 22, indicam uma redução na transmissão, para 632,8 nm, em função do aumento da energia depositada na amostra. Essa redução de transmissão segue uma tendência linear. Conforme hipótese inicial, a absorbância aumenta com o tempo de irradiação, sugerindo a ocorrência de conversão dímero monômero. Visando verificar possíveis modificações no comportamento transiente da absorbância em função da quantidade relativa entre dímeros e monômeros na solução, foram medidas as amostras menos concentradas. Na Figura 23 estão os resultados para a concentração de 300 µM de azul de toluidina em solução aquosa. O aumento da absorbância em função do tempo se assemelha com os resultados encontrados para 400 µM, indicando a dominância do fenômeno de conversão dímero-monômero. Com relação ao ∆, Figura 24, se observa comportamento semelhante ao encontrado para a concentração de 400 µM, porém com maior espalhamento de dados para potências de excitação superiores a 6 mW. As concentrações mais baixas, 200 e 100 µM também foram caracterizadas quanto à absorbância transiente, Figura 25 e Figura 27. Nestes casos, observa-se o aparecimento de um comportamento diferente do registrado nas amostras anteriores. Verifica-se um espalhamento maior dos dados e principalmente, o aparecimento de curvas com notável redução na absorbância. Essa redução é notada principalmente nos resultados encontrados para a solução de 100 µM. 52 O cálculo de ∆ para as concentrações de 200 e 100 µM, Figura 26 e Figura 28, indica uma mudança de regime, impulsionado por amostras que reduziram a absorbância e passaram a transmitir mais luz, em determinadas potências de excitação, como 11 mW para a solução de 200 µM e 4,5; 7,3; 8,52; 10,3 e 11,1 mW para a solução de 100 µM. Figura 21: Absorbância transiente normalizada, para solução aquosa de azul de toluidina na concentração de 400 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). Figura 22: Delta de transmissão entre os tempos 0 e 1 s, para a solução aquosa na concentração de 400 µM. Valores obtidos a partir de curvas normalizadas de transmissão. 53 Figura 23: Absorbância transiente para solução aquosa de azul de toluidina na concentração de 300 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). Figura 24: Delta de transmissão entre os tempos 0 e 1 s, para solução aquosa na concentração de 300 µM. Valores obtidos a partir de curvas normalizadas de transmissão. 54 Figura 25: Absorbância transiente para azul de toluidina em solução aquosa na concentração de 200 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). Figura 26: Delta de transmissão entre os tempos 0 e 1 s, para a concentração de 200 µM, diluída em água. Valores obtidos a partir de curvas normalizadas de transmissão. 55 Figura 27: Absorbância transiente para solução aquosa de azul de toluidina na concentração de 100 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). Figura 28: Delta de transmissão entre os tempos 0 e 1 s, para a solução aquosa na concentração de 100 µM. Valores obtidos a partir de curvas normalizadas de transmissão. 56 4.8. Registros para Azul de Toluidina diluído em álcool etílico Conforme os resultados apresentados na Figura 10 que comprovam a baixa agregação do corante Azul de Toluidina em álcool etílico, se escolheu uma concentração para registrar a absorbância transiente e comparar com os resultados obtidos com o mesmo corante diluído em água destilada. Inicialmente, para definir qual solução seria caracterizada, foi medida a intensidade de luz transmitida para a amostra de 300 µM com potência laser máxima de 12,5 mW. O resultado demonstrou uma forte redução na transmissão, com recuperação parcial da absorbância para tempos maiores, conforme Figura 29. Figura 29: Redução na transmissão de sinal, atribuída ao expressivo efeito de lente térmica, fazendo com que o feixe adquirisse diâmetro maior que aquele do detector. A agregação do corante estudado não é favorecida em etanol e, portanto, espera-se que a conversão dímero monômero não ocorra de forma expressiva e tampouco o aumento da absorção por este processo no comprimento de onda de excitação de 632,8 nm. Partindo deste princípio, o resultado apresentado na Figura 29 pode ter sofrido influência de um artefato. Para identificar a origem do fenômeno medido, foram realizadas novas aquisições e atribuiu-se a variação encontrada à desfocalização do sinal induzida pelo efeito pronunciado de lente térmica no etanol, bem como ao aparecimento de anéis de interferência por processo de automodulação de fase. Aparentemente, 57 após 100 ms do início da irradiação o anel mais externo sai da área sensível do detector, provocando uma queda na intensidade de sinal. Foi verificado também que a divergência do sinal com o aparecimento dos anéis sofre uma redução após 1 s de irradiação, tornando a coletar energia do anel mais externo. Tal fenômeno pode estar relacionado à dinâmica de transporte de massa via convecção térmica no corante, bem como à redução do gradiente térmico, na seção transversal do feixe, devido à difusão do calor depositado na amostra. Foram tomadas medidas com o detector 13DSI007, posicionado o mais próximo possível da amostra, de modo a coletar todo o feixe transmitido pela amostra. Porém, neste caso, com a densidade de potência elevada devido à proximidade com o foco do feixe, pode ocorrer saturação no detector. Para verificar se a saturação ocorreu foi feita nova medida utilizando um filtro de densidade óptica neutra para atenuar o feixe laser garantindo o funcionamento do detector na faixa de trabalho. Em um primeiro momento foi medida a transmissão pela amostra e registrado o sinal. Após esta medida foi adicionado um filtro entre a amostra e o detector e medida a transmissão pela amostra novamente. Os sinais foram comparados e verificou-se uma diferença entre as curvas, atribuída à saturação do detector. Para corrigir a saturação do detector, observado nas medidas anteriores, foi então adotado um novo detector com área útil 10x maior, o 13DSI011, cujo tempo de resposta fora caracterizado no início deste trabalho. Devido à área maior do novo detector, foi possível posicioná-lo mais distante da amostra, porém, garantindo a coleta de todo o sinal. Para uma solução etanólica de Azul de Toluidina com concentração de 300 µM, foi medida a absorbância transiente para diferentes intensidades de excitação. Os resultados estão apresentados na Figura 30. Na medida em que a potência de excitação aumenta ocorre um aumento na transmissão, indicando que a conversão dímeromonômero não é o fenômeno dominante neste caso. O efeito dominante agora é o branqueamento óptico (foto bleaching). Como a atenuação exercida pelo Azul de Toluidina em solução etanólica é muito forte para o comprimento de onda de 632,8 nm utilizado para excitação, a relação sinal ruído fica prejudicada inviabilizando medidas com amostras mais concentradas neste solvente. Devido à baixa dimerização em etanol, medidas com concentrações menores não foram realizadas. 58 Avaliando o ∆, para cada condição de excitação, tem-se uma tendência de aumento da transmissão em função do aumento da energia acumulada na amostra, conforme pode ser verificado na Figura 31. Figura 30: Transmitância transiente para o azul de toluidina em solução etanólica na concentração de 300 µM, e diferentes potências ópticas de excitação (λ=632,8 nm). Figura 31: Delta de transmissão entre os tempos 0 e 1 s, para solução etanólica na concentração de 300 µM. Valores obtidos a partir de curvas normalizadas de transmissão. 59 Os resultados alcançados pelo cálculo do delta entre 0 e 1 s nas diferentes concentrações, tanto para água destilada quanto para etanol, carregam informações do limiar de ocorrência da conversão dímero-monômero. Correlacionando os coeficientes angulares, calculados através do ajuste linear aos dados de delta, em função da concentração obtém-se o panorama apresentado na Figura 32. Os resultados indicam que o espalhamento de dados observado nas amostras mais diluídas está relacionado com a transição entre fenômenos. Para soluções mais concentradas a conversão dímeromonômero é dominante. Porém, conforme a concentração diminui outro fenômeno, o branqueamento óptico (foto bleaching), se manifesta até se tornar dominante em concentrações com pouca agregação molecular. Figura 32: Coeficiente angular obtido a partir do ajuste linear aos dados de delta de transmissão. 60 5. DISCUSSÃO Para se estudar a influência da densidade de energia depositada em um meio absorvedor, foram criados dois ambientes de estudo cuja diferença fora promovida pelo solvente. Um dos meios deveria favorecer a agregação das moléculas e o outro inibir. A agregação das moléculas de Azul de Toluidina pode ser induzida facilmente pela adoção de um solvente mais polar. Comparando os solventes comumente empregados em soluções químicas temos a seguinte relação por ordem crescente de polaridade: Hexano, heptano < ciclohexano < tricloroetano < tolueno < diclorometano < clorofórmio < éter etílico < acetona < propanol < etanol < metanol < acetonitrila < água. Considerando a relação apresentada, o tempo de medida e a volatilidade foram escolhidos, a água por ser o mais polar entre os solventes e o etanol por ter polaridade inferior a água. A agregação, embora represente um problema para aplicações biomédicas como a TFD, por reduzir a absorção e consequentemente a eficiência fotodinâmica do corante, atrai grande interesse para outras áreas, como no desenvolvimento de dispositivos optoeletrônicos (D´ILARIO; MARTINELLI, 2006). Para se avaliar a agregação e sua influência nas propriedades fotofísicas dos corantes podem ser empregadas diferentes técnicas espectroscópicas. As técnicas espectroscópicas são ferramentas muito importantes e que estão intimamente ligadas ao sucesso de qualquer aplicação que envolva interação da matéria com radiação luminosa. Através dessas técnicas pode-se determinar, por exemplo, o melhor comprimento de onda para excitação, a intensidade dos efeitos de agregação, a influência de características do meio, como pH e temperatura, na eficiência de conversão e/ou reação da molécula, entre outras. Dentre essas técnicas, a espectroscopia de absorção de luz está entre as técnicas mais utilizadas e representa um método poderoso para caracterização e identificação de materiais. O espectro de absorção é normalmente determinado matematicamente pela medida da transmitância através da amostra em função do comprimento de onda da luz incidente. Além do método de transmitância, a técnica de lentes térmicas (LT) tem sido largamente utilizada para caracterização da absorção. A LT é uma técnica foto térmica que mede a distorção do feixe de luz induzido pelo calor depositado na amostra pela propagação do feixe (HUNG et al., 2004). Quando um meio é 61 iluminado por uma radiação laser com perfil Gaussiano, parte da energia incidente é absorvida por moléculas no estado fundamental, que são excitadas para níveis energéticos maiores. O excesso de energia adquirida pela molécula pode ser dissipado por diversas formas. O decaimento não radiativo produz aumento localizado de temperatura, criando um gradiente de índice de refração no meio, que atuará como uma lente óptica, chamada lente térmica (KURIAN et al., 2003). Existe uma importante diferença entre o espectro de absorbância, medido através de transmitância, e o espectro de lente térmica. O método LT mede a energia absorvida pelos materiais na forma de calor. O método de absorbância mede o total de energia perdida pelo feixe durante a propagação no meio. O espectro de absorbância e de LT serão os mesmos se não existir nenhum outro efeito além do aquecimento do meio. No entanto, em meios que exibem intensa fluorescência, Raman ou outros tipos de espalhamento de luz, o espectro de absorbância pode não ser o mesmo que o espectro de LT (HUNG et al., 2004). Considerando que o Azul de Toluidina tem baixo rendimento quântico de fluorescência e ainda não exibe outros fenômenos competitivos à absorção, como o espalhamento, pode-se empregar o método de medida do espectro de absorção por transmitância. Garantindo fidelidade e baixa complexidade da técnica. Foram adquiridos inicialmente espectros de absorbância para as diferentes concentrações de Azul de Toluidina em água destilada para verificar a formação de agregados. Como esperado, em função da alta concentração preparada (500 µM), ocorreu agregação sinalizada pelo aparecimento de uma banda em 588 nm ± 2 nm. Conforme relatado por D´ilario e Martinelli (2006) em seu estudo sobre as propriedades de agregação do Azul de Toluidina. Os autores investigaram, por espectroscopia UV-Visível, o fenômeno de agregação do Azul de Toluidina em água para diferentes concentrações. Os resultados encontrados para o dímero confirmaram a ocorrência de agregação tipo H, com deslocamento da banda de absorção para o azul, com centro da banda em 580 nm para o dímero e 640 nm para o monômero. Além do dímero, os autores investigaram as características espectrais quando da formação de agregado de ordens maiores. Em contrapartida, considerando a solução de Azul de Toluidina diluído em álcool etílico observou-se a ausência de outras bandas de absorção além do monômero, indicando a baixa formação de agregados. Para que ocorra a formação de agregados é necessário que a energia ganha pelo dímero quando solvatado seja 62 superior à energia de dispersão. Conforme resultados encontrados por Homem de Mello et al. (2007) utilizando geometria cristalográfica e posteriormente por Bettanin (2011) o qual, simulando a dimerização de moléculas de Azul de Metileno, foi constatada a presença de uma pequena energia de dispersão repulsiva entre os monômeros, porém, esta é compensada pela energia ganha pelo dímero quando solvatado, sendo possível a formação de dímeros para solventes mais polares. O aumento da absorção óptica pelo corante, observado nos resultados das amostras diluídas em água destilada, pode ter basicamente, duas origens: absorção por moléculas no estado excitado ou conversão direta dímero–monômero. Para que aconteça absorção pelas moléculas é necessária incidência de determinada quantia de energia em comprimento de onda compatível com a absorção da molécula em tempo curto o suficiente para que ocorra a inversão da população que se encontra no estado fundamental, de baixa energia, para o estado excitado. O aumento da absorção acontecerá em função do aumento da secção transversal, que é maior para o estado excitado quando comparado com o estado fundamental (LU et. al., 2011). Este tipo de medida é explorada pela técnica de Bombeio e Prova para determinar parâmetros como a dinâmica da absorção não linear e a cinética da formação e relaxação de produtos de longa duração (PRZHONSKA et. al., 1998). Przhonska et al. (1998) utilizaram a técnica de Bombeio e Prova como uma das ferramentas para investigar absorção óptica não linear de corantes polimetina em meio líquido e sólido, quanto à dinâmica de absorção e cinética de formação e relaxação destes. Os autores utilizaram radiação laser a 532 nm em pulso único de 30 ps com repetição entre 0,5 e 10 Hz e energia entre 10 e 150 µJ para bombeio. Nesse caso transmitância do feixe de prova diminui durante o pulso de bombeio. A cinética da repopulação do estado fundamental (recuperar a transmitância inicial) é diferente em etanol e PUA (acrilato de poliuretano), resultando em tempo de decaimento de estados excitados mais longo em meio polimérico. A formação de dímeros é favorecida em soluções altamente concentradas, de forma que as moléculas tendem a se aproximar e a energia entre elas alcance um patamar suficiente para mantê-las unidas. No trabalho de D´Ilario e Martinelli (2006) foi estudada, em modelo computacional, a agregação de moléculas de Azul de Toluidina em água e encontrou-se que a energia para agregados diméricos varia entre 70,8753 e 74,9263 Kcal/mol dependendo da orientação das moléculas. 63 Para a agregação paralela, que é encontrada nas formações diméricas de moléculas de Azul de Toluidina, a transição entre o estado fundamental e estado excitado pela divisão da energia do estado excitado do monômero durante a dimerização é proibida, que resulta em um deslocamento para o azul (D´ILARIO E MARTINELLI, 2006). Neste trabalho objetivou-se acumular energia na amostra através da irradiação por longo período, 4 s, em comprimento de onda coincidente com o centro da banda de absorção de forma que durante os ciclos de excitação e relaxamento das moléculas seja emitida energia em forma de calor. O calor acumulado promoverá uma vibração mecânica que superará a energia de atração dos agregados induzindo a conversão dímeromonômero. O não favorecimento da agregação em função do aumento de temperatura foi verificado por Liu; Zou; Um (2010). Os autores constataram que aumento de temperatura até 37°C não favorece a agregação. Com o aumento dos monômeros maior será a absorção do meio e naturalmente menor será a transmissão, até atingir o equilíbrio entre a conversão dímero monômero e monômero dímero. A acumulação de calor pode induzir a ocorrência de microbolhas que por sua vez podem ter um efeito interferente na transmissão do feixe laser. Porém, o aumento na temperatura em função da energia depositada no meio foi controlado, de forma a não atingir a ebulição. Nos resultados encontrados para as amostras diluídas em água destilada se observou que para baixas concentrações ocorre, além da conversão esperada, o fenômeno de branqueamento, que implica no aumento do sinal transmitido. Quanto maior a concentração da solução, menor se torna a influência do branqueamento no sinal transmitido. A partir da concentração de 300 µM a conversão dímero monômero se sobrepõe, elevando a capacidade de atenuação do meio, alcançando o equilíbrio após 500 ms do início da irradiação. O aumento na capacidade de absorção para as soluções mais concentradas, embora presente, não tem sido relatado nos estudos de degradação de corantes. Esses estudos são em sua maioria destinados a avaliar corantes inseridos em matrizes sólidas para aplicações como holografia ou conversão energética. Dois fatores principais contribuem para a não evidencia do aumento da absorção, que seriam o tempo de irradiação que se entende por vários minutos (YUNUS, SHENG, 2004) e as reações 64 fotoquímicas com o substrato que produzem formas leuco reduzidas do corante (CARRETERO et. al., 1998). Durante as medidas de transmitância nas amostras preparadas com álcool etílico se observou um fenômeno de divergência no feixe transmitido. Essa divergência no feixe foi ocasionada pela alteração no índice de refração da solução. O índice de refração de um material pode ser alterado devido à polarização eletrônica induzida no mesmo por um feixe óptico intenso. Porém, também pode ser alterado pelo aquecimento do material, induzido pelo feixe incidente. Esta modificação, tanto por origens térmicas quanto eletrônicas, é responsável por diversos efeitos ópticos não lineares, tais como, os efeitos de auto focalização e auto desfocalização. O aumento da temperatura do meio pode modificar significativamente o índice de refração do material. Este efeito, chamado de lente térmica, difere da refração não linear de origem eletrônica, por apresentar um tempo de resposta muito lento, possui um caráter não local devido ao processo de condução de calor e não pode ser associado à polarização não linear. No entanto, ele pode interferir na manipulação do feixe usada para a realização de chaveamento óptico, uma vez que podemos interpretar a variação do índice de refração de um material com a intensidade de um feixe como uma combinação de efeitos ópticos não lineares de origens eletrônica e térmica (CASTRO, 2010). Para que ocorra a divergência ou convergência do feixe de luz laser ao passar pelo material a condição determinante será a variação da velocidade deste. Considerando um feixe com perfil espacial de intensidade gaussiano incidindo sobre um meio, o material apresentará uma distribuição espacial não uniforme do índice de refração. Como a velocidade de propagação de uma onda eletromagnética em um meio é dada por: υ6 = c n Observa-se que quanto maior for o valor de 8, menor será a velocidade e quanto menor for 8, maior será esta velocidade. Consequentemente, a frente de onda do feixe terá velocidades de propagação diferentes em cada ponto do material. Considerando um material que apresente índice de refração não linear 8 positivo (térmico ou eletrônico), o índice de refração será maior no centro que em sua periferia. Desta forma o material irá atuar como lente convergente. Por sua vez, 65 um material que apresente 8 negativo, o índice de refração será menor no centro que em sua periferia. Desta forma o material irá atuar como lente divergente (ZHA, HU, JIN, 1994). No caso da solução etanólica, por se tratar de um solvente menos polar, quando comparado com a água, ter-se-á majoritariamente monômeros que por sua vez absorverão fortemente a radiação laser. Verifica-se, também, uma tendência contrária aos resultados obtidos com água destilada, ou seja, a absorbância diminui com o tempo de excitação. Essa redução na absorbância pode ser explicada pela ocorrência de saturação óptica e não terá a competição do processo de conversão dímero-monômero, devido à presença inexpressiva de agregados. O cálculo do delta para as curvas de transmissão normalizadas possibilitou a identificação de uma tendência de transição entre fenômenos em função da concentração. Verifica-se nos resultados para alta concentração, onde a formação de agregados é maior e consequentemente a conversão dímeromonômero é mais intensa, que a tendência de variação do coeficiente angular em função da potência de excitação é linear no sentido de aumento da absorbância. Com a redução da concentração, embora ocorra um pequeno espalhamento dos dados, é possível medir uma redução no coeficiente angular que tende a 0 para a concentração mais baixa. O coeficiente angular 0 indica o equilíbrio entre o fenômeno de conversão dímero-monômero e o fotobranqueamento. A solução em álcool etílico apresentou a mesma tendência de linearidade, encontrada com a respectiva concentração em água destilada, porém, com relação ao aumento da transmitância. Indicando uma correlação entre os fenômenos. 66 6. CONCLUSÕES A absorção óptica transiente para o composto Azul de Toluidina foi registrada em meio aquoso para concentrações que variaram entre 100 e 400 µM. O fenômeno transiente registrado para o Azul de Toluidina teve duração média superior para água destilada do que para etanol, confirmando o fenômeno de conversão dímero-monômero, visto que o transiente encontrado para a solução etanólica deve-se a conversões eletrônicas. Os resultados encontrados com as soluções em água destilada e álcool etílico podem ser correlacionados quanto ao coeficiente angular extraído a partir da amplitude dos sinais de transmitância. Desta forma, para coeficiente angular positivo, com relação à transmitância, o fenômeno dominante será o foto branqueamento, por sua vez, se o coeficiente angular for negativo o fenômeno dominante será a conversão direta entre dímeros e monômeros. A conversão dímero-monômero ocorre já em baixas concentrações, desde que a solução apresente dimerização. Porém, este fenômeno irá competir com outros, como o foto branqueamento. Os resultados deste trabalho indicam que o limiar para aparecimento da conversão dímero-monômero está em torno de 100 µM em solução aquosa. 67 REFERÊNCIAS BIBLIOGRÁFICAS ACKROYD, R.; KELTY, C.; BROWN, N. et al. The history of Photodetection and Photodynamic Therapy. Photochem. Photobiol. 75(5):656-669, 2001. ALLISON, R.R.; DOWNIE, G.H.; CUENCA, R. et al. Photosensitizers in clinical PDT. Photodiagnosis Photodyn Ther. 1:27-42, 2004. AMARAL, L.; VIVEIROS, M.; KRISTIANSEN, J.E. Phenothiazines: potential alternatives for the management of antibiotic resistant infections of tuberculosis and malaria in developing countries. Trop. Med. Int. Health. 6(12):1016-1022, 2001. ANTONOV, L.; GERGOV, G.; PETROV, V. et al. UV-Vis spectroscopic and chemometric study on the aggregation of ionic dyes in water. Talanta. 49:99-106, 1999. ASANO, R.; NAGAMI, A.; FUKUMOTO, Y. et al. Synthesis and biological evaluation of new chlorine derivatives as potential photosensitizers for photodynamic therapy. Bioorgan. Med. Chem. 21:2298-2304, 2013. BETTANIN, F. Estudo químico-quântico de corantes catiônicos e aniônicos para aplicações em terapia fotodinâmica. 2011. 100p. Dissertação (Mestrado em Ciência & Tecnologia – Química) – Centro de Ciência Naturais e Humanas, Universidade Federal do ABC, Santo André. BRAJATO, P. Síntese e caracterização do sistema vítreo B2O3-BaO-SiO2-. Al2O3. 2010. 108p. Dissertação (Mestrado – Programa de Pós-Graduação Interunidades em Ciência e Engenharia de Materiais – Caracterização e Aplicação de Materiais) – Escola de Engenharia de São Carlos, Instituto de Física de São Carlos, Instituto de Química de São Carlos da Universidade de São Paulo, São Carlos. BRENNETOT, R.; GEORGES, J. Investigation of non-linear absorption effects in pulsed-laser thermal lens spectrometry of dyes solutions. Spectrochim. Acta A. 55:381-395, 1999. BUCK, S.T.G. Relação entre eficiência fotodinâmica, citotoxidade e propriedades moleculares de corantes para aplicação em terapia fotodinâmica. 2009. 93p. Dissertação (Mestrado em Ciências – Química Analítica) – Instituto de Química de São Carlos, Universidade de São Paulo, São Paulo. CARRETERO, L.; BLAYA, S.; FIMIA, A. et al., Study of the quantum yield and molar absorptivity for a dye photobleaching in a holographic recording material. Proc. Soc. Photo-Opt. Inst. Eng. 3294:91-98, 1998. CASTRO, H.P.S. Caracterização óptica e termo-óptica de sistemas coloidais de nanopartículas. 2010. 122p. Dissertação (Mestrado em Física da Matéria Condensada) – Instituto de Física, Universidade Federal de Alagoas, Maceió. 68 Chemical book (online). Disponível em http://www.chemicalbook.com/ProductChem icalPropertiesCB6373243_EN.htm. Acesso em 25 de maio de 2014. CHOUDHARY, S.; NOURI, K.; ELSAIE, M.L. Photodynamic therapy in dermatology: a review. Lasers Med. Sci. 24:971-980, 2009. COMINI, L.R.; FERNANDEZ, I.M.; RUMIE VITTAR, N.B. et al. Photodynamic activity of anthraquinones isolated from Heterophyllaea pustulata Hook f. (Rubiaceae) on MCF-7 c3 breast cancer cells. Phytomedicine. 18:1093-1095, 2011. D´ILARIO, L.; MARTINELLI, A. Toluidine blue: aggregation properties and structural aspects. Modelling Simul. Mater. Sci. Eng. 14:581-595, 2006. ENK, C.D.; LEVI, A. Low-irradiance red LED traffic lamps as light source in PDT for actinic keratoses. Photodermatol. Photomed. 28:332-334, 2012. FERRAZ, R.C.M.C.; FONTANA, C.R.; RIBEIRO, A.P. et al. Chemiluminescence as a PDT light source for microbial control. J. Photochem. Photobiol. B. 103:87-92, 2011. GASPARETTO, A.; LAPINSKI, T.F.; ZAMUNER, S.R. et al. Extracts from Alternanthera maritima as natural photosensitizers in photodynamic antimicrobial chemotherapy (PACT). J. Photochem. Photobiol. B. 99:15-20, 2010. GIROLDO, L.M.; FELIPE, M.P.; OLIVEIRA, M.A. et al. Photodynamic antimicrobial chemotherapy (PACT) with methylene blue increases membrane permeability in Candida albicans. Lasers Med. Sci. 24:109-112, 2009. GIRONÉS, N.; BUENO, J.L.; CARRIÓN, J. et al. The efficacy of photochemical treatment with methylene blue and light for the reduction of Trypanosoma cruzi in infected plasma. Vox Sanguinis. 91:285-291, 2006. GONZALES, F.P.; SILVA, S.H.; ROBERTS, D. W. et al. Photodynamic Inactivation of Conidia of the Fungi Metarhizium anisopliae and Aspergillus nidulans with Methylene Blue and Toluidine Blue. Photochem. Photobiol. 86:653-661, 2010. GOULART, R.C.; BOLEAN, M.; PAULINO, T.P. et al. Photodynamic Therapy in Planktonic and Biofilm Cultures of Aggregatibacter actinomycetemcomitans. Photomed. Laser Surg. 28:S53-S60, 2010. GUTTMANN, P.; EHRILICH, P. Ûber die Wirkung des Methylenblau bei Malaria. in: THE COLLECTED PAPERS OF PAUL EHRLICH. Berlin: Pergamon, 1960, v.3, 914. HASHIMOTO, M.C.E.; TOFFOLI, D.J.; PRATES, R.A. et al. Photodynamic inactivation of antibiotic resistant strain of Pseudomonas aeruginosa in vivo. In 12th World Congress of the International Photodynamic Association. International Society for Optics and Photonics. 7380: 73803F-1 - 73803F-7, 2009. 69 HAUKVIK, T, BRUZELL, E., KRISTENSEN, S. et al. Photokilling of bactéria by curcumin in different aqueous preparations. Studies on curcumin and curcuminoids XXXVII. Pharmazie. 64:666-673, 2009. HOMEM-DE-MELLO, P.; MENNUCCI, B.; TOMASI, J.; SILVA, A. B. F. Cationic dye dimers: a theoretical study. Theor. Chem. Acc. 118: 305-314, 2007. HUNG, J.; MARCANO, A.; CASTILLO, J. et al. Thermal lensing and absorbance spectra of a fluorescent dye solution. Chem. Phys. Lett. 386:206-210, 2004. ILANCHELIAN, M.; RAMARAJ, R. Binding Interactions of Toluidine Blue O with Escherichia Coli DNA: Formation of Bridged Structure. J. Fluoresc. 21:1439-1453, 2011. JUNAID, M.; CHOUDHARY, M.M.; SOBANI, Z.A. et al. A comparative analysis of toluidine blue with frozen section in oral squamous cell carcinoma. World J. Surg. Oncol. 10:57, 2012. KASHA, M. Energy transfer mechanisms and the molecular exciton model for molecular aggregates. Radiat. Res. 20:55-71, 1963. KASHA, M.; RAWLS, H.R.; ASHRAF EL-BAYOUMI, M. The exciton model in molecular spectroscopy. 1965, Copenhagen, Dinamarca. VIII European Congress on Molecular Spectroscopy. Copenhagen, Dinamarca. 11(3-4):371-392, 1965. KOLÁROVÁ, H.; MOSINGER, J.; LENOBEL, R. et al. In vitro toxicity testing of supramolecular sensitizers for photodynamic therapy. Toxicol. in Vitro. 17:775-778, 2003. KULBACKA, J.; POLA, A.; MOSIADZ, D. et al. Cyanines as Efficient Photosensitizers inf Photodynamic Reaction: Photophysical Properties and in vitro Photodynamic Activity. Biochemistry-US. 76(4):473-479, 2011. KURIAN, A.; UNNIKRISHNAN, K.P.; GEORGE, D.S. et al. Thermal lens spectrum of organic dyes using optical parametric oscillator. Spectrochim. Acta A. 59:487-491, 2003. LIU, J.; ZOU, A.; UM, B. Toluidine blue: Aggregation properties and distribution behavior in surfactin micelle solution. Colloid Surface B. 75:496-500, 2010. LU, Y.T.; GE, J.F.; XU, Q.F. et al. Third-order nonlinear optical properties of the phenothiazinium chlorides at 532 nm. Dyes Pigments. 89:70-75, 2011. MACDONALD, I.J.; DOUGHERTY, T.J.. Basic principles of photodynamic therapy. J. Porphyr. Phthalocya. 5:105-129, 2001. MOTTA, A.A.; GIAVINA-BIANCHI, P. Reações adversas a drogas (R.A.D.). Rev. Med. 84(1):10-17, 2005. 70 MUNIN, E.; GIROLDO, L. M.; ALVES, L. P. et al. Study of germ tube formation by Candida albicans after photodynamic antimicrobial chemotherapy (PACT). J. Photochem. Photobiol. B. 88:16-20, 2007. MUSTAFA, F.H.; JAAFAR, M.S. Comparison of wavelength-dependent penetration depths of lasers in different types of skin in photodynamic therapy. Indian J. Phys. 87(3):203-209, 2013. NIELSEN, K.P.; JUZENIENE, A.; JUZENAS, P. et al. Choice of Optimal Wavelength for PDT: The Significance of Oxygen Depletion. Photochem. Photobiol. 81:11901194, 2005. ORMOND, A.B.; FREEMAN, H.S. Dye Sensitizers for Photodynamic Therapy. Materials. 6:817-840, 2013. PERUSSI, J.R. Inativação Fotodinâmica de Microrganismos. Quim. Nova. 30(4):988-994, 2007. PRZHONSKA, O.V.; LIM, J.H.; HAGAN, D.J. et al. Nonlinear light absorption of polymethine dyes in liquid and solid media. J. Opt. Soc. Am. B. 15(2): 802-809, 1998. QUIMBY, R.S. Photonics and Lasers: An Introduction. New Jersey: John Wiley & Sons, 2006. 519p. SERRA, F.; TERENTJEV, E.M. Nonlinear dynamics photobleaching of dyes. J. Chem. Phys. 128:224510, 2008. of absorption and SOUZA, R.C.; JUNQUEIRA, J.C.; ROSSONI, R.D. et al. Comparison of the photodynamic fungicidal efficacy of methylene blue, toluidine blue, malachite green and low-power laser irradiation alone against Candida albicans. Lasers Med. Sci. 25:385-389, 2010. STERNBERG, E.D.; DOLPHIN, D. Porphyrin-based Photosensitizers for use in Photodynamic Therapy. Tetrahedron. 54:4151-4202, 1998. TAVARES, A.; CARVALHO, C.M.B.; FAUSTINO, M.A. et al. Antimicrobial Photodynamic Therapy: Study of Bacterial Recovery Viability and Potential Development of Resistance after Treatment. Mar. Drugs. 8:91-105, 2010. WAINWRIGHT, M. The development of phenothiazinium Photodiagnosis Photodyn. Ther. 2:263-272, 2005. photosensitisers. WAINWRIGHT, M.; GIDDENS, R.M. Phenothiazinium photosensitisers: choices in synthesis and application. Dyes Pigments. 57:245-257, 2003. WANG, H., LU, L., ZHU, S. et al. The Phototoxicity of Xanthene Derivative Against Escherichia coli, Staphylococcus aureus, and Saccharomyces cerevisiae. Curr. Microbiol. 52:1-5, 2006. 71 WILLIAMS, D.F. On the mechanisms of biocompatibility. Biomaterials. 1-13, 2008 YUNUS, W.M.M.; SHENG, C.K. Photodegradation study of methylene blue (MB) trapped in poly (methyl methacrylate) (PMMA) matrix. Suranaree J. Sci. Technol. 11:138-142, 2004. ZHA, Z.H.; HU, Y; JIN, E.P. How to make uniform beam produce self-focusing or selfdefocusing effects. In. NONLINEAR OPTICAL MATERIALS FOR SWITCHING AND LIMITING, 2229, 1994, Orlando, FL. PROCEEDINGS OF THE SOCIETY OF PHOTO-OPTICAL INSTRUMENTATION ENGINEERS (SPIE), Orlando, FL, 1994, 206-209.
Baixar