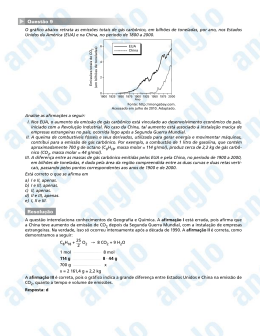
Questão 20 Estudos recentes indicam que as águas do aqüífero Guarani (um dos maiores reservatórios subterrâneos de água doce conhecidos no planeta) estão sendo contaminadas. O teor de nitrogênio já atinge, em determinados locais, valores acima do nível de tolerância do organismo humano. Em adultos, o nitrogênio, na forma de nitrito, atua na produção de nitrosaminas e nitrosamidas, com elevado poder cancerígeno. Considerando as equações químicas a seguir, NO2− ( aq) + H + ( aq) HNO2 ( aq) (produção do ácido nitroso no estômago) HNO2 ( aq) + (CH 3 )2 NH ( aq) (CH 3 )2 NNO ( aq) + H2O ( l) (produção da nitrosamina) determine a massa da nitrosamina que pode ser produzida a partir de um litro de água cujo teor em nitrito seja igual a 9,2 mg. Apresente seus cálculos. Massas molares, em g⋅mol −1 : NO2− = 46 e (CH 3 )2 NNO = 74. Resposta Cálculo da massa de nitrosamina: 9,2 ⋅10 −3 g NO2− ⋅ 1 mol NO2− 1 mol nitrosamina ⋅ ⋅ 46 g NO2− 1 mol NO2− 14243 14442444 3 m. molar ⋅ relação estequiométrica 74 g nitrosamina = 0,0148 g nitrosamina 1 1mol 44nitrosamina 42444 3 m. molar Questão 21 passa para a fase aquosa, enquanto que o N2 permanece quase que totalmente na atmosfera. Desenhe a estrutura da molécula de CO2 e explique, utilizando equações químicas, a passagem do CO2 para a fase aquosa. Resposta A fórmula estrutural da molécula do CO2 é: O C O A passagem do CO2(g) para a fase aquosa pode ser representada pelas seguintes equações: CO2(g) CO2(aq) CO2(aq) + H 2O( l) H 2CO3(aq) H 2CO3(aq) + − H(aq) + HCO3(aq) Questão 22 Para determinar o tempo em que certa quantidade de água permaneceu em aqüíferos subterrâneos, pode-se utilizar a composição isotópica com relação aos teores de trítio e de hidrogênio. A água da chuva apresenta a relação 13 H / 11H = 1,0 ⋅ 10−17 e medições feitas na água de um aqüífero mostraram uma relação igual a 6,25 ⋅ 10−19 . Um átomo de trítio sofre decaimento radioativo, resultando em um átomo de um isótopo de hélio, com emissão de uma partícula β− . Forneça a equação química para o decaimento radioativo do trítio e, sabendo que sua meia-vida é de 12 anos, determine por quanto tempo a água permaneceu confinada no aqüífero. Resposta A equação nuclear para o decaimento radioativo do trítio pode ser representada por: 3 1H → 23 He + −01 β Determinação do tempo em que a água permaneceu confinada no aqüífero, pela análise da relação 13 H/ 11H: As moléculas de N2 e de CO2 , presentes na −17 t 5,0 ⋅ 10 −18 t 2,5 ⋅ 10 −18 t atmosfera, apresentam momento dipolar re- 1,0 ⋅ 10 sultante igual a zero. Em contato com a água, t 1,25 ⋅ 10 −18 t 6,25 ⋅ 10 −19 cujas moléculas apresentam momento dipolar resultante diferente de zero (solvente polar), Como passaram-se 4 períodos de meia-vida (t), o uma fração considerável do CO2 atmosférico tempo total decorrido é de 4 ⋅ 12 = 48 anos. química 2 Questão 23 Uma das principais fontes de energia térmica utilizadas atualmente no Estado de São Paulo é o gás natural proveniente da Bolívia (constituído principalmente por metano). No entanto, devido a problemas políticos e econômicos que causam eventuais interrupções no fornecimento, algumas empresas estão voltando a utilizar o GLP (gás liquefeito de petróleo, constituído principalmente por butano). Forneça as equações químicas para a combustão de cada um desses gases e calcule os volumes de cada um deles que produzem 22,4 litros de CO2 . Resposta As equações de combustão dos dois gases são: CH4(g) + 2 O2(g) → CO2(g) + 2 H 2O(g) 13 O2(g) → 4 CO2(g) + 5 H 2O(g) 2 Cálculo do volume de metano e butano, considerando que os gases estão nas CNTP e que 1 mol de CO2 corresponde a 22,4 L: C4 H10(g) + 1 mol CO2 ⋅ 1 mol CH4 22,4 L CH4 = ⋅ 1 mol CO2 1 mol CH4 4244 3 14243 14 eq. química v. molar = 22,4 L CH4 1 mol CO2 ⋅ 1 mol C4 H10 22,4 L C4 H10 = ⋅ 1 mol C4 H10 4 mol CO2 3 144244 3 144244 eq. química v. molar Agente oxidante Potencial-padrão de redução (em meio ácido) − Eo (V) Cl2 1,36 H2O2 1,78 − 1,63 OCl MnO4− 1,51 O3 2,07 Considerando apenas os parâmetros termodinâmicos apresentados, forneça o nome do agente que é menos eficiente para a oxidação de material orgânico e escreva a equação que representa a semi-reação de redução desse agente. Resposta Considerando-se apenas o E o , o menos eficiente agente oxidante é o cloro (Cl 2 ), pois apresenta o menor potencial-padrão de redução. A equação da semi-reação de redução do cloro é: Cl 2(g) + 2 e − 2 Cl−(aq) Questão 25 A oxidação de um ácido graxo para obtenção de energia em nosso organismo envolve, entre outras, as seguintes etapas: 1.ª etapa – oxidação (ou desidrogenação) 2.ª etapa – hidratação 3.ª etapa – oxidação Dadas as fórmulas estruturais a seguir CH3 (CH2)n = 5,6 L C4 H10 Questão 24 Uma das vantagens da utilização de reagentes oxidantes na purificação da água, comparando com outros tipos de tratamento, é que os produtos da oxidação química de compostos orgânicos são apenas o dióxido de carbono e a água. Na tabela a seguir são listados alguns agentes oxidantes com seus potenciais-padrão de redução. CH CH2 COO _ (I) OH CH3 (CH2)n CH CH3 (CH2)n C CH COO CH2 COO _ (II) _ (III) O CH3 (CH2)n CH2 CH2 COO _ (IV) indique qual o reagente e o produto para cada uma das etapas, na ordem indicada, dando os nomes das funções químicas que são formadas após cada uma das reações. química 3 Resposta A seqüência correta é: IV. H 3C (CH2)n CH2 COO CH2 _ 1ª etapa desidrogenação II. H 3C (CH2)n CH CH insaturação 2ª etapa I. H 3C COO _ hidratação (adição de água) (CH2)n CH CH2 COO _ OH álcool 3ª etapa oxidação III. H 3C (CH2)n C CH2 COO _ O cetona Química – prova tranqüila A prova apresentou enunciados bem elaborados, abordando tópicos importantes de Química e bastante atuais, como o problema do abastecimento de água e a troca do gás natural pelo GLP em indústrias brasileiras. Em muitos aspectos, inclusive o da dificuldade, esta prova foi muito semelhante à do ano anterior. Química Orgânica 17% Estrutura da Matéria 33% Química Geral e Descritiva 33% FísicoQuímica 17% A resolução da prova de Língua Portuguesa estará disponível no site www.etapa.com.br
Baixar