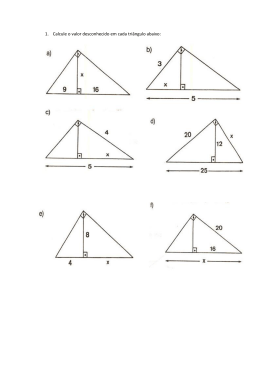
CEM-004 –Termodinâmica dos Sólidos – 1° semestre 2015. Lista de exercícios (1) 10/03/2015 1. Defina propriedades intensivas e propriedades extensivas, classificando cada uma das seguintes propriedades: Densidade – Kg/m3. Numero de átomos-grama de alumina num bloco de alumina – Moles. Energia potencial de um sistema num campo gravitacional – J. A concentração molar de NaCl numa solução de sal – Moles/m3 . O calor absorvido por um gás sendo comprimido em um cilindro – J. 2. Calor e trabalho são equivalentes? 3. É possível representar um arranjo policristalino de uma fase em particular por uma equação de estado? 4. Calcule o trabalho realizado por um mol de um gás ideal quando é comprimido isotermicamente de 500 m3 para 100 m3 a temperatura ambiente. 5. Descreva e exemplifique como calcular trabalhos de superfície, elétrico e magnético. 6. Defina capacidade calorífica. Discuta a variação da capacidade calorífica com a temperatura para o Fe, e para o Cu, esquematizadas nas figuras abaixo. 7. Quais os fatores que contribuem para a capacidade calorífica dos polímeros, dos metais e das cerâmicas? 8. Em função da resposta anterior; podemos generalizar entre metais, cerâmicas ou polímeros, sobre quem tem maior e menor Cp? Justifique. 9. Qual a diferença (e o que esta diferença significa) entre a entalpia molar da Ag sólida a 500 K e a entalpia molar a 298 K? 10. Calcule a variação de entalpia da seguinte reação a 1300 K: Ag (l) + ½ Cl2 (g) = AgCl (l) 11. Calcule o calor de formação, ΔH0298, do carbeto de alumínio <Al4C3>, conhecendo-se o seu calor de combustão: <Al4C3> + 6[O2] = 2 <Al2O3> + 3[CO2] ΔH0298 = -4328 kJ/mol 12. Calcule , ΔH0800, para a seguinte reação, com a maior precisão que for possível: 3 AgCl(l) + B(s) = BCl3(g) + Ag(s) 13. Calcule o calor da reação, ΔH01273, para: <MnSiO3> = <MnO> + <SiO2> 14. Calcule o calor da reação, ΔH01300, para: 2Al + 1,5O2 = Al2O3
Download