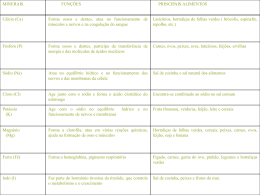
Olimpíada de Química do Rio Grande do Sul – 2011 Questão 2: O grafite e o diamante são substâncias simples e naturais do elemento carbono. Outras estruturas de substâncias simples do carbono, como o fulereno-60, fulereno-70 e nanotubos de carbono, são substâncias sintéticas. A seguir as imagens com os modelos dessas substâncias. CATEGORIA EM-1 Nº INSCRIÇÃO: ____________ PARTE 1 – TESTES DE ESCOLHA SIMPLES Algumas características estruturais: As 15 questões que constituem esta parte da prova deverão ter suas respectivas respostas transcritas para a grade na folha de respostas. Para cada questão CORRETA será atribuído 0,4 ponto. Para cada questão ERRADA será descontado 0,1 ponto. As questões em BRANCO não serão computadas. DIAMANTE – cada átomo de carbono se conecta diretamente a quatro outros carbonos. GRAFITE, FULERENOS 60 E 70, NANOTUBO – cada átomo de carbono se conecta diretamente a três outros carbonos. Questão 1: Sobre dois elementos, Y e X, são feitas as afirmações: De acordo com o exposto acima e seus conhecimentos, faça a análise das afirmações: ELEMENTO Y: é um elemento representativo e metálico do quarto período periódico que forma um óxido de fórmula Y2O. I. Todas as estruturas mostradas na imagem são diferentes formas alotrópicas do elemento carbono. II. Em todas as estruturas acima, os átomos de carbono estão conectados por ligações químicas covalentes, sendo que todos os átomos têm octeto completo. III. A geometria das ligações adotadas pelo carbono não são iguais em todas as estruturas. No diamante os carbonos adotam geometria tetraédrica, enquanto que nas demais estruturas abordadas, o carbono adota geometria trigonal. IV. Devido às suas diferenças estruturais, as substâncias abordadas apresentam diferentes propriedades físicas, como dureza, tenacidade e densidade. ELEMENTO X: é um elemento não metálico que, no estado fundamental tem raio atômico maior que o cloro. Forma com magnésio um composto do tipo MgX2. Faça a análise das afirmações, julgando se são verdadeiras (V) ou falsas (F): 1 – O elemento Y é um metal alcalino terroso. 2 – O elemento X pode ser o flúor, formando com sódio o sal NaF. 3 – O composto MgX2 é iônico, tendo ambos os íons configuração de gás nobre. 4 – A associação entre Y e X produz o composto com fórmula YX. São corretas as afirmações: A associação correta está na alternativa: a) Apenas I e II. b) Apenas III e IV. c) Apenas I, II e IV. d) Apenas I, II e III. e) Todas, I, II, III e IV. a) 1-F / 2-F / 3-V / 4-F b) 1-F / 2-F / 3-V / 4-V c) 1-F / 2-V / 3-F / 4-V d) 1-V / 2-F / 3-V / 4-V e) 1-V / 2-V / 3-F / 4-F ~1~ Olimpíada de Química do Rio Grande do Sul – 2011 Categoria EM1 Questão 3: Abaixo você encontra cinco amostras de metais em barra. Marque a alternativa da amostra que tem o maior número de átomos metálicos: Questão 5: Considerando os seguintes sistemas: I. Solução de ácido clorídrico II. Solução de ácido sulfúrico III. Solução de soda cáustica IV. Solução de hidróxido de ferro III V. Solução de ácido cianídrico. Sabendo que todas são de soluções eletrolíticas, aqueles que, adaptados a um fio condutor e uma lâmpada, após a passagem de corrente elétrica através da solução, fariam a lâmpada acender fortemente seria(am): 24 587 g de Níquel 5 mols de Cromo 3,01x10 átomos de Ferro 648 g de Prata 788 g de Ouro (a) (b) (c) (d) (e) a) Todas b) I, II e III c) IV e V d) Somente V e) Somente III Questão 4: O chamado soro caseiro é uma tecnologia social que consiste na preparação e administração de uma mistura de água, açúcar e sal de cozinha, recomendado para prevenir a desidratação resultante de vômitos e diarreias. Com a diarreia ou vômito ocorre perda de água e sais minerais pelo organismo. A função do soro caseiro, por via oral, é a de reposição desses elementos perdidos. O soro deve ser tomado à vontade, cada 20 minutos, e após cada evacuação líquida se houver diarreia. Questão 6: O cloreto de sódio, principal componente do sal de cozinha, emite luz de coloração amarela, quando colocado numa chama. Com base na teoria atômica, classifique as afirmações abaixo em falso ou verdadeiro: ( ) Os elétrons do cátion, ao receberem energia da chama, saltam de uma camada mais externa para uma mais interna, emitindo luz amarela. ( ) Qualquer outro sal também produziria a mesma coloração. ( ) A luz amarela emitida na queima é devido ao ânion deste sal. ( ) A emissão da luz amarela corresponde a um fenômeno físico. ( ) Os elétrons do cátion, ao receberem energia da chama, saltam de uma camada mais interna para uma mais externa e, ao perderem a energia recebida, emitem-na sob a forma de luz amarela. A ordem correta é: a) Com base nas informações do texto e da imagem, marque a alternativa correta: F, V, V, F, F b) F, F, F, V, V c) V, V, F, F, V d) F, V, F, V, V e) F, F, V, V,V Questão 7: A magnetita, importante minério de ferro que deu origem às bússolas, forma-se no interior da Terra, pela reação expressa na equação química: a) O soro caseiro é preparado pela mistura exclusiva de substâncias orgânicas sólidas em água. b) Pelo esquema evidenciado na imagem, pode-se perceber que a massa de açúcar é o dobro da massa de sal, se o soro for preparado corretamente. c) Todos os componentes da mistura resultante na preparação do soro caseiro são classificados como substâncias simples. d) O soro caseiro é uma solução eletrolítica, devido à presença do eletrólito forte, cloreto de sódio. e) Os componentes sólidos do soro caseiro podem ser facilmente obtidos por filtração simples da mistura. a FeO(s) + b CO2 (g) → x Fe3O4 (s) + y CO (g) Os coeficientes estequiométricos a, b, x e y, que tornam a equação balanceada são, respectivamente: a) 2, 2, 1, 1. b) 3, 1, 1, 1. c) 3, 2, 3, 2. d) 1, 2, 3, 1. e) 2, 3, 1, 1. ~2~ Olimpíada de Química do Rio Grande do Sul – 2011 Categoria EM1 Questão 8: Em nosso cotidiano existe uma grande variedade de sais que estão presentes na formação dos mais diversos materiais, como é o caso do carbonato de cálcio. Esse sal é encontrado nas cascas de ovos, no mármore, no calcário, nas pérolas e nos recifes de corais e é obtido em reações do óxido de cálcio com dióxido de carbono. Determine o volume de dióxido de carbono, nas CNTP, produzido pela decomposição de 350 g de carbonato de cálcio. a) b) c) d) e) Questão 11: Ao fazer incidir partículas radioativas numa lâmina metálica de ouro, Rutherford observou que a maioria das partículas atravessava a lâmina, algumas desviavam e poucas refletiam. Várias conclusões foram retiradas dessas experiências, exceto a de que: a) o núcleo é a região mais densa do átomo. b) o átomo apresenta, predominantemente, espaços vazios. c) o núcleo é praticamente do tamanho do átomo. d) os elétrons giram em torno do núcleo para garantir a neutralidade elétrica do átomo. e) o núcleo atômico apresenta carga elétrica positiva. 56 L 74 L 83,6 L 78,4 L 25,7 L Questão 12: O elemento X reage com o elemento Y, conforme o processo: Questão 9: A Tabela Periódica é um dos conceitos mais importantes da química. Seu desenvolvimento é um exemplo de como descobertas científicas podem ser feitas pelo uso da perspicácia, para organizar dados coletados por um grande número de cientistas, durante muitos anos. Comparando os elementos cálcio e bromo na Tabela Periódica dada, assinale a alternativa correta. Z d) CO e N2O 2- + X Questão 13: A água é uma substância de valor inestimável, por ter permitido a criação e manutenção da vida neste planeta. Isso pode ser atribuído às suas propriedades singulares. Considere as seguintes afirmações sobre a água: I. Sua molécula apresenta ligações covalentes bastante polarizadas. II. Solubiliza substâncias de baixa polaridade, como os hidrocarbonetos. III. Sua molécula tem forma geométrica não-linear. IV. É capaz de formar pontes de hidrogênio. Quais estão corretas? a) Apenas III. b) Apenas I e IV. c) Apenas II e IIII. d) Apenas I, III e IV. e) I, II, III e IV. Entre os pares de óxidos relacionados, qual é o constituído apenas por óxidos que provocam a chuva ácida? c) NO2 e SO3 1- a) Z ganha elétrons de X. b) X ganha elétrons de Z. c) X e Z cedem elétrons. d) X e Z perdem elétrons. e) X e Z ganham elétrons. Questão 10: Em grandes cidades (devido às indústrias e ao grande número de veículos), e em regiões muito industrializados (com refinarias de petróleo, indústrias metalúrgicas, etc.), o ar vai acumulando grandes quantidades de ácido nítrico e ácido sulfúrico. Esses ácidos acabam retornando à superfície por meio da chuva, dando origem ao fenômeno chamado chuva ácida. Essa chuva ácida pode alterar a composição do solo e das águas, comprometendo as lavouras, as florestas e a vida aquática. Também pode corroer edifícios, estátuas e monumentos históricos, o que já acontece em vários lugares da Europa e nas ruínas maias do México. b) CO2 e MgO + X Z Nesse processo: a) O bromo tem maior afinidade eletrônica, pois, com a adição de um elétron, ocorre uma maior liberação de energia. b) O raio do bromo é maior, pois ele tem maior número de camadas eletrônicas. c) A energia de ionização do cálcio é maior, pois é mais difícil retirar um elétron desse elemento do que do bromo. d) Ambos os elementos têm propriedades químicas semelhantes, pois estão no mesmo período. e) O bromo é mais eletropositivo, pois, no período, a eletropositividade cresce com o aumento do número atômico. a) Na2O e NO2 3- e) CO e NO ~3~ Olimpíada de Química do Rio Grande do Sul – 2011 1+ (g) Questão 14: Na transformação Na(g) + E → Na Categoria EM1 - + e , E representa: a) eletroafinidade b) eletronegatividade c) caráter metálico d) energia reticular e) energia de ionização Questão 17: As questões seguintes são relativas unicamente aos elementos mencionados na tabela abaixo, que estão identificados arbitrariamente pelas letras do alfabeto, que nada tem a ver com seus respectivos símbolo: Questão 15: A floresta Amazônica, em um ano normal, sem seca, absorve cerca de 1,5 bilhão de toneladas de gás carbônico. Em 2005, a floresta Amazônica sofreu uma seca marcante e emitiu cerca de 5 bilhões de toneladas de gás carbônico. Isto se deu, porque as árvores mortas passaram a emitir este gás, contribuindo para um aumento do efeito estufa. (categoria I) A respeito do CO2 temos as seguintes afirmativas: A H D J I. A molécula é polar e possui geometria linear. II. O número de oxidação do carbono é - 4 III. É um gás que contribui para a formação de um ácido fraco e instável, em contato com a água. IV. Dois mols deste gás ocupam 44,8 L, nas CNTP, e possuem uma massa de 88 g. V. Os elementos que formam a molécula são classificados como não metais. b) I, II, IV e V C F G I K L B a) Disponha os elementos, localizados no quarto período, em ordem crescente de raio atômico. Estão corretas: a) I, II, III, IV e V E c) III, IV, V d) I, IV e) II, IV b) Disponha os elementos, localizados no segundo período, em ordem crescente de energia de ionização. PARTE 2 – QUESTÕES ANALÍTICO-EXPOSITIVAS: c) Considerando os ânions formados pelos elementos F e G, qual possui maior raio iônico? As questões numeradas de 16 a 20 são descritivas e devem ser respondidas na folha de respostas. Para cada questão correta será atribuído 0,8 ponto. d) Considerando os cátions formados pelos elementos J e C, qual possui maior raio iônico? Questão 16: 416 g de uma mistura sólida, contendo cloretos de sódio, bário e prata, foram tratadas com água deionizada, à temperatura ambiente. O cloreto insolúvel foi separado e à mistura, adicionou-se excesso de solução de ácido sulfúrico, ocorrendo a formação de um precipitado que, após lavado e seco, pesou 116,5 g de produto puro. e) Qual o subnível mais energético do elemento A, na sua configuração fundamental? f) Qual o elemento de maior eletropositividade? Baseado no descrito acima: g) Qual o elemento de maior eletronegatividade? a) Fazer um fluxograma, identificando todos os processos físicos de separação envolvidos, bem como, os produtos resultantes em todas as etapas. h) Qual a representação do íon formado pelo elemento genérico E? b) Calcular a percentagem em massa de sal de bário, presente na mistura inicial. ~4~ Olimpíada de Química do Rio Grande do Sul – 2011 Categoria EM1 Questão 18: A amônia, nas condições ambientes, é um composto gasoso, usado como matéria-prima para diversas substâncias, por exemplo, na fabricação de fertilizantes agrícolas, explosivos para fins militares, gás de refrigeração, etc. É preparada através de síntese direta com gás hidrogênio (processo Haber-Bosch). Na fabricação de fertilizantes e de explosivos, usa-se um sal, obtido a partir da sua reação com ácido nítrico. Questão 20: Atualmente, muito da tecnologia que nos rodeia é fruto de diversas pesquisas, sendo que muitas delas envolvem a Química. Os airbags automotivos são constituídos por uma mistura química que produz uma reação em uma fração de segundo após uma colisão. Em uma primeira etapa, a azida de sódio (NaN3) sofre reação de decomposição, formando sódio metálico (Na) e gás nitrogênio (N2), responsável por inflar o airbag. Com relação à amônia: a) Qual a sua geometria molecular? a) Escreva a equação de reação balanceada, para a decomposição da azida de sódio; b) Escreva a equação de ionização que ocorre, quando é dissolvida em água, citando o nome comercial da solução obtida. b) Escreva a estrutura de Lewis, para a substância molecular envolvida na reação considerada; c) Ao entrar em contato com gás clorídrico, produz um determinado sal. Qual a cor que a solução aquosa desse sal desenvolverá, na presença de fenolftaleína? Explique. c) Considere que, em uma colisão, 1,8 mol de gás nitrogênio inflou um airbag. Calcule o volume de gás nitrogênio liberado, nas CNTP, e a massa de azida de sódio que sofreu decomposição, considerando rendimento total. d) Faça as reações de síntese: da amônia e da formação de seu sal, conforme texto acima. Boa Prova! Questão 19: Consulte a tabela abaixo, e responda ao que se pede, sobre a substância A: PF (ºC) PE (ºC) d (g/mL) 350 820 1,5 0 Solubilidade a 20 C (g/100mL H2O) 70 0 a) Qual o volume mínimo de água a 20 C, necessária para dissolver 280 g da substância A? Demonstre o cálculo. b) Indique o intervalo de temperatura em que a substância será líquida: c) Indique o intervalo de temperatura em que a substância será sólida: d) Indique o intervalo de temperatura em que a substância será gasosa: ~5~ Olimpíada de Química do Rio Grande do Sul – 2011 Categoria EM1 GABARITO EM-1 Questão Resposta 1 B E A D B B B D A C C B D E C 2 3 4 5 6 7 8 9 10 11 12 13 14 15 ~6~
Download