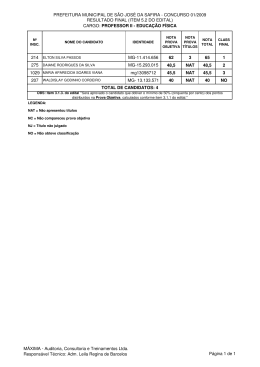
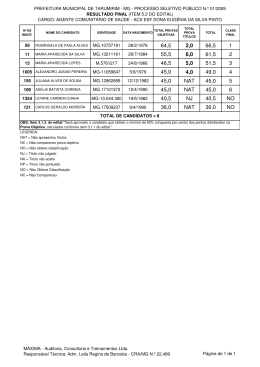
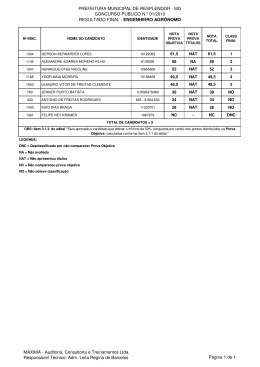
Inovação biomédica e políticas públicas: o desenvolvimento de testes para diagnóstico de HIV e hepatites virais no Brasil Koichi Kameda Doutorando CERMES3-EHESS / IMS-UERJ • Mercado de teste diagnóstico é menor do que o de outros produtos para saúde (meds, vacinas), mas exige contínuo investimento em P&D em razão do curto tempo de vida dessas tecnologias • Brasil é 6o mercado para teste diagnóstico ($ 674 milhões em 2009) e ainda com ampla dependência tecnológica (ex. Testes de carga viral de HIV e HCV adquiridos no primeiro semestre 2014 foram todos importados) • Irrelevância do setor privado (nacional e internacional) na produção local de kit diagnóstico e crescente importância de laboratórios públicos (Bio-Manguinhos e, mais recentemente, Fiocruz-Paraná) • Importância crescente de multiteste e testes rápidos, testes point-of-care Eixos da pesquisa 1 – Estudar a dinâmica do setor de testes para diagnóstico de HIV e hepatites virais no Brasil 2 – Estudar o desenvolvimento local dessas tecnologias (teste NAT “brasileiro”, multiteste baseado em microarranjos líquidos), incluindo a análise do papel dos laboratórios públicos envolvidos (Bio-Manguinhos, Fiocruz-Paraná) 3 – Compreender a importância dos testes rápidos e point-of-care, os quais são mais convenientes para pacientes e profissionais de saúde (papel da clínica na inovação e utilização desses testes, tais como o multiteste para a Rede Cegonha) Data 08/02/13 14/04/14 31/07/14 04/08/14 Entrevistados Diretor do Instituto Carlos Chagas (Fiocruz-Paraná) Ex-secretária técnica da Rede de Cooperação Tecnológica em DST/Aids Coordenadora da GESTEC/Fiocruz Vice-diretor de produção de Bio-Manguinhos Coodernador do Departamento de Reagentes para Diagnóstico, Bio04/08/14 Manguinhos Coordenador do Programa para Desenvolvimento Tecnológico de 04/08/14 Reagentes para Diagnóstico, Bio-M 04/08/14 Tecnologista, projeto microarranjos líquidos, Bio-Manguinhos 08/08/14 Ex-diretor de Bio-Manguinhos Coordenadora do NIT-Bio-Manguinhos 11/08/14 Ex-coordenadora de laboratórios, Departamento de DST/Aids 14/08/14 Representante, Coordenação de Laboratórios, Departamento de DST/Aids 14/08/14 Pesquisador IBMP, coordenador do projeto microarranjos e projeto 02/09/14 multiteste para Rede Cegonha 03/09/14 Coordenador do NIT-ICC 03/09/14 Vice-diretora de parcerias do Instituto Carlos Chagas 03/09/14 Pesquisador IBMP, projeto Sepsis 03/09/14 Coordenadora do NIT-IBMP 04/09/14 Diretor do Instituto Carlos Chagas (Fiocruz-Paraná) 04/09/14 Diretor do IBMP (Fiocruz-Paraná) 04/09/14 Gerente de qualidade do IBMP Pesquisador do IBMP, projeto PodiTrodi (diagnóstico para Chagas) 04/09/14 04/09/14 Professor do Departamento de Física da UFPR Nacionalização de insumos para diagnóstico • Diferentes estratégias para nacionalização de insumos: transferência de tecnologia (testes rápido e confirmatório DPP HIV), desenvolvimento interno em consórcio e adaptação de tecnologia (teste NAT, multiteste baseado em microarranjos líquidos, multiteste para Rede Cegonha) • Dificuldades para negociar transferência de tecnologia com laboratórios privados, que propõem apenas transferência parcial ou interrupção da produção com o término do contrato Teste de ácido nucleico (NAT) • Teste baseado na amplificação de ácidos nucleicos (NAT) para triagem de bolsas de sangue permite detecção durante o período da janela imunológica, aumentando segurança transfusional • Componentes do NAT desenvolvidos por Bio-Manguinhos, UFRJ e Instituto de Biologia Molecular do Paraná (IBMP). Fiocruz obteve patente para um componente do kit – vírus calibrador • No início dos anos 2000, quando foi constituído projeto NAT brasileiro, não havia teste NAT registrado no Brasil e previsão de preço de $50 por determinação. O kit desenvolvido por Bio-Manguinhos/IBMP custa hoje $6-7 por paciente e detecta HIV/HCV (em breve incluirá HBV) Instituto Nacional de Ciência e Tecnologia em Diagnóstico • Rede multidisciplinar e multi-institucional (FiocruzParaná, Bio-Manguinhos, UFPR, UTFPR etc.) para desenvolver componentes de multiteste baseado em microarranjos líquidos para triagem de sangue: parceria com empresa Luminex e gradual nacionalização de componentes (anticorpos, antígenos, microesferas de poliestireno) • INCT resultou em outros projetos de desenvolvimento como o multiteste rápido para a Rede Cegonha – doenças similares e inicialmente com adaptação de tecnologia de microarranjos para um multiteste point-of-care. Multiteste é alvo de PDP para transferir tecnologia para setor produtivo. Próximos passos 1 – Dar prosseguimento a estudos de laboratório para compreender especificidades, desafios e oportunidades relacionados ao desenvolvimento de duas tecnologias – NAT e multiteste baseado em microarranjos líquidos 2 – Estudar os aspectos de propriedade intelectual na área de testes e tendências de patenteamento no Brasil 3 - Abordar os aspectos regulatórios do registro de testes para diagnóstico 4 – Compreender as vantagens de se adotar testes rápidos e point-of-care, assim como desafios relacionados a implementação desses testes no SUS
Download